Aufgabe 3 – Biochemie
Es wird vermutet, dass Porphyrien, eine Gruppe erblich bedingter Stoffwechselstörungen, zur Legende von Vampiren (Abbildung 1) führten. Allen Porphyrie-Formen ist gemeinsam, dass die Herstellung der farbgebenden Nichtprotein-Komponente Häm des roten Blutfarbstoffs Hämoglobin (Abbildungen 2a und 2b) durch eine Genmutation gestört ist. Dies führt zu einem Mangel an funktionsfähigen Erythrocyten. Die Haut der Betroffenen ist blass und kalt. Hinzu kommt die legendäre Lichtunverträglichkeit.

Abb. 1: „Vampir“

Abb. 2a: Hämoglobin (schematisch)
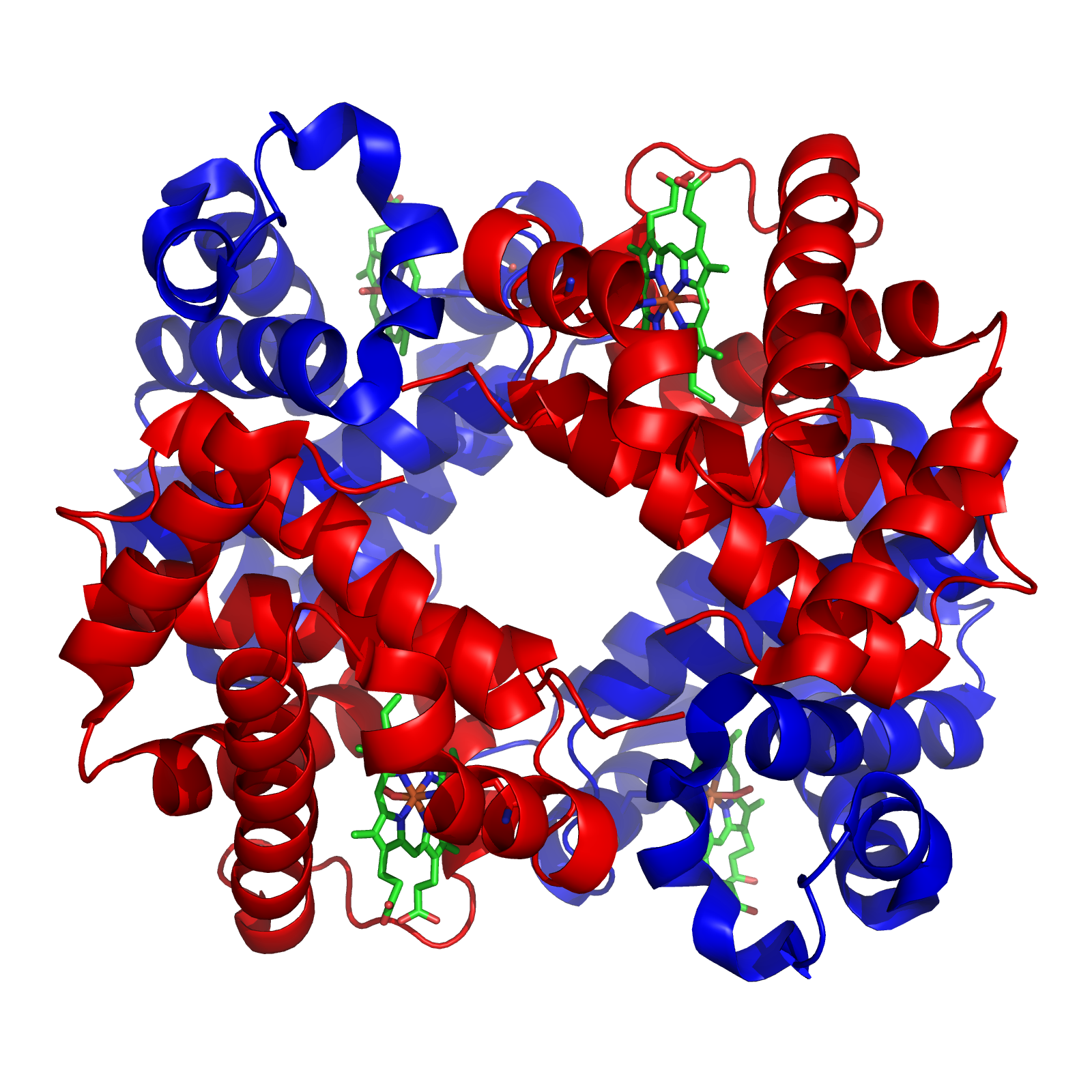
Abb. 2b: Hämoglobin (Bändermodell)
1
Beschreibe die in den Abbildungen 2a und 2b dargestellten Strukturebenen des Proteins Hämoglobin. Nenne die Kräfte und Bindungen, die diese jeweils stabilisieren.
Die verschiedenen Porphyrie-Formen beruhen auf Defekten von Enzymen in der Biosynthese des Häms. Abbildung 3 zeigt auszugsweise den Syntheseweg sowie mutationsbedingte Krankheitsbilder (Porphyrien).
3 VP
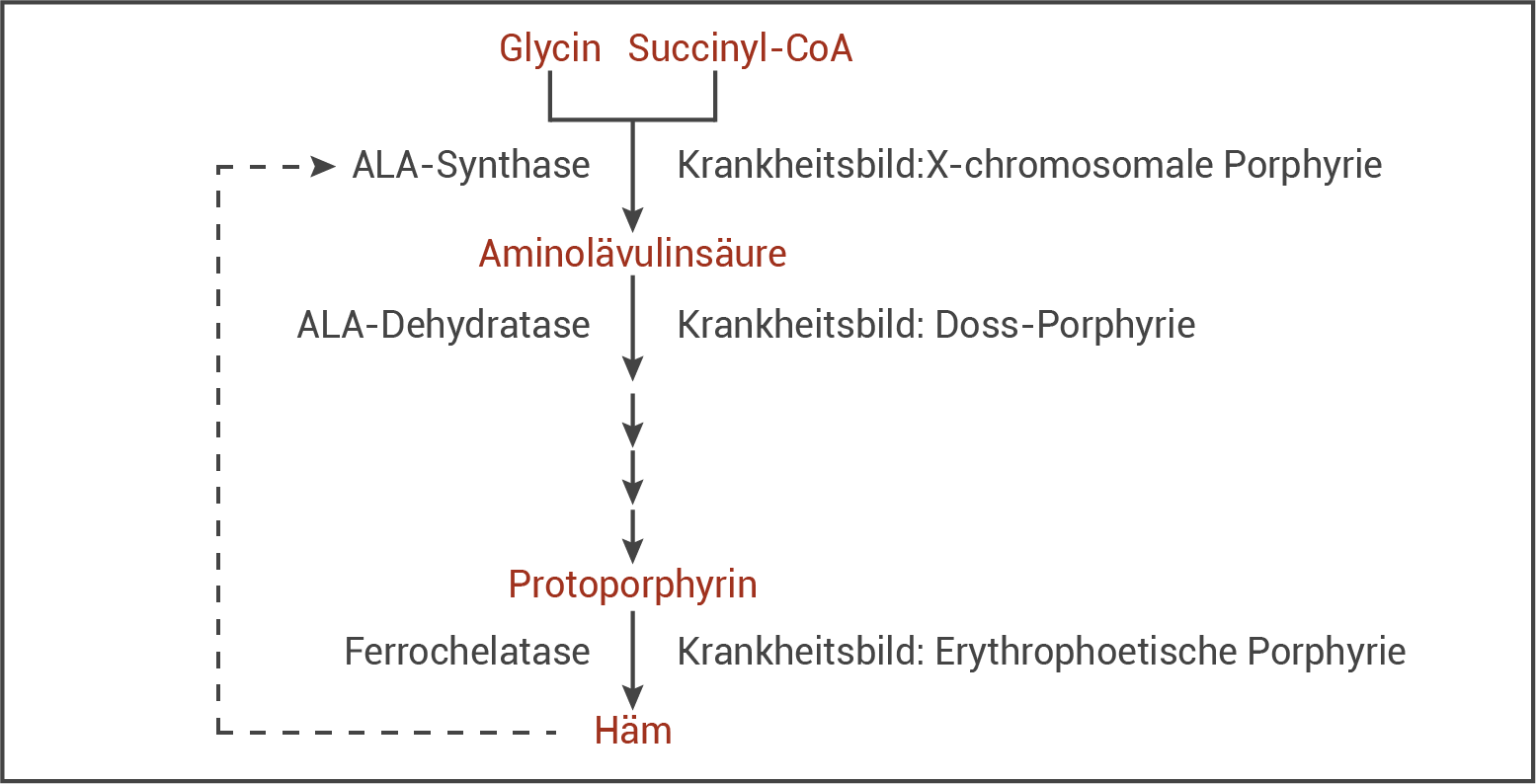
Abb. 3: Genwirkkette der Häm-Synthese und Krankheitsbilder bei entsprechenden Enzymdefekten (vereinfachte Darstellung)
2.1
Erkläre am Beispiel der Häm-Synthese den Begriff Genwirkkette.
2 VP
2.2
Begründe, warum verschiedene Mutationen in dieser Genwirkkette immer eine Blutarmut zur Folge haben, darüber hinaus aber verschiedene Krankheitssymptome verursachen.
Da die defekten Enzyme meist noch eine geringe Aktivität aufweisen, können der Häm-Mangel und die damit einhergehende Blutarmut durch Regulation der Häm-Biosynthese zumindest vermindert werden.
2 VP
3.1
Gib eine mögliche Erklärung für die mutationsbedingte reduzierte Enzymaktivität.
2 VP
3.2
Erläutere unter Verwendung von Abbildung 3, wie die Häm-Synthese auf Enzymebene normalerweise reguliert wird und wie bei einer Porphyrie-Erkrankung diese Regulation dem Häm-Mangel zumindest teilweise entgegenwirkt.
3 VP
3.3
Stelle den zugrunde liegenden Mechanismus dieser Enzymregulation mithilfe beschrifteter Schemazeichnungen dar (Größe etwa ½ Seite).
Bei den Porphyrie-Formen treten neben dem Häm-Mangel weitere Symptome auf. So kommt es bei Patienten mit Erythropoetischer Porphyrie zu verbrennungsähnlichen Symptomen der Haut. Ursache hierfür ist in der Haut angereichertes Protoporphyrin, das mithilfe von Sonnenlicht Sauerstoffradikale bildet, die das Hautgewebe schädigen. Die Betroffenen meiden daher das Licht. Eine natürliche Reaktion des Körpers auf Sonnenlicht ist die Freisetzung des Melanocyten-stimulierenden Hormons (
3 VP
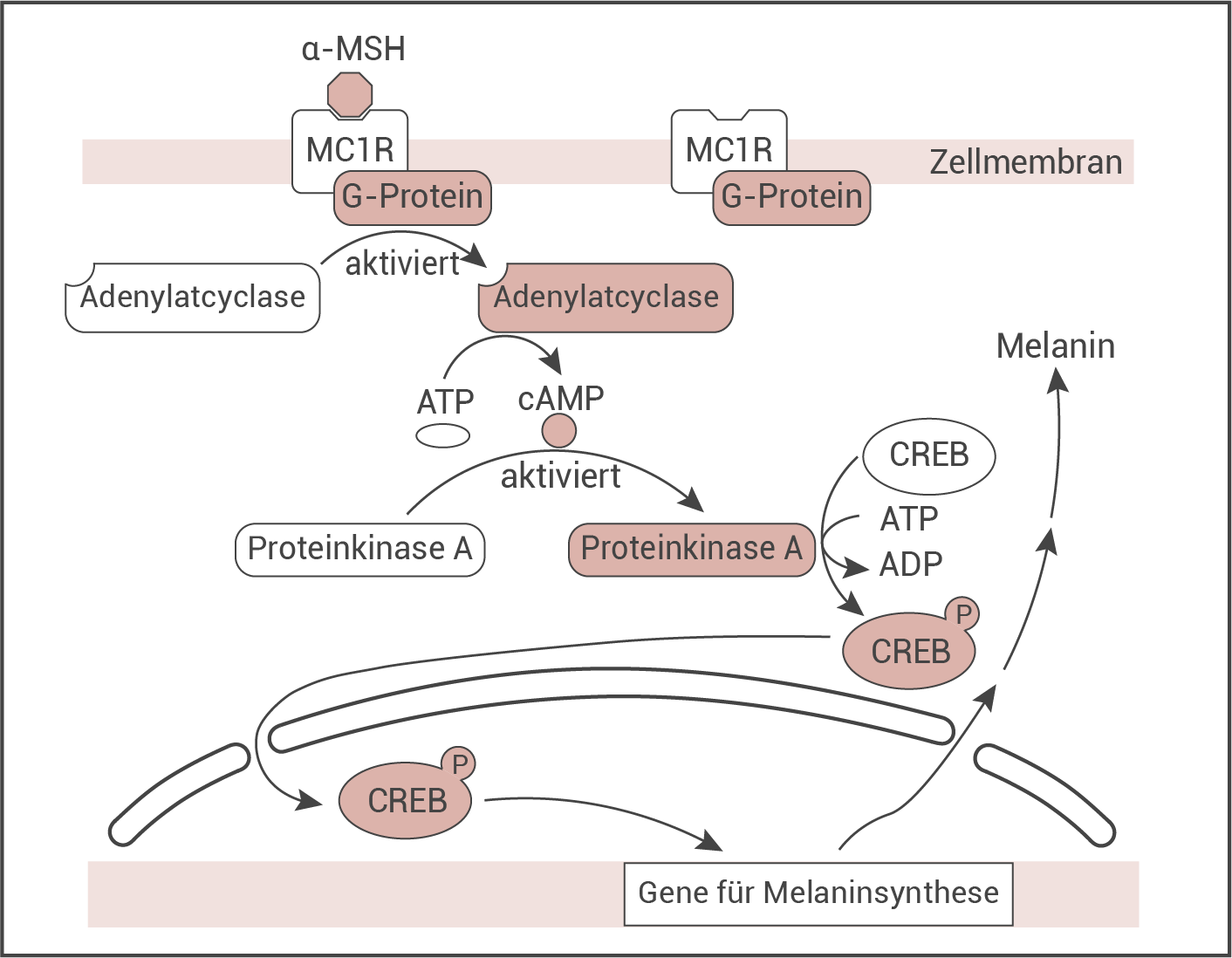
Abb. 4: Wirkung von  -MSH auf die Melaninproduktion in Hautzellen (stark vereinfacht)
-MSH auf die Melaninproduktion in Hautzellen (stark vereinfacht)
4
Beschreibe die in Abbildung 4 dargestellten Prozesse und erkläre, wie wenige  -MSH-Moleküle in einer Zelle eine starke Melaninbildung auslösen.
-MSH-Moleküle in einer Zelle eine starke Melaninbildung auslösen.
Da Heilung nicht möglich ist, steht für Patienten mit Erythropoetischer Porphyrie der Schutz vor Sonnenlicht im Vordergrund. Im Dezember 2014 wurde hierfür in der EU ein Medikament mit dem Wirkstoff Afamelanotid zur Behandlung von erwachsenen Patienten mit Erythropoetischer Porphyrie zugelassen. Dieses löst die Bräunung der Haut aus, ohne dass ein Kontakt mit Sonnenlicht stattgefunden hat.
3 VP
5
Gib eine mögliche Erklärung für die Wirkungsweise von Afamelanotid und für das Phänomen, dass der Wirkstoff sogar wirksamer als die körpereigene Substanz ist.
Bildnachweise [nach oben]
2 VP
20 VP
Zephyris (Richard Wheeler), 1GZX Haemoglobin, CC BY-SA 3.0
1
Beschreibung der dargestellten Strukturebene:
Das Protein Hämoglobin weist eine Quartärstruktur aus, die aus vier Polypeptidketten besteht (siehe Abb. 2a: zwei - und zwei
- und zwei  -Ketten). Diese liegen jeweils in Tertiärstruktur vor (dreidimensionale Anordnung der Primär- und Sekundärstruktur) und als Sekundärstrukturen sind nur
-Ketten). Diese liegen jeweils in Tertiärstruktur vor (dreidimensionale Anordnung der Primär- und Sekundärstruktur) und als Sekundärstrukturen sind nur  -Helices zu sehen.
Nennung der stabilisierenden Kräfte und Bindungen:
-Helices zu sehen.
Nennung der stabilisierenden Kräfte und Bindungen:

Das Protein Hämoglobin weist eine Quartärstruktur aus, die aus vier Polypeptidketten besteht (siehe Abb. 2a: zwei

2.1
Erklärung des Begriffs Genwirkkette:
Für die Synthese des Häms (Stoffwechselendprodukt) sind mehrere aufeinanderfolgende Reaktionsschritte nötig. Das Produkt jeder enzymatisch katalysierten Reaktion dient dabei als Substrat für die nachfolgende Reaktion und jede Reaktion wird jeweils durch ein spezifisches Enzym katalysiert (in Abb. 3 sind ALA-Synthase, ALA-Dehydratase und Ferrochelatase genannt). Dabei wird jedes Enzym von einem eigenen Gen codiert. Die Abfolge solcher voneinander abhängigen Reaktionen (in einer Stoffwechselkette), die von den Produkten verschiedener Gene gesteuert werden, wird Genwirkkette genannt.
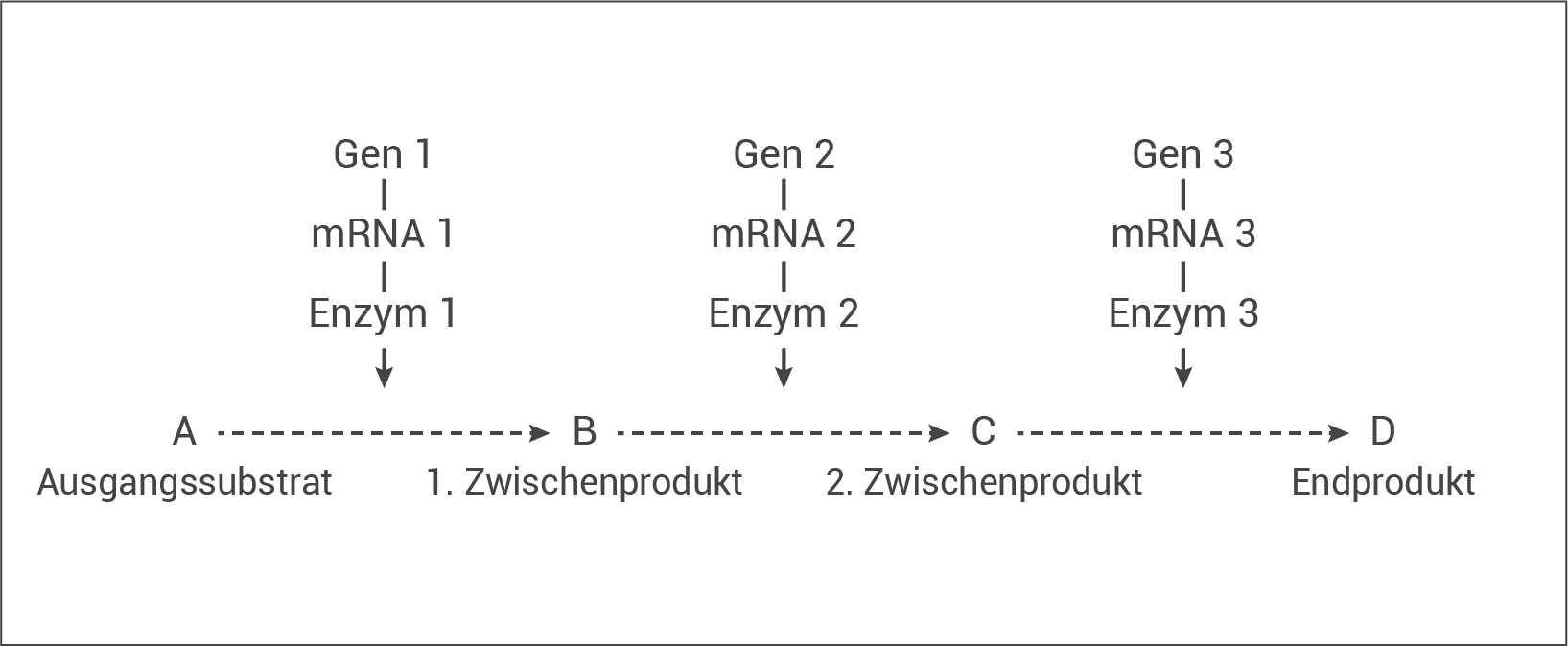
Für die Synthese des Häms (Stoffwechselendprodukt) sind mehrere aufeinanderfolgende Reaktionsschritte nötig. Das Produkt jeder enzymatisch katalysierten Reaktion dient dabei als Substrat für die nachfolgende Reaktion und jede Reaktion wird jeweils durch ein spezifisches Enzym katalysiert (in Abb. 3 sind ALA-Synthase, ALA-Dehydratase und Ferrochelatase genannt). Dabei wird jedes Enzym von einem eigenen Gen codiert. Die Abfolge solcher voneinander abhängigen Reaktionen (in einer Stoffwechselkette), die von den Produkten verschiedener Gene gesteuert werden, wird Genwirkkette genannt.

(Abbildung nicht verlangt)
2.2
Begründung der Blutarmut und der begleitenden Krankheitssymptome:
Häm als Endprodukt der Stoffwechselkette kann nur gebildet werden, wenn alle Teilreaktionen der Häm-Biosynthese ablaufen. Wenn es aufgrund einer Genmutation zum Defekt eines codierten Enzyms kommt, wird die Gen- und Enzymwirkkette abgebrochen. Daraus folgt ein Häm-Mangel, der die Blutarmut bedingt und wodurch es zu einer Anreicherung eines bestimmten Zwischenprodukts (welches in höheren Konzentrationen möglicherweise toxisch ist) bzw. zu einem Mangel des Folgeprodukts (welches u.U. auch als Substrat in einem anderen Stoffwechselweg benötigt wird) kommt. Infolge daraus, welches Gen der Genwirkkette von der Mutation betroffen ist, resultieren unterschiedliche Krankheitssymptome.
Häm als Endprodukt der Stoffwechselkette kann nur gebildet werden, wenn alle Teilreaktionen der Häm-Biosynthese ablaufen. Wenn es aufgrund einer Genmutation zum Defekt eines codierten Enzyms kommt, wird die Gen- und Enzymwirkkette abgebrochen. Daraus folgt ein Häm-Mangel, der die Blutarmut bedingt und wodurch es zu einer Anreicherung eines bestimmten Zwischenprodukts (welches in höheren Konzentrationen möglicherweise toxisch ist) bzw. zu einem Mangel des Folgeprodukts (welches u.U. auch als Substrat in einem anderen Stoffwechselweg benötigt wird) kommt. Infolge daraus, welches Gen der Genwirkkette von der Mutation betroffen ist, resultieren unterschiedliche Krankheitssymptome.
3.1
Mögliche Erklärung für die mutationsbedingte reduzierte Enzymaktivität:
Die Bindungsaffinität des Substrats zum aktiven Zentrum ist entscheidend für die Anzahl an Reaktionen pro Zeit (Wechselzahl), die ein Enzym katalysiert. Bei einer lediglich geringfügigen Veränderung der räumlichen Struktur (Konformation) des aktiven Zentrums eines Enzyms durch eine Mutation, kann das Enzym immer noch Substrate umsetzen. Das Substrat bindet allerdings weniger gut an das aktive Zentrum, weswegen die Umsetzung mit einer reduzierten Reaktionsgeschwindigkeit erfolgt (geringere Enzymaktivität).
Die Bindungsaffinität des Substrats zum aktiven Zentrum ist entscheidend für die Anzahl an Reaktionen pro Zeit (Wechselzahl), die ein Enzym katalysiert. Bei einer lediglich geringfügigen Veränderung der räumlichen Struktur (Konformation) des aktiven Zentrums eines Enzyms durch eine Mutation, kann das Enzym immer noch Substrate umsetzen. Das Substrat bindet allerdings weniger gut an das aktive Zentrum, weswegen die Umsetzung mit einer reduzierten Reaktionsgeschwindigkeit erfolgt (geringere Enzymaktivität).
3.2
Erläuterung der Regulation der Häm-Synthese:
Die Regulation der Häm-Synthese geschieht durch eine Endprodukthemmung (feed back inhibition), wodurch eine bedarfsgerechte Synthese von Häm sichergestellt wird. Die ALA-Synthase, das Schlüsselenzym der Häm-Biosynthesekette, wird durch das Endprodukt Häm (konzentrationsabhängig) gehemmt. Das geschieht infolge einer verringerten Bildung von Aminolävulinsäure, die als Ausgangssubstrat für die weiteren Teilreaktionen des Häm-Biosynthesewegs dient. Den ganzen Stoffwechselweg über setzt sich dieser initiale Mangel hinfort und führt schlussendlich am Ende der Stoffwechselkette zu einer reduzierten Synthese des Endprodukts Häm. Erläuterung der entgegenwirkenden Regulation:
Bei einer Porphyrie-Erkrankung werden weniger ALA-Synthasen inhibiert, da der mutationsbedingte Mangel an Häm zu einer Reduktion der Endprodukthemmung führt. Die Synthese von Aminolävulinsäure ist folglich bei Erkrankten nicht so stark reduziert. Die unterschiedlichen Porphyrie-Formen beruhen meist auch auf Mutationen, die zu einer geringeren Enzymaktivität führen, weshalb dem jeweiligen funktionseingeschränkten Enzym zumindest genügend Substrate zur Verfügung stehen. Dadurch wird der Häm-Mangel am Ende der Stoffwechselkette etwas kompensiert.
Die Regulation der Häm-Synthese geschieht durch eine Endprodukthemmung (feed back inhibition), wodurch eine bedarfsgerechte Synthese von Häm sichergestellt wird. Die ALA-Synthase, das Schlüsselenzym der Häm-Biosynthesekette, wird durch das Endprodukt Häm (konzentrationsabhängig) gehemmt. Das geschieht infolge einer verringerten Bildung von Aminolävulinsäure, die als Ausgangssubstrat für die weiteren Teilreaktionen des Häm-Biosynthesewegs dient. Den ganzen Stoffwechselweg über setzt sich dieser initiale Mangel hinfort und führt schlussendlich am Ende der Stoffwechselkette zu einer reduzierten Synthese des Endprodukts Häm. Erläuterung der entgegenwirkenden Regulation:
Bei einer Porphyrie-Erkrankung werden weniger ALA-Synthasen inhibiert, da der mutationsbedingte Mangel an Häm zu einer Reduktion der Endprodukthemmung führt. Die Synthese von Aminolävulinsäure ist folglich bei Erkrankten nicht so stark reduziert. Die unterschiedlichen Porphyrie-Formen beruhen meist auch auf Mutationen, die zu einer geringeren Enzymaktivität führen, weshalb dem jeweiligen funktionseingeschränkten Enzym zumindest genügend Substrate zur Verfügung stehen. Dadurch wird der Häm-Mangel am Ende der Stoffwechselkette etwas kompensiert.
3.3
Schematische Darstellung des Mechanismus der Enzymregulation:
Im ersten Schritt der Enzymregulation entsteht aus zwei Edukten (Glycin und Succinyl-CoA) ein Produkt (Aminolävulinsäure) und ist für diese entscheidend. Die schematische Darstellung muss also zwei Substrate im aktiven Zentrum berücksichtigen und es muss sich um eine reversible allosterische Regualtion handeln: Eine kompetitive Hemmung ist nicht wahrscheinlich, da die zahlreichen Teilreaktionen zu einer geringen Ähnlichkeit des Endprodukt mit einem der beiden Ausgangssubstrate (Glycin, Succinyl-CoA) führt.
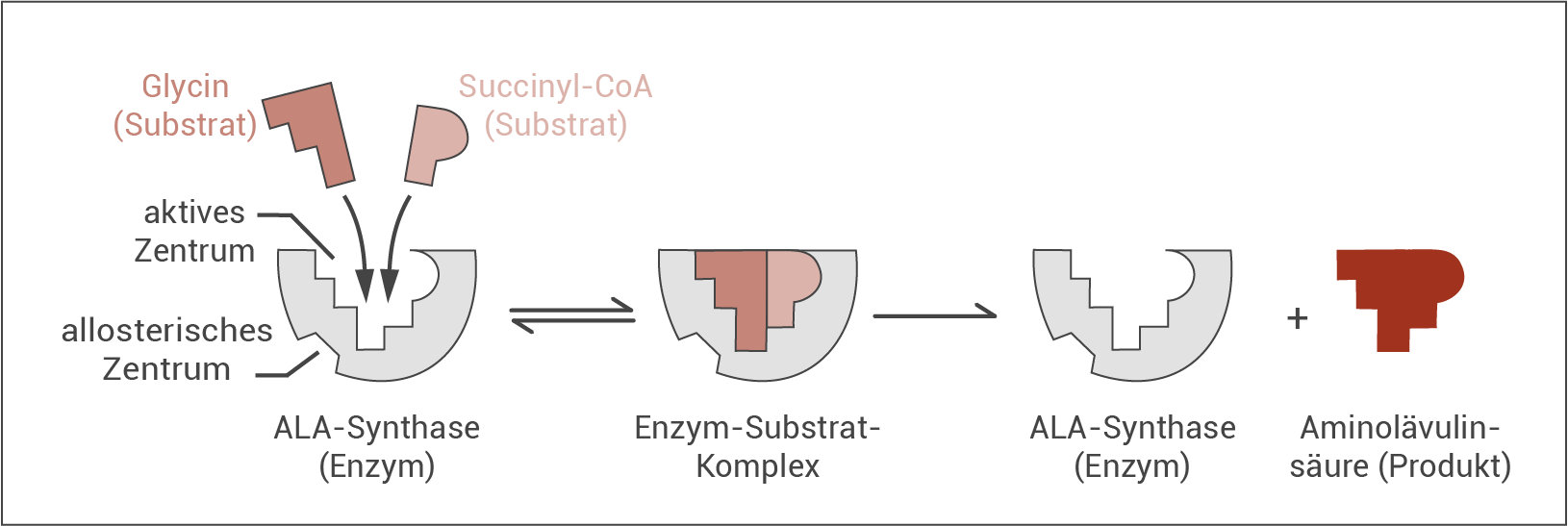
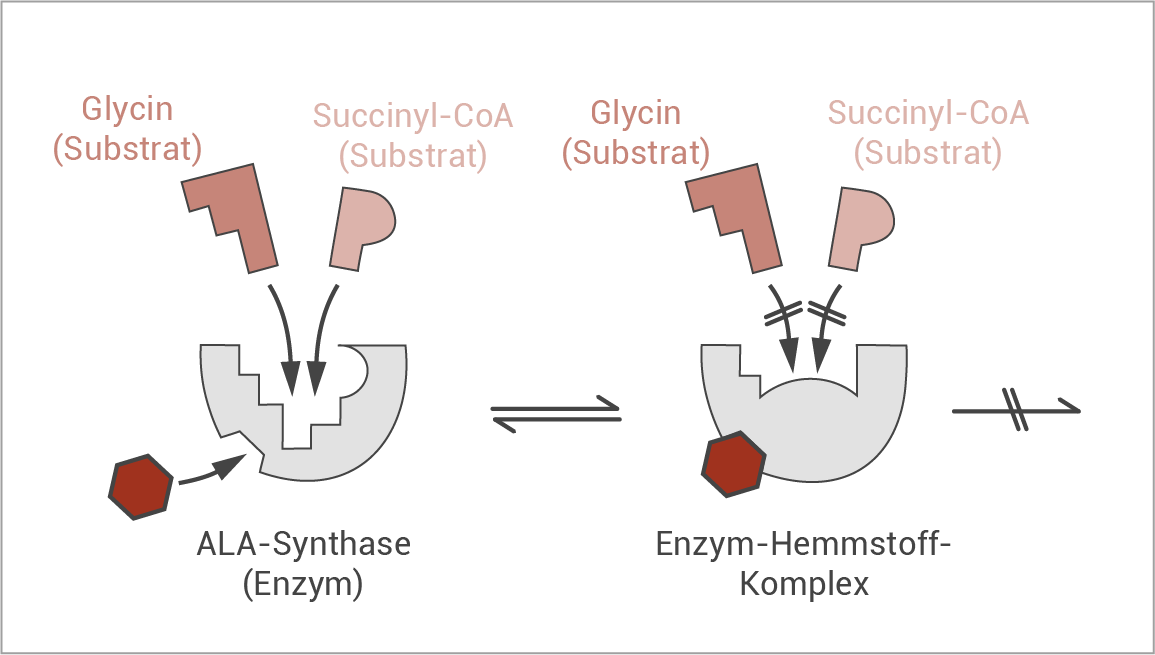
Im ersten Schritt der Enzymregulation entsteht aus zwei Edukten (Glycin und Succinyl-CoA) ein Produkt (Aminolävulinsäure) und ist für diese entscheidend. Die schematische Darstellung muss also zwei Substrate im aktiven Zentrum berücksichtigen und es muss sich um eine reversible allosterische Regualtion handeln: Eine kompetitive Hemmung ist nicht wahrscheinlich, da die zahlreichen Teilreaktionen zu einer geringen Ähnlichkeit des Endprodukt mit einem der beiden Ausgangssubstrate (Glycin, Succinyl-CoA) führt.

Abb.: Enzymreaktion ohne Häm

Abb.: allosterische Enzymhemmung durch Häm
4
Beschreibung der dargestellten Prozesse:
 -MSH-Moleküle (nur eine erforderlich):
-MSH-Moleküle (nur eine erforderlich):
- Ein
-MSH-Molekül bindet (spezifisch) auf der extrazellulären Seite an den MC1R-Rezeptor, der in die Zellmembran integriert ist (Schlüssel-Schloss-Prinzip).
- Ein auf der cytoplasmatischen Seite an den MC1R-Rezeptor gekoppelte G-Protein wird dadurch aktiviert, welches das Enzym Adenylatcyclase aktiviert.
- Das aktivierte Adenylatcyclase katalysiert nun die Umsetzung von ATP in cAMP (second messenger), welches (das Enzym) Proteinkinase A aktiviert.
- Durch die aktivierte Proteinkinase A wird die Übertragung einer Phosphatgruppe von ATP auf CREB-Moleküle katalysiert (Phosphorylierung). Hierbei wird ATP zu ADP umgesetzt und es entstehen aktivierte CREB-Moleküle. Aufgrund der Phosphorylierung können diese durch die Kernporen in den Zellkern eindringen.
- Es erfolgt die Transkription der Gene für die Melaninsynthese, die durch die aktivierten CREB-Moleküle (Transkriptionsfaktoren) bewirkt wird.
- Über die Kernporen gelangen die Gen-Transkripte (mRNA) ins Cytoplasma, welche an Ribosomen in Enzyme zur Melaninsynthese translatiert werden. Diese katalysieren die Bildung des Hautfarbstoffs Melanin im Cytoplasma der Hautzellen.
- Die Enzyme Adenylatcyclase und Proteinkinase A werden innerhalb der Signaltransduktionskaskade aktiviert. Ein einziges dieser aktivierten Enzyme kann die Umwandlung von zahlreichen Substratmolekülen katalysieren, wodurch es zu einer massiven Verstärkung des Signals kommt und deshalb zu einer starken intrazellulären Melaninbildung.
- Solange das
-MSH-Molekül an den MC1R-Rezeptor gebunden ist, werden vorhandene Adenylatcyclasen durch das aktivierte G-Protein aktiviert. Die Bindung eines
-MSH-Moleküls bewirkt daher die Aktivierung zahlreicher Adenylatcyclasen, woraus ein Verstärkereffekt innerhalb des Signaltransduktionswegs folgt und Melanin stark gebildet wird.
5
Mögliche Erklärung für die Wirkungsweise und stärkere Wirkung von Afamelanotid (nur eine erforderlich):
- Rezeptorebene (extrazellulär): Afamelanotid und das Melanocyten-stimulierende Hormon (
-MSH) ähneln sich im chemischen und räumlichen Bau. Wenn es mit einer höheren Affinität an den MC1R-Rezeptor bindet oder langsamer abgebaut wird, dann ist das Medikament wirksamer als die körpereigene Substanz.
- Enzymebene (Cytoplasma): Afamelanotid ist klein und lipophil und durchdringt in hoher Konzentration die Biomembran, woraufhin zahlreiche Enzyme des Signaltransduktionswegs (z.B. Adenylatcyclasen) im Cytoplasma (mit hoher Affinität) aktiviert werden. Im Zuge dessen ist es wirksamer als die körpereigene Substanz.
- Ebene der DNA (im Zellkern): Afamelanotid durchdringt die Biomembran, da es klein und lipophil ist. Es bindet an einen Rezeptor im Cytoplasma und gelangt als besonders wirksamer Transkriptionsfaktor der Gene für die Melaninsynthese in den Zellkern.