Aufgabe 2 – Immunbiologie, Genetik
Tsetsefliegen sind in weiten Teilen Afrikas verbreitet. Sie sind Zwischenwirte von begeißelten, eukaryotischen Einzellern der Gattung Trypanosoma. Trypanosomen verursachen beim Menschen die Schlafkrankheit. Bei einem Stich durch die Tsetsefliege werden bis zu 20 000 Trypanosomen übertragen. Sie gelangen in den Blutkreislauf und vermehren sich durch Zellteilung. Die gesamte Zelloberfläche dieser Einzeller wird von einem einzigen Proteintyp bedeckt, dem so genannten „variant surface glycoprotein“ (VSG). Trypanosomen sind in der Lage, immer wieder neue VSG-Varianten zu bilden.
Nach einer Infektion mit Trypanosomen kann man einen zyklischen Krankheitsverlauf erkennen. In Abbildung 1 ist dieser anhand der Konzentration der Trypanosomen und Antikörper im Blut dargestellt.
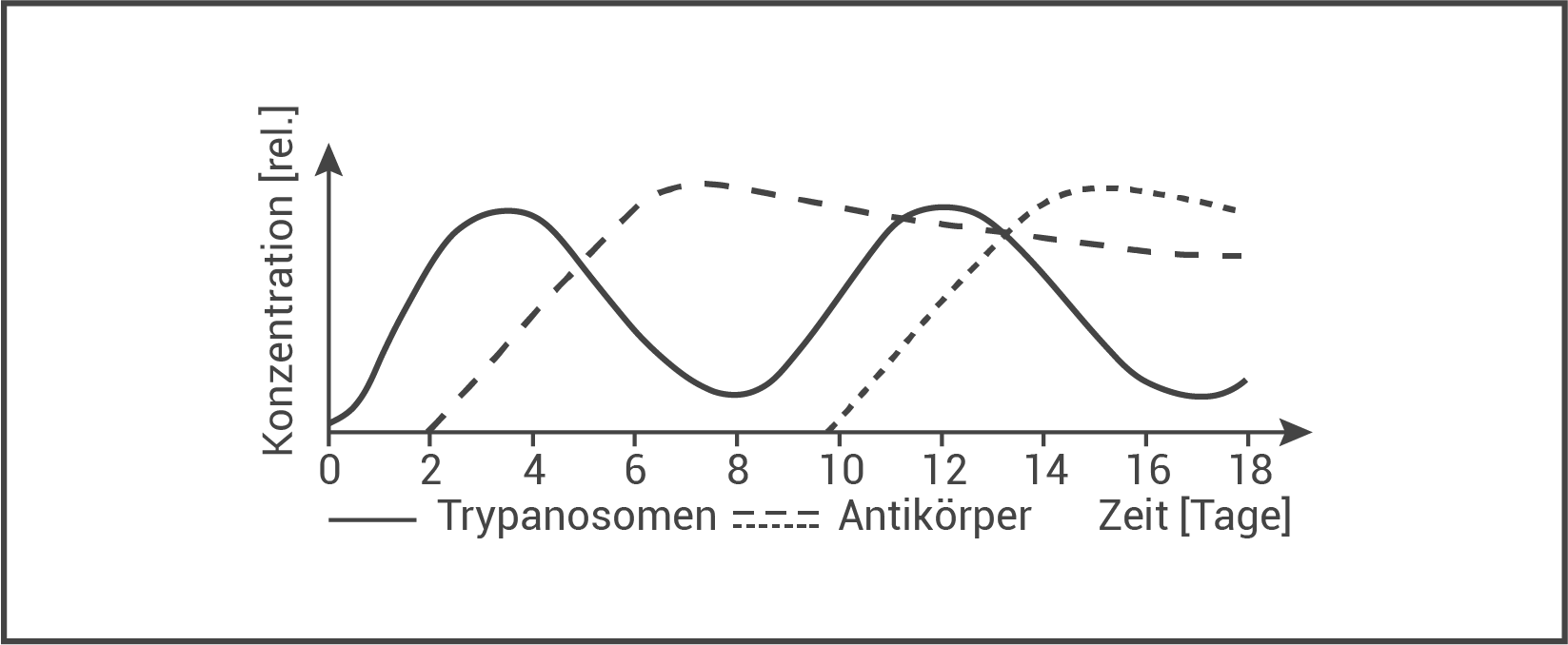

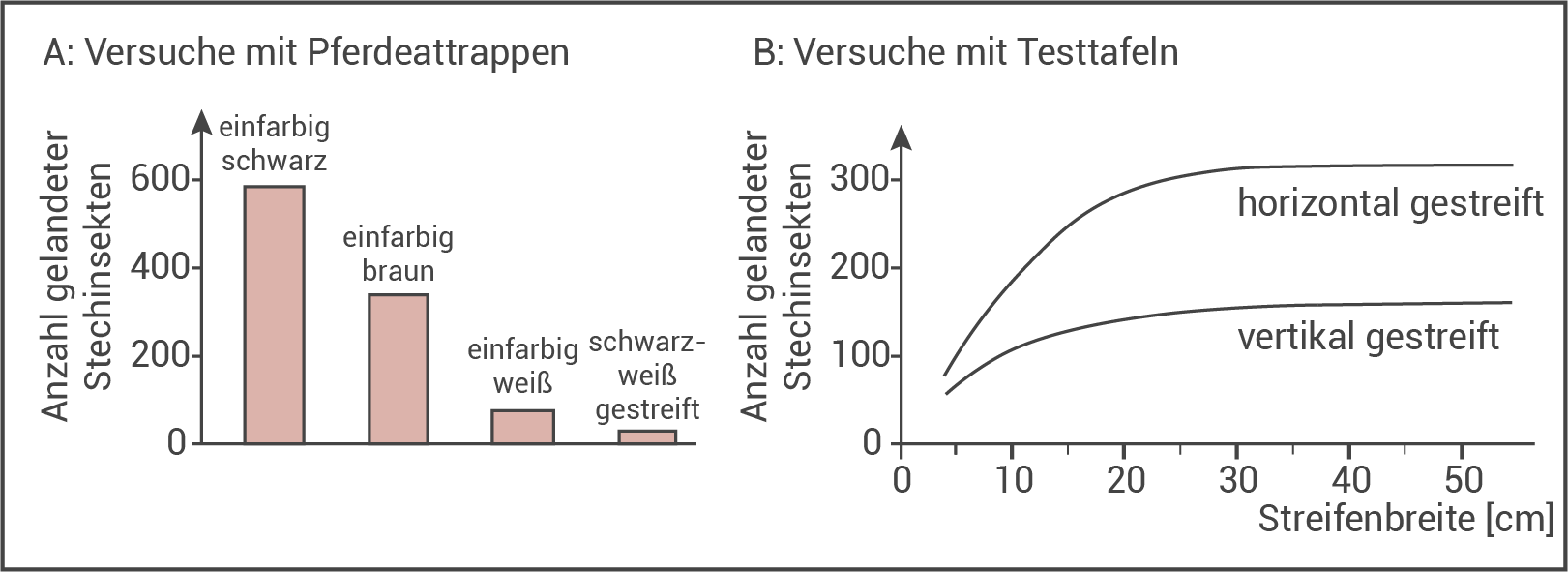
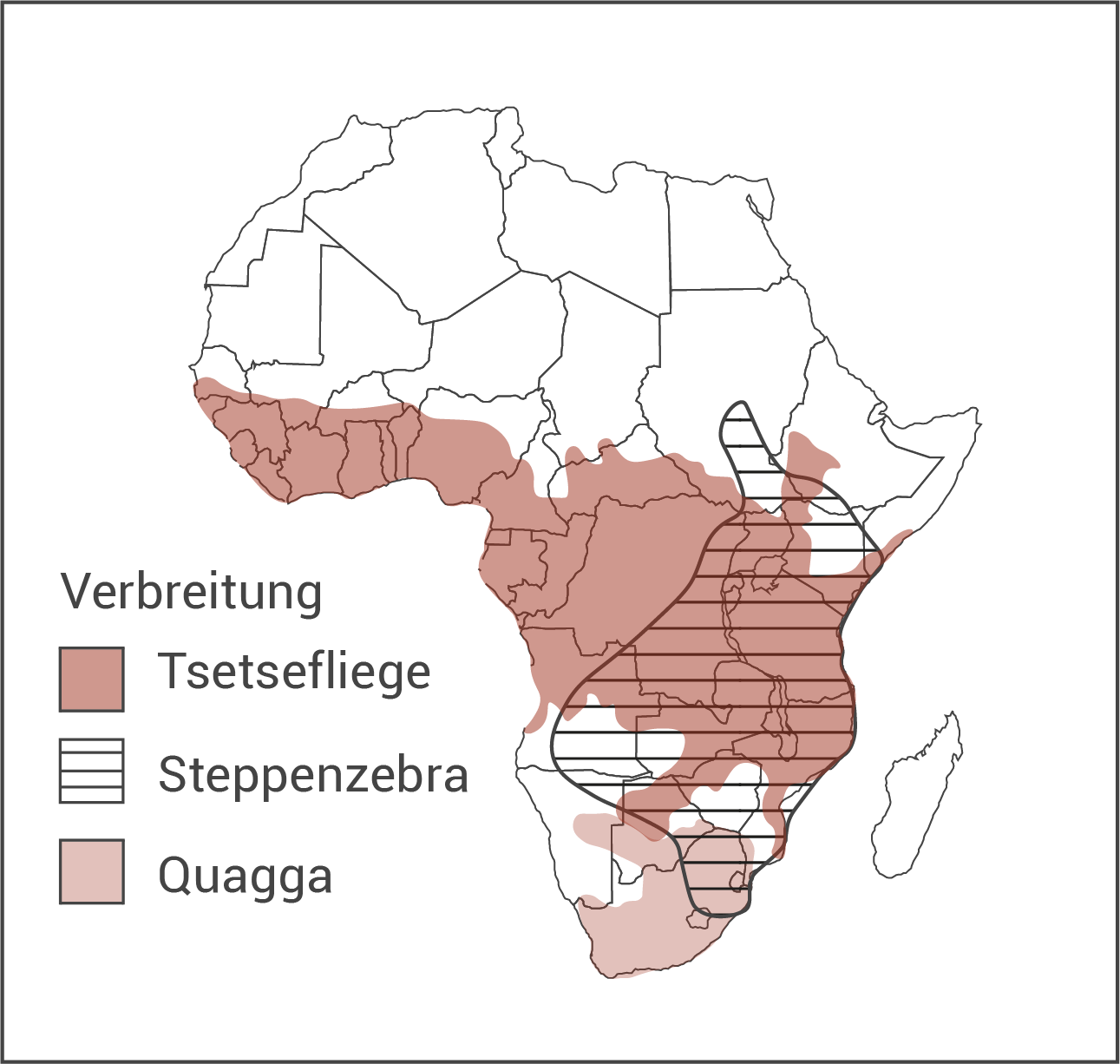
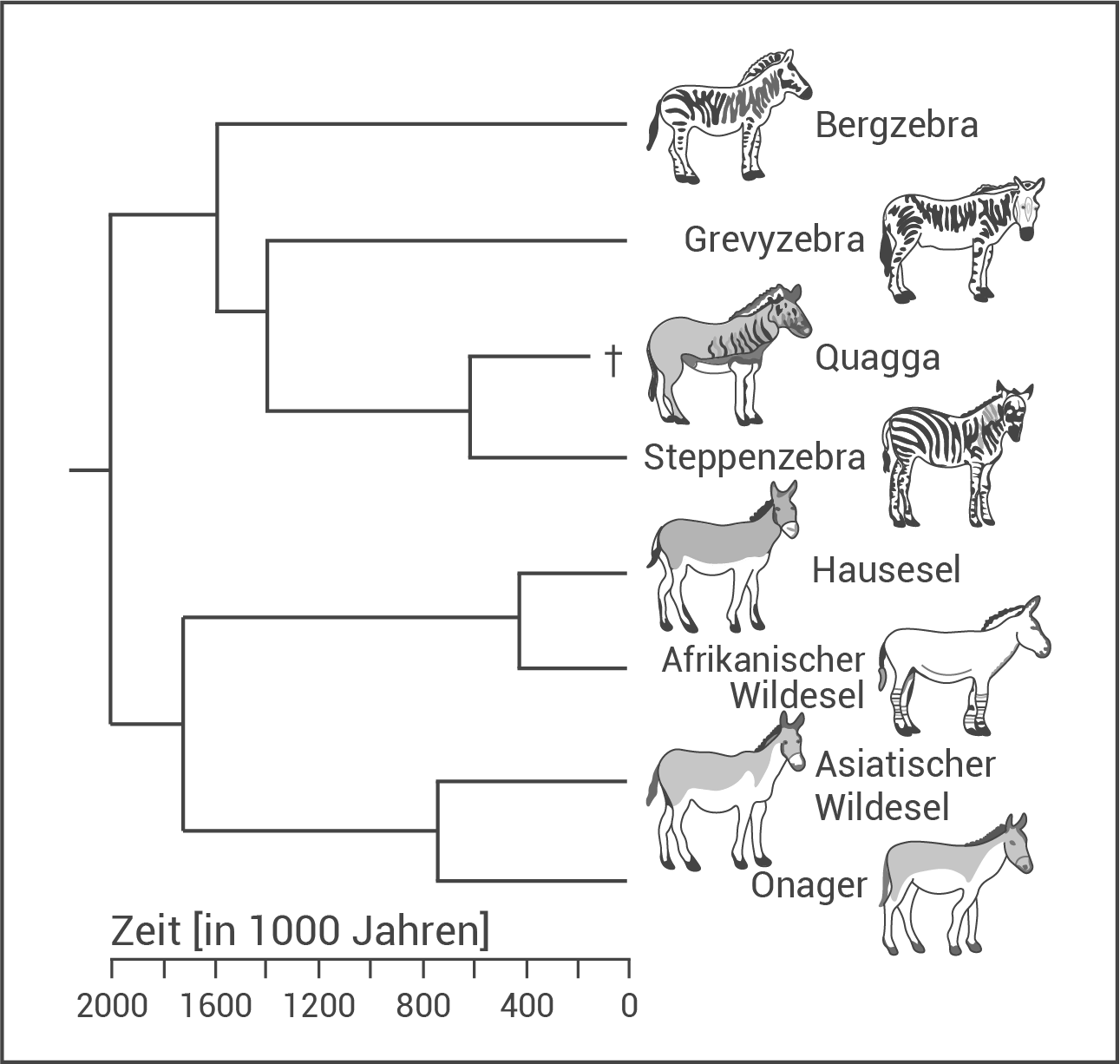

Abb.1: Konzentrationsverlauf von Trypanosomen und Antikörpern im Blut
1.1
Beschreibe die humorale Immunantwort, die im Körper des mit Trypanosomen Infizierten bis zum 8. Tag abläuft.
4 VP
1.2
Erkläre anhand von Abbildung 1 und unter Verwendung des Vortextes den zyklischen Verlauf der Trypanosomen-Konzentration. Erkläre, weshalb trotz ablaufender Immunantwort keine Immunität entsteht.
3 VP
Eine Infektion mit Trypanosomen führt bei Individuen aus der Familie der Pferdeartigen zur tödlichen Nagana-Seuche. Wissenschaftler vermuten, dass Zebras aufgrund ihres Fellmusters von stechenden Insekten wie der Tsetsefliege visuell schlecht wahrgenommen werden. Dies machen sich Reitsportausstatter zunutze und werben für zebraartig gestreifte Pferdedecken (Abbildung 2). Forscher untersuchten diese Vermutung mit unterschiedlich bemalten Pferdeattrappen sowie mit verschiedenen schwarz-weiß gestreiften Testtafeln. Sie zählten, wie viele Insekten in einem Zeitraum von drei Wochen auf diesen Versuchsgegenständen landeten (Abbildung 3).

Abb. 2: Pferdedecke

Abb. 3: Versuchsergebnisse
2
Nenne die Eigenschaften einer möglichst wirksamen Pferdedecke und begründe diese anhand der Versuchsergebnisse (Abbildung 3).
Es wird davon ausgegangen, dass Tsetsefliegen auch eine Rolle in der Evolution der Pferdeartigen gespielt haben. Abbildung 4 zeigt die Verbreitung der Tsetsefliege, des Steppenzebras und des Quaggas auf dem afrikanischen Kontinent im Jahr 1820. Abbildung 5 zeigt einen Ausschnitt aus dem Stammbaum der Pferdeartigen.
2 VP

Abb. 4: Verbreitungsgebiete im Jahr 1820

Abb. 5: Ausschnitt aus dem Stammbaum der Pferdeartigen (Quagga ausgerottet)
3.1
Erkläre auf Grundlage der Synthetischen Evolutionstheorie die Musterung des Steppenzebras (Abbildung 5). Berücksichtige dabei auch Abbildung 4 sowie die Versuchsergebnisse aus Abbildung 3.
4 VP
3.2
Erläutere mithilfe der Abbildung 5, ob die fehlende Streifung auf dem Rücken des Quaggas ein ursprüngliches oder ein abgeleitetes Merkmal ist. Gib unter Verwendung von Abbildung 4 eine mögliche Erklärung für die weitgehend fehlende Musterung des Quaggas.
3 VP
3.3
Beschreibe ein molekularbiologisches Verfahren zur Überprüfung der Verwandtschaftsverhältnisse von Hausesel, Afrikanischem Wildesel und Steppenzebra. Erläutere die zu erwartenden experimentellen Ergebnisse für die drei genannten Arten bei dem von dir beschriebenen Verfahren.
4 VP
20 VP
1.1
Beschreibung der humoralen Immunantwort:
- Erkennungsphase: Der Stich der Tsetsefliege überträgt Trypanosomen, welche durch Makrophagen als körperfremdes Glyoprotein auf der Zelloberfläche erkannt werden. Diese Erreger werden phagozytiert, in Bruchstücke zerlegt und mithilfe spezieller Membranproteine (MHC II) auf der Membranoberfläche der Makrophagen präsentiert. Nach dem Schlüssel-Schloss-Prinzip binden ruhende spezifische T-Helferzellen mit ihren spezifischen T-Zell-Rezeptoren an die präsentierten Antigen(fragmente). Es wird daraufhin der Signalstoff (Zytokin) der Makrophagen ausgeschüttet. Dieser aktiviert T-Helferzellen, welche zur Teilung (Proliferation) und Differenzierung in aktive T-Helfer- und T-Helfer-Gedächtniszellen angeregt werden. Währenddessen erkennen spezielle B-Lymphozyten mit passenden Rezeptoren die Antigene auf der Zelloberfläche der Trypanosomen. Diese Erreger werden ebenfalls phagozytiert und nach intrazellulärer Zerkleinerung über MHC II-Proteine auf der Membranoberfläche der B-Lymphozyten präsentiert. Die davor aktivierten T-Helferzellen binden über ihre spezifischen T-Zell-Rezeptoren an die an der Membranoberfläche präsentierten Antigen(fragment)e und schütten daraufhin Signalstoffe (Zytokine) aus.
- Differenzierungsphase: Durch die ausgeschütteten Signalstoffe werden die spezifischen B-Lymphozyten zur Vermehrung (Proliferation) und Differenzierung in Plasmazellen und B-Gedächtniszellen angeregt.
- Wirkungsphase: Die Plasmazellen produzieren spezifische Antikörper, die vor allem gegen das "variant surface glycoprotein" der Trypanosomen sind. Auf der Zelloberfläche der Erreger bilden die freigesetzten Antikörper mit den Glycoproteinen Antigen-Antikörper-Komplexe, welche dann von Makrophagen phagozytiert werden.
1.2
Erklärung des zyklischen Verlaufs der Trypanosomen-Konzentration:
Es wird empfohlen zunächst den zyklischen Verlauf der Trypanosomen-Konzentration zu beschreiben und aus dem Vortext lässt sich schließen, dass die beiden Kurven die Konzentrationen unterschiedlicher Antikörper darstellen. Beschreibung: Die Trypanosomen-Konzentration startet bei einem sehr geringen Anfangswert und steigt nach einer kurzen "Anlaufsphase" bis zum zweiten Tag nach der Infektion nahezu linear. Die Kurve wird daraufhin flacher, bis sie ca. am dritten Tag ein Maximum erreicht. Die anschließend sinkende Trypanosomen-Konzentration erreicht am ca. achten Tag ein Minimum, liegt aber dennoch deutlich über dem Nullwert der Trypanosomen-Konzentration im Blut. Dieser Kurvenverlauf wiederholt sich. Erklärung: Während der ersten beiden Tage nach der Infektion findet eine ungestörte Zellteilung der Trypanosomen statt, die den anfänglichen linearen Anstieg erklären. Infolge der Dauer der Erkennungs- und Differenzierungsphase im Zuge der humoralen Immunantwort sind die Plasmazellen erst ab dem zweiten Tag verfügbar, die für die Bildung spezifischer Antikörper gegen die zu dieser Zeit die Zelloberfläche bedeckende VSG-Variante zuständig sind. Die Konzentration dieser Antikörper im Blut steigt vom zweiten Tag linear an, weswegen der Anstieg der Trypanosomen-Konzentration im Blut durch die Bildung von Antigen-Antikörper-Komplexen langsamer wird. Durch die zunehmende Antikörper-Konzentration im Blut sinkt die Trypanosomen-Konzentration ab dem dritten Tag bis auf ein Minimum ab. Trotz gleichbleibender Antikörperproduktion werden jedoch nicht alle Trypanosomen abgetötet, sondern deren Konzentration steigt sogar wieder linear an. Daraus folgt, dass die vorhandenen Antikörper wirkungslos geworden sind, da einige Trypanosomen eine neue Variante ihres Oberflächenproteins gebildet haben, an die die bestehenden Antikörper nun nicht mehr binden können. Gleichzeitig sind die Proteine für das Immunsystem ein neues Antigen, gegen das nach einer erneuten Erkennungs- und Differenzierungsphase wieder spezifische Antikörper durch neue Plasmazellen gebildet werden. Die folgende Wirkungsphase bewirkt eine erneute Senkung der Trypanosomen-Konzentration im Blut. Erklärung, weshalb keine Immunität entsteht:
Es entstehen immer wieder Trypanosomen mit neuen VSG-Varianten, weswegen die noch über viele Tage vorhandenen Antikörper und die gebildeten B-und T-Helfer-Gedächtniszellen unwirksam sind. Diese sind für eine schnelle Immunatwort, also für eine Immunität verantwortlich.
Es wird empfohlen zunächst den zyklischen Verlauf der Trypanosomen-Konzentration zu beschreiben und aus dem Vortext lässt sich schließen, dass die beiden Kurven die Konzentrationen unterschiedlicher Antikörper darstellen. Beschreibung: Die Trypanosomen-Konzentration startet bei einem sehr geringen Anfangswert und steigt nach einer kurzen "Anlaufsphase" bis zum zweiten Tag nach der Infektion nahezu linear. Die Kurve wird daraufhin flacher, bis sie ca. am dritten Tag ein Maximum erreicht. Die anschließend sinkende Trypanosomen-Konzentration erreicht am ca. achten Tag ein Minimum, liegt aber dennoch deutlich über dem Nullwert der Trypanosomen-Konzentration im Blut. Dieser Kurvenverlauf wiederholt sich. Erklärung: Während der ersten beiden Tage nach der Infektion findet eine ungestörte Zellteilung der Trypanosomen statt, die den anfänglichen linearen Anstieg erklären. Infolge der Dauer der Erkennungs- und Differenzierungsphase im Zuge der humoralen Immunantwort sind die Plasmazellen erst ab dem zweiten Tag verfügbar, die für die Bildung spezifischer Antikörper gegen die zu dieser Zeit die Zelloberfläche bedeckende VSG-Variante zuständig sind. Die Konzentration dieser Antikörper im Blut steigt vom zweiten Tag linear an, weswegen der Anstieg der Trypanosomen-Konzentration im Blut durch die Bildung von Antigen-Antikörper-Komplexen langsamer wird. Durch die zunehmende Antikörper-Konzentration im Blut sinkt die Trypanosomen-Konzentration ab dem dritten Tag bis auf ein Minimum ab. Trotz gleichbleibender Antikörperproduktion werden jedoch nicht alle Trypanosomen abgetötet, sondern deren Konzentration steigt sogar wieder linear an. Daraus folgt, dass die vorhandenen Antikörper wirkungslos geworden sind, da einige Trypanosomen eine neue Variante ihres Oberflächenproteins gebildet haben, an die die bestehenden Antikörper nun nicht mehr binden können. Gleichzeitig sind die Proteine für das Immunsystem ein neues Antigen, gegen das nach einer erneuten Erkennungs- und Differenzierungsphase wieder spezifische Antikörper durch neue Plasmazellen gebildet werden. Die folgende Wirkungsphase bewirkt eine erneute Senkung der Trypanosomen-Konzentration im Blut. Erklärung, weshalb keine Immunität entsteht:
Es entstehen immer wieder Trypanosomen mit neuen VSG-Varianten, weswegen die noch über viele Tage vorhandenen Antikörper und die gebildeten B-und T-Helfer-Gedächtniszellen unwirksam sind. Diese sind für eine schnelle Immunatwort, also für eine Immunität verantwortlich.
2
Nennung der Eigenschaften einer möglichst wirksamen Pferdedecke:
Schwarz-weiß gestreift; schmale, vertikale Streifen Begründung der Wirksamkeit:
Schwarz-weiß gestreift; schmale, vertikale Streifen Begründung der Wirksamkeit:
- Aus den Versuchsergebnissen in Abb. 3 A lässt sich entnehmen, dass in einem Zeitraum von drei Wochen bis zu 14-mal mehr Stechinsekten auf einfarbig bemalten Pferdeattrapen landeten als auf schwarz-weiß gestreiften Pferdeattrappen. Die Anzahl gelandeter Stechinsekten variierte allerdings auch je nach Farbe: Schwarze Attrappen zogen die meisten Tiere an, weiße Attrappen am wenigsten.
- Aus dem Versuch mit Testtafeln in Abb. 3 B lässt sich entehmen, dass die Landehäufigkeit zum einen von der Streifenbreite, zum anderen von der Ausrichtung abhängt. Bei sehr schmalen Streifen spielt die Ausrichtung allerdings kaum eine Rolle. Der Kurvenverlauf zeigt, dass die Anzahl gelandeter Tiere mit zunehmender Streifenbreite bis auf ein Maximum anstieg. Dabei landeten stets mehr Stechinsekten auf Testtafeln mit horizontalen Streifen und die wenigsten Stechinsekten (ca. 50) auf vertikal gestreiften Teststreifen mit den schmalsten Streifen (
5 cm).
3.1
Erklärung der Musterung des Steppenzebras:
Bei einer Population von Vorfahren der Steppenzebras, die vor ca. 2 - 1,6 Millionen Jahre in Afrika lebte, wiesen die Individuen aufgrund von Mutation und Rekombination (Neukombination des Erbguts bei der sexuellen Fortpflanzung) unterschiedliche phänotypische Fellfarben und Musterungen auf (Variabilität innerhalb einer Population). Durch Einwanderung in das Verbreitungsgebiet der Tsetseflieger oder durch Ausbreitung der Tesetsefliege in das Verbreitungsgebiet der Vorfahren (bedingt durch Umweltveränderungen) kam es zum Selektionsvorteil von Tieren mit schmalen, vertikalen Streifen. Diese konnten die verfügbaren Ressourcen im Verbreitungsgebiet ohne Beeinträchtigung nutzen, da sie von den Insekten schlechter erkannt und deswegen kaum gestochen wurden (Vergleich Abb. 3). Durch eine geringe intraspezifische Konkurrenz und die Erschließung neuer Ressourcen kam es bei diesen Individuen zu einer höheren reproduktiven Fitness. Daraus folgte ein höherer Fortpflanzungserfolg, durch den von Generation zu Generation die Häufigkeit derjenigen Allele, die für die Ausprägung schmaler, vertikaler Streifenmuster codieren (transformierende Selektion), im Genpool der Population stieg. So verbreiteten sich die Steppenzebras über weite Teile des (v.a. östlichen) Verbreitungsgebiets der Tsetsefliege.
Bei einer Population von Vorfahren der Steppenzebras, die vor ca. 2 - 1,6 Millionen Jahre in Afrika lebte, wiesen die Individuen aufgrund von Mutation und Rekombination (Neukombination des Erbguts bei der sexuellen Fortpflanzung) unterschiedliche phänotypische Fellfarben und Musterungen auf (Variabilität innerhalb einer Population). Durch Einwanderung in das Verbreitungsgebiet der Tsetseflieger oder durch Ausbreitung der Tesetsefliege in das Verbreitungsgebiet der Vorfahren (bedingt durch Umweltveränderungen) kam es zum Selektionsvorteil von Tieren mit schmalen, vertikalen Streifen. Diese konnten die verfügbaren Ressourcen im Verbreitungsgebiet ohne Beeinträchtigung nutzen, da sie von den Insekten schlechter erkannt und deswegen kaum gestochen wurden (Vergleich Abb. 3). Durch eine geringe intraspezifische Konkurrenz und die Erschließung neuer Ressourcen kam es bei diesen Individuen zu einer höheren reproduktiven Fitness. Daraus folgte ein höherer Fortpflanzungserfolg, durch den von Generation zu Generation die Häufigkeit derjenigen Allele, die für die Ausprägung schmaler, vertikaler Streifenmuster codieren (transformierende Selektion), im Genpool der Population stieg. So verbreiteten sich die Steppenzebras über weite Teile des (v.a. östlichen) Verbreitungsgebiets der Tsetsefliege.
3.2
Erläuterung der Merkmalsherkunft:
Der Stammbaum der Pferdeartigen zeigt, dass bereits der gemeinsame Vorfahre von Quagga, Berg-, Grevy- und Steppenzebra vor 1,6 Mio. Jahren komplett gestreift war. Daraus lässt sich schließen, dass dieses Merkmal ein ursprüngliches, also plesiomorphes Merkmal sein muss. Bei einem gemeinsamen Vorfahren mit fehlender Rückenstreifung müsste angenommen werden, dass das Merkmal der vollständigen Streifung innerhalb dieser monophyletischen Gruppe mehrmals (mind. dreimal) unabhängig voneinander enstanden wäre (Abb. A). Neben der Unwahrscheinlichkeit, widerspricht dies außerdem dem Prinzip der sparsamsten Erklärung (Parsimonie-Prinzip), weswegen es sich bei der fehlenden Rückenstreifung des Quaggas höchstwahrscheinlich um ein abgeleitetes (apomorphes) Merkmal handelt (Abb. B).
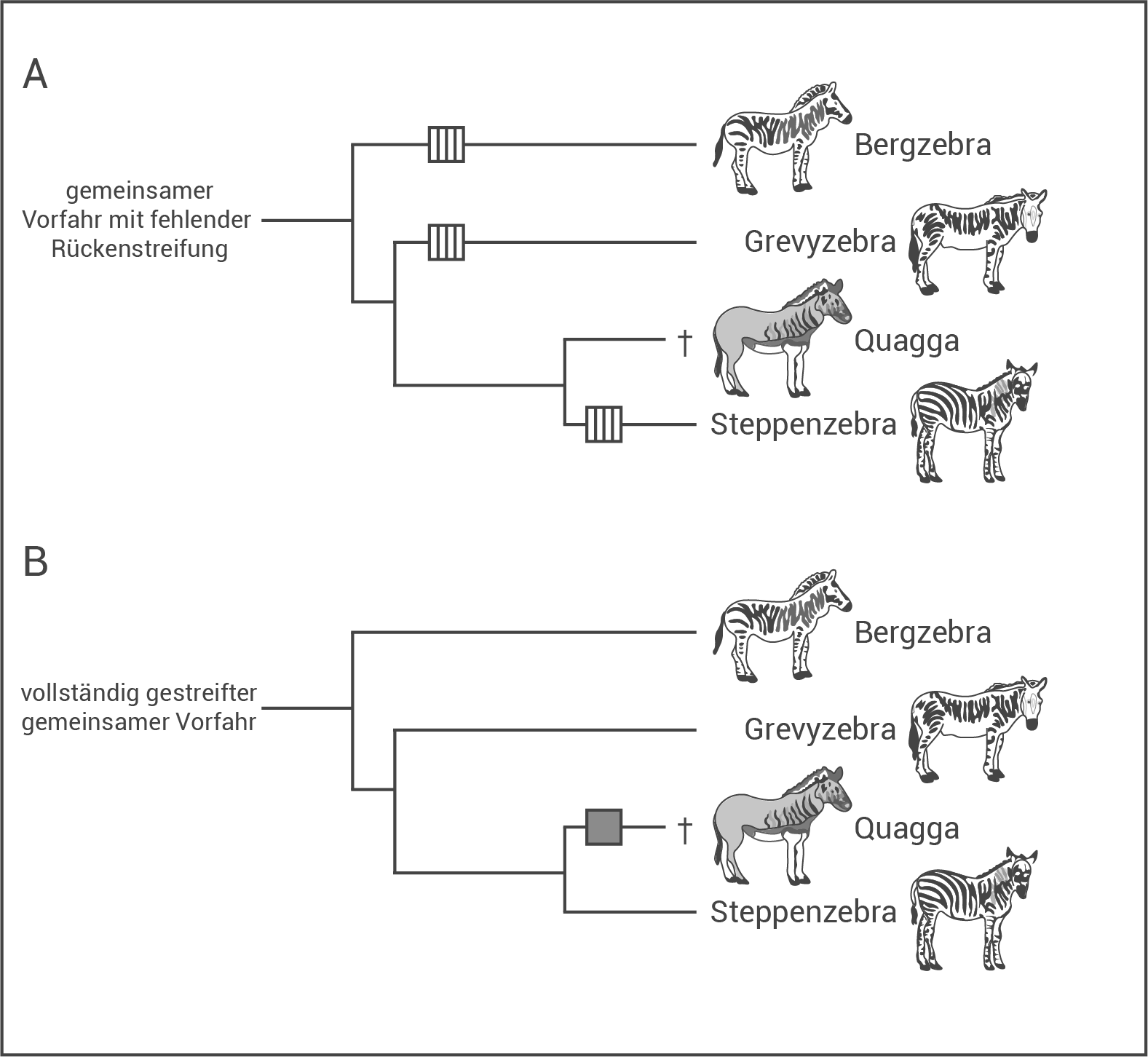 Mögliche Erklärung: Um die weitgehend fehlende Musterung des Quaggas zu erklären wird Abb. 4 betrachtet. Aus dieser lässt sich erkennen, dass im Verbreitungsgebiet der Quaggas (äußerster Süden des afrikanischen Kontinents) keine Tsetsfliegen vorkommen und die Streifung (als Schutz vor den Stechinsekten) in diesem Gebiet keinen Selektionsvorteil brachte. Möglicherweise war eine kontrastreiche, auffällige Streifung der direkten Quagga-Vorfahren hier sogar eher ein Selektionsnachteil. Eine viel größere Rolle spielten vermutlich andere Selektionsfaktoren, wie z.B. Fressfeinde, welche langfristig zu einer besseren Tarnung, einer Reduktion des Streifenmusters (Rücken und Beine) und einer an die Umgebung angepassten Fellfarbe (vermutlich braun) führten.
Mögliche Erklärung: Um die weitgehend fehlende Musterung des Quaggas zu erklären wird Abb. 4 betrachtet. Aus dieser lässt sich erkennen, dass im Verbreitungsgebiet der Quaggas (äußerster Süden des afrikanischen Kontinents) keine Tsetsfliegen vorkommen und die Streifung (als Schutz vor den Stechinsekten) in diesem Gebiet keinen Selektionsvorteil brachte. Möglicherweise war eine kontrastreiche, auffällige Streifung der direkten Quagga-Vorfahren hier sogar eher ein Selektionsnachteil. Eine viel größere Rolle spielten vermutlich andere Selektionsfaktoren, wie z.B. Fressfeinde, welche langfristig zu einer besseren Tarnung, einer Reduktion des Streifenmusters (Rücken und Beine) und einer an die Umgebung angepassten Fellfarbe (vermutlich braun) führten.
Der Stammbaum der Pferdeartigen zeigt, dass bereits der gemeinsame Vorfahre von Quagga, Berg-, Grevy- und Steppenzebra vor 1,6 Mio. Jahren komplett gestreift war. Daraus lässt sich schließen, dass dieses Merkmal ein ursprüngliches, also plesiomorphes Merkmal sein muss. Bei einem gemeinsamen Vorfahren mit fehlender Rückenstreifung müsste angenommen werden, dass das Merkmal der vollständigen Streifung innerhalb dieser monophyletischen Gruppe mehrmals (mind. dreimal) unabhängig voneinander enstanden wäre (Abb. A). Neben der Unwahrscheinlichkeit, widerspricht dies außerdem dem Prinzip der sparsamsten Erklärung (Parsimonie-Prinzip), weswegen es sich bei der fehlenden Rückenstreifung des Quaggas höchstwahrscheinlich um ein abgeleitetes (apomorphes) Merkmal handelt (Abb. B).

(Abbildungen nicht verlangt; dienen zur Veranschaulichung)
3.3
Beschreibung eines molekularbiologischen Verfahrens (nur ein Verfahren erforderlich):
Mögliche Antworten sind molekularbiologische Verfahren auf der Ebene der Nukleinsäuren (z.B. DNA-Hybridisierungstest oder DNA-Sequenzanalyse) oder auch auf der Ebene der Proteine (z.B. Serum-Präzipitin-Test oder Aminosäuresequenzanalyse wichtiger Proteine). Beschreibung des DNA-Hybridisierungstests (vereinfacht):
DNA-Hybridisierungstest:
Aus Abb. 5 lässt sich entnehmen, dass der Afrikanische Wildesel mit dem Hausesel näher verwandt ist als mit dem Steppenzebra: Erst vor ca. 400 000 Jahren haben sich die Entwicklungslinien der beiden Eselarten aufgetrennt, jedoch haben alle drei Arten einen gemeinsamen Vorfahren, der vor über 2 Millionen Jahren lebte. Je länger sich eine Art getrennt von den anderen entwickelte, desto mehr Mutationen manifestierten sich auf der DNA. Daraus folgt eine unterschiedliche Basensequenz. Somit kann gesagt werden, dass es in Hybrid-Doppelsträngen von Afrikanischem Wildesel und Hausesel zu mehr komplementären Basenpaarungen und Wasserstoffbrückenbindungen kommt als in Hybrid-Doppelsträngen von Afrikanischem Wildesel und Steppenzebra. Der Schmelzpunkt der Hybrid-DNA "Afrikanischer Wildesel/Hausesel" müsste deswegen näher am Schmelzpunkt der artreinen DNA des Afrikanischen Wildesels sein als der Schmelzpunkt der Hybrid-DNA "Afrikanischer Wildesel/Steppenzebra". Serum-Präzipitin-Test:
Der Stammbaum in Abb. 5 zeigt, dass sich die Entwicklungslinien der beiden Eselarten erst vor ca. 400 000 Jahren aufgetrennt haben. Der gemeinsame Vorfahre aller drei Arten lebte jedoch bereits vor über 2 Millionen Jahren. Durch Mutationen in einer Entwicklungslinie ist die Basensequenz und damit die Proteinausstattung umso unterschiedlicher, je weiter die Artaufspaltung zurückliegt. Der Afrikanische Wildesel und der Hausesel sind sich somit genetisch ähnlicher als Afrikanischer Wildesel mit Steppenzebra. Auch Gene, die Serumproteine codieren, sind davon betroffen. Daraus folgt, dass Proteine (=Antigene) im Blutserum des Afrikanischen Wildesels und des Hausesels einander ähnlicher sind als die Proteine von Afrikanischem Wildesel/Hausesel und Steppenzebra. Beim Präzipitin-Test lässt sich deswegen eine stärkere Ausfällung bei der Mischung des Testserums mit dem Blutserums des Hausesels erwarten als bei der Mischung des Testserums mit dem Blutserums des Steppenzebras. Die nähere Verwandtschaft zwischen Afrikanischem Wildesel und Hausesel im Vergleich zum Steppenzebra lässt sich hiermit bestätigen.
Mögliche Antworten sind molekularbiologische Verfahren auf der Ebene der Nukleinsäuren (z.B. DNA-Hybridisierungstest oder DNA-Sequenzanalyse) oder auch auf der Ebene der Proteine (z.B. Serum-Präzipitin-Test oder Aminosäuresequenzanalyse wichtiger Proteine). Beschreibung des DNA-Hybridisierungstests (vereinfacht):
- Aus den Zellen der drei zu vergleichenden Arten wird DNA isoliert.
- Durch Spaltung der DNA-Doppelstränge in DNA-Einzelstränge wird eine charakteristische Viskositätsänderung der Lösung bewirkt. Diese wird gemessen, womit anschließend der Schmelzpunkt der artreinen DNA des Afrikanischen Wildesels bestimmt wird.
- Die isolierte DNA (des zu untersuchenden Tiers) und die DNA des Afrikanischen Wildesels werden in einem Versuchsansatz gemischt. Dieser Ansatz wird auf ca. 95 °C erhitzt, sodass sich die DNA-Doppelstränge in Einzelstränge teilen (Denaturierung).
- Beim Abkühlen werden Hybrid-Doppelstränge der DNA der beiden Arten gebildet.
- Nun wird der Schmelzpunkt der Hybrid-Doppelstränge bestimmt. Dabei gilt, je näher die beiden Arten miteinander verwandt sind, desto mehr komplementäre Basenpaarungen bilden sich über Wasserstoffbrückenbindungen aus und desto näher liegt der Schmelzpunkt der Hybrid-Doppelstränge an dem der artreinen DNA des Wildesels.
- Einem Afrikanischen Wildesel wird Blut entnommen, welches anschließend isoliert wird.
- Anschließend wird das Serum einem möglichst weit entferntem Testtier (z.B. Kaninchen) injiziert. Daraufhin erfolgt eine aktive Immunantwort gegen die fremden Blutserumproteine.
- Zur Gewinnung des Blutserums wird dem Testtier nach einigen Wochen Blut entnommen, welches spezifische Antikörper gegen Blutserumeiweiße des Afrikanischen Wildesels enthält.
- Das Testserum wird mit dem Blutserum des Afrikanischen Wildesels vermischt (Eichung des Tests), woraufhin die im Testserum enthaltenen Antikörper mit den Serumproteinen (Antigene) des Wildesels zu Antigen-Antikörper-Komplexen verklumpen (präzipitieren). Dabei wird der maximale Verklumpungsgrad erreicht, welcher als 100 %-Marke definiert wird.
- Zuletzt werden die Blutseren der Tierarten, deren Verwandtschaftsgrad zum Wildesel gemessen werden soll, mit dem Testserum vermischt (hier: Hausesel und Steppenzebra). Je stärker die Verklumpung (Präzipitation) ausfällt, desto ähnlicher sind die Blutserumproteine und desto größer die Verwandtschaft.
DNA-Hybridisierungstest:
Aus Abb. 5 lässt sich entnehmen, dass der Afrikanische Wildesel mit dem Hausesel näher verwandt ist als mit dem Steppenzebra: Erst vor ca. 400 000 Jahren haben sich die Entwicklungslinien der beiden Eselarten aufgetrennt, jedoch haben alle drei Arten einen gemeinsamen Vorfahren, der vor über 2 Millionen Jahren lebte. Je länger sich eine Art getrennt von den anderen entwickelte, desto mehr Mutationen manifestierten sich auf der DNA. Daraus folgt eine unterschiedliche Basensequenz. Somit kann gesagt werden, dass es in Hybrid-Doppelsträngen von Afrikanischem Wildesel und Hausesel zu mehr komplementären Basenpaarungen und Wasserstoffbrückenbindungen kommt als in Hybrid-Doppelsträngen von Afrikanischem Wildesel und Steppenzebra. Der Schmelzpunkt der Hybrid-DNA "Afrikanischer Wildesel/Hausesel" müsste deswegen näher am Schmelzpunkt der artreinen DNA des Afrikanischen Wildesels sein als der Schmelzpunkt der Hybrid-DNA "Afrikanischer Wildesel/Steppenzebra". Serum-Präzipitin-Test:
Der Stammbaum in Abb. 5 zeigt, dass sich die Entwicklungslinien der beiden Eselarten erst vor ca. 400 000 Jahren aufgetrennt haben. Der gemeinsame Vorfahre aller drei Arten lebte jedoch bereits vor über 2 Millionen Jahren. Durch Mutationen in einer Entwicklungslinie ist die Basensequenz und damit die Proteinausstattung umso unterschiedlicher, je weiter die Artaufspaltung zurückliegt. Der Afrikanische Wildesel und der Hausesel sind sich somit genetisch ähnlicher als Afrikanischer Wildesel mit Steppenzebra. Auch Gene, die Serumproteine codieren, sind davon betroffen. Daraus folgt, dass Proteine (=Antigene) im Blutserum des Afrikanischen Wildesels und des Hausesels einander ähnlicher sind als die Proteine von Afrikanischem Wildesel/Hausesel und Steppenzebra. Beim Präzipitin-Test lässt sich deswegen eine stärkere Ausfällung bei der Mischung des Testserums mit dem Blutserums des Hausesels erwarten als bei der Mischung des Testserums mit dem Blutserums des Steppenzebras. Die nähere Verwandtschaft zwischen Afrikanischem Wildesel und Hausesel im Vergleich zum Steppenzebra lässt sich hiermit bestätigen.