Aufgabe 3 – Malaria, Immunbiologie
Malaria ist die häufigste Infektionskrankheit der Tropen und Subtropen. Malaria-Erkrankte zeigen grippeähnliche Symptome wie hohes Fieber, Schüttelfrost, Kopf- und Gliederschmerzen. Erreger der Malaria sind einzellige eukaryotische Parasiten, die Plasmodien. Diese werden durch den Stich einer infizierten weiblichen Anopheles-Mücke (siehe Abb. 1) auf den Menschen übertragen. Im Menschen dringen die Plasmodien in die roten Blutzellen (Erythrozyten) ein und vermehren sich darin stark. Nach einer gewissen Zeit platzen befallene Erythrozyten und geben zahlreiche Erreger zusammen mit deren Stoffwechselprodukten ins Blutplasma frei. Diese Erreger können daraufhin weitere Erythrozyten befallen.

Abb. 1: Anopheles-Mücke
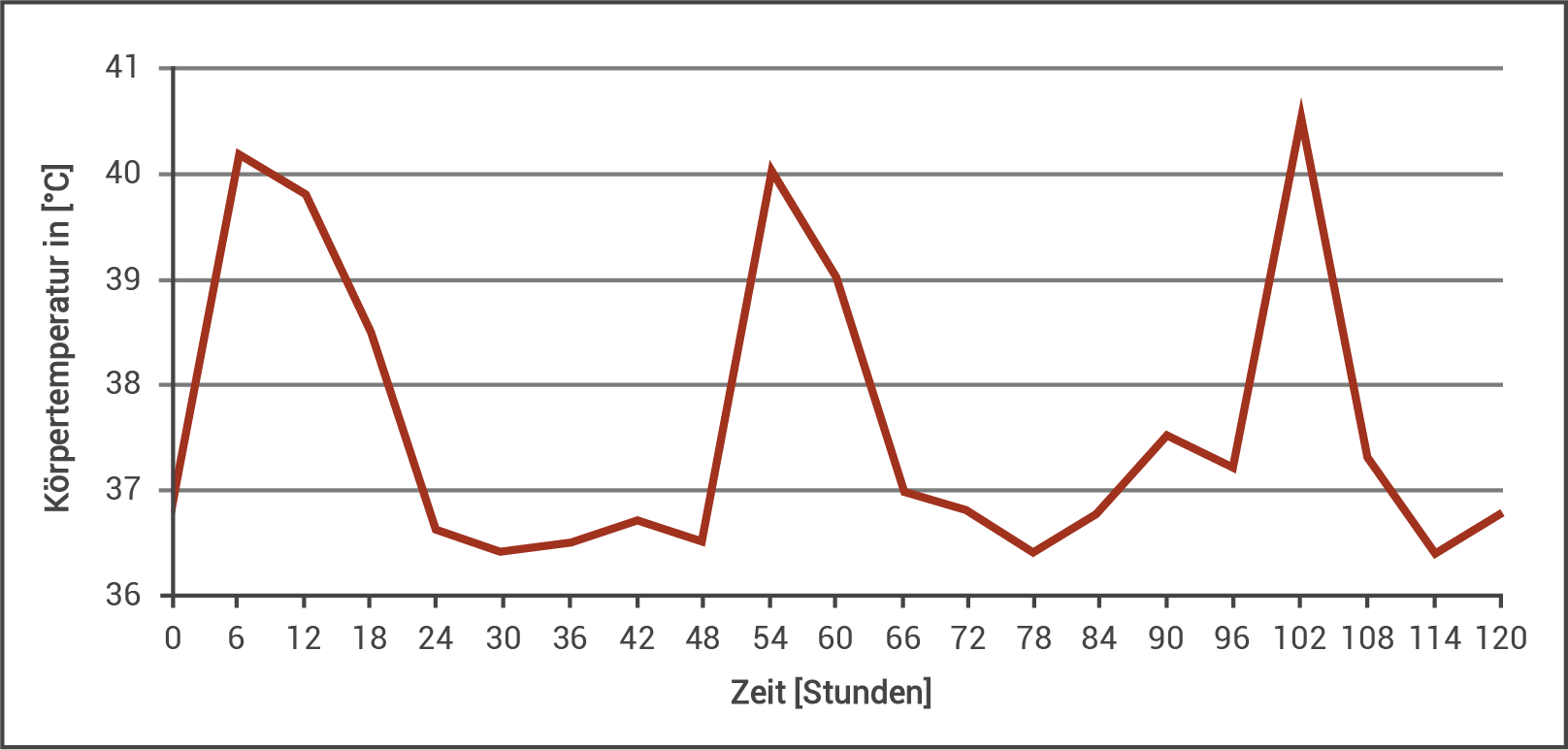
Abb. 2: Zeitlicher Verlauf der Körpertemperatur eines Malaria-Erkrankten
1.1
Beschreibe den in Abbildung 2 gezeigten Verlauf der Körpertemperatur eines Malaria-Erkrankten und gib eine mögliche Erklärung für diesen Verlauf. Erkläre die biologische Bedeutung einer erhöhten Körpertemperatur im Rahmen einer Infektion.
3 VP
1.2
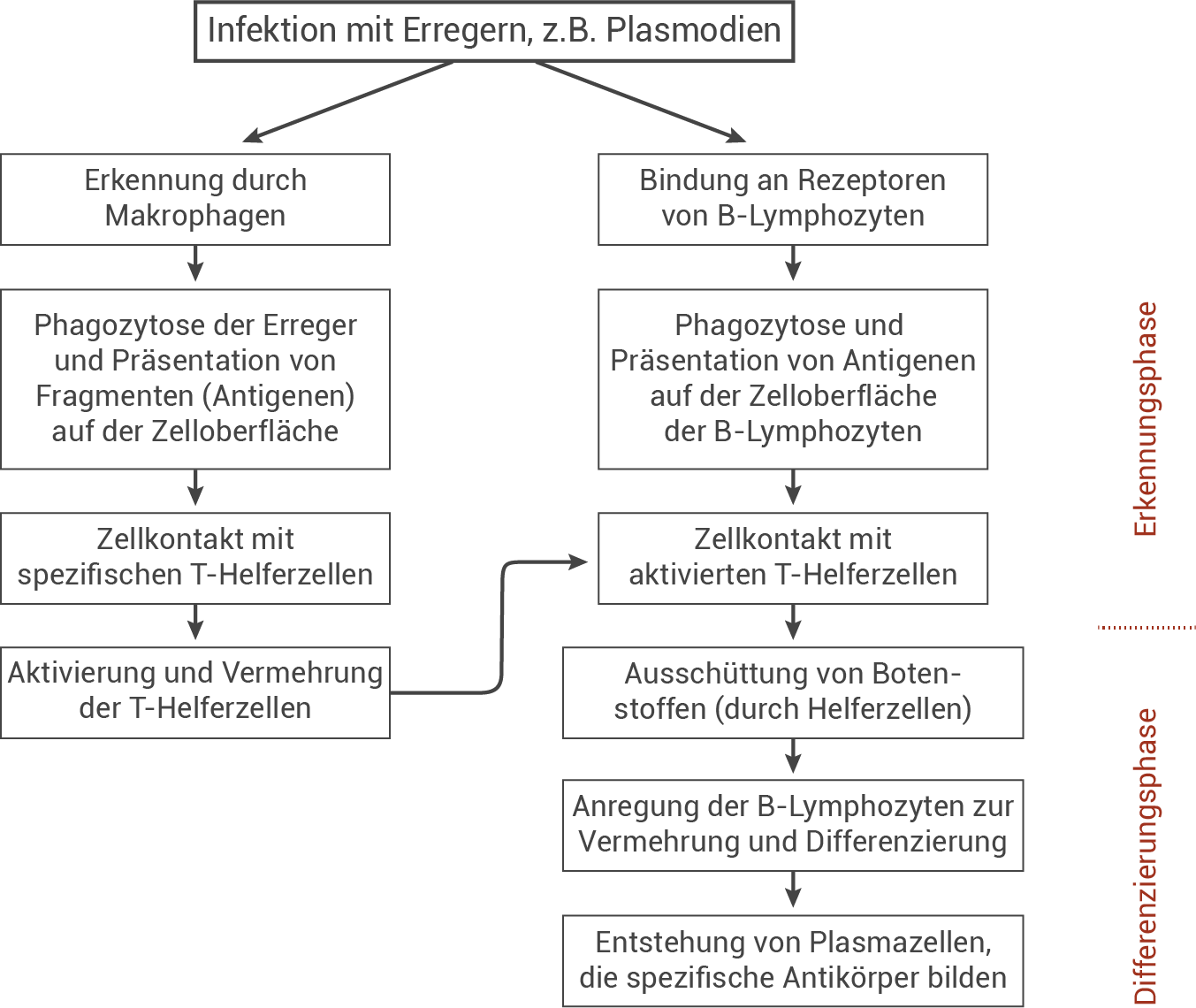
Stelle die Vorgänge, die nach einer Infektion zur Bildung spezifischer Antikörper führen, in Form eines Verlaufsschemas dar.
Die einzelligen Plasmodien durchlaufen einen Entwicklungszyklus mit einem Wirtswechsel zwischen Mensch und Anopheles-Mücke. In menschlichen Erythrozyten vermehren sich die Erreger ungeschlechtlich, während sie sich in der Mücke geschlechtlich fortpflanzen.
3 VP
2
Erläutere jeweils einen Vorteil der ungeschlechtlichen Vermehrung und der geschlechtlichen Fortpflanzung.
2 VP
In Malaria-Gebieten hat man festgestellt, dass dort eine genetisch bedingte Erkrankung, die Sichelzellkrankheit, gehäuft auftritt. Ursache hierfür ist eine veränderte Form des in Erythrozyten vorkommenden Proteins Hämoglobin, das bei gesunden Menschen ausschließlich in Form von Hämoglobin A (HbA) vorliegt, während bei der Sichelzellkrankheit das Hämoglobin S (HbS) gebildet wird. Bei Menschen, die das HbS-Allel homozygot (reinerbig) tragen, nehmen die Erythrozyten bei Sauerstoffmangel eine sichelförmige Struktur an (siehe Abb. 3) und führen so zur Verstopfung von Blutgefäßen. Heterozygote (mischerbige) Träger, die neben HbS ausreichend HbA bilden können, zeigen nur leichte Krankheitssymptome. In Abbildung 4 sind DNA-Ausschnitte der beiden Hämoglobin-Allele dargestellt.
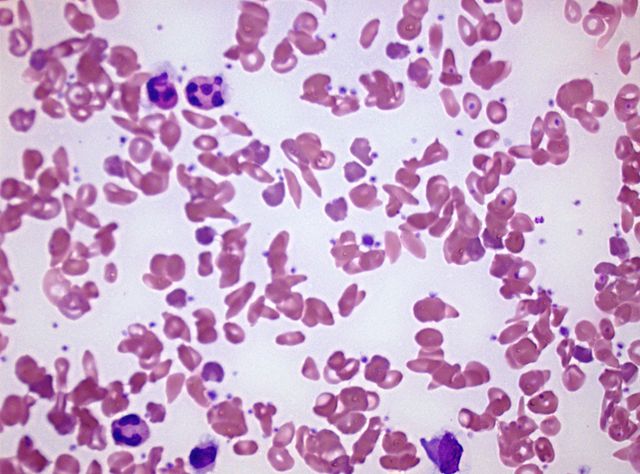
Abb. 3: Normale und sichelförmige Erythrozyten

Abb. 4: Einander entsprechende DNA-Ausschnitte des HbA- und des HbS-Allels
3
Ermittle mit Hilfe der Codesonne (siehe Anlage) die Aminosäuresequenzen zu den in Abbildung 4 dargestellten DNA-Ausschnitten der beiden Hämoglobin-Allele. Gib eine mögliche Erklärung für die veränderte Raumstruktur von HbS.
Zur Diagnose der Sichelzellkrankheit dient eine molekulargenetische Untersuchung. Zuerst wird DNA isoliert und der entsprechende Bereich mit Hilfe einer Polymerasekettenreaktion (PCR) vervielfältigt. Diese vervielfältigten DNA-Abschnitte werden dann mit dem Restriktionsenzym Mstll geschnitten und anschließend durch eine Gelelektrophorese aufgetrennt (siehe Abb. 5 und Abb. 6).
2 VP

Abb. 5: Erkennungssequenz und Schnittstelle von Mstll
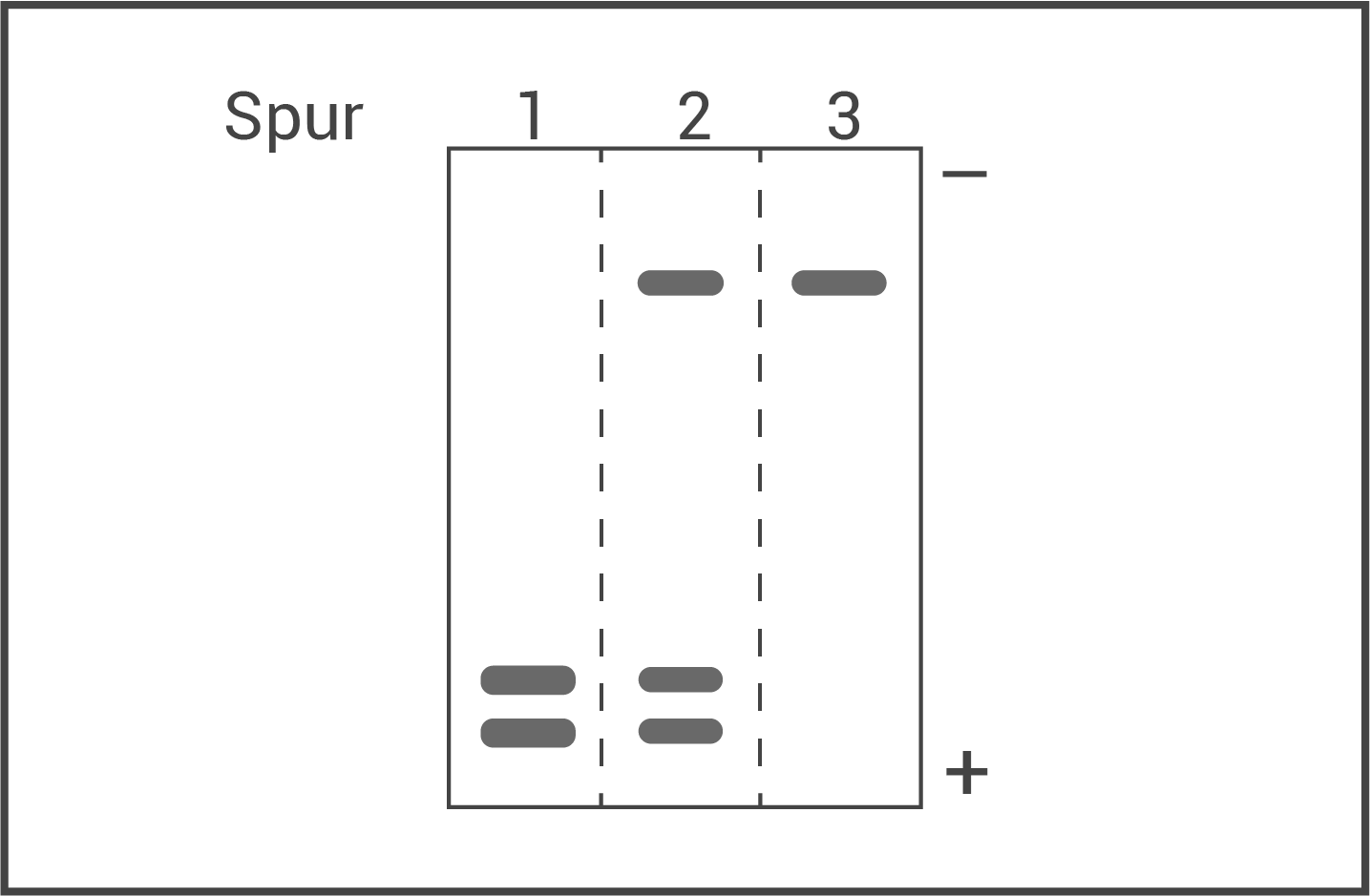
Abb. 6: Ergebnis der Gelelektrophorese
4
Erläutere mit Hilfe der Abbildungen 4 und 5 das Ergebnis der Gelelektrophorese in Abbildung 6. Ordne die Spuren 1, 2 und 3 begründet einem gesunden Menschen, einem homozygoten und einem heterozygoten Träger des HbS-Allels zu.
Ein neuer Test mit dem Namen HemoTypeSC™ ist bei der Erkennung der Sichelzellkrankheit sehr erfolgreich. Für diesen Test entnimmt man einen Tropfen Blut und gibt diesen in eine definierte Menge destillierten Wassers. Anschließend wird der untere Teil eines Teststreifens in diese Testflüssigkeit eingetaucht. Nach zehn Minuten kann am Bandenmuster des Teststreifens abgelesen werden, ob das Blut HbA und/oder HbS enthält (siehe Abb. 7).
4 VP
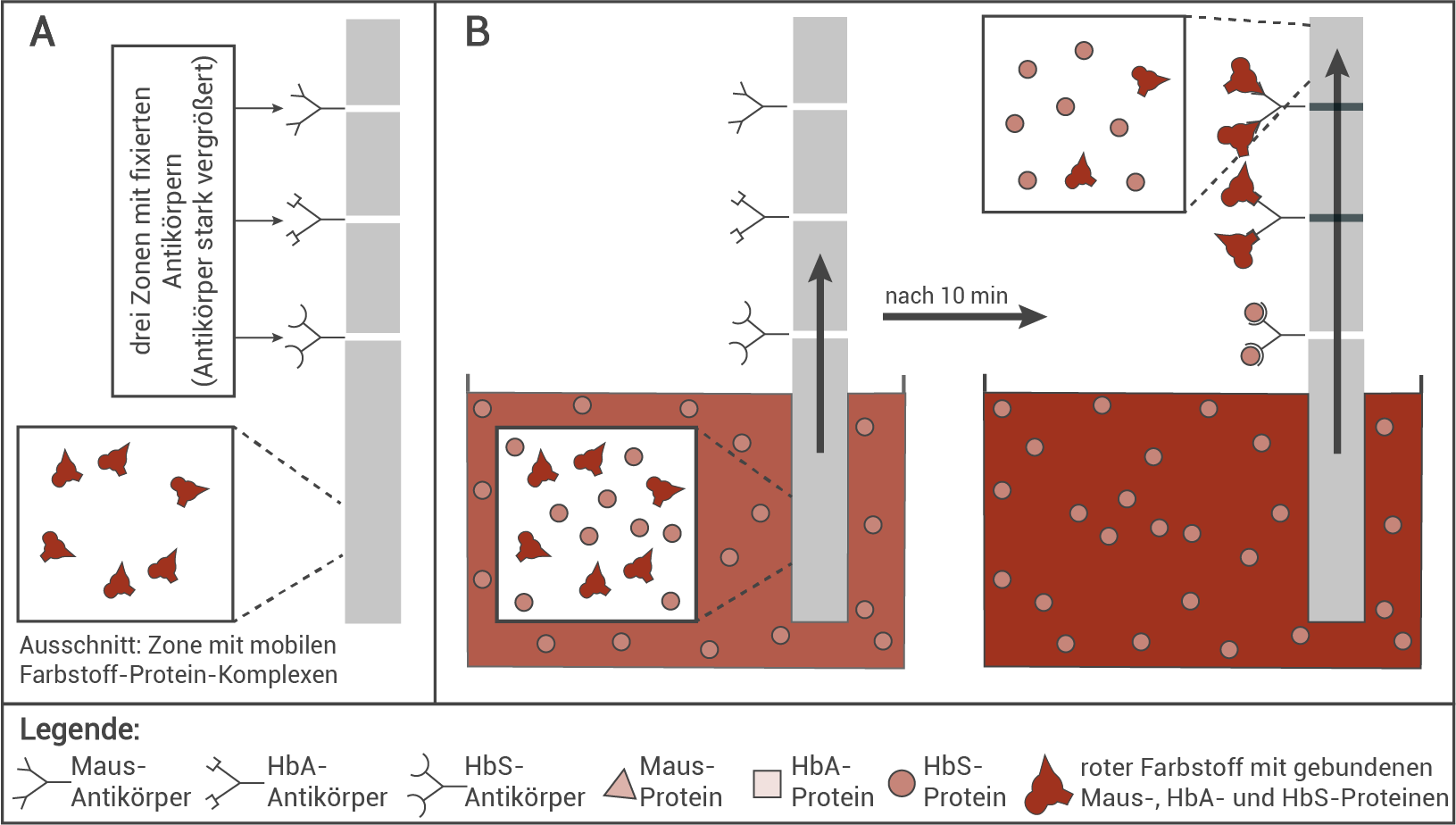
Abb. 7: (A) Aufbau des HemoTypeSC ™ -Teststreifens und (B) Ablauf des Tests, stark schematisiert.
5.1
Erkläre, warum der Teststreifen in ein Gemisch aus Blut und destilliertem Wasser und nicht direkt ins Blut eingetaucht wird. Erläutere mit Hilfe von Abbildung 7 die Funktionsweise des Teststreifens. Gehe dabei auch auf die Bedeutung der mobilen Farbstoff-Protein-Komplexe sowie der fixierten Maus-Antikörper ein.
4 VP
5.2
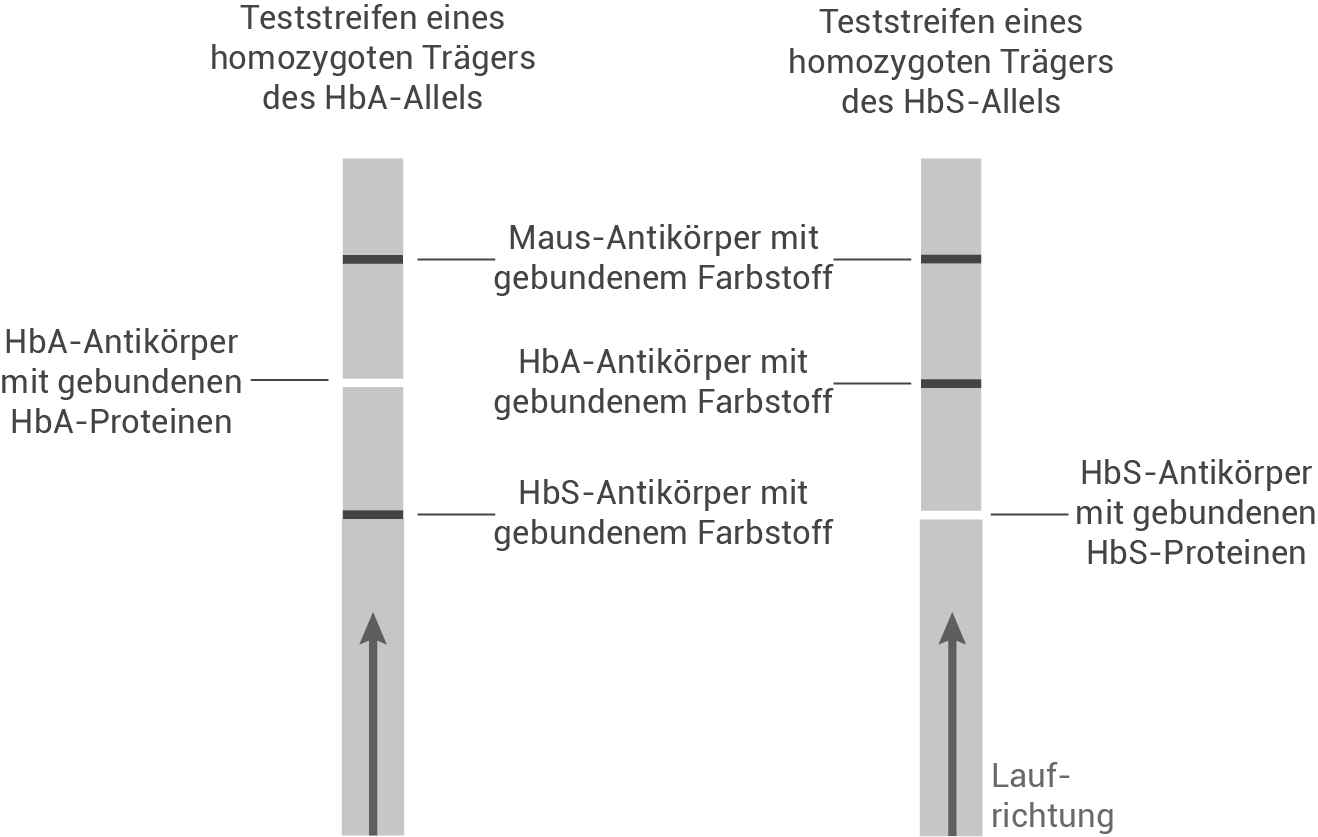
Zeichne einen Teststreifen, der das Bandenmuster für einen homozygoten Träger des HbA-Allels zeigt, und daneben einen Teststreifen, der das Bandenmuster für einen homozygoten Träger des HbS-Allels zeigt.
Bildnachweise [nach oben]
2 VP
20 VP
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Beschreibung des gezeigten Verlaufs:
In Abb. 2 sind die zyklischen Veränderungen der Körpertemperatur (in °C) eines Malaria-Erkrankten zu sehen, die sich über einen Zeitraum von fünf Tagen erstrecken. Alle Stunden erfolgt ein Fieberschub. Innerhalb eines Zyklus steigt hierbei die Körpertemperatur in den ersten sechs Stunden von ca.
Stunden erfolgt ein Fieberschub. Innerhalb eines Zyklus steigt hierbei die Körpertemperatur in den ersten sechs Stunden von ca.  auf
auf  an und sinkt anschließend innerhalb von
an und sinkt anschließend innerhalb von  bis
bis  Stunden wieder auf die Normaltemperatur. Zwischen den Fieberschüben sind nahezu fieberfreie Tage zu erkennen.
Mögliche Erklärung:
Stunden wieder auf die Normaltemperatur. Zwischen den Fieberschüben sind nahezu fieberfreie Tage zu erkennen.
Mögliche Erklärung:
Es erfolgt ein zyklisches (zeitgleiches) Platzen der befallenen Erythrozyten wodurch es im Blut zu einem schnellen Anstieg der Erreger (und damit zur Zugänglichkeit von deren Oberflächenantigenen) und deren möglicherweise giftigen Stoffwechselprodukte kommt. Daraufhin werden durch Botenstoffe Reaktionen des Immunsystems ausgelöst, die mit Fieberschüben verbunden sind. Diese bewirken eine erhebliche Reduktion der Erregerkonzentration im Blut des Infizierten, woraufhin das Fieber zurückgeht. Ein neuer Zyklus wird ausgelöst wenn es einigen Erregern gelingt, neue Erythrozyten zu infizieren. Biologische Bedeutung von erhöhter Körpertemperatur (nur eine erforderlich):
In Abb. 2 sind die zyklischen Veränderungen der Körpertemperatur (in °C) eines Malaria-Erkrankten zu sehen, die sich über einen Zeitraum von fünf Tagen erstrecken. Alle
Es erfolgt ein zyklisches (zeitgleiches) Platzen der befallenen Erythrozyten wodurch es im Blut zu einem schnellen Anstieg der Erreger (und damit zur Zugänglichkeit von deren Oberflächenantigenen) und deren möglicherweise giftigen Stoffwechselprodukte kommt. Daraufhin werden durch Botenstoffe Reaktionen des Immunsystems ausgelöst, die mit Fieberschüben verbunden sind. Diese bewirken eine erhebliche Reduktion der Erregerkonzentration im Blut des Infizierten, woraufhin das Fieber zurückgeht. Ein neuer Zyklus wird ausgelöst wenn es einigen Erregern gelingt, neue Erythrozyten zu infizieren. Biologische Bedeutung von erhöhter Körpertemperatur (nur eine erforderlich):
- Vermehrung der Erreger wird gehemmt (hier: Plasmodien)
- Schnellerer Ablauf von körpereigenen Abwehrreaktionen wie z.B. die Synthese von Antikörpern und Signalstoffen des Immunsystems (Reaktionsgeschwindigkeit-Temperatur-Regel).
1.2
Verlaufsschema:

2
Erläuterung der Vorteile:
- Ungeschlechtliche Vermehrung: In den Erythrozyten können durch einfache Zellteilungen (Mitosen) sehr schnell viele (genetisch identische) Nachkommen erzeugt werden. Wenn die Erythrozyten gleichzeitig Platzen werden dadurch sehr viele Erreger freigesetzt, die eine große Zahl weiterer Zellen befallen können bevor die Immunantwort vollständig ausgeprägt wurde.
- Geschlechtliche Fortpflanzung: Da das Erbgut unterschiedlicher Geschlechtszellen rekombiniert werden kann, ist die Entstehung neuer Phänotypen möglich, die z.B. eine höhere Varianz der Antigene (Oberflächenproteine auf der Zellmembran der Plasmodien) aufweisen. Daraus folgt ein besserer Schutz der Erreger vor der Immunantwort des Menschen, weil bei einer erneuten Infektion (wegen den unbekannten Antigenen) keine rasche sekundäre Immunreaktion erfolgen kann.
3
Ermittlung der Aminosäuresequenzen von HbA und HbS:
 Mögliche Erklärung für die veränderte Raumstruktur von HbS:
Mögliche Erklärung für die veränderte Raumstruktur von HbS:
Das HbS-Allel besitzt an dritter Stelle im dargestellten Basentriplett (an Position 2) anstatt Thymin die Base Adenin (Punktmutation). Nach Transkription und Translation wird dadurch die Primärstruktur, also die AS-Abfolge, des HbS im Vergleich zu HbA an einer Stelle verändert:
Glutaminsäure, mit einer negativ geladenen hydrophilen Seitenkette, wird durch Valin, mit einer hydrophoben Seitenkette, ersetzt. Daraus folgt eine Veränderung der Wechselwirkungen zwischen den Aminosäureresten, die für die Stabilisierung der Tertiärstruktur der Polypeptidkette verantwortlich sind. Die Raumstruktur (Konformation) des HbS verändert sich im Vergleich zu derjenigen des HbA.

Das HbS-Allel besitzt an dritter Stelle im dargestellten Basentriplett (an Position 2) anstatt Thymin die Base Adenin (Punktmutation). Nach Transkription und Translation wird dadurch die Primärstruktur, also die AS-Abfolge, des HbS im Vergleich zu HbA an einer Stelle verändert:
Glutaminsäure, mit einer negativ geladenen hydrophilen Seitenkette, wird durch Valin, mit einer hydrophoben Seitenkette, ersetzt. Daraus folgt eine Veränderung der Wechselwirkungen zwischen den Aminosäureresten, die für die Stabilisierung der Tertiärstruktur der Polypeptidkette verantwortlich sind. Die Raumstruktur (Konformation) des HbS verändert sich im Vergleich zu derjenigen des HbA.
4
Erläuterung des Ergebnisses der Gelelektrophorese:
Die Erkennungssequenz, also die Schnittstelle des Restriktionsenzyms MstII (Abb. 5) ist im gezeigten Ausschnitt (Abb. 4) gegeben, im Ausschnitt des HbS-Allels dagegen nicht.
 Durch den Basentausch wurde die Sequenz des HbS-Allels verändert und enthält keine Schnittstelle für das Restriktionsenzym MstII mehr. Die enstandenen PCR-Produkte können dadurch nicht mehr geschnitten und in der anschließenden Gelelektrophorese aufgetrennt werden. Hiermit ergibt sich für das HbS-Allel bei Restriktionsverdau mit MstII ein einziges langes Fragment. Beim HbA-Allel hingegen entstehen zwei kurze Fragmente. Je kürzer ein DNA-Fragment ist, desto schneller und weiter ist bei der Gelelektrophorese die Wanderung in einer bestimmten Zeit in Richtung des Pluspols. In Abb. 6 ist in den Spuren 2 und 3 eine Bande nahe dem Minuspol zu sehen (Ansammlung langer Fragmente mit kurzer Wanderstrecke) und in Spur 1 und 2 zwei Banden nahe dem Pluspol (Ansammlungen zweier unterschiedlicher kurzer Fragmente mit langer Wanderstrecke).
Zuordnung der Spuren:
Durch den Basentausch wurde die Sequenz des HbS-Allels verändert und enthält keine Schnittstelle für das Restriktionsenzym MstII mehr. Die enstandenen PCR-Produkte können dadurch nicht mehr geschnitten und in der anschließenden Gelelektrophorese aufgetrennt werden. Hiermit ergibt sich für das HbS-Allel bei Restriktionsverdau mit MstII ein einziges langes Fragment. Beim HbA-Allel hingegen entstehen zwei kurze Fragmente. Je kürzer ein DNA-Fragment ist, desto schneller und weiter ist bei der Gelelektrophorese die Wanderung in einer bestimmten Zeit in Richtung des Pluspols. In Abb. 6 ist in den Spuren 2 und 3 eine Bande nahe dem Minuspol zu sehen (Ansammlung langer Fragmente mit kurzer Wanderstrecke) und in Spur 1 und 2 zwei Banden nahe dem Pluspol (Ansammlungen zweier unterschiedlicher kurzer Fragmente mit langer Wanderstrecke).
Zuordnung der Spuren:
Die Erkennungssequenz, also die Schnittstelle des Restriktionsenzyms MstII (Abb. 5) ist im gezeigten Ausschnitt (Abb. 4) gegeben, im Ausschnitt des HbS-Allels dagegen nicht.

- Spur 1: gesunder Mensch
Im unteren Bereich des Gels (Pluspol) lassen sich die beiden dicken Banden zwei kurzen Fragmenten mit langer Wanderstrecke zuordnen. Daraus lässt sich schließen, dass die getestete Person zwei identische Allelen mit Restriktionsschnittstelle für MstII besitzt und daher homozygoter Träger des HbS-Allels ist. - Spur 2: heterozygoter Träger des HbS-Allels
Die obere Bande entspricht einem langen Fragment ohne Schnittstelle für MstII, deren zurückgelegte Strecke im Gel nur kurz ist. Die beiden Banden am Pluspol entsprechen zwei kurzen Fragmenten. Diese sind vermutlich durch Restriktionsverdau enstanden. Daraus folgt, dass diese Person über ein HbA-Allel (mit Restriktionsschnittstelle für MstII) und ein HbS-Allel (ohne Schnittstelle) verfügt. - Spur 3: homozygoter Träger des HbS-Allels
Im oberen Bereich des Gels ist nur eine dicke Bande vorhanden, die auf eine Person mit zwei identischen Allelen ohne Restriktionsschnittstelle hindeutet. Es sind nur (ungeschnittene) lange Fragmente mit kurzer Wanderstrecke vorhanden.
5.1
Erklärung für das Eintauchen in ein Gemisch:
Das verwendete Verfahren (Abb. 7) basiert auf einem Antikörper Test zur Erkennung von HbA- und HbS-Proteinen. Wenn ein Tropfen Blut in destilliertes Wasser gegeben wird, geraten die im Blut vorhandenen Erythrozyten in ein hypotones Medium. Aufgrund des osmotisch bedingten Wassereinstroms platzen diese daraufhin auf, wodurch das in den Zellen vorhandene Hämoglobin freigesetzt wird und durch den Teststreifen nachgewiesen werden kann. Erläuterung der Funktionsweise des Teststreifens:
Abb. B zeigt die Bindung von ausschließlich HbS-Proteinen an den fixierten HbS-Antikörpern nach Aufsteigen der Testflüssigkeit (bei Anwesenheit von HbS-Proteinen). Daraus lässt sich schließen, dass die HbS-Proteine die Farbstoffmoleküle kompetitiv verdrängen und deswegen in einer höheren Konzentration vorliegen müssen. Alternativ wäre es möglich, dass die HbS-Proteine den Teststreifen schneller durchwandern, da sie kleiner als die Farbstoffmoleküle sind. Die HbS-, HbA- und Maus-Antikörper sind auf dem Teststreifen in einem gewissen Abstand von unten nach oben und in je einem Bereich fixiert. Der untere Bereich des Testreifens weist eine Zone mit roten mobilen Farbstoffen vor, welche jeweils mit HbS-, HbA- und Maus-Protein gekoppelt sind. Durch das Eintauchen in die Blutprobe steigt die Lösung auf und die Farbstoffmoleküle und die Hb-Proteine (aus dem Blut der Testperson) wandern in die Bereiche der fixierten Antikörper. Die Hb-Proteine liegen dort in einer höheren Konzentration vor und verdrängen deshalb die Farbstoffmoleküle an den Antikörperbindestellen.
Abb. B demonstriert den Ablauf eines homozygoten Trägers des HbS-Allels. Hier befinden sich in der Testflüssigkeit nur HbS-Proteine. Diese werden von den fixierten Antikörpern gebunden, weswegen der rote Farbstoff nicht an die HbS-Antikörper binden kann. Die Bande ensteht, weil die Farbstoffmoleküle aufgrund der fehlenden HbA-Proteine im Bereich der fixierten HbA-Antikörper binden. Eine weitere Bande entsteht im Bereich der fixierten Maus-Antikörper, dabei dient die oberste als Kontrolle:
Damit der Test sicher als Nachweis funktioniert, muss die Testflüssigkeit bis in die Bereiche der für diese Proteine spezifischen, fixierten Antikörper wandern. Das kann sichergestellt werden, wenn die mobilen Farbstoff-Protein-Komplexe an die obersten Maus-Antikörper binden und somit eine rote Kontrollbande auf dem Teststreifen erzeugt wird.
Das verwendete Verfahren (Abb. 7) basiert auf einem Antikörper Test zur Erkennung von HbA- und HbS-Proteinen. Wenn ein Tropfen Blut in destilliertes Wasser gegeben wird, geraten die im Blut vorhandenen Erythrozyten in ein hypotones Medium. Aufgrund des osmotisch bedingten Wassereinstroms platzen diese daraufhin auf, wodurch das in den Zellen vorhandene Hämoglobin freigesetzt wird und durch den Teststreifen nachgewiesen werden kann. Erläuterung der Funktionsweise des Teststreifens:
Abb. B zeigt die Bindung von ausschließlich HbS-Proteinen an den fixierten HbS-Antikörpern nach Aufsteigen der Testflüssigkeit (bei Anwesenheit von HbS-Proteinen). Daraus lässt sich schließen, dass die HbS-Proteine die Farbstoffmoleküle kompetitiv verdrängen und deswegen in einer höheren Konzentration vorliegen müssen. Alternativ wäre es möglich, dass die HbS-Proteine den Teststreifen schneller durchwandern, da sie kleiner als die Farbstoffmoleküle sind. Die HbS-, HbA- und Maus-Antikörper sind auf dem Teststreifen in einem gewissen Abstand von unten nach oben und in je einem Bereich fixiert. Der untere Bereich des Testreifens weist eine Zone mit roten mobilen Farbstoffen vor, welche jeweils mit HbS-, HbA- und Maus-Protein gekoppelt sind. Durch das Eintauchen in die Blutprobe steigt die Lösung auf und die Farbstoffmoleküle und die Hb-Proteine (aus dem Blut der Testperson) wandern in die Bereiche der fixierten Antikörper. Die Hb-Proteine liegen dort in einer höheren Konzentration vor und verdrängen deshalb die Farbstoffmoleküle an den Antikörperbindestellen.
Abb. B demonstriert den Ablauf eines homozygoten Trägers des HbS-Allels. Hier befinden sich in der Testflüssigkeit nur HbS-Proteine. Diese werden von den fixierten Antikörpern gebunden, weswegen der rote Farbstoff nicht an die HbS-Antikörper binden kann. Die Bande ensteht, weil die Farbstoffmoleküle aufgrund der fehlenden HbA-Proteine im Bereich der fixierten HbA-Antikörper binden. Eine weitere Bande entsteht im Bereich der fixierten Maus-Antikörper, dabei dient die oberste als Kontrolle:
Damit der Test sicher als Nachweis funktioniert, muss die Testflüssigkeit bis in die Bereiche der für diese Proteine spezifischen, fixierten Antikörper wandern. Das kann sichergestellt werden, wenn die mobilen Farbstoff-Protein-Komplexe an die obersten Maus-Antikörper binden und somit eine rote Kontrollbande auf dem Teststreifen erzeugt wird.
5.2
Zeichnung der Teststreifen: