Aufgabe 1 – Neurobiologie, Genetik
Viele der im mittel- und südamerikanischen Regenwald lebenden Froscharten der Familie Den-drobatidae (Baumsteigerfrösche) sondern über ihre Haut giftige Alkaloide ab. Das vom Pfeilgiftfrosch Phyllobates terribilis abgegebene Alkaloid Batrachotoxin  wirkt an den Axonen seiner Fressfeinde als starkes Nervengift, Phyllobates selbst ist unempfindlich gegen
wirkt an den Axonen seiner Fressfeinde als starkes Nervengift, Phyllobates selbst ist unempfindlich gegen 
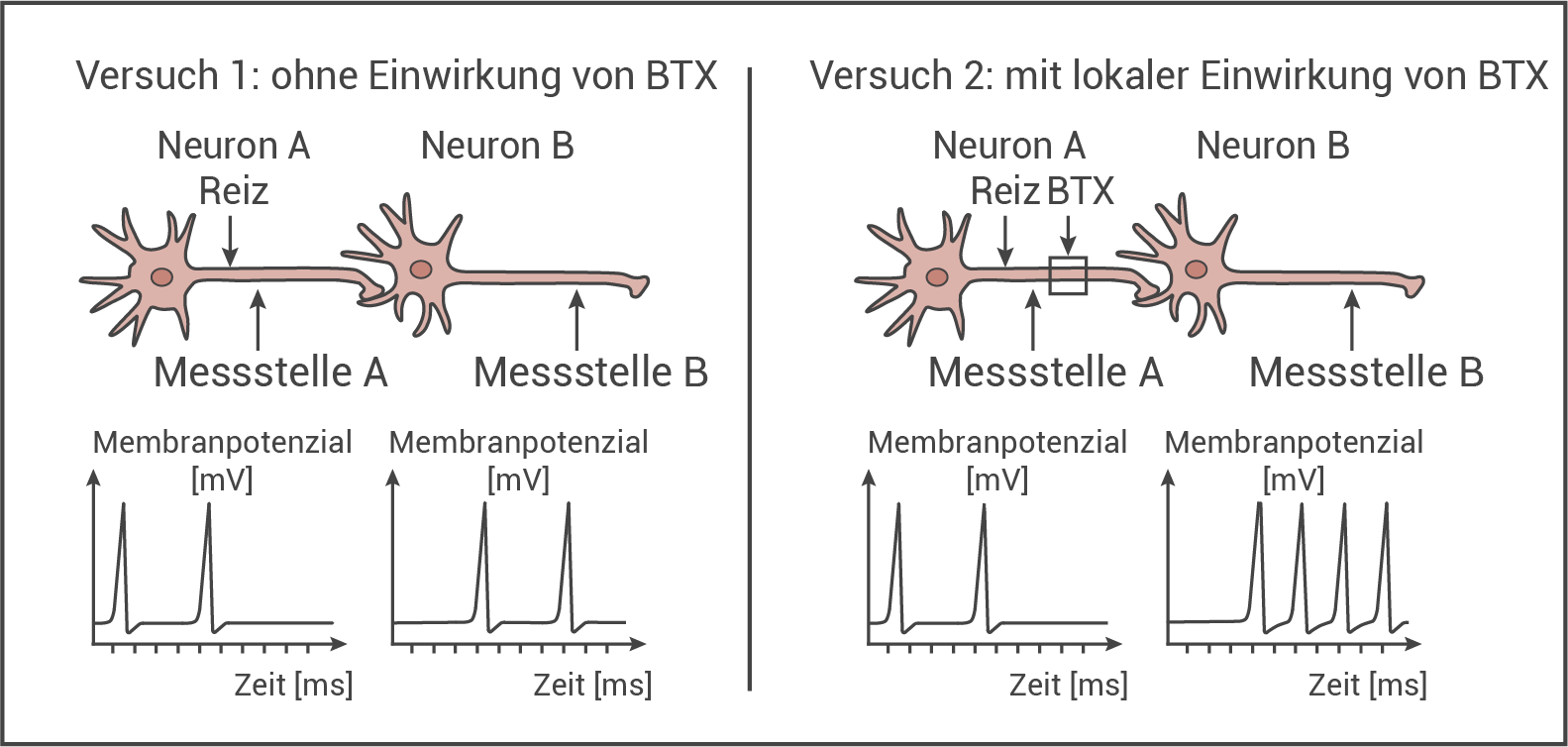
 näher zu untersuchen, wurden Neuronen von Ratten gereizt und die Erregungsleitung gemessen. Abbildung 1 zeigt den Versuchsaufbau und die Versuchsergebnisse.
näher zu untersuchen, wurden Neuronen von Ratten gereizt und die Erregungsleitung gemessen. Abbildung 1 zeigt den Versuchsaufbau und die Versuchsergebnisse.
 -Moleküle durch die Zellmembran ins Zellinnere von Neuronen diffundieren können. Im Cytoplasma angekommen, werden sie protoniert und dadurch positiv geladen
-Moleküle durch die Zellmembran ins Zellinnere von Neuronen diffundieren können. Im Cytoplasma angekommen, werden sie protoniert und dadurch positiv geladen  In dieser Form können sie die Zelle nicht mehr verlassen.
In dieser Form können sie die Zelle nicht mehr verlassen.
 auf der Zellinnenseite an Natriumionenkanäle binden. Die Bindung erfolgt im Bereich einer polaren Aminosäure. Abbildung 2 zeigt Ausschnitte der sich entsprechenden Aminosäuresequenzen des Natriumionenkanals einer Ratte und eines Pfeilgiftfrosches. Tabelle 1 zeigt die Polarität einiger relevanter Aminosäuren.
auf der Zellinnenseite an Natriumionenkanäle binden. Die Bindung erfolgt im Bereich einer polaren Aminosäure. Abbildung 2 zeigt Ausschnitte der sich entsprechenden Aminosäuresequenzen des Natriumionenkanals einer Ratte und eines Pfeilgiftfrosches. Tabelle 1 zeigt die Polarität einiger relevanter Aminosäuren.

 nicht selbst synthetisieren können, nehmen sie das Gift über ihre Nahrung auf. Als Nahrungsquelle werden hierbei beispielsweise Käfer aus der Familie der Melyridae in Betracht gezogen, welche das Gift enthalten.
nicht selbst synthetisieren können, nehmen sie das Gift über ihre Nahrung auf. Als Nahrungsquelle werden hierbei beispielsweise Käfer aus der Familie der Melyridae in Betracht gezogen, welche das Gift enthalten.
1.1
Erläutere die molekularen Grundlagen des Ruhepotenzials unter Berücksichtigung der beteiligten Ionen und Ionenkanäle.
3 VP
1.2
Erkläre auf molekularer Ebene, wodurch es bei Aktionspotenzialen zu einer immer gleich starken Depolarisation kommt.
Um den Mechanismus der Giftwirkung von
2 VP

Abb.1: Messungen an Neuronen von Ratten (vereinfacht)
2
Beschreibe die Ergebnisse der dargestellten Versuche 1 und 2. Entwickle eine Hypothese zur Wirkungsweise von  Gehe dabei sowohl auf den möglichen Wirkmechanismus am Axon als auch auf die Folgen für die Erregungsweiterleitung an der Synapse und auf die Folgen für den gesamten Organismus ein.
Gehe dabei sowohl auf den möglichen Wirkmechanismus am Axon als auch auf die Folgen für die Erregungsweiterleitung an der Synapse und auf die Folgen für den gesamten Organismus ein.
Untersuchungen zeigen, dass unpolare
4 VP
3.1
Erkläre, weshalb  und
und  eine Zellmembran unterschiedlich gut durchdringen können.
eine Zellmembran unterschiedlich gut durchdringen können.
Bei Ratten kann
2 VP

Abb.1: Konzentrationsverlauf von Trypanosomen und Antikörpern im Blut
| Aminosäure | Abkürzung | Polarität |
|---|---|---|
| Alanin | Ala | unpolar |
| Asparagin | Asn | stark polar |
| Asparaginsäure | Asp | stark polar |
| Isoleucin | Ile | unpolar |
| Serin | Ser | stark polar |
| Threonin | Thr | schwach polar |
| Valin | Val | unpolar |
Tab. 1: Polarität einiger Aminosäuren
3.2
Begründe mithilfe der Codesonne (siehe Anhang), welche Mutation in der DNA wahrscheinlich zur Änderung der Aminosäure an Position 429 (Ser  Ala) geführt hat.
Ala) geführt hat.
2 VP
3.3
Erläutere mithilfe von Tabelle 1, welche der durch Mutationen hervorgerufenen Änderungen in der Aminosäuresequenz des Pfeilgiftfrosches (Abbildung 2) zur Ausbildung der Unempfindlichkeit gegenüber BTX geführt haben könnten.
geführt haben könnten.
Da Pfeilgiftfrösche
2 VP
4
Beschreibe eine Versuchsreihe mit noch ungiftigen Jungfröschen, die den Einfluss der Melyridae-Käfer als Nahrung auf die Giftkonzentration in der Haut von Pfeilgiftfröschen untersucht.
Pfeilgiftfrösche sind meist sehr auffällig gefärbt. Oft gibt es im gleichen Gebiet andere ungiftige Froscharten mit derselben Färbung („Nachahmer“). Dieses Phänomen wird als Mimikry bezeichnet.
3 VP
5
Erläutere, weshalb die Population der „Nachahmer“ immer deutlich kleiner ist als die der „Vorbilder“.
2 VP
20 VP
1.1
Erläuterung der molekularen Grundlagen des Ruhepotenzials:
Damit das Ruhepotenzial zustande kommen kann, ist die selektive Permeabilität der Axonmembran für verschiedene Ionenspezies entscheidend. Der Öffnungszustand der in die Membran eingelagerten Ionenkanäle bestimmt die Durchlässigkeit. Die (nicht spannungssensitiven) -Ionenkanäle sind ständig offen, während die meistens
-Ionenkanäle sind ständig offen, während die meistens  -Ionenkanäle im Ruhezustand geschlossen sind. Außerdem gibt es
-Ionenkanäle im Ruhezustand geschlossen sind. Außerdem gibt es  -Ionenkanäle, die wenig durchlässig für
-Ionenkanäle, die wenig durchlässig für  -Ionen sind.
-Ionen sind.
Es herrscht infolge eines aktiven Ionentransports eine unterschiedliche Ionenverteilung im Inneren der Nervenzelle und im Außenmedium: Im Inneren des Axons ist ein großer Überschuss an positiv geladenen -Ionen sowie großen Protein-Anionen vorhanden. Die Membran ist für Letzteres komplett impermeabel. Außerhalb der Zelle befindet sich ein großer Überschuss an
-Ionen sowie großen Protein-Anionen vorhanden. Die Membran ist für Letzteres komplett impermeabel. Außerhalb der Zelle befindet sich ein großer Überschuss an  -Ionen (positiv) und
-Ionen (positiv) und  -Ionen (negativ).
Folge: Es kommt zu einem Ausstrom von
-Ionen (negativ).
Folge: Es kommt zu einem Ausstrom von  -Ionenkanälen entlang des Konzentrationsgefälles, da die
-Ionenkanälen entlang des Konzentrationsgefälles, da die  -Ionenkanäle auch im Ruhezustand geöffnet sind. Dadurch wird eine Spannung, die Potenzialdifferenz, aufgebaut. Wandern positiv geladene Kaliumionen aus der Zelle, hinterlassen sie unkompensierte negative Ladungen (v.a. Protein-Anionen), wodurch das Zellinnere gegenüber dem Außenmedium negativ geladen ist. Das Ruhepotenzial stellt sich als dynamisches Gleichgewicht zwischen der Tendenz zum Ausgleich der Konzentrationen und der Tendenz zum Ausgleich der Ladungen (bei ca.
-Ionenkanäle auch im Ruhezustand geöffnet sind. Dadurch wird eine Spannung, die Potenzialdifferenz, aufgebaut. Wandern positiv geladene Kaliumionen aus der Zelle, hinterlassen sie unkompensierte negative Ladungen (v.a. Protein-Anionen), wodurch das Zellinnere gegenüber dem Außenmedium negativ geladen ist. Das Ruhepotenzial stellt sich als dynamisches Gleichgewicht zwischen der Tendenz zum Ausgleich der Konzentrationen und der Tendenz zum Ausgleich der Ladungen (bei ca.  ) ein.
Erhaltung des Ruhepotenzials: Die Axonmembran ist nur wenig durchlässig für
) ein.
Erhaltung des Ruhepotenzials: Die Axonmembran ist nur wenig durchlässig für  -Ionen, wodurch es zu einem geringen Na
-Ionen, wodurch es zu einem geringen Na -Ioneneinstrom entlang des Konzentrationsgradienten in das Axon kommt. Durch diesen Leckstrom würde der Zusammenbruch des Ruhepotenzials folgen. Damit der Konzentrationsunterschied aufrechterhalten wird transportiert die Natrium-Kalium-Pumpe fortwährend
-Ioneneinstrom entlang des Konzentrationsgradienten in das Axon kommt. Durch diesen Leckstrom würde der Zusammenbruch des Ruhepotenzials folgen. Damit der Konzentrationsunterschied aufrechterhalten wird transportiert die Natrium-Kalium-Pumpe fortwährend  -Ionen aus dem Zellinneren nach außen. Das erfolgt unter ATP-Verbrauch und im Austausch gegen
-Ionen aus dem Zellinneren nach außen. Das erfolgt unter ATP-Verbrauch und im Austausch gegen  -Ionen.
-Ionen.
Damit das Ruhepotenzial zustande kommen kann, ist die selektive Permeabilität der Axonmembran für verschiedene Ionenspezies entscheidend. Der Öffnungszustand der in die Membran eingelagerten Ionenkanäle bestimmt die Durchlässigkeit. Die (nicht spannungssensitiven)
Es herrscht infolge eines aktiven Ionentransports eine unterschiedliche Ionenverteilung im Inneren der Nervenzelle und im Außenmedium: Im Inneren des Axons ist ein großer Überschuss an positiv geladenen
1.2
Erklärung der gleich starken Depolarisation:
Bei der Depolarisation eines Bereichs der Axonmembran (durch z.B. einen äußeren Reiz oder ein anderes Aktionspotenzial) bis zum Schwellenwert, öffnen sich spannungsgesteuerte Natriumionenkanäle. Durch eine positive Rückkoppelung kommt es zu einer lokalen Öffnung aller noch geschlossenen -Ionenkanäle (Alles-oder-nichts-Prinzip) und damit zu einem schnellen und starken
-Ionenkanäle (Alles-oder-nichts-Prinzip) und damit zu einem schnellen und starken  -Ioneneinstrom (Diffusion gemäß elektrochemischem Gradienten). Daraus folgt die Umpolung der Membran(spannung) von ca.
-Ioneneinstrom (Diffusion gemäß elektrochemischem Gradienten). Daraus folgt die Umpolung der Membran(spannung) von ca.  bis auf ca.
bis auf ca.  Anschließend schließen sich die spannungsgesteuerten
Anschließend schließen sich die spannungsgesteuerten  -Ionenkanäle wieder rasch und es öffnen sich verzögert die spannungsgesteuerten
-Ionenkanäle wieder rasch und es öffnen sich verzögert die spannungsgesteuerten  -Ionenkanäle.
-Ionenkanäle.
Die Öffnung der Natriumionenkanäle dauert mit ca. immer gleich lang. Alle Kanäle dieses Typs im Bereich der überschwelligen Depolarisation öffnen sich infolge positiver Rückkoppelung, wodurch es stets zu einem maximal möglichen Natriumioneneinstrom kommt. Wird der Schwellenwert überschritten erfolgt immer die maximal mögliche Depolarisation und somit eine gleich starke Depolarisation.
immer gleich lang. Alle Kanäle dieses Typs im Bereich der überschwelligen Depolarisation öffnen sich infolge positiver Rückkoppelung, wodurch es stets zu einem maximal möglichen Natriumioneneinstrom kommt. Wird der Schwellenwert überschritten erfolgt immer die maximal mögliche Depolarisation und somit eine gleich starke Depolarisation.
Bei der Depolarisation eines Bereichs der Axonmembran (durch z.B. einen äußeren Reiz oder ein anderes Aktionspotenzial) bis zum Schwellenwert, öffnen sich spannungsgesteuerte Natriumionenkanäle. Durch eine positive Rückkoppelung kommt es zu einer lokalen Öffnung aller noch geschlossenen
Die Öffnung der Natriumionenkanäle dauert mit ca.
2
Beschreibung der Versuchsergebnisse:
Die Versuchsbeschreibung ist nicht erforderlich, empfiehlt sich aber für die Verständlichkeit und Übersichtlichkeit. Versuchsbeschreibung: An den Axonen sind zwei Ratten-Neuronen (Neurone A und B) nacheinander geschaltet, an welchen je an einer Stelle (Messststelle A und B) nach künstlicher Reizung von Neuron A eine intrazelluläre Ableitung des Membranpotenzials durchgeführt wird.
durchgeführt wird.
Da an die spannungsgesteuerten
an die spannungsgesteuerten  -Ionenkanäle von Neuron A bindet, wird die Durchlässigkeit für
-Ionenkanäle von Neuron A bindet, wird die Durchlässigkeit für  -Ionen beeinflusst, z.B. durch Verhinderung der Schließung nach
-Ionen beeinflusst, z.B. durch Verhinderung der Schließung nach  infolge einer Veränderung der räumlichen Struktur. In diesem Bereich kommt es daraufhin zu einem verlängerten
infolge einer Veränderung der räumlichen Struktur. In diesem Bereich kommt es daraufhin zu einem verlängerten  -Ioneneinstrom und zu einer lokalen Dauerdepolarisation. Nachfolgende benachbarte Axonabschnitte zeigen nun eine ständige Neubildung von Aktionspotenzialen (APs). Das setzt sich bis zur Synapse fort und bewirkt dort einen verstärkten
-Ioneneinstrom und zu einer lokalen Dauerdepolarisation. Nachfolgende benachbarte Axonabschnitte zeigen nun eine ständige Neubildung von Aktionspotenzialen (APs). Das setzt sich bis zur Synapse fort und bewirkt dort einen verstärkten  -Ioneneinstrom, wodurch die Transmitterausschüttung in den synaptischen Spalt erhöht wird. Es folgt die vermehrte Öffnung transmittergesteuerter
-Ioneneinstrom, wodurch die Transmitterausschüttung in den synaptischen Spalt erhöht wird. Es folgt die vermehrte Öffnung transmittergesteuerter  -Ionenkanäle in der postsynaptischen Membran von Neuron B. Durch den daraus resultierenden starken
-Ionenkanäle in der postsynaptischen Membran von Neuron B. Durch den daraus resultierenden starken  -Ioneneinstrom in die postsynaptische Zelle, wird die postsynaptische Depolarisation (EPSP) an Neuron B verstärkt (ggf. gepaart mit einer zeitlichen Summation der auflaufenden postsynaptischen Potenziale) und generiert dadurch APs am Axonhügel mit einer erhöhten Frequenz. Bei Motoneuronen kann dies zu einer Dauererregung und Verkrampfung der innervierten Muskulatur (starre Lähmung) führen, wodurch es z.B. zum Tod durch Atem- und/ oder Herzstillstand kommt.
-Ioneneinstrom in die postsynaptische Zelle, wird die postsynaptische Depolarisation (EPSP) an Neuron B verstärkt (ggf. gepaart mit einer zeitlichen Summation der auflaufenden postsynaptischen Potenziale) und generiert dadurch APs am Axonhügel mit einer erhöhten Frequenz. Bei Motoneuronen kann dies zu einer Dauererregung und Verkrampfung der innervierten Muskulatur (starre Lähmung) führen, wodurch es z.B. zum Tod durch Atem- und/ oder Herzstillstand kommt.
Die Versuchsbeschreibung ist nicht erforderlich, empfiehlt sich aber für die Verständlichkeit und Übersichtlichkeit. Versuchsbeschreibung: An den Axonen sind zwei Ratten-Neuronen (Neurone A und B) nacheinander geschaltet, an welchen je an einer Stelle (Messststelle A und B) nach künstlicher Reizung von Neuron A eine intrazelluläre Ableitung des Membranpotenzials
- Versuch 1: Hier werden die Spannungsverläufe an den Messstellen A und B nach künstlicher Reizung ohne die Einwirkung von
dargestellt: Messstelle A zeigt nach der Reizung während der Messzeit zwei Aktionspotenziale (APs) im Abstand von ca.
Auch an Messstelle B werden nach ca.
zwei APs im gleichen zeitlichen Abstand abgeleitet.
- Versuch 2: Hier werden die Spannungsverläufe an den Messstellen A und B nach künstlicher Reizung und lokaler
-Einwirkung an Axon A dargestellt: Die Messstelle A weist einen identischen Spannungsverlauf wie in Versuch 1 auf (zwei APs im zeitlichen Abstand von ca.
). An Messstelle B werden jedoch nach ca.
erneut APs registriert, die eine höhere Anzahl und eine erhöhte Frequenz aufweisen (vier APs im zeitlichen Abstand von ca.
).
Da
3.1
Erklärung der unterschiedlich guten Membrangängigkeit von  und
und 
Dass unpolare und positiv geladene Moleküle unterschiedlich permeabel sind, lässt sich anhand des molekularen Aufbaus der Zellmembran erklären. Der grundlegende Aufbau besteht aus einer Lipiddoppelschicht aus Phospholipiden, deren hydrophobe, unpolare Fettsäurereste nach innen ragen. Ohne Transportmechanismus ist es für größere polare/geladene Moleküle unmöglich die Membran zu passieren. Das Alkaloid ist unpolar (im nicht protonierten Zustand) und kann daher leicht durch die Lipiddoppelschicht diffundieren.
ist unpolar (im nicht protonierten Zustand) und kann daher leicht durch die Lipiddoppelschicht diffundieren.  beschreibt den geladenen, protonierten Zustand und ist damit hydrophil. Die Zellmembran kann nicht mehr passiert werden.
Oder: Eine weitere Möglichkeit wäre, dass BTX
beschreibt den geladenen, protonierten Zustand und ist damit hydrophil. Die Zellmembran kann nicht mehr passiert werden.
Oder: Eine weitere Möglichkeit wäre, dass BTX an polare Bereiche in der Membran (ein- oder aufgelagerte Proteine) bindet.
an polare Bereiche in der Membran (ein- oder aufgelagerte Proteine) bindet.
Dass unpolare und positiv geladene Moleküle unterschiedlich permeabel sind, lässt sich anhand des molekularen Aufbaus der Zellmembran erklären. Der grundlegende Aufbau besteht aus einer Lipiddoppelschicht aus Phospholipiden, deren hydrophobe, unpolare Fettsäurereste nach innen ragen. Ohne Transportmechanismus ist es für größere polare/geladene Moleküle unmöglich die Membran zu passieren. Das Alkaloid
3.2
Begründung der wahrscheinlichsten Mutation für die Änderung:
Mutationen ereignen sich immer auf der Ebene der DNA, weswegen die mRNA-Tripletts erst übersetzt werden müssen. Die Ursache für die Änderung der Aminosäure an Position 429 von Serin nach Alanin wurde am wahrscheinlichsten durch eine Mutation verursacht, bei der möglichst viele Basenpaare des codierenden Tripletts verändert wurden. Die Codierung von Serin erfolgt über sechs Tripletts, bei denen sich zwei "Grund-Tripletts" unterscheiden lassen: 3'-TCG/A-5' oder 3'-AGX-5' (X = eine der vier Basen). Alanin wird nur über ein "Grund-Triplett" codiert: 3'-CGX-5'.
Am wahrscheinlichsten ist also eine Mutation der ersten Base des "Grund-Tripletts": 3'-AGX-5' zu 3'-CGX-5' (z.B. 3'-AGA-5' zu 3'CGA-5').
Mutationen ereignen sich immer auf der Ebene der DNA, weswegen die mRNA-Tripletts erst übersetzt werden müssen. Die Ursache für die Änderung der Aminosäure an Position 429 von Serin nach Alanin wurde am wahrscheinlichsten durch eine Mutation verursacht, bei der möglichst viele Basenpaare des codierenden Tripletts verändert wurden. Die Codierung von Serin erfolgt über sechs Tripletts, bei denen sich zwei "Grund-Tripletts" unterscheiden lassen: 3'-TCG/A-5' oder 3'-AGX-5' (X = eine der vier Basen). Alanin wird nur über ein "Grund-Triplett" codiert: 3'-CGX-5'.
Am wahrscheinlichsten ist also eine Mutation der ersten Base des "Grund-Tripletts": 3'-AGX-5' zu 3'-CGX-5' (z.B. 3'-AGA-5' zu 3'CGA-5').
3.3
Erläuterung, welche Mutationen zur BTX -Unempfindlichkeit geführt haben könnten:
-Unempfindlichkeit geführt haben könnten:
Die AS-Sequenz der Ratte repräsentiert das ursprüngliche Merkmal bzw. den ursprünglichen Zustand, auch wenn es sich um einen Vertreter eines evolutiv viel jüngeren Taxons (Säugetier) handelt. BTX bindet im Bereich einer polaren Aminosäure an
bindet im Bereich einer polaren Aminosäure an  -Ionenkanäle. Es lässt sich ableiten, dass eine Mutation, die zu einer Unempfindlichkeit gegenüber
-Ionenkanäle. Es lässt sich ableiten, dass eine Mutation, die zu einer Unempfindlichkeit gegenüber  führt, eine schlechtere Bindungsmöglichkeit von
führt, eine schlechtere Bindungsmöglichkeit von  an diese Kanäle zur Folge haben muss. Möglich wäre der Austausch einer polaren gegen eine unpolare bzw. eine schwächer polare Aminosäure des Kanalproteins. In den Aminosäuresequenzen von Ratte und Frosch ist von den fünf Unterschieden (Position 429, 433, 445, 1 583, 1 584) nur Position 429 (stark polares Ser
an diese Kanäle zur Folge haben muss. Möglich wäre der Austausch einer polaren gegen eine unpolare bzw. eine schwächer polare Aminosäure des Kanalproteins. In den Aminosäuresequenzen von Ratte und Frosch ist von den fünf Unterschieden (Position 429, 433, 445, 1 583, 1 584) nur Position 429 (stark polares Ser  unpolares Ala) und Position 1 584 (stark polares Asn
unpolares Ala) und Position 1 584 (stark polares Asn  schwach polares Thr) möglich. An den anderen Positionen führen die Unterschiede zu keiner Veränderung in der Polarität, womit sich als Ursache für die Unempfindlichkeit nicht infrage kommen.
schwach polares Thr) möglich. An den anderen Positionen führen die Unterschiede zu keiner Veränderung in der Polarität, womit sich als Ursache für die Unempfindlichkeit nicht infrage kommen.
Die AS-Sequenz der Ratte repräsentiert das ursprüngliche Merkmal bzw. den ursprünglichen Zustand, auch wenn es sich um einen Vertreter eines evolutiv viel jüngeren Taxons (Säugetier) handelt. BTX
4
Beschreibung einer Versuchsreihe:
Bei einer wissenschaftlichen Versuchsreihe ist es wichtig, dass immer der gleiche Parameter verändert wird. Alle anderen Versuchsbedingungen müssen gleich bleiben und es wird eine Negativkontrolle benötigt. Eine genügend große Zahl an Proben von verschiedenen Tieren gewährleistet statistisch signifikante Ergebnisse. Es wird eine ausreichend große Anzahl noch ungiftiger Jungtiere in mehrere Gruppen aufgeteilt und unter gleichen Bedingungen (Futtermenge, Temperatur, Luftfeuchtigkeit, Bewuchs und Größe des Terrariums) gehalten. Dabei werden die Gruppen über einen längeren Zeitraum mit einer unterschiedlich hohen Menge an Melyridae-Käfern gefüttert, wobei eine Kontrollgruppe keine Melyridae-Käfer in der Nahrung enthält (Negativkontrolle). Nun wird in gleichbleibenden, regelmäßigen Abständen die -Konzentration in der Haut der Jungtiere ermittelt. Möglich ist z.B. das Entnehmen von Hautabstrichen oder Hautproben und die Durchführung eines ELISA-Tests oder die Bestimmung der Giftwirkung an isolierten Neuronen. Die ermittelten Konzentrationen werden anschließend mit den anderen Gruppen und der Kontrollgruppe verglichen und durch statistische Auswertung kann dadurch der Einfluss der Melyridae-Käfer auf die Giftkonzentration in der Haut hergeleitet werden.
-Konzentration in der Haut der Jungtiere ermittelt. Möglich ist z.B. das Entnehmen von Hautabstrichen oder Hautproben und die Durchführung eines ELISA-Tests oder die Bestimmung der Giftwirkung an isolierten Neuronen. Die ermittelten Konzentrationen werden anschließend mit den anderen Gruppen und der Kontrollgruppe verglichen und durch statistische Auswertung kann dadurch der Einfluss der Melyridae-Käfer auf die Giftkonzentration in der Haut hergeleitet werden.
Bei einer wissenschaftlichen Versuchsreihe ist es wichtig, dass immer der gleiche Parameter verändert wird. Alle anderen Versuchsbedingungen müssen gleich bleiben und es wird eine Negativkontrolle benötigt. Eine genügend große Zahl an Proben von verschiedenen Tieren gewährleistet statistisch signifikante Ergebnisse. Es wird eine ausreichend große Anzahl noch ungiftiger Jungtiere in mehrere Gruppen aufgeteilt und unter gleichen Bedingungen (Futtermenge, Temperatur, Luftfeuchtigkeit, Bewuchs und Größe des Terrariums) gehalten. Dabei werden die Gruppen über einen längeren Zeitraum mit einer unterschiedlich hohen Menge an Melyridae-Käfern gefüttert, wobei eine Kontrollgruppe keine Melyridae-Käfer in der Nahrung enthält (Negativkontrolle). Nun wird in gleichbleibenden, regelmäßigen Abständen die
5
Erläuterung des Verhältnisses von "Nachahmern" und "Vorbildern":
Potenzielle Fressfeinde wie Schlangen und Vögel haben in der Regel erlernt, auffällig gefärbte Pfeilgiftfrösche zu meiden und sich damit vor -Vergiftungen zu schützen. Ungiftige Froscharten, die ähnlich gefärbt sind ("Nachahmer"), profitieren ebenfalls von der abschreckenden Wirkung der Warntracht der "Vorbilder". Wenn ungiftige Arten das Aussehen verwandter giftiger Arten "imitieren", wird das Mimikry genannt. Diese (Schutz-)Mimikry funktioniert allerdings nur, solange die Wahrscheinlichkeit eine gefährliche Art zu erbeuten für den Räuber höher ist, als die einer gleich aussehenden ungiftigen Art. Wenn die Population der ungiftigen Art größer wird, nimmt die Wirksamkeit der Warntracht zunehmend ab. Dadurch werden die Tiere vermehrt erbeutet und der Selektionsdruck wird höher.
-Vergiftungen zu schützen. Ungiftige Froscharten, die ähnlich gefärbt sind ("Nachahmer"), profitieren ebenfalls von der abschreckenden Wirkung der Warntracht der "Vorbilder". Wenn ungiftige Arten das Aussehen verwandter giftiger Arten "imitieren", wird das Mimikry genannt. Diese (Schutz-)Mimikry funktioniert allerdings nur, solange die Wahrscheinlichkeit eine gefährliche Art zu erbeuten für den Räuber höher ist, als die einer gleich aussehenden ungiftigen Art. Wenn die Population der ungiftigen Art größer wird, nimmt die Wirksamkeit der Warntracht zunehmend ab. Dadurch werden die Tiere vermehrt erbeutet und der Selektionsdruck wird höher.
Potenzielle Fressfeinde wie Schlangen und Vögel haben in der Regel erlernt, auffällig gefärbte Pfeilgiftfrösche zu meiden und sich damit vor