Aufgabe 5 – Genetik
Das menschliche Gehirn ist ein höchst komplexes Organ. Geistige Behinderungen können vielfältige Ursachen haben: So können unter anderem Mutationen des Syngap1-Gens zu einem veränderten Syngap1-Protein führen. Abbildung 1 zeigt die dreidimensionale Struktur eines unveränderten Syngap1-Proteins.
1
Nenne die in Abbildung 1 dargestellten Strukturebenen des Syngap1-Proteins und die sie jeweils stabilisierenden Wechselwirkungen bzw. Bindungen.
Das Syngap1-Protein besteht aus 1343 Aminosäuren. Mutationen im Syngap1-Gen können zu unterschiedlich schwerer geistiger Behinderung führen. Abbildung 2 zeigt Ausschnitte sich entsprechender Aminosäuresequenzen des Syngap1-Proteins einer gesunden und zweier von einer Mutation betroffener Personen.
2 VP
.png)
Abb. 1: Syngap1-Protein (Bändermodell)

Abb. 2: Ausschnitte sich entsprechender Aminosäuresequenz des Syngap1-Proteins verschiedener Personen
2
Gib mithilfe der Codesonne (siehe Anlage) eine mögliche DNA-Sequenz für das Syngap1-Protein einer gesunden Person an. Erläutere, welche Mutation am wahrscheinlichsten zur Änderung der Aminosäuresequenz bei Person 1 geführt hat.
Syngap1-bedingte geistige Behinderungen sind vor allem auf synaptische Funktionsstörungen zurückzuführen. Die Anzahl der Natriumionenkanäle in der postsynaptischen Membran unterliegt der Regulation des Ras-Signalwegs (Abb. 3a). Das Syngap1-Protein ist ein Schlüsselprotein dieses Signalwegs.
3 VP
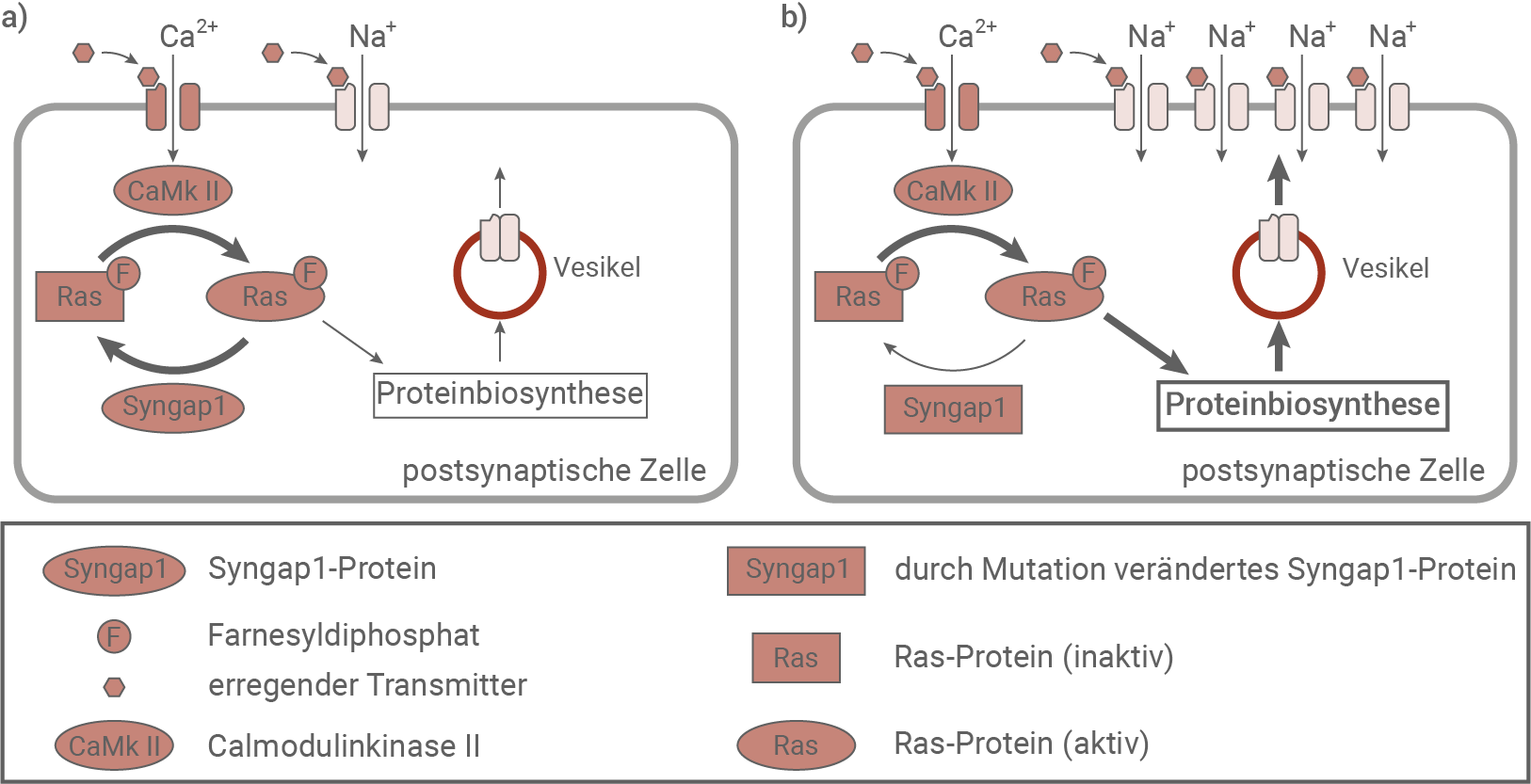
Abb. 3: Ras-Signalweg und Auswirkungen auf die postsynaptische Zelle mit a) unverändertem und b) durch Mutation verändertem Syngap1-Protein (stark vereinfacht)
3.1
Beschreibe die in Abbildung 3 a) dargestellten Vorgänge und erkläre die Funktion des Syngap1-Proteins für die Regulation der Anzahl der Natriumionenkanäle in der postsynaptischen Membran (Abb. 3).
3 VP
3.2
Erläutere die Auswirkungen eines durch Mutation veränderten Syngap1-Proteins auf die postsynaptische Zelle (Abb. 3 b)). Vergleiche die Auswirkungen der Mutationen der Personen 1 und 2 (Abb. 2) auf den Ras-Signalweg und erkläre damit den unterschiedlichen Grad der synaptischen Funktionsstörung der Personen 1 und 2 .
Mithilfe eines ELISA-Tests kann die Konzentration des unveränderten Syngap1-Proteins in Gewebeproben bestimmt werden. Dabei kommen Antikörper zum Einsatz, die spezifisch an das Syngap1-Protein binden können. Die enzymgekoppelten Antikörper verfügen über ein Enzym, das die Umwandlung einer zugesetzten farblosen Farbstoffvorstufe in einen gelben Farbstoff katalysiert. Die Auswertung des Tests erfolgt über die Messung der Farbintensität. Um von der Farbintensität auf die Konzentration des Syngap1-Proteins in der Gewebeprobe schließen zu können, wird eine Eichkurve benötigt, welche eine Zuordnung der Farbintensitäten zu definierten Syngap1-Konzentrationen ermöglicht (Abb. 4).
4 VP
4
Beschreibe das Vorgehen, wie im Labor eine Eichkurve (Abb. 4) erstellt werden kann. Erkläre, warum die Steigung der Kurve mit zunehmender Konzentration des Syngap1-Proteins abnimmt.
4 VP
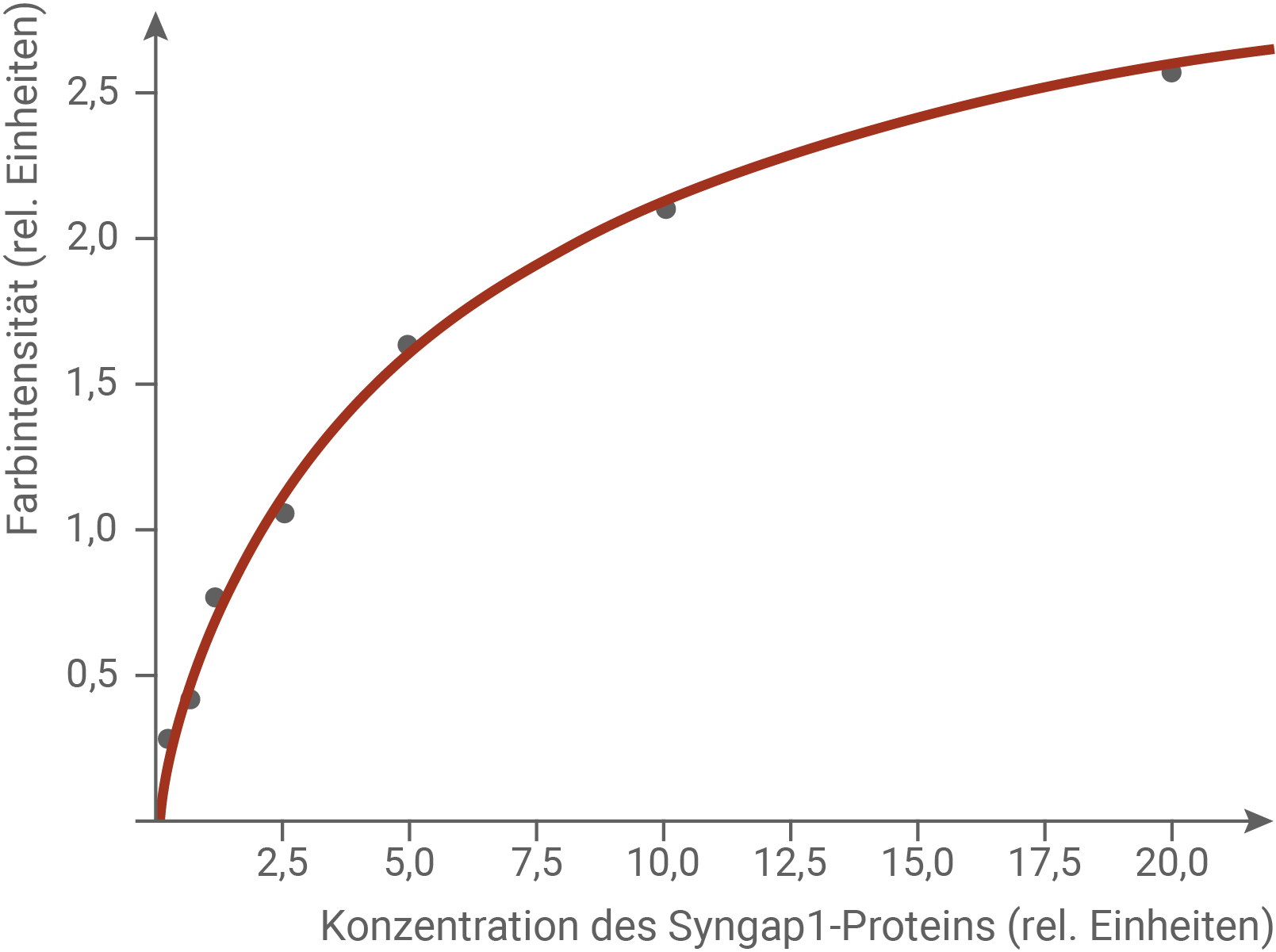
Abb. 4: Eichkurve zur Bestimmung der Konzentration des Syngap1-Proteins
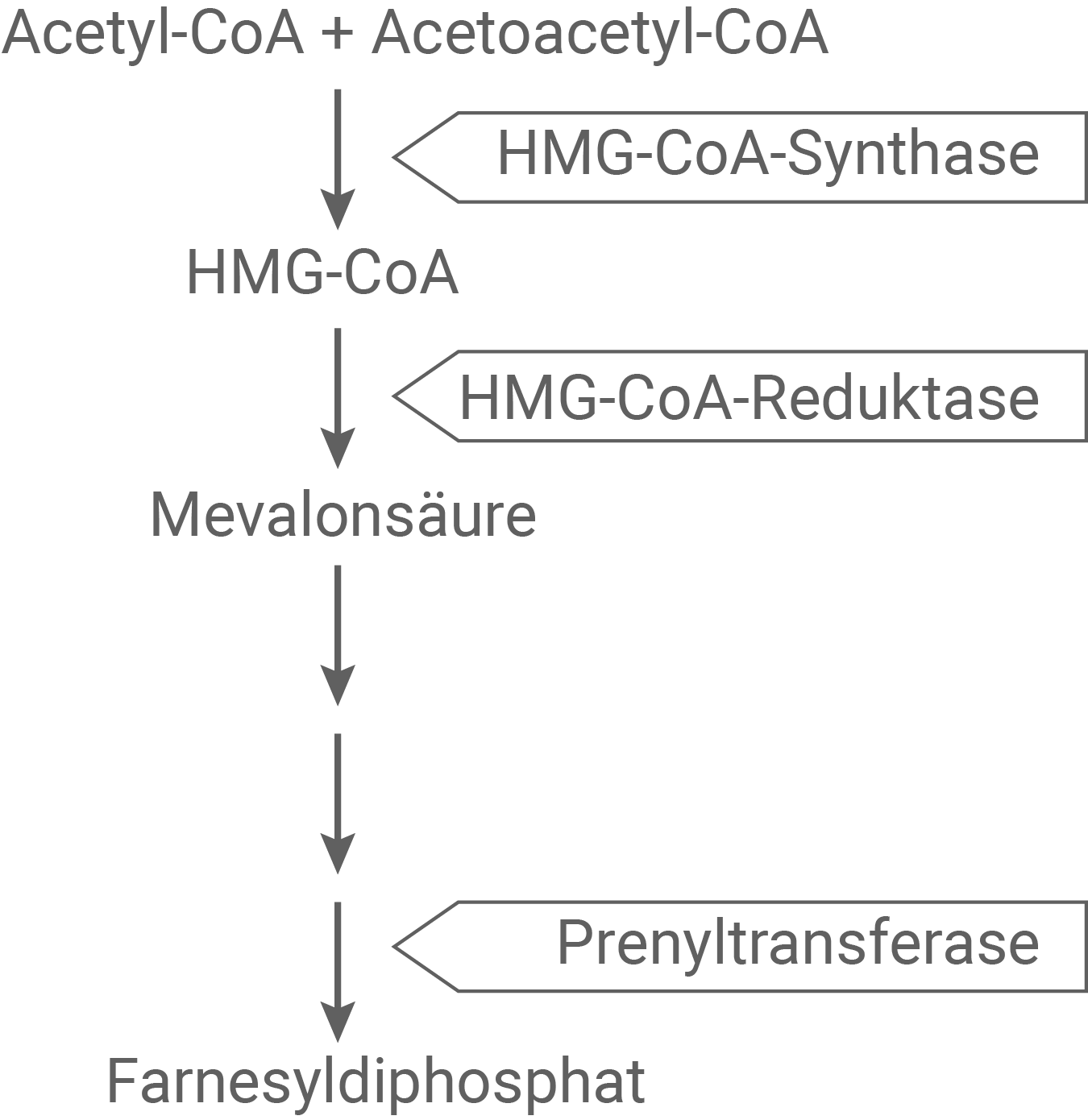
Abb. 5a: Ausschnitt aus dem Biosyntheseweg des Farnesyldiphosphats
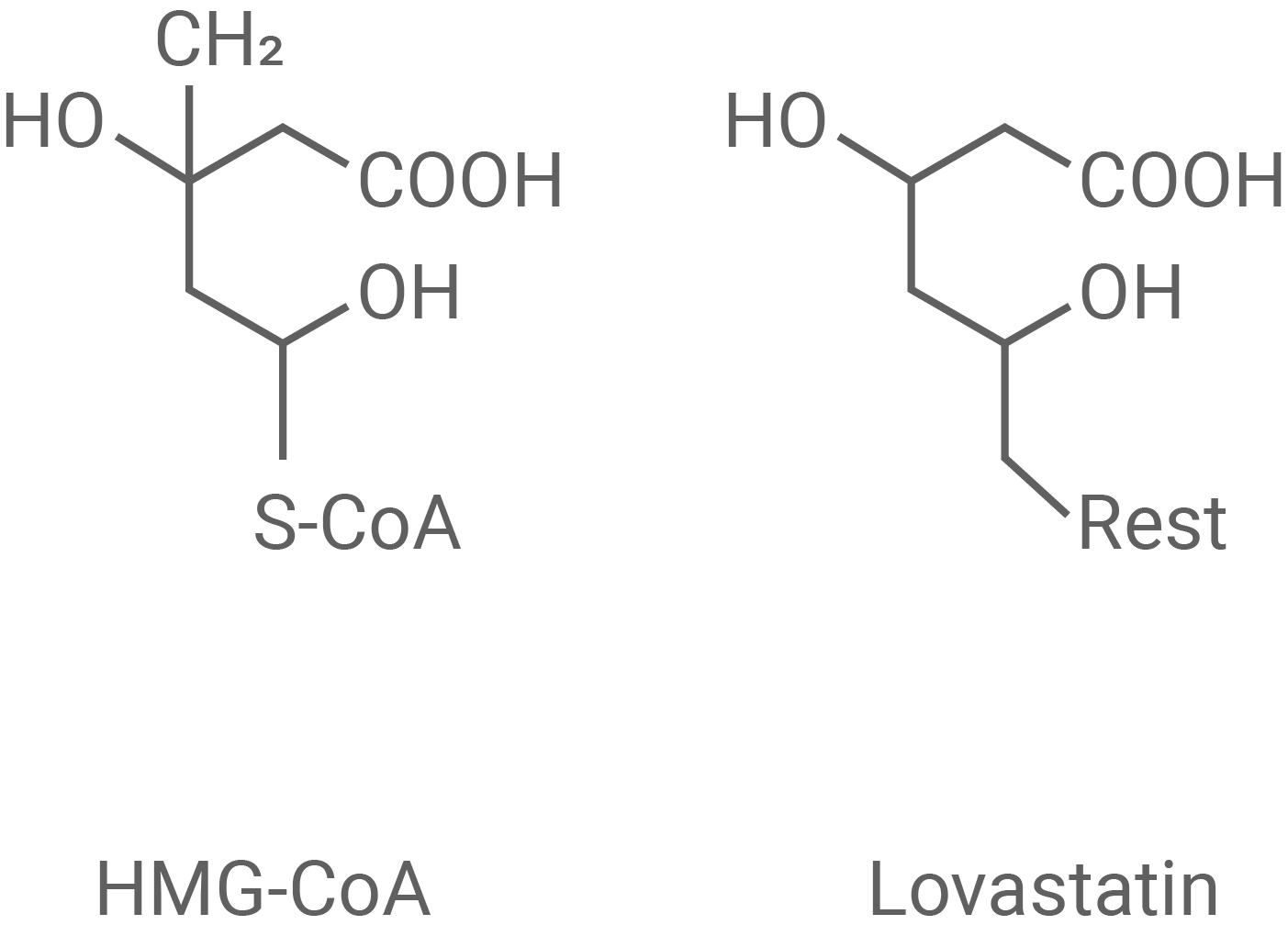
Abb. 5b: Strukturformeln von HMG-CoA und Lovastatin
5
Erläutere die Wirkung von Lovastatin (Abb. 5) und erkläre mithilfe von Abbildung 3 den erwarteten therapeutischen Nutzen.
4 VP
20 VP
Bildnachweise [nach oben]
Swiss Institute of Bioinformatics SWISS-MODEL | Q96PV0 (SYGP1_HUMAN), SWISS-MODEL | Terms Of Use
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Dargestellte Strukturebenen des Syngap1-Proteins und stabilisierende Wechselwirkungen bzw. Bindungen:
Es lässt sich die Sekundärstruktur mit den typischen  Helices,
Helices,  Faltblättern, und Haarnadelschleifen erkennen. Für die Sekundärstruktur sind die Wasserstoffbrücken zwischen Peptid-Gruppen charakteristisch. Die dreidimensionale Tertiärstruktur ist gekennzeichnet durch Wasserstoffbrücken, ionische Wechselwirkungen (bzw. Ionenbindungen), Van-der-Waals-Wechselwirkungen und Disulfidbrücken zwischen Aminosäureresten.
Faltblättern, und Haarnadelschleifen erkennen. Für die Sekundärstruktur sind die Wasserstoffbrücken zwischen Peptid-Gruppen charakteristisch. Die dreidimensionale Tertiärstruktur ist gekennzeichnet durch Wasserstoffbrücken, ionische Wechselwirkungen (bzw. Ionenbindungen), Van-der-Waals-Wechselwirkungen und Disulfidbrücken zwischen Aminosäureresten.
2
Mögliche DNA-Sequenz für das Syngap1-Protein bei einer gesunden Person:
- mRNA-Sequenz: 5' CAC AUA GAG AGG GAG GAG UAC AAG UUG 3'
- DNA-Sequenz: 3' GTG TAT CTC TCC CTC CTC ATG TTC AAC 5'
3.1
In Abbildung 3 a) dargestellte Vorgänge:
Ein erregender Transmitterstoff öffnet ligandengesteuerte Calcium-Ionenkanäle (und Natrium-Ionenkanäle), wodurch es zu einem Einstrom von Calcium-Ionen (und Natrium-Ionen) kommt. Durch den Calcium-Ioneneinstrom wird CaMKII aktiviert, und katalysiert die Umwandlung von inaktivem Ras-Protein in aktives Ras-Protein. Dadurch wird die Proteinbiosynthese aktiviert und es werden Vesikel mit Natriumionen-Kanalproteinen gebildet. Die Vesikel verschmelzen mit der postsynaptischen Membran, und werden in die Membran eingebaut. Das aktive Ras-Protein wird durch Syngap1 in inaktives Ras-Protein umgewandelt, und die Proteinbiosynthese kommt zum Erliegen. Syngap1 kontrolliert dabei über die Menge und Dauer der Anwesenheit von aktivem Ras-Protein die Proteinbiosynthese der Natriumionen-Kanalproteine und damit auch die Anzahl der Natriumionenkanäle.
3.2
Auswirkungen eines durch Mutation veränderten Syngap1-Proteins auf die postsynaptische Zelle:
Die Umwandlung des inaktiven Ras-Proteins in aktives Ras-Protein durch CaMKII erfolgt wie bei gesunden Personen. Jedoch kann das durch die Mutation veränderte Syngap1-Protein die Rückumwandlung in inaktives Ras-Protein nicht mehr so effizient ausführen. Die Proteinbiosynthese wird dadurch stärker aktiviert, und es kommt zu einer erhöhten Bildung von Vesikeln mit Natriumionen-Kanalproteinen. Dadurch wird auch die Dichte der Natrium-Ionenkanäle in der postsynaptischen Membran erhöht.
Vergleich der Auswirkungen der Mutationen der Personen 1 und 2 auf den Ras-Signalweg:
Bei Person 1 führt die Mutation im Syngap1-Gen durch den Austausch einer Aminosäure zu einer leicht veränderten Proteinvariante des Syngap1-Proteins. Bei Person 2 führt das vorzeitige Stoppcodon zu einer verkürzten Aminosäurekette und damit zu einem verkürztem Syngap1-Protein. Bei Person 1 ist die Kontrolle der Produktion und des Einbaus der Natriumionen-Kanalproteine zwar gestört, aber noch möglich. Bei Person 2 kann keine Kontrolle der Produktion und des Einbaus der Natriumionen-Kanalproteine mehr stattfinden. Es kommt zu einer synaptischen Funktionsstörung, und bei Person 2 ist die geistige Behinderung vermutlich stärker ausgeprägt als bei Person 1.
4
Vorgehen zum Erstellen einer Eichkurve im Labor:
Es werden sieben Proben mit definierten Konzentrationen des Syngap1-Proteins in mehrfachem Ansatz hergestellt. Mit allen Proben wird der ELISA-Test (mit den gleichen Reagenzien und konstanten Parametern) durchgeführt, und die jeweilige Farbintensität jeder Probe (photometrisch) bestimmt. Für die Ansätze mit gleicher Proteinkonzentration wird der Durchschnittswert der gemessenen Farbintensitäten gebildet. Auf Basis der entstehenden Durchschnittswerte für jede Proteinkonzentration wird eine Regressionskurve erstellt. Die Kurve stellt die gemessenen Farbintensitäten in Abhängigkeit der Konzentration des Syngap1-Proteins dar.
Abnahme der Steigung der Kurve bei erhöhten Protein-Konzentrationen:
Bei der abgebildeten Kurve ist zu erkennen, dass mit zunehmender Proteinkonzentration der Proben die Farbintensität zunimmt. Das bedeutet, dass bei höheren Proteinkonzentrationen die Anzahl der an die Syngap1-Proteine gebundenen, enzymgekoppelten Antikörper steigt. Durch die zunehmend höhere Enzym-Konzentration werden die in konstanter Menge zugegeben Substrate (Farbstoffvorstufen) zum einschränkenden Faktor, wodurch die Steigung der Kurve abnimmt.
5
Wirkung von Lovastatin und erwarteter therapeutischer Nutzen:
HMG-CoA und Lovastatin weisen Bereiche auf, die sich in ihrer Struktur ähneln. Daher konkurrieren die beiden Stoffe um die Bindung am aktiven Zentrum der HMG-CoA-Reduktase. Bindet Lovastatin, so kommt es zur kompetitiven Hemmung der HMG-CoA-Reduktase. Infolgedessen wird weniger bzw. keine Mevalonsäure und dementsprechend weiger oder gar kein Farnesyldiphosphat gebildet. Es werden weniger Ras-Proteine aktiviert. Eine geringere Aktivierung von Ras-Proteinen kompensiert die durch die Mutation des Syngap1-Gens verstärkt ablaufende Proteinbiosynthese. Die Synthese und der Einbau von Natriumionen-Kanalproteinen wird verringert. Dadurch kann auch die synaptische Funktionsstörung bzw. die geistige Behinderung vermindert werden.