Aufgabe 3 – Immunbiologie
Das SARS-CoV-2-Virus ist ein RNA-Virus. Es besitzt ein charakteristisches Oberflächen-Protein (Spike-Protein), das für die Aufnahme des Virus in Körperzellen wichtig ist. mRNA-Impfstoffe gegen SARS-CoV-2 enthalten einen mRNA-Abschnitt, der für dieses Spike-Protein codiert. Um ihre Aufnahme in Körperzellen zu ermöglichen, wird die mRNA mit Lipiden umhüllt, sodass sogenannte mRNA-Lipidnanopartikel (LNP) entstehen. Darüber hinaus enthalten die LNP den lipophilen Stoff Cholesterin (Abb. 1). Die LNP sind nach der intramuskulären Injektion eine Zeit lang stabil und ermöglichen die Aufnahme der mRNA in nur wenige Muskelzellen. Studien haben gezeigt, dass die Lipidnanopartikel nicht zellschädigend sind.
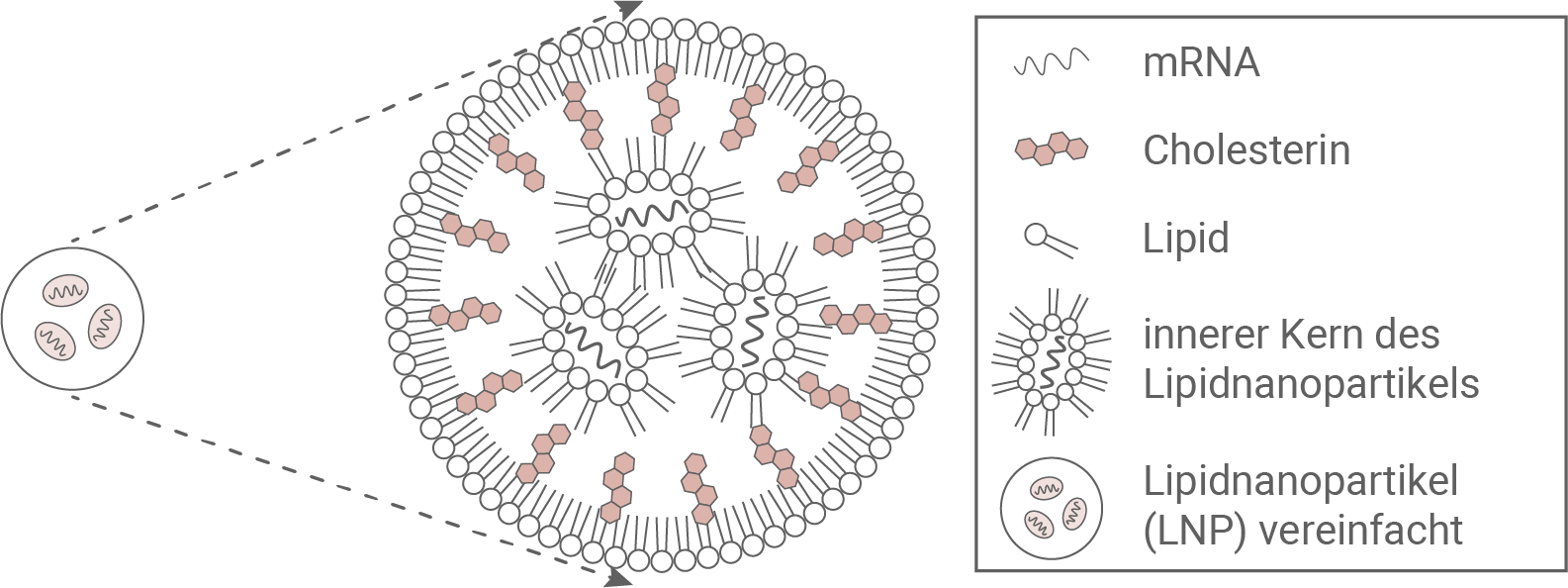
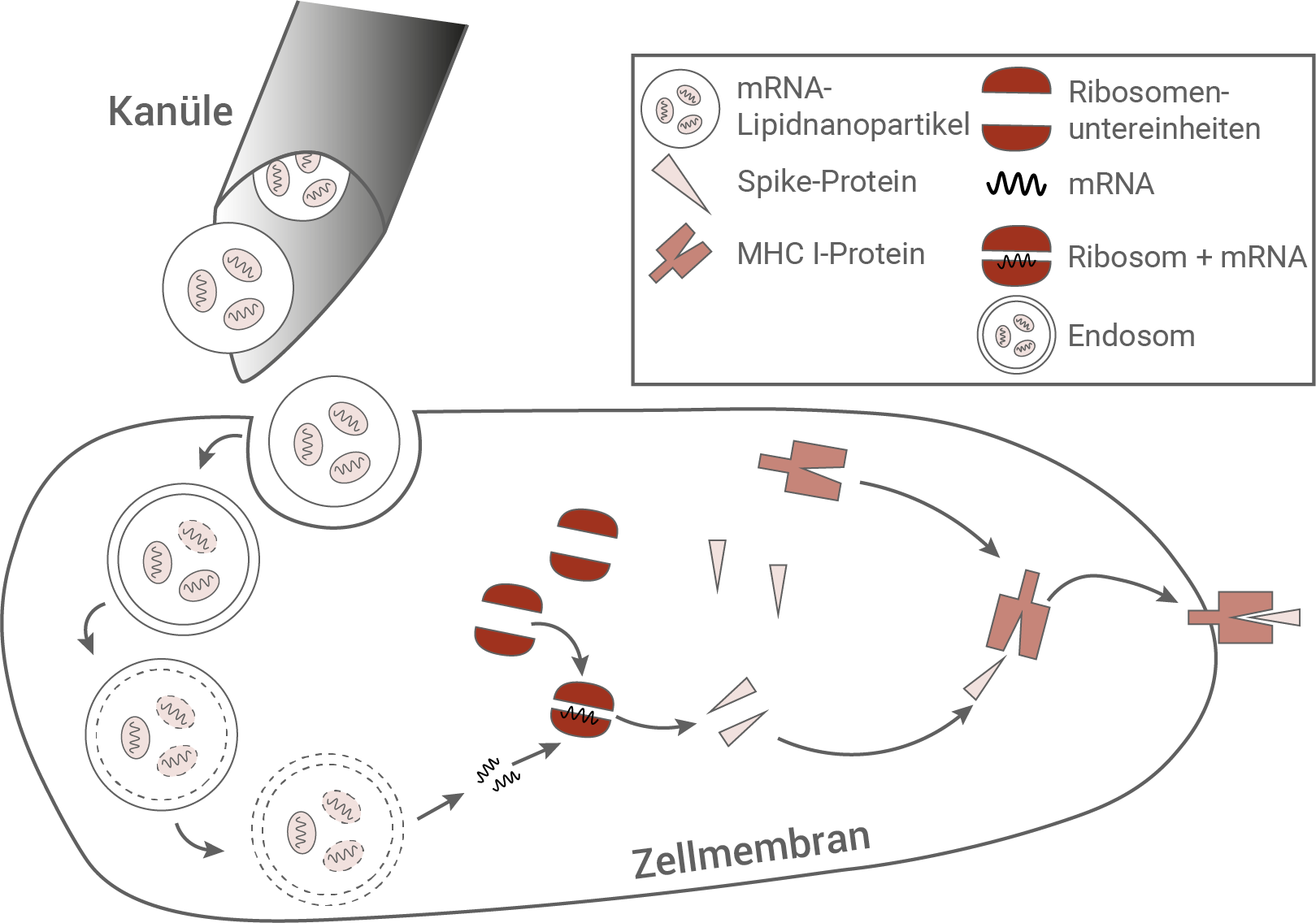
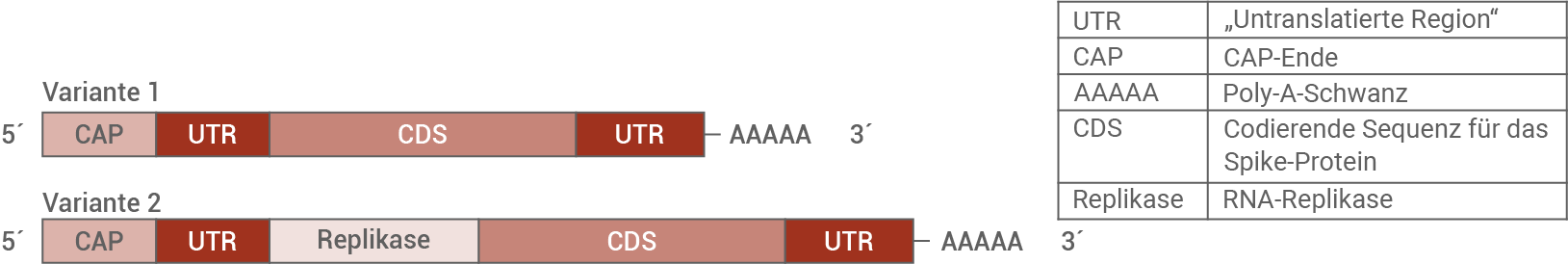
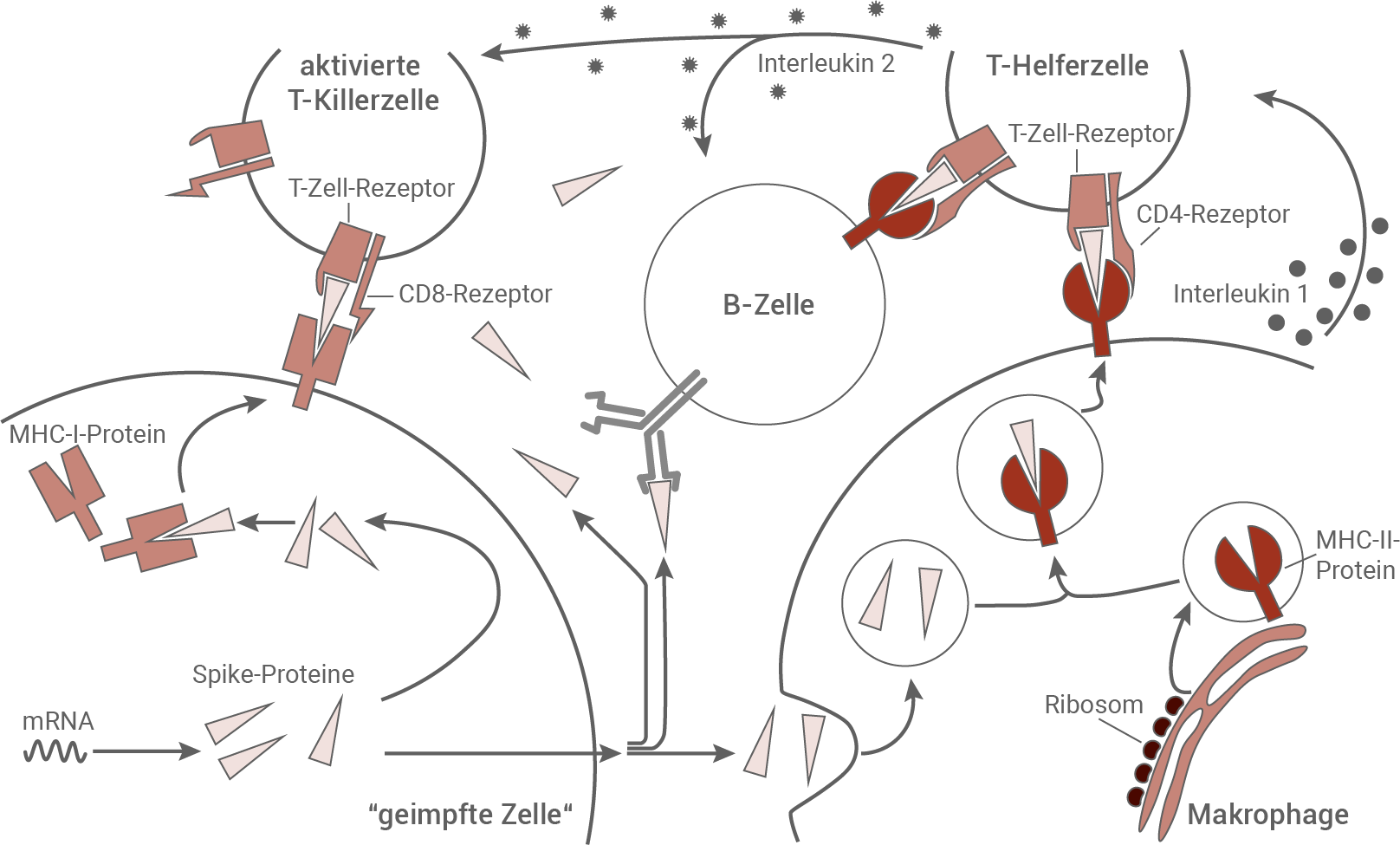
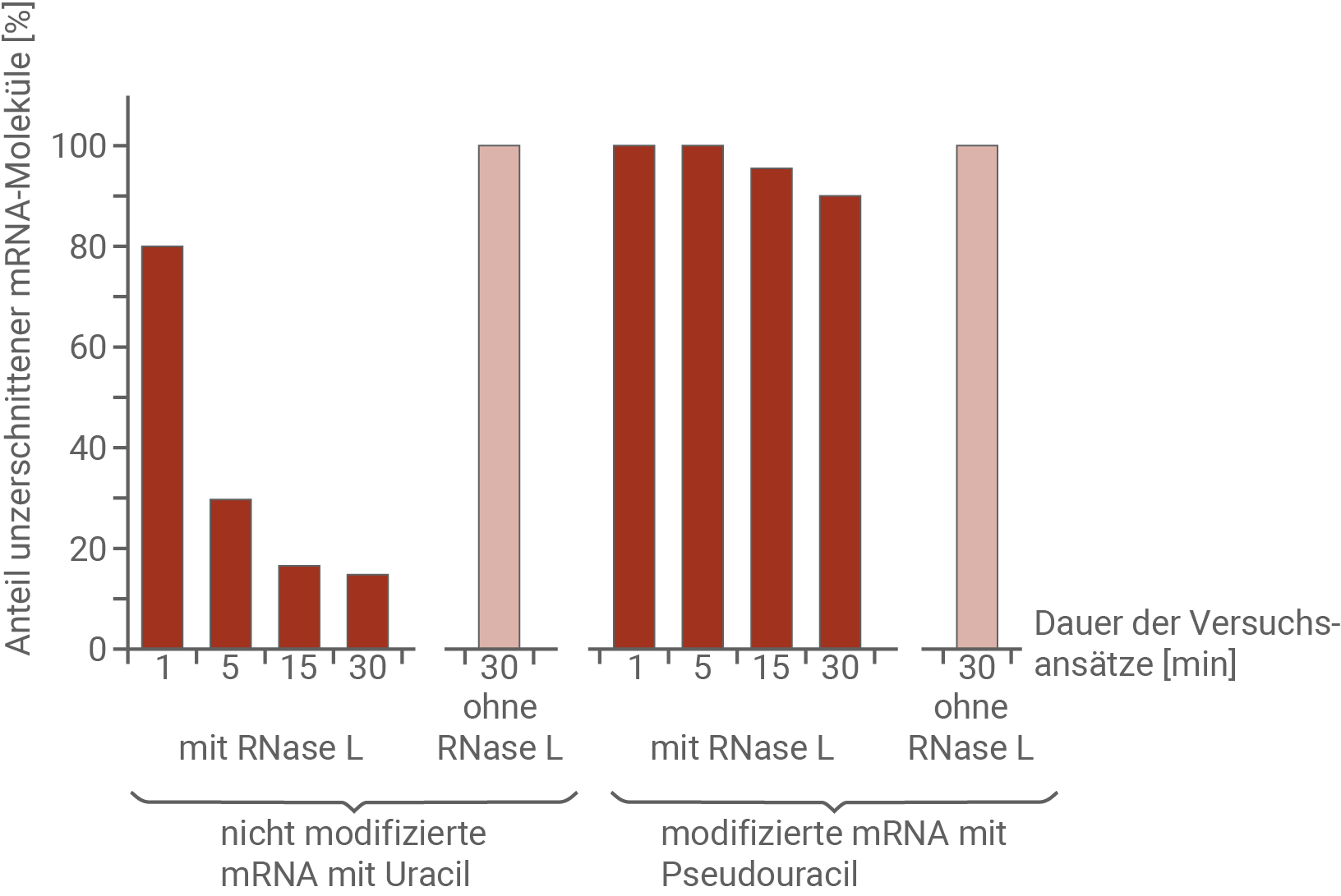

Abb. 1: Lipidnanopartikel (schematisch)
1
Vergleiche den Bau eines LNP (Abb. 1) mit der Struktur einer Zellmembran nach dem Flüssig-Mosaik-Modell (drei Angaben).
Abbildung 2 zeigt die Vorgänge in einer Körperzelle nach einer Impfung mit einem mRNA-Impfstoff.
3 VP

Abb. 2: Vorgänge in einer Körperzelle nach einer Impfung mit mRNA-Impfstoff (schematisch)
2
Beschreibe die in Abbildung 2 dargestellten Vorgänge nach der Impfung mit einem mRNA-Impfstoff.
Da mRNA-Moleküle in Zellen relativ instabil sind, befinden sich an deren Enden ein CAP-Ende und ein Poly-A-Schwanz, die vor dem Abbau durch RNasen schützen. Momentan existieren zwei Varianten von mRNA-Impfstoffen. Bei beiden Varianten kommt ein künstlich hergestelltes mRNA-Konstrukt zum Einsatz (Abb. 3). Eine der Varianten enthält zusätzlich eine Nukleotidsequenz für eine RNA-Replikase. Dabei handelt es sich um eine spezifische RNA-Polymerase, die natürlicherweise in manchen RNA-Viren vorkommt.
3 VP

Abb. 3: mRNA der beiden Impfstoffvarianten
3
Erläutere, wie die zusätzlich eingefügte Nukleotidsequenz für Replikase die Wirkung des mRNA-Impfstoffes beeinflusst.
Abbildung 4 zeigt die Immunreaktion, die nach der Aufnahme der mRNA im Körper stattfinden.
2 VP

Abb. 4: Immunreaktionen nach einer Impfung mit mRNA-Impfstoff (vereinfacht)
4
Erläutere mithilfe der Abbildung 4 die Prozesse, die ausgehend von der mRNA im Körper der geimpften Person ausgelöst werden und zu einer Immunität der geimpften Person führen.
Manche Impfstoff-Hersteller verwenden in ihren Lipidnanopartikeln eine modifizierte mRNA, bei der die Base Uracil durch Pseudouracil ersetzt wurde, welche die Translation nicht beeinträchtigt. Durch in-vitro-Versuche fand man heraus, dass es bei der Wirksamkeit des Impfstoffes einen Unterschied zwischen modifizierter und nicht modifizierter mRNA gibt. In den Versuchsansätzen (Abb. 5) spielt die Oligoadenyl-Synthetase (OAS) eine Schlüsselrolle, die durch Binden an die mRNA aktiviert wird. In der Folge wird die RNase L aktiviert, welche die Spaltung der mRNA katalysiert.
6 VP

Abb. 5: Ergebnisse von jeweils fünf Versuchsansätzen mit unmodifizierter und modifizierter mRNA
5.1
Beschreibe die in Abbildung 5 dargestellten Ergebnisse und gib eine mögliche Erklärung für den Zusammenhang zwischen Modifizierung und RNase L-Aktivität.
4 VP
5.2
Begründe, welcher der beiden mRNA-Impfstoffe die bessere Wirksamkeit zeigt.
2 VP
20 VP
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Vergleich eines LNP mit der Struktur einer Zellmembran nach dem Flüssig-Mosaik-Modell:
| Gemeinsamkeiten | Unterschiede |
|---|---|
| Aufbau aus Lipiden | Einschichtige Lipidhülle bei LNP |
| Enthalten Cholesterin | Keine Proteineinlagerungen bei LNP |
| Nach außen hydrophil | Keine Glycokalyx bei LNP |
2
Vorgänge in einer Körperzelle nach einer Impfung mit einem mRNA-Impfstoff:
Das LNP wird durch Endocytose in die Körperzelle aufgenommen, und in Form eines Endosoms in der Zelle transportiert. Die beiden Membranen, die die mRNA-Partikel umgeben, lösen sich auf. Die mRNA wird freigegeben und zu den Ribosomen transportiert. Die beiden ribosomalen Untereinheiten lagern sich an die mRNA-Sequenz an, und bilden einen funktionellen Translationsapparat. Bei der anschließenden Translation werden die Spike-Proteine synthetisiert. Diese binden komplementär an das MHCI-Protein. Dieser Komplex wird an der Außenseite der Zellmembran präsentiert.
3
Beeinflussung der Wirkung des mRNA-Impfstoffes durch die zusätzlich eingefügte Nukleotidsequenz für Replikase:
Wird ein Replikase-Gen zusätzlich in die Zelle eingeschleust, wird die Ziel-mRNA vervielfältigt. Eine erhöhte mRNA-Konzentration in den Zellen führt zu einer erhöhten Translationsfrequenz. Es werden mehr Spike-Proteine synthetisiert, und die Wirkung des Impfstoffes ist stärker.
4
Immunreaktion nach einer Impfung mit mRNA-Impfstoff:
Durch die Translation der mRNA in den Körperzellen der geimpften Person entstehen Spike-Proteine. Diese werden freigegeben oder im Komplex mit MHC-I-Proteinen an der Oberfläche der Zellmembran präsentiert. Freigesetzte Spike-Proteine werden von Makrophagen erkannt, und phagocytiert. Im Makrophage verschmelzen die in Vesikel verpackten Spike-Proteine mit Vesikeln, die das MHC-II-Protein enthalten. An der Zelloberfläche werden (Fragmente) des Spike-Proteins auf MHC-II-Proteinen präsentiert. Über den T-Zell-Rezeptor und den CD4-Rezeptor binden spezifische T-Helferzellen an den auf der Oberfläche des Makrophagen präsentierten Komplex. Durch Interleukin 1 werden die spezifischen T-Helferzellen aktiviert. Darauf folgt die humorale Immunreaktion. Dabei binden spezifische B-Zellen Spike-Proteine, die von der geimpften Zelle freigegeben wurden. Die Proteine werden aufgenommen und an der Oberfläche von MHC-II-Proteinen präsentiert. Die B-Zelle wird durch Binden der spezifischen T-Helferzelle an die auf der Oberfläche der B-Zelle präsentierten Spike-Proteine, und durch Ausschüttung von Interleukin 2 aus der T-Helferzelle aktiviert. Die B-Zellen differenzieren sich zu Plasmazellen und bilden daraufhin Antikörper sowie B-Gedächtniszellen. Bei der zellulären Immunreaktion binden spezifische T-Killerzellen mit T-Zell-Rezeptor und CD8-Rezeptor an geimpfte Körperzellen, die Spike-Proteine über MHC-1-Proteine präsentieren. Die spezifischen T-Killerzellen werden durch Interleukin 2 aktiviert und bilden T-Gedächtniszellen.
5.1
In Abbildung 5 dargestellte Ergebnisse und Zusammenhang zwischen Modifizierung und RNase L-Aktivität:
Dargestellt ist die Abhängigkeit der Menge unzerschnittener mRNA von der Zeit der Einwirkung der RNase L mit Unterscheidung zwischen nicht modifizierter mRNA mit Uracil und modifizierter mRNA mit Pseudouracil. Bei der nicht modifizierten mRNA ist deutlich zu erkennen, dass mit fortschreitender Zeit immer weniger unzerschnittene Moleküle übrig bleiben (Von 80 % nach einer Minute auf 50 % nach fünf Minuten, und auf unter 20 % nach 30 Minuten). Die RNase L freie Kontrollprobe ist nach 30 Minuten unverändert. Im Versuchsansatz mit modifizierter mRNA nimmt der Anteil unzerschnittener mRNA kaum ab. Nach 30 Minuten sind noch etwa 90 % unzerschnittene mRNA-Moleküle vorhanden. Auch hier zeigt der Kontrollansatz keinerlei Veränderung nach 30 Minuten. Eine mögliche Erklärung könnte sein, dass die OAS durch die Modifizierung schlechter an die mRNA-Sequenz binden, dadurch nur geringer aktiviert werden, und die Spaltung der mRNA schlechter katalysieren kann. Insgesamt wird die mRNA dadurch langsamer abgebaut.
5.2
Bessere Wirksamkeit des Impfstoffes:
Der Impfstoff mit der modifizierten Base sollte eine bessere Wirksamkeit zeigen, da in diesem Fall die empfindliche mRNA nicht so schnell durch RNasen abgebaut wird. Die Translation ist effizienter und es entstehen mehr Spike-Proteine.