Aufgabe 3 – Chymosin
Hinweis: Von den vier Aufgaben sollen in der Prüfung drei ausgewählt und bearbeitet werden.
Zur Käseherstellung versetzt man in einem ersten Arbeitsschritt Milch mit einem enzymhaltigen Extrakt (Lab). Dies führt zum Verklumpen von Milcheiweißen – es entsteht Käsebruch, der gepresst und gesalzen wird und zu Käse heranreift. Lab enthält das Enzym Chymosin, eine Protease, welche in Schleimhautzellen (Abb. 2) des Labmagens von Kälbern gebildet wird. Das zugehörige Pro-Chymosin-Gen codiert für eine Vorstufe (Pro-Chymosin) des Chymosins. Durch Exocytose gelangt das Pro-Chymosin in das saure Milieu des Magens und wird dort durch Abspaltung eines Teiles der Aminosäurekette in das wirksame Enzym Chymosin umgewandelt.

Abb. 1: Lab
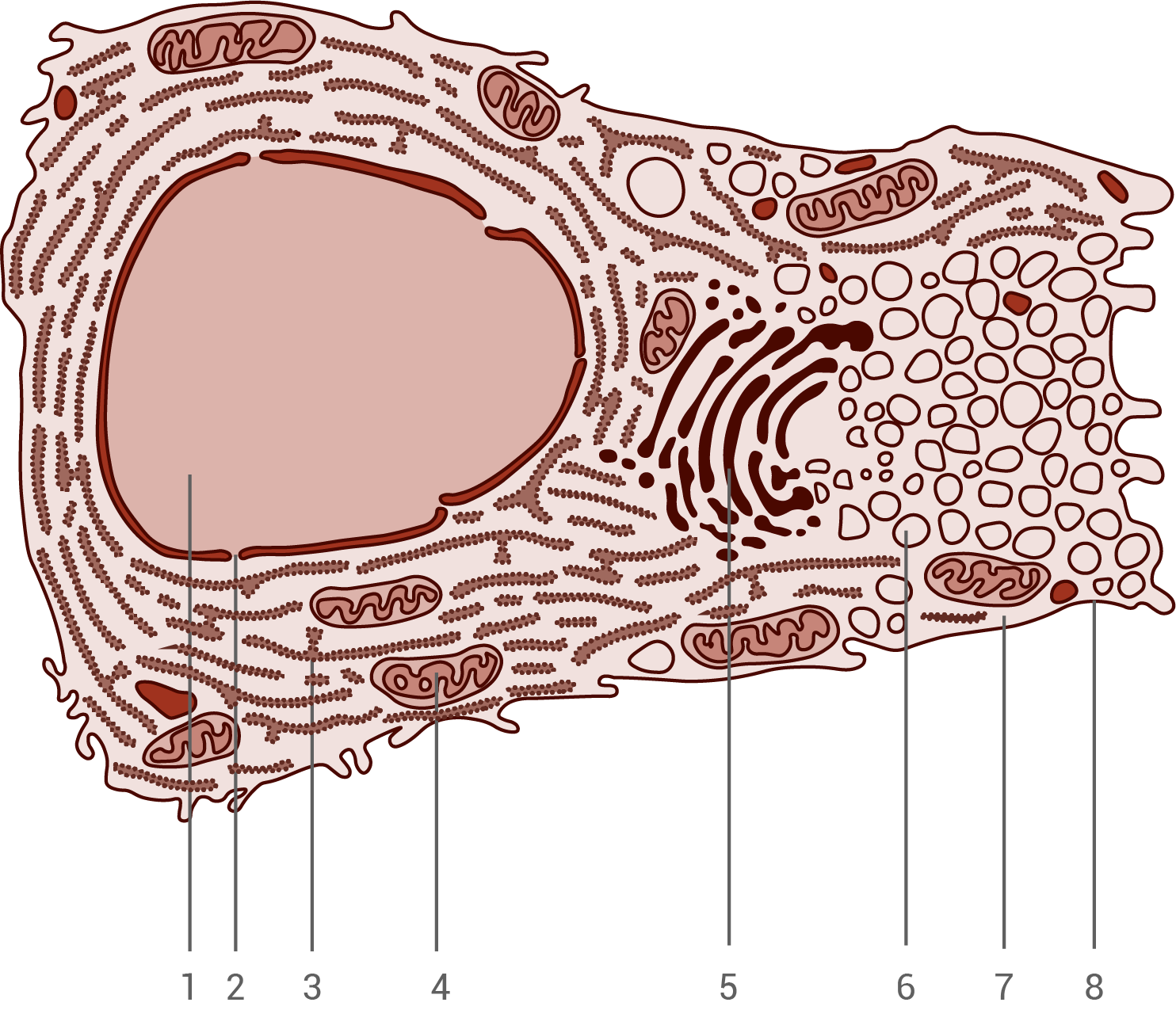
Abb. 2: Schleimhautzelle des Labmagens (schematisch)
1.1
Benenne die in Abbildung 2 mit den Ziffern 1 bis 8 versehenen Strukturen.
4 BE
1.2
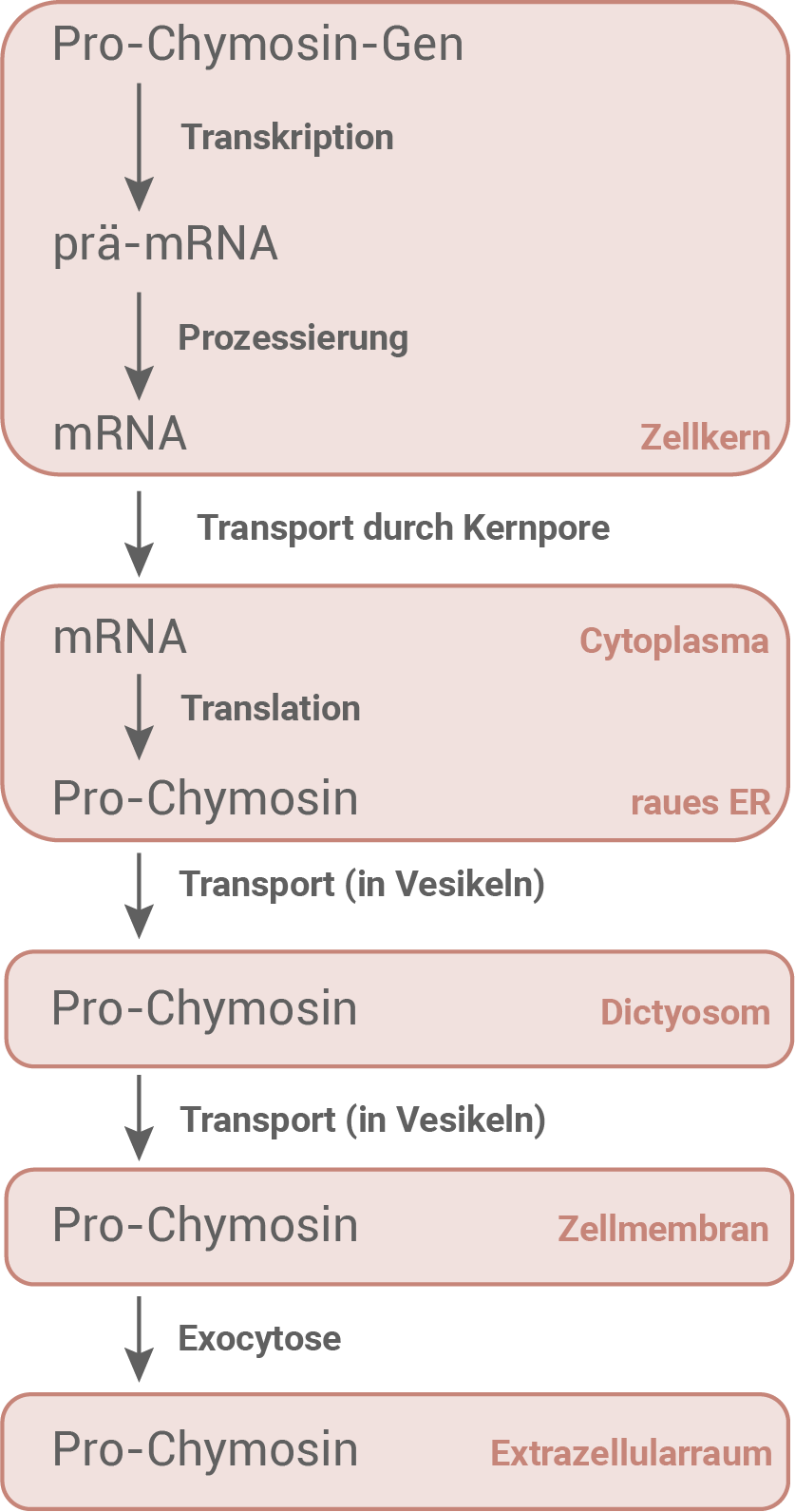
Stelle die Schritte der Bildung und des Transports des Pro-Chymosins ausgehend vom Gen bis zur Exocytose in Form eines Verlaufsschemas dar. Ordne in Deiner Darstellung den Schritten die jeweiligen Zellstrukturen zu.
8 BE
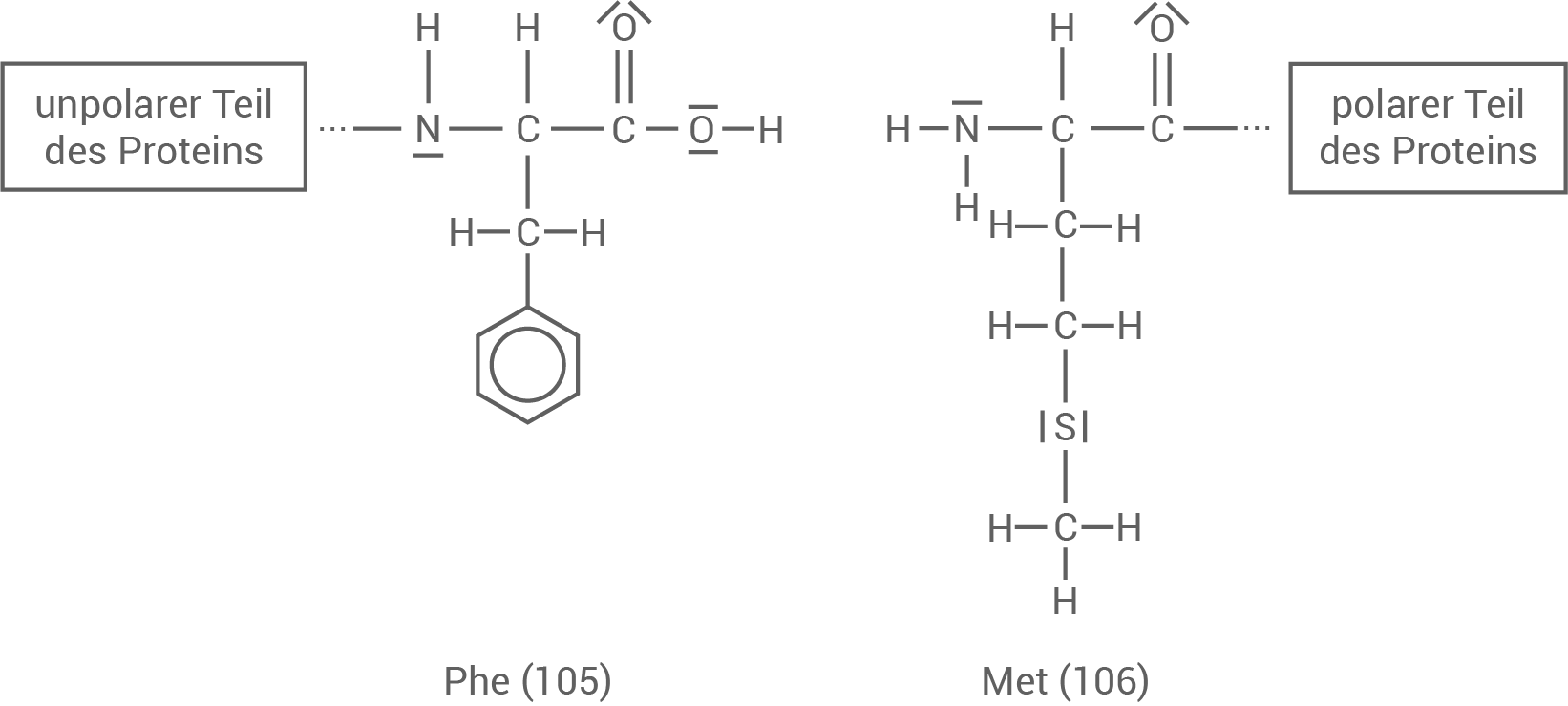
Chymosin ist eine Protease. Sie katalysiert spezifisch die hydrolytische Spaltung von Peptidbindungen zwischen den Aminosäuren Phenylalanin (Phe) und Methionin (Met). Im Kälbermagen wird durch die katalytische Wirkung des Chymosins der polare Teil der Muttermilcheiweiße (Aminosäuren 106-169), welcher die Wasserlöslichkeit der Milcheiweiße ermöglicht, abgetrennt. Dies führt zur Verklumpung und somit zu einer besseren Verdaubarkeit der Milcheiweiße. Abbildung 3 zeigt einen molekularen Ausschnitt aus der Polypeptidkette des Milcheiweißes.
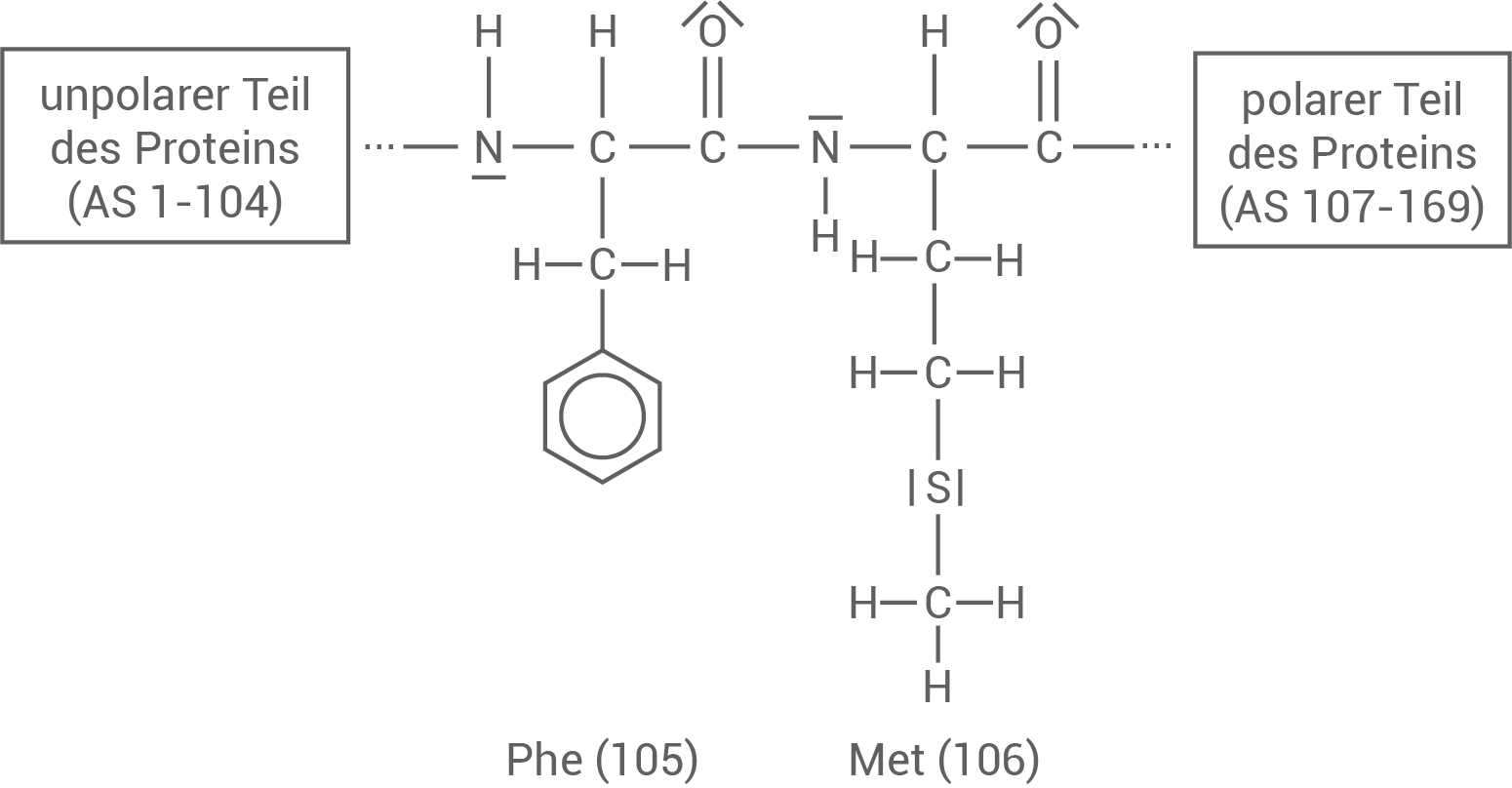
Abb. 3: Molekularer Ausschnitt der Polypeptidkette des Milcheiweißes
2
Stelle unter Verwendung von Abb. 3 die Produkte nach Einwirken des Chymosins dar.
In der industriellen Käseproduktion wird gentechnisch hergestelltes Pro-Chymosin genutzt. Dazu werden z. B. Bakterien der Art Escherichia coli (E. coli) gentechnisch so verändert, dass sie Pro-Chymosin im großen Maßstab produzieren können. Abbildung 4a und 4b zeigen den Aufbau des dafür verwendeten DNA-Fragments mit dem Pro-Chymosin-Gen und des Plasmids mit den jeweiligen Schnittstellen für verschiedene Restriktionsenzyme.
4 BE
3.1
Nenne die grundlegenden Schritte der Plasmidtechnik zur Herstellung einer Kultur gentechnisch veränderter Bakterien.
4 BE
3.2
Begründe, welche der in den Abbildungen 4a bzw. 4b genannten Restriktionsenzyme für die Herstellung eines geeigneten rekombinanten Plasmids verwendet werden können und welche nicht.
6 BE

Abb. 4a: Aufbau des DNA-Fragments
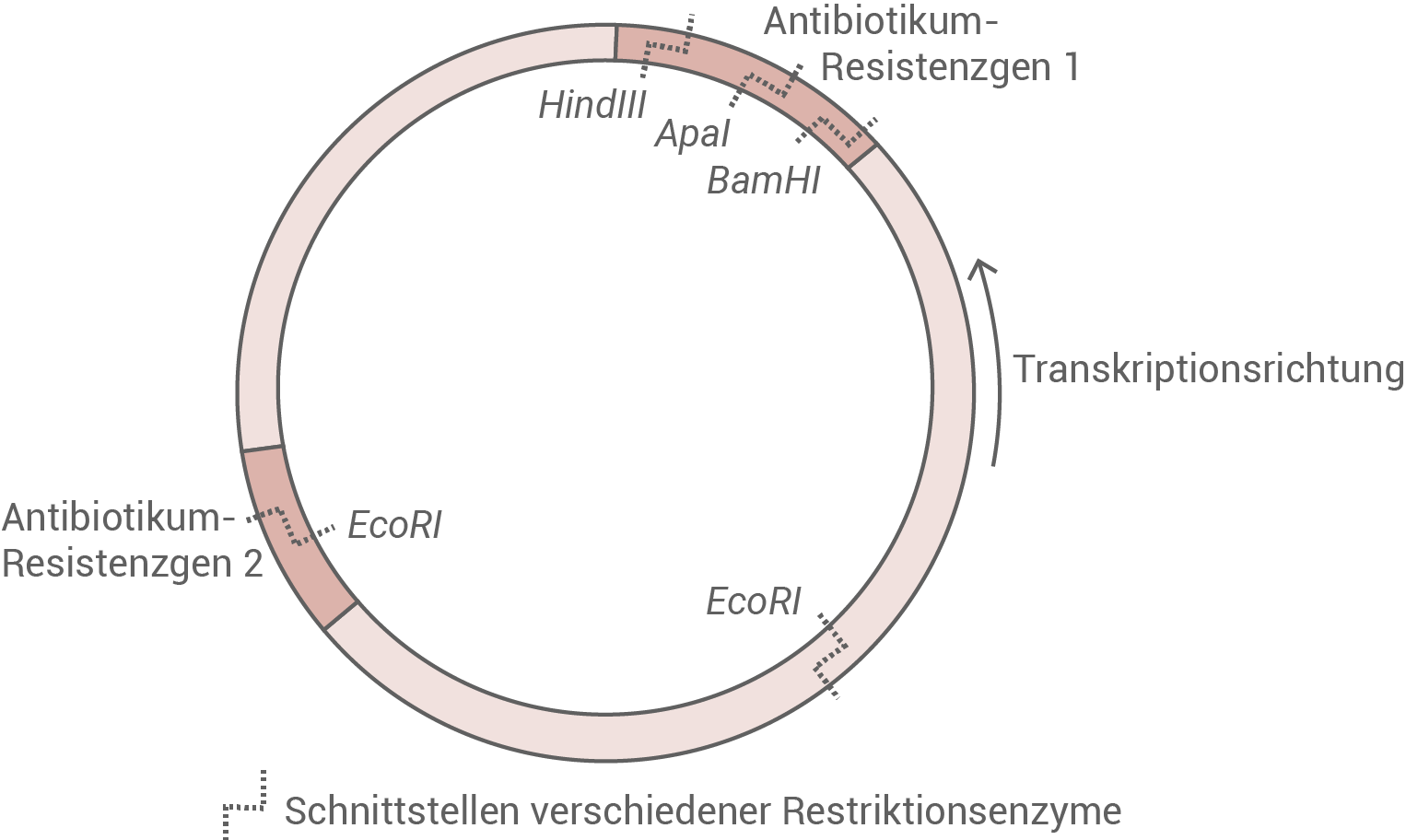
Abb. 4b: Plasmid (schematische Darstellung)
Um auf die Aktivierung des Pro-Chymosins durch Säure verzichten zu können, wäre alternativ auch eine direkte Herstellung des wirksamen Chymosins unter Verwendung eines entsprechend modifizierten Gens denkbar. In diesem Fall würde ein steuerbares Plasmid (Abb. 5) eingesetzt werden, welches zusätzlich den lac-Promotor mit lac-Operator sowie das entsprechende Regulatorgen aufweist.
Durch Zugabe von Laktose kann dadurch die Genexpression des modifizierten Gens induziert werden.
Durch Zugabe von Laktose kann dadurch die Genexpression des modifizierten Gens induziert werden.
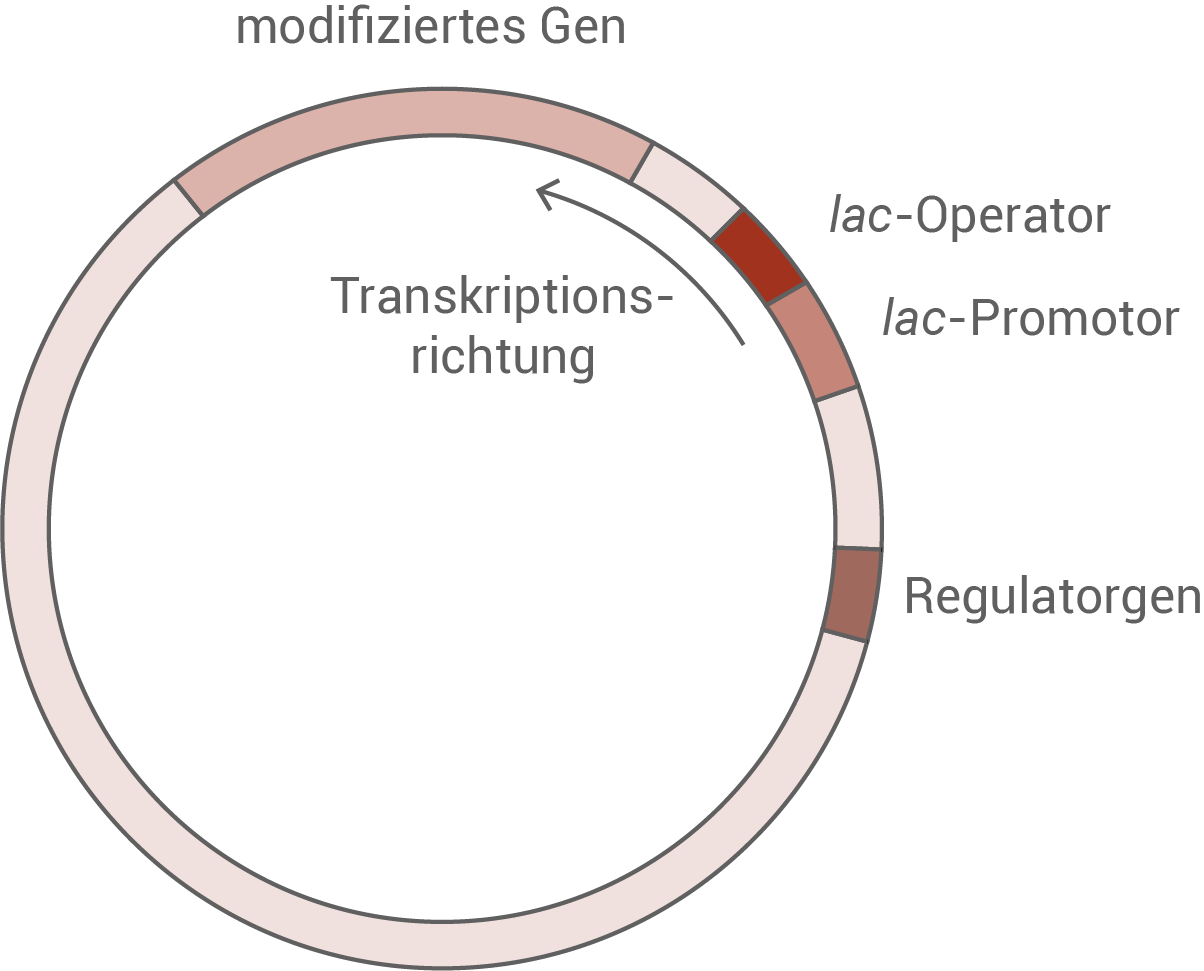
Abb. 5: Steuerbares Plasmid
4.1
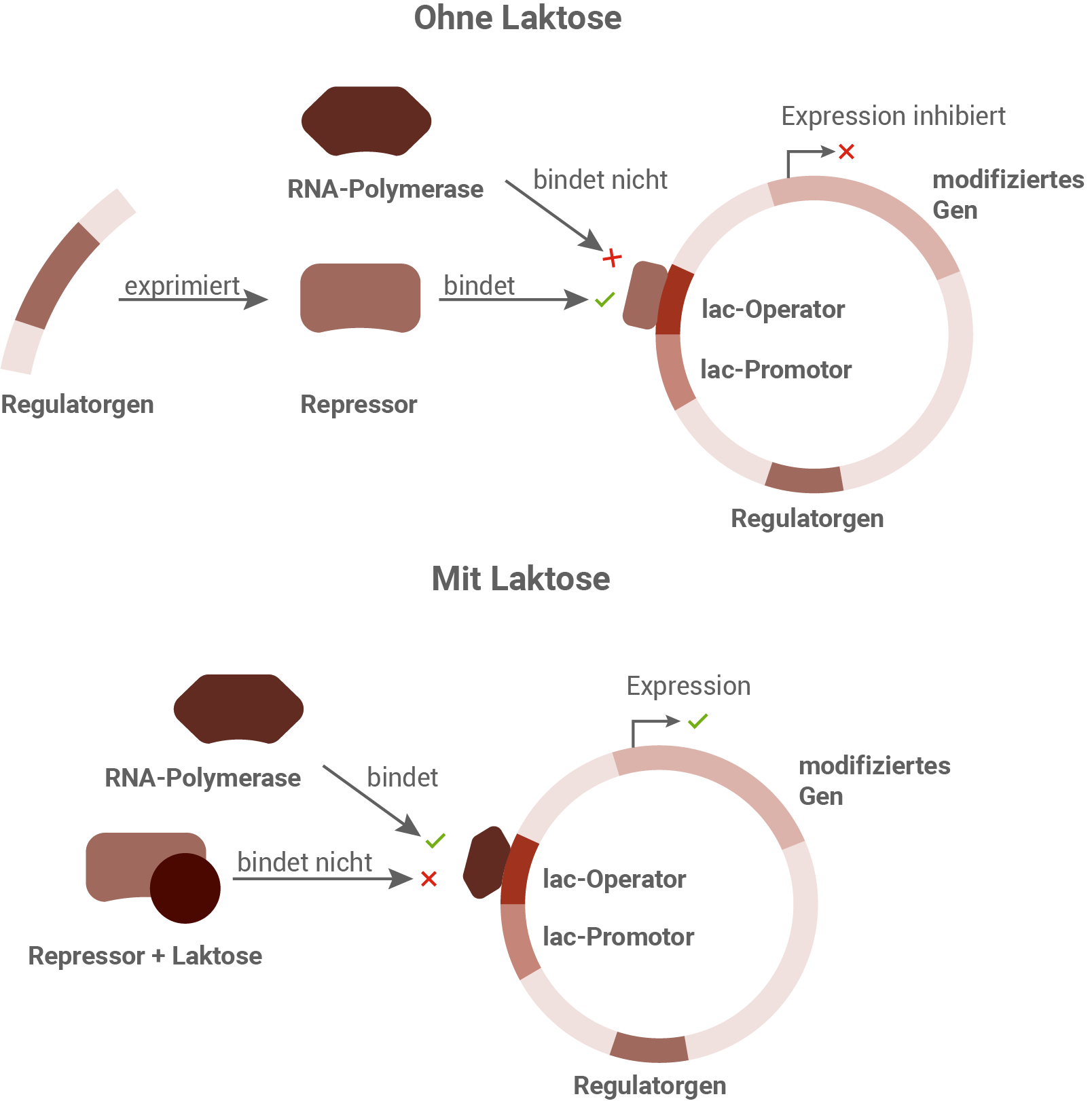
Stelle anhand beschrifteter Schemazeichnungen dar, wie Laktose die Expression des modifizierten Gens im steuerbaren Plasmid auslöst.
8 BE
4.2
Begründe, dass zur Produktion des wirksamen Chymosins durch eine Kultur transgener Bakterien ein steuerbares Plasmid eingesetzt werden sollte.
6 BE
40 BE
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Dargestellte Strukturen:
- Zellkern
- Kernpore
- Raues endoplasmatisches Retikulum
- Mitochondrium
- Dictyosom (Golgi-Apparat)
- Vesikel
- Cytoplasma
- Zellmembran
1.2
Bildung und Transport des Pro-Chymosins:

2
Produkte nach Einwirken des Chymosins:

3.1
Schritte der Plasmidtechnik zur Herstellung gentechnisch veränderter Bakterien:
- Erzeugung passender Überhänge von Fremdgen und Plasmid durch Restriktionsenzyme
- Ligation von Fremdgen und Plasmid
- Transformation in die Bakterienkultur
- Selektion der positiven (transgenen) Bakterien
3.2
Geeignete Restriktionsenzyme:
ApaI sollte nicht verwendet werden, da es keine Schnittstelle im Fremdgen aufweist, und das Fremdgen daher nicht in das Plasmid integrieren würde. EcoRI weist zwei Schnittstellen im Plasmid auf. Daher sollte es nicht verwendet werden. Ansonsten könnte es passieren, dass das Fremdgen nicht im Resistenzgen integriert. Eine Selektion wäre dann nicht mehr möglich. HindIII und BamHI weisen Schnittstellen im Fremdgen und in einem Resistenzgen des Plasmids auf. Durch eine Kombination dieser Restriktionsenzyme wird das Fremdgen aus dem Fragment ausgeschnitten, und kann in Resistenzgen 1 integrieren. Die Orientierung des Fremdgens im Plasmid stimmt mit der Transkriptionsrichtung beider Fragmente überein. HindIII und BamHI eignen sich daher für die Herstellung eines rekombinanten Plasmids.
4.1
Expression des modifizierten Gens im steuerbaren Plasmid:

4.2
Einsatz eines steuerbaren Plasmids:
Aktives Chymosin ist eine Protease. Wird das Gen unkontrolliert und kontinuierlich exprimiert, so könnte Chymosin unspezifisch verschiedene Proteine hydrolysieren, und das Wachstum der transgenen Bakterien stören, oder diese ganz abtöten. Dadurch wäre keine gentechnische Gewinnung des wirksamen Chymosins möglich.