Aufgabe 4 – Neurobiologie, Biochemie
Der Wirkstoff Morphin gehört zu den wichtigsten Mitteln zur Behandlung starker Schmerzen. Er ist ein Bestandteil des Opiums, des getrockneten Milchsaftes der Kapselfrüchte des Schlafmohns. Morphin bindet an Opioidrezeptoren in der präsynaptischen Membran von Nervenzellen der Schmerzbahn. Dadurch wird die Erregungsweiterleitung zwischen Nervenzellen der Schmerzbahn eingeschränkt und das Schmerzempfinden des Patienten gesenkt. Als Nebenwirkungen treten Atem- und Kreislaufbeschwerden auf.

Abb. 1: Schlafmohn
1
Beschreibe die Prozesse, die bei der Erregungsübertragung an einer Synapse ablaufen vom Eintreffen eines Aktionspotenzials bis zur Erregung der nachgeschalteten Zelle.
Um den Wirkmechanismus des Morphins zu verstehen, wurden Experimente an Nervenzellen durchgeführt. Hierbei entdeckten die Forscher, dass bei der Wirkung des Morphins das membrangebundene Enzym Adenylatcyclase und die Menge an cAMP (cyclisches Adenosinmonophosphat) eine entscheidende Rolle spielen. Abbildung 2 zeigt schematisch die Vorgänge an der präsynaptischen Membran des Endknöpfchens ohne und mit Morphin.
3 VP
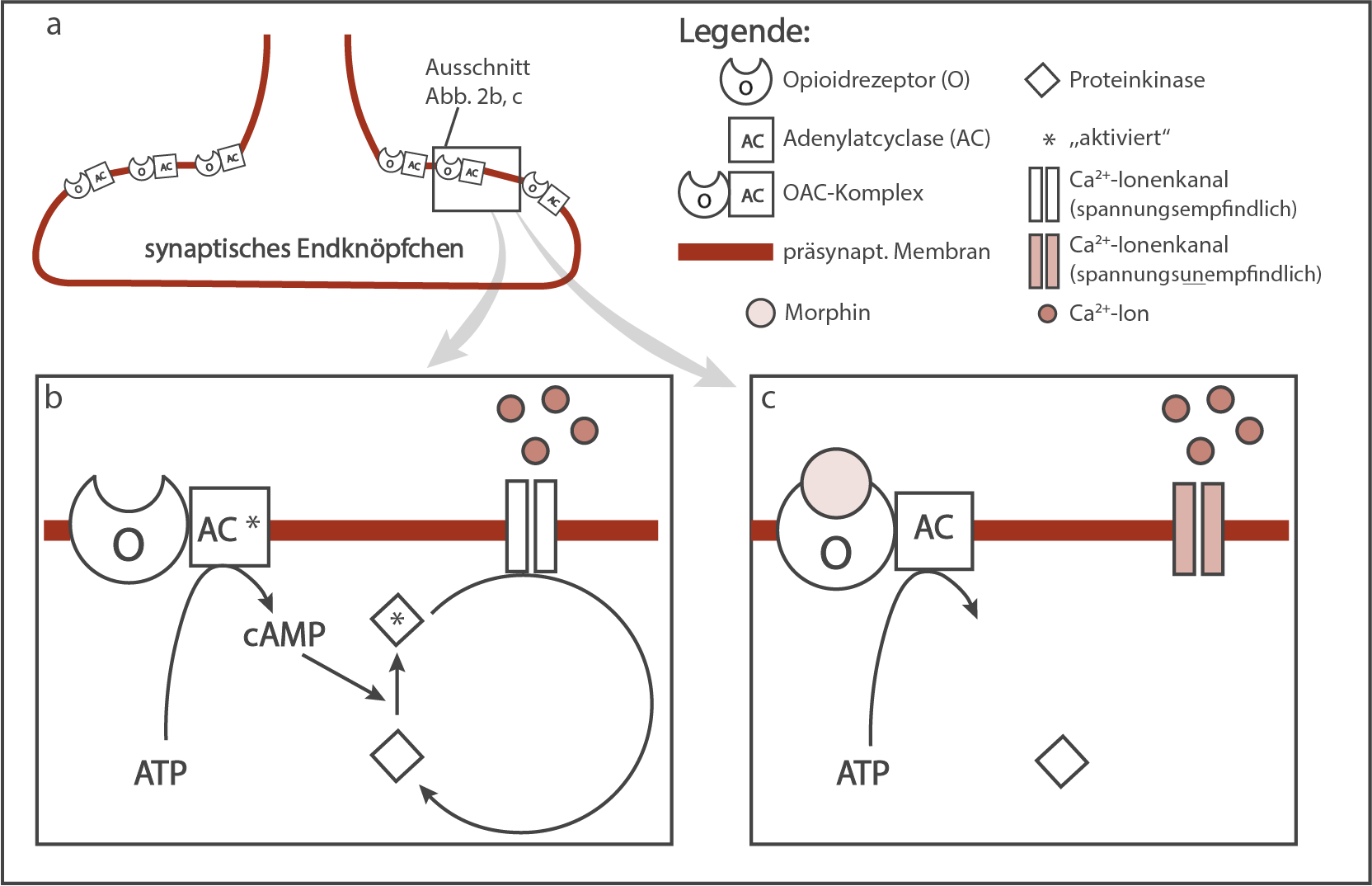
Abb. 2: a) Synaptisches Endknöpfchen mit OAC-Komplexen; b) und c) Vorgänge an der präsynaptischen Membran einer Nervenzelle ohne und mit Morphin (vereinfacht)
2
Erläutere unter Berücksichtigung von Abbildung 2 die schmerzstillende Wirkung des Morphins.
Bei länger andauernder Morphingabe stellt sich bei den Konsumenten bald eine Toleranz gegenüber dem Medikament ein. Das bedeutet, dass bei gleicher Morphindosis zunehmend weniger schmerzunterdrückende Wirkung erreicht wird. Um trotzdem eine Wirkung zu erreichen, muss die Dosis erhöht werden, was zur Abhängigkeit von Morphin führen kann. Diese Abhängigkeit macht sich besonders dann bemerkbar, wenn Morphin abrupt abgesetzt wird. Dabei treten Entzugserscheinungen auf, wie z. B. das Empfinden starker Schmerzen ohne entsprechend starke Schmerzreize. Abbildung 3 zeigt, wie sich die cAMP-Konzentratiön im Cytoplasma und die Anzahl der Opioidrezeptor-Adenylatcyclase-Komplexe (OAC-Komplexe) in der Zellmembran des Endknöpfchens bei Morphingabe und Morphinentzug verändern.
3 VP
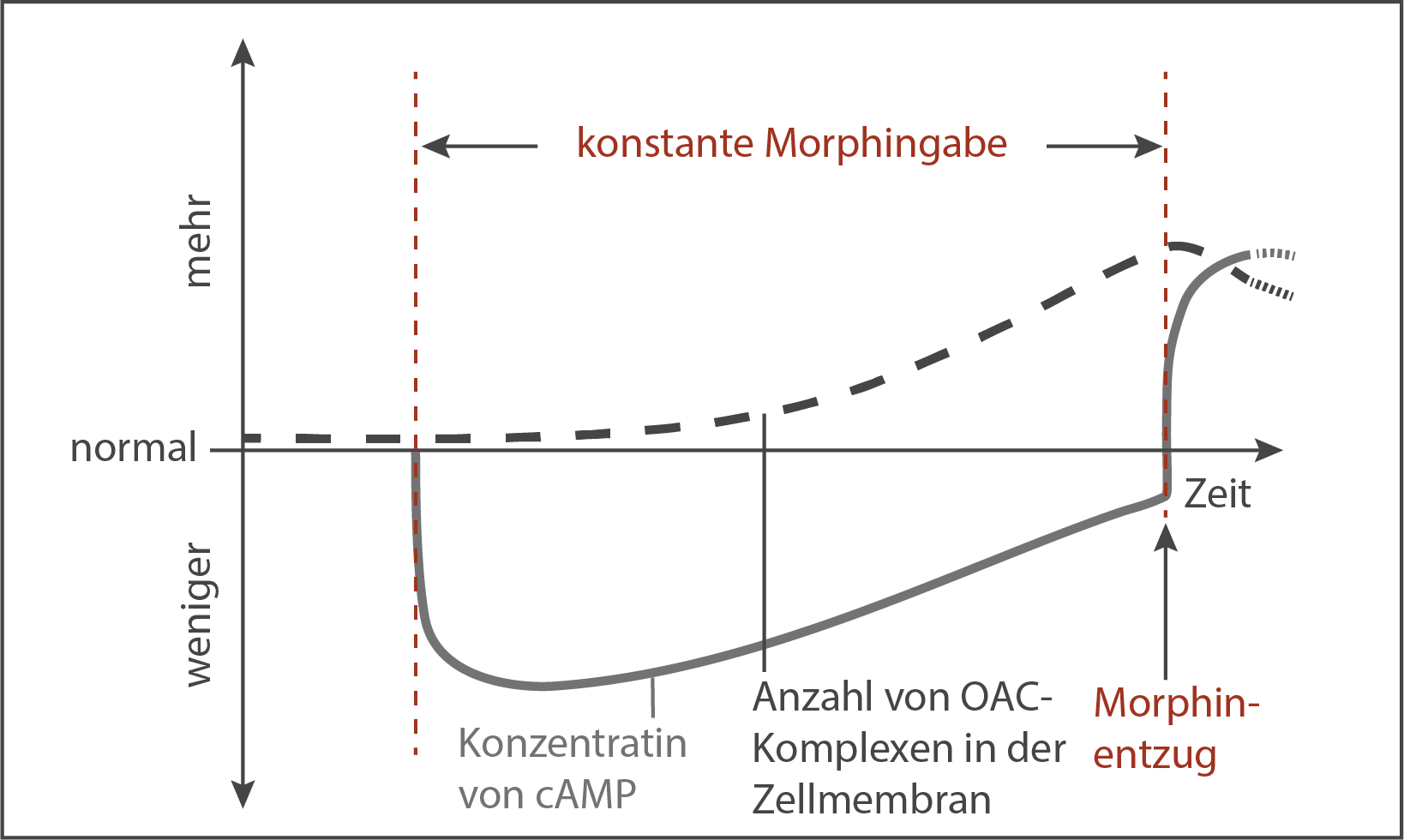
Abb. 3: Konzentration von cAMP und Anzahl OAC-Komplexe bei Morphingabe und Morphinentzug
3.1
Erkläre mithilfe der Abbildung 3 die Entwicklung der Toleranz bei der konstanten Gabe von Morphin.
3 VP
3.2
Erläutere mithilfe der Abbildung 3 das Zustandekommen der starken Schmerzen beim plötzlichen Entzug von Morphin.
Bei einer Schmerzbehandlung kann es zu einer Überdosierung und damit zu einer Vergiftung durch Morphin kommen. Hierbei kommt es zu starken Nebenwirkungen, die lebensbedrohlich werden können. Der Betroffene fällt in tiefe Bewusstlosigkeit, der Blutdruck sinkt und es kommt zum tödlichen Atemstillstand. Mithilfe des Medikaments Naloxon kann einer Morphinvergiftung entgegengewirkt werden. Abbildung 4 zeigt die Strukturformeln und die Wirkdauer von Naloxon und Morphin.
3 VP
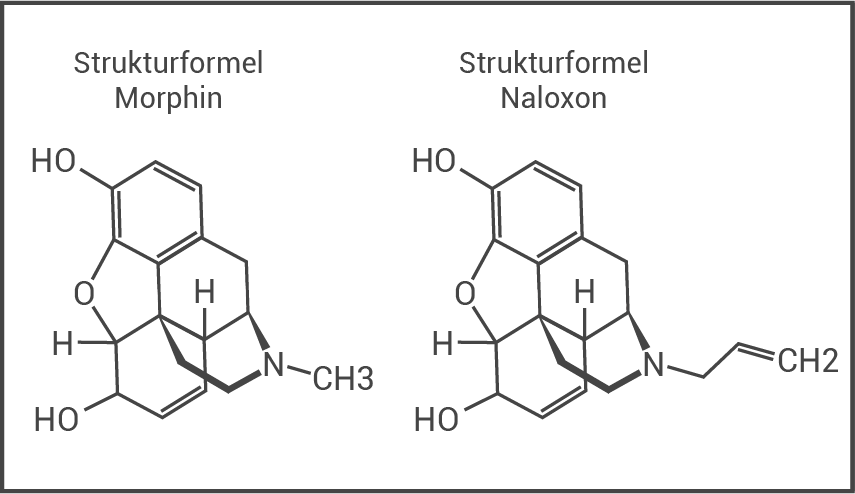
Abb. 4a: Strukturformel von Morphin und Naloxon
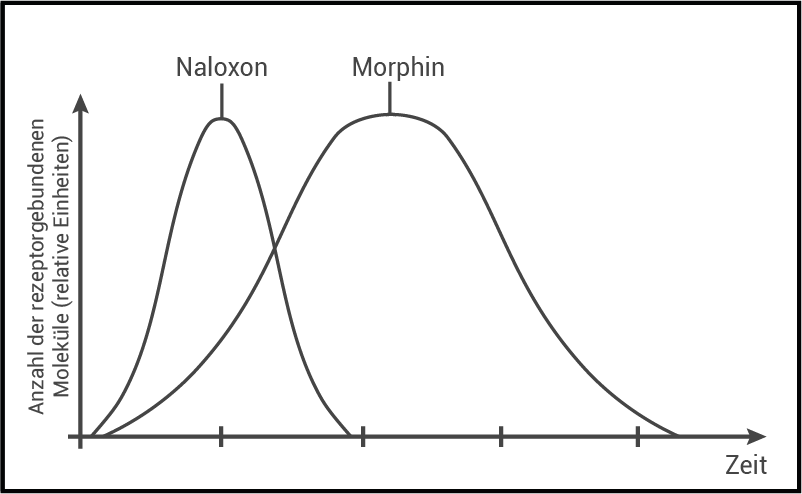
Abb. 4b: Bindung von Naloxon und Morphin an Opioidrezeptoren in Abhängigkeit von der Zeit
4.1
Beschreibe mithilfe von Abbildung 4a einen möglichen molekularen Mechanismus, der die Wirkung von Naloxon erklärt.
2 VP
4.2
Begründe mithilfe von Abbildung 4b, weshalb Naloxon bei einer Morphinvergiftung als Medikament eingesetzt werden kann und hierbei mehrmals verabreicht werden muss.
Die Gewinnung von Morphin aus dem Milchsaft des Schlafmohns ist sehr aufwändig. Deshalb versucht man seit langem Vorstufen des Morphins gentechnisch zu erzeugen. Wissenschaftlern ist es vor wenigen Jahren gelungen, E. coli-Bakterien gentechnisch so zu verändern, dass sie eine Vorstufe des Morphins, das Reticulin, synthetisieren. Um die fremden Gene in die Bakterienzellen einzufügen, haben sie rekombinante Plasmide hergestellt, die eine DNA-Sequenz mit den Genen enthält, welche für notwendige Enzyme der Biosynthese von Reticulin codieren.
3 VP
5
Beschreibe, wie das rekombinante Plasmid aufgebaut sein muss, um damit eine Selektion der rekombinanten Bakterien zu ermöglichen. Erkläre ein entsprechendes Selektionsverfahren.
3 VP
20 VP
1
Beschreibung der Prozesse an der Synapse:
 -Ionenkanälen, IPSP, Hyperpolarisation) dargestellt.
-Ionenkanälen, IPSP, Hyperpolarisation) dargestellt.
- Die Erregungsleitung bewirkt das Auslösen eines Aktionspotenzials/ einer Aktionspotenzialfolge am Axonende.
- Durch die folgende Depolarisation werden die spannungsgesteuerten Ca
-Ionenkanäle geöffnet und Ca
-Ionen strömen ein.
- Die Ca
-Ionen sind der Grund für die Wanderung der synaptischen Vesikel zur präsynaptischen Membran. Die folgende Membranverschmelzung (Exocytose) bewirkt die Entleerung des Inhalts (z.B. Acetylcholin) in den synaptischen Spalt.
- Die Transmittermoleküle diffundieren zur postsynaptischen Membran und binden an Membranrezeptoren, die mit Na
-Ionenkanälen gekoppelt sind (ligandengesteuerte Ionenkanäle).
- Es folgt die Öffnung der Na
-Ionenkanäle, Na
-Ionen strömen in die postsynaptische Zelle ein und es kommt zur Depolarisation der postsynaptischen Membran in Form eines erregenden postsynaptischen Potenzials (EPSP).
- Das Erreichen des Schwellenwertes erregt die nachgeschaltete Zelle.
2
Erläuterung der schmerzstillenden Wirkung des Morphins:
Die Opioidrezeptoren in der präsynaptischen Membran sind mit dem Enzym AC gekoppelt (OAC-Komplexe). Bei Besetzung des Rezeptors mit Morphin, kommt es zur Blockade vom Enzym AC. Das bedeutet, das Enzym ist inaktiv und katalysiert nicht die Umwandlung von ATP in cAMP, wodurch die Konzentration an cAMP gering ist. Daraus folgt, dass das Enzym Proteinkinase nicht aktiviert werden kann und die Ca -Ionenkanäle in der Membran der Endknöpfchen spannungsunempfindlich bleiben. Sie bleiben dadurch geschlossen (trotz Depolarisation) und es strömen keine Ca
-Ionenkanäle in der Membran der Endknöpfchen spannungsunempfindlich bleiben. Sie bleiben dadurch geschlossen (trotz Depolarisation) und es strömen keine Ca -Ionen ein.
-Ionen ein.
Es folgt das Ausbleiben der Vesikelwanderung, der Transmitterentleerung und der Depolarisation der postsynaptischen Membran. Die nachgeschaltete Nervenzelle wird nicht erregt und somit erfolgt keine Weiterleitung der Erregung auf Schmerzbahnen zum Gehirn. Es kommt nicht zur Schmerzempfindung. (Es wird nur die Erläuterung der Morphinwirkung (Abb. 2c) als Gegensatz zu Abb. 2b verlangt. Die Beschreibung der Wirkungskette sollte allerdings bei der Schmerzwahrnehmung im Gehirn, nicht an der Synapse, enden.)
Die Opioidrezeptoren in der präsynaptischen Membran sind mit dem Enzym AC gekoppelt (OAC-Komplexe). Bei Besetzung des Rezeptors mit Morphin, kommt es zur Blockade vom Enzym AC. Das bedeutet, das Enzym ist inaktiv und katalysiert nicht die Umwandlung von ATP in cAMP, wodurch die Konzentration an cAMP gering ist. Daraus folgt, dass das Enzym Proteinkinase nicht aktiviert werden kann und die Ca
Es folgt das Ausbleiben der Vesikelwanderung, der Transmitterentleerung und der Depolarisation der postsynaptischen Membran. Die nachgeschaltete Nervenzelle wird nicht erregt und somit erfolgt keine Weiterleitung der Erregung auf Schmerzbahnen zum Gehirn. Es kommt nicht zur Schmerzempfindung. (Es wird nur die Erläuterung der Morphinwirkung (Abb. 2c) als Gegensatz zu Abb. 2b verlangt. Die Beschreibung der Wirkungskette sollte allerdings bei der Schmerzwahrnehmung im Gehirn, nicht an der Synapse, enden.)
3.1
Entwicklung der Morphintoleranz:
Zu Beginn nimmt die cAMP-Konzentration durch das Morphin schnell ab. Durch die konstante Morphingabe vermehren sich die OAC-Komplexe in der Membran, wodurch bei gleichbleibender Morphinkonzentration immer mehr Opioidrezeptoren unbesetzt bleiben. Die AC-Aktivierung nimmt wieder zu, die cAMP-Konzentration steigt folglich wieder an und die Schmerzempfindlichkeit bzw. die Morphintoleranz nimmt zu.
Zu Beginn nimmt die cAMP-Konzentration durch das Morphin schnell ab. Durch die konstante Morphingabe vermehren sich die OAC-Komplexe in der Membran, wodurch bei gleichbleibender Morphinkonzentration immer mehr Opioidrezeptoren unbesetzt bleiben. Die AC-Aktivierung nimmt wieder zu, die cAMP-Konzentration steigt folglich wieder an und die Schmerzempfindlichkeit bzw. die Morphintoleranz nimmt zu.
3.2
Erläuterung der starken Schmerzen:
Wird plötzlich Morphin entzogen, kommt es zum Anstieg der cAMP-Konzentration. Das resultiert aus einer höheren Anzahl der OAC-Komplexe, durch die viel mehr Rezeptorkomplexe als vor der Morphintoleranz mit unbesetzten aktiviert werden können. Daraus folgt eine starke Aktivität der Proteinkinasen und eine hohe Spannungsempfindlichkeit der Ca -Ionenkanäle, die einen starken Ca
-Ionenkanäle, die einen starken Ca -Ioneneinstrom bei Erregung der Synapse, eine große Transmitterausschüttung und schlussendlich eine starke Erregung der schmerzleitenden Nervenbahnen bewirken. Es erfolgt eine starke Schmerzempfindung im Gehirn (Schmerzzentrum).
-Ioneneinstrom bei Erregung der Synapse, eine große Transmitterausschüttung und schlussendlich eine starke Erregung der schmerzleitenden Nervenbahnen bewirken. Es erfolgt eine starke Schmerzempfindung im Gehirn (Schmerzzentrum).
Wird plötzlich Morphin entzogen, kommt es zum Anstieg der cAMP-Konzentration. Das resultiert aus einer höheren Anzahl der OAC-Komplexe, durch die viel mehr Rezeptorkomplexe als vor der Morphintoleranz mit unbesetzten aktiviert werden können. Daraus folgt eine starke Aktivität der Proteinkinasen und eine hohe Spannungsempfindlichkeit der Ca
4.1
Beschreibung eines möglichen Mechanismus:
Naloxon und Morphin ähneln sich in ihrer chemischen Molekülstruktur und können daher um das Andocken am Opioidrezeptor konkurrieren. Dabei wird jedoch nicht die Adenylatcyclase bzw. der OAC-Komplex deaktiviert. Damit wird die Gegenwirkung (antagonistische Wirkung) zu Morphin (durch kompetitive Hemmung) erklärt.
Naloxon und Morphin ähneln sich in ihrer chemischen Molekülstruktur und können daher um das Andocken am Opioidrezeptor konkurrieren. Dabei wird jedoch nicht die Adenylatcyclase bzw. der OAC-Komplex deaktiviert. Damit wird die Gegenwirkung (antagonistische Wirkung) zu Morphin (durch kompetitive Hemmung) erklärt.
4.2
Begründung als Gegenmittel:
Abb. 4b zeigt, dass Naloxon viel schneller an die Opioidrezeptoren bindet als Morphin, da eine höhere Affinität zwischen Naloxon und Rezeptorprotein besteht. Die Morphinmoleküle werden vom Rezeptormolekül verdrängt und heben die Wirkung des Morphins auf (je nach Dosierung). Aus Abb. 4b lässt sich aber auch schließen, dass Naloxon kürzer wirkt als Morphin. Außerdem nimmt die Konzentration der rezeptorgebundenen Naloxonmoleküle schneller ab, da bei Naloxon vermutlich eine schnellere Ausscheidung oder ein schnellerer Abbau erfolgt.
Naloxon muss mehrfach nacheinander verabreicht werden, damit die frei gewordenen Opioidrezeptoren nicht wieder von den länger wirksamen Morphinmolekülen besetzt werden.
Abb. 4b zeigt, dass Naloxon viel schneller an die Opioidrezeptoren bindet als Morphin, da eine höhere Affinität zwischen Naloxon und Rezeptorprotein besteht. Die Morphinmoleküle werden vom Rezeptormolekül verdrängt und heben die Wirkung des Morphins auf (je nach Dosierung). Aus Abb. 4b lässt sich aber auch schließen, dass Naloxon kürzer wirkt als Morphin. Außerdem nimmt die Konzentration der rezeptorgebundenen Naloxonmoleküle schneller ab, da bei Naloxon vermutlich eine schnellere Ausscheidung oder ein schnellerer Abbau erfolgt.
Naloxon muss mehrfach nacheinander verabreicht werden, damit die frei gewordenen Opioidrezeptoren nicht wieder von den länger wirksamen Morphinmolekülen besetzt werden.
5
Beschreibung des rekombinanten Plasmids:
Damit eine Selektion der rekombinanten Bakterien ermöglicht wird, müssen sie Plasmide enthalten, die zusätzlich zum Reticulin-Gen noch mit einem weiteren charakteristischen Gen ausgestattet sind. Dieses muss ein Selektionsverfahren ermöglichen, weshalb beispielsweise Resistenzgene, das -Galactosidase-Gen oder Leuchtgene möglich sind.
Erklärung eines Selektionsverfahrens:
-Galactosidase-Gen oder Leuchtgene möglich sind.
Erklärung eines Selektionsverfahrens:
Beispiel eines Leuchtgens als Markergen:
Die Expression der Gene für die Reticulinsynthese wird mit einem Markergen gekoppelt, welches z.B. für das fluoreszierende Protein GFP codiert. Wenn die Bakterienkolonien mit UV-Licht beleuchtet werden, können die rekombinierten Stämme durch die grüne Fluoreszenz selektiert werden.
Damit eine Selektion der rekombinanten Bakterien ermöglicht wird, müssen sie Plasmide enthalten, die zusätzlich zum Reticulin-Gen noch mit einem weiteren charakteristischen Gen ausgestattet sind. Dieses muss ein Selektionsverfahren ermöglichen, weshalb beispielsweise Resistenzgene, das
Beispiel eines Leuchtgens als Markergen:
Die Expression der Gene für die Reticulinsynthese wird mit einem Markergen gekoppelt, welches z.B. für das fluoreszierende Protein GFP codiert. Wenn die Bakterienkolonien mit UV-Licht beleuchtet werden, können die rekombinierten Stämme durch die grüne Fluoreszenz selektiert werden.