Aufgabe 4 – Evolution
Der Nacktmull (Heterocephalus glaber, Abb. 1) ist eine außergewöhnliche Nagetierart der Halbwüsten Ostafrikas. Er lebt in Kolonien von bis zu  Tieren unterirdisch in engen Gangsystemen und weist im Vergleich zu anderen Nagetier-Arten (z. B. Ratte, siehe Abb. 2) einen besonderen Körperbau auf.
Tieren unterirdisch in engen Gangsystemen und weist im Vergleich zu anderen Nagetier-Arten (z. B. Ratte, siehe Abb. 2) einen besonderen Körperbau auf.
1
Beschreibe eine charakteristische Angepasstheit im Körperbau des Nacktmulls an seine Lebensweise und erläutere die Entstehung dieser Angepasstheit auf der Grundlage der synthetischen Evolutionstheorie.
3 VP
Außer im Körperbau unterscheiden sich Nacktmulle von anderen Säugetierarten durch eine verminderte Schmerzempfindlichkeit. Schmerzauslösende Reize werden bei Säugetieren von Schmerzsinneszellen registriert. Dabei handelt es sich um spezielle Nervenzellen, die in der Membran ihrer Dendriten Calciumionen-Kanäle aufweisen. Die durch einen Reiz hervorgerufene Veränderung der Calciumionen-Leitfähigkeit (siehe Abb. 3) führt letztendlich zur Bildung von Aktionspotenzialen am Axon der Schmerzsinneszelle.
2
Erkläre anhand der Messergebnisse (siehe Abb. 3), wie es zur Ausbildung eines Aktionspotenzials am Axon der Schmerzsinneszelle kommt. Begründe, welche Ergebnisse du bei entsprechenden Messungen am Nacktmull erwarten würdest.
4 VP
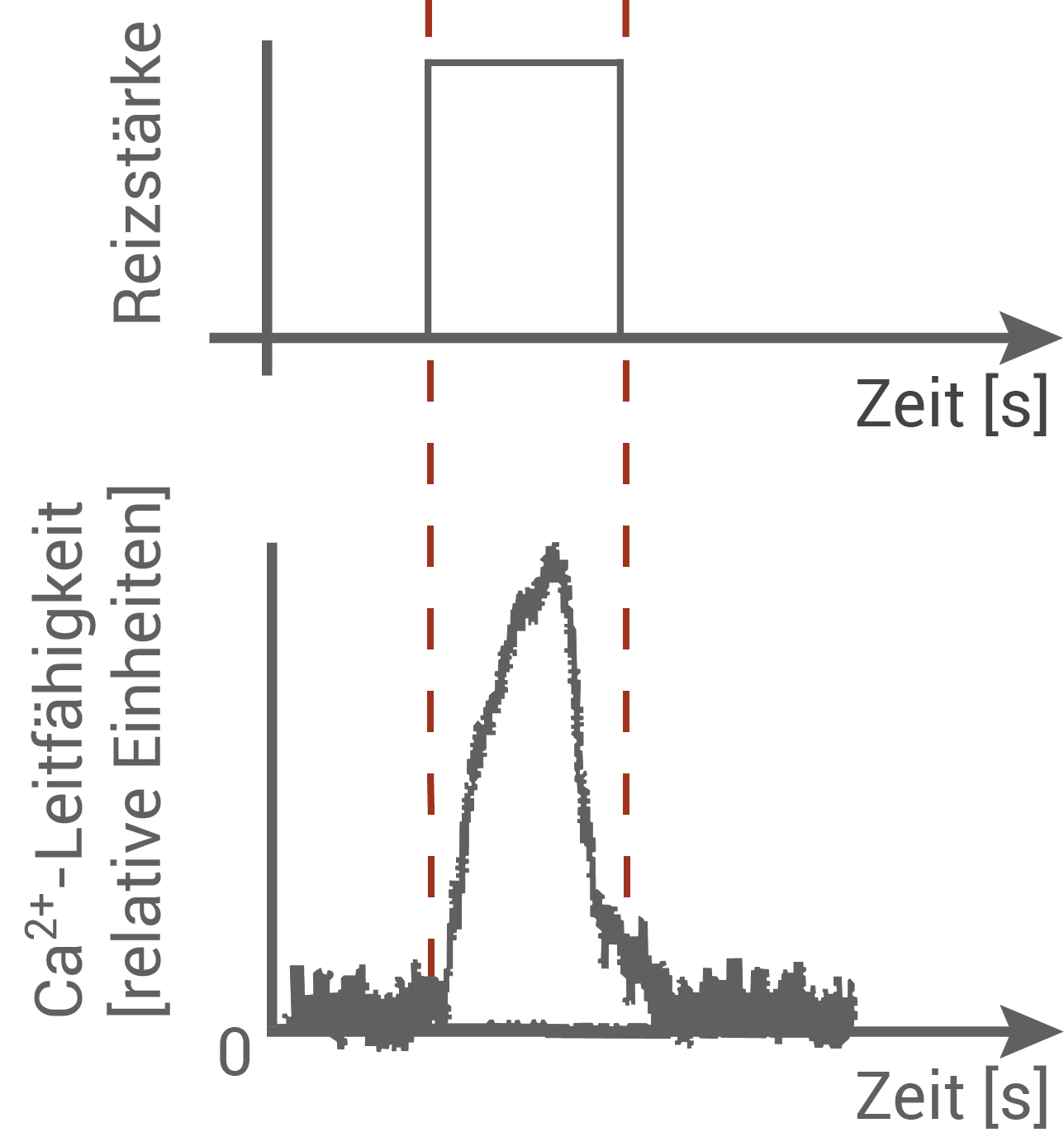
Abb. 3: Messungen an Schmerzsinneszellen
3.1
Erläutere mithilfe von Abbildung 4A die Wirkung von NGF auf die Schmerzempfindlichkeit der Ratte.
3 VP
3.2
Vergleiche die beiden möglichen Modelle (siehe Abb. 4C) mit dem NGF-Rezeptor der Ratte und erkläre die verminderte Schmerzempfindlichkeit des Nacktmulls.
2 VP
3.3
Ermittle die wahrscheinlichste DNA-Nukleotid-Sequenz für die 533. Aminosäure des NGF-Rezeptors des Nacktmulls (siehe Abb. 4B) und begründe deine Vermutung.
3 VP
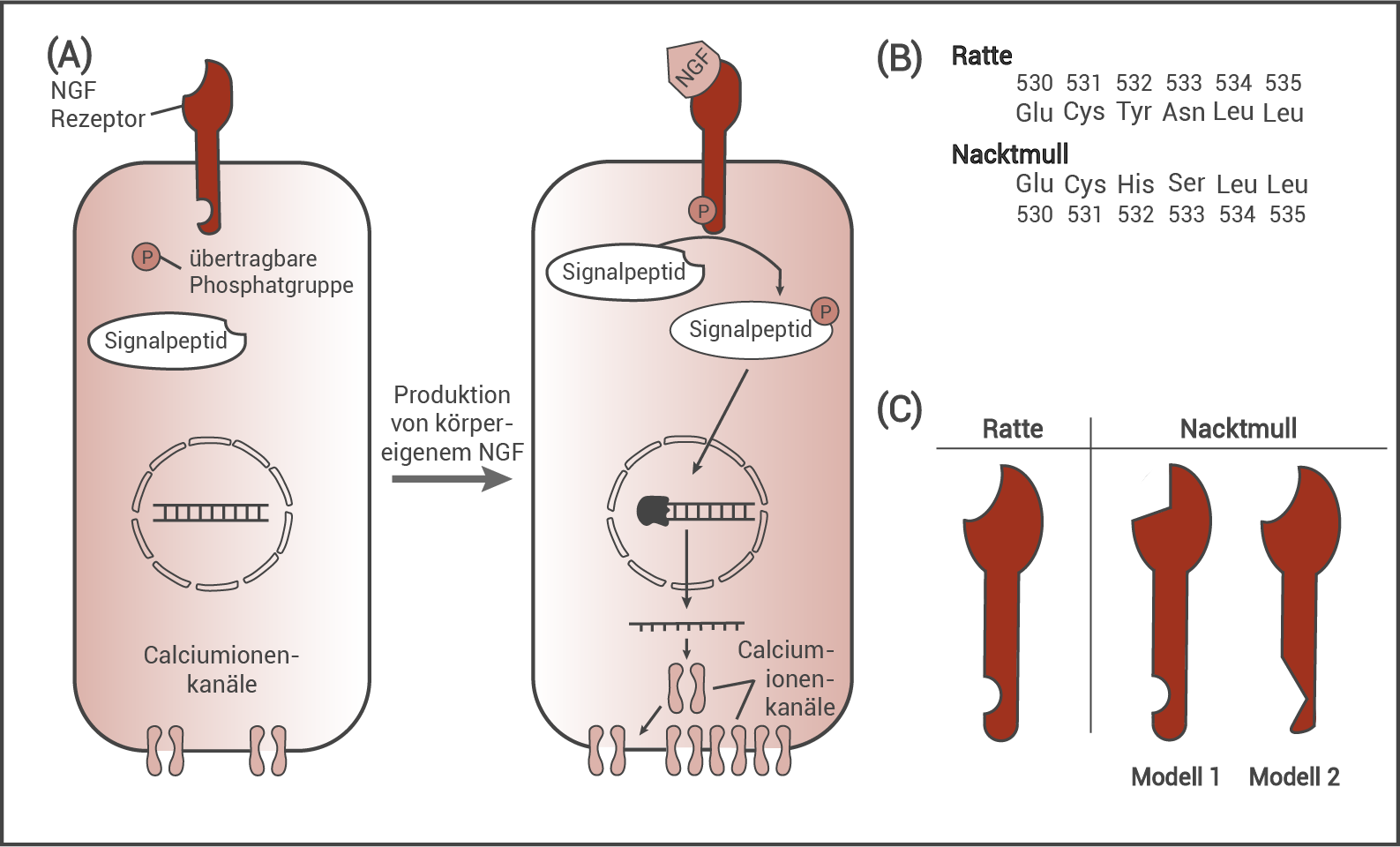
Abb. 4: (A) Intrazellulärer Signalweg an einer Schmerzsinneszelle; (B) Ausschnitt aus den Aminosäuresequenzen des NGF-Rezeptors bei Ratte und Nacktmull; (C) Modelle 1 und 2 zur Form des NGF-Rezeptors
Zur Überprüfung, welches der beiden Modelle zur Form des NGF-Rezeptors beim Nacktmull (siehe Abb. 4C) zutreffender ist, wurde folgendes Experiment durchgeführt: In Zellen von Säugetieren wurden gezielt Gene eingeführt und in Zellkulturen exprimiert. Man kultivierte so Zellen mit Ratten-NGF-Rezeptoren und solche mit Nacktmull-NGF-Rezeptoren. Außerdem konnten durch Einführung rekombinierter Ratten-Nacktmull-Gene auch Zellkulturen erzeugt werden, bei denen neu kombinierte (chimäre) NGF-Rezeptoren exprimiert wurden. Diese chimären NGF-Rezeptoren bestanden in ihrem extrazellulären Teil aus Ratten-NGF-Rezeptoren und in ihrem intrazellulären Teil aus Nacktmull-NGF-Rezeptoren. Außerdem exprimierten alle Zellkulturen auch die Calciumionen-Kanäle. An den Zellkulturen wurden Experimente mit NGF durchgeführt, deren Ergebnisse in Abbildung 5 dargestellt sind.
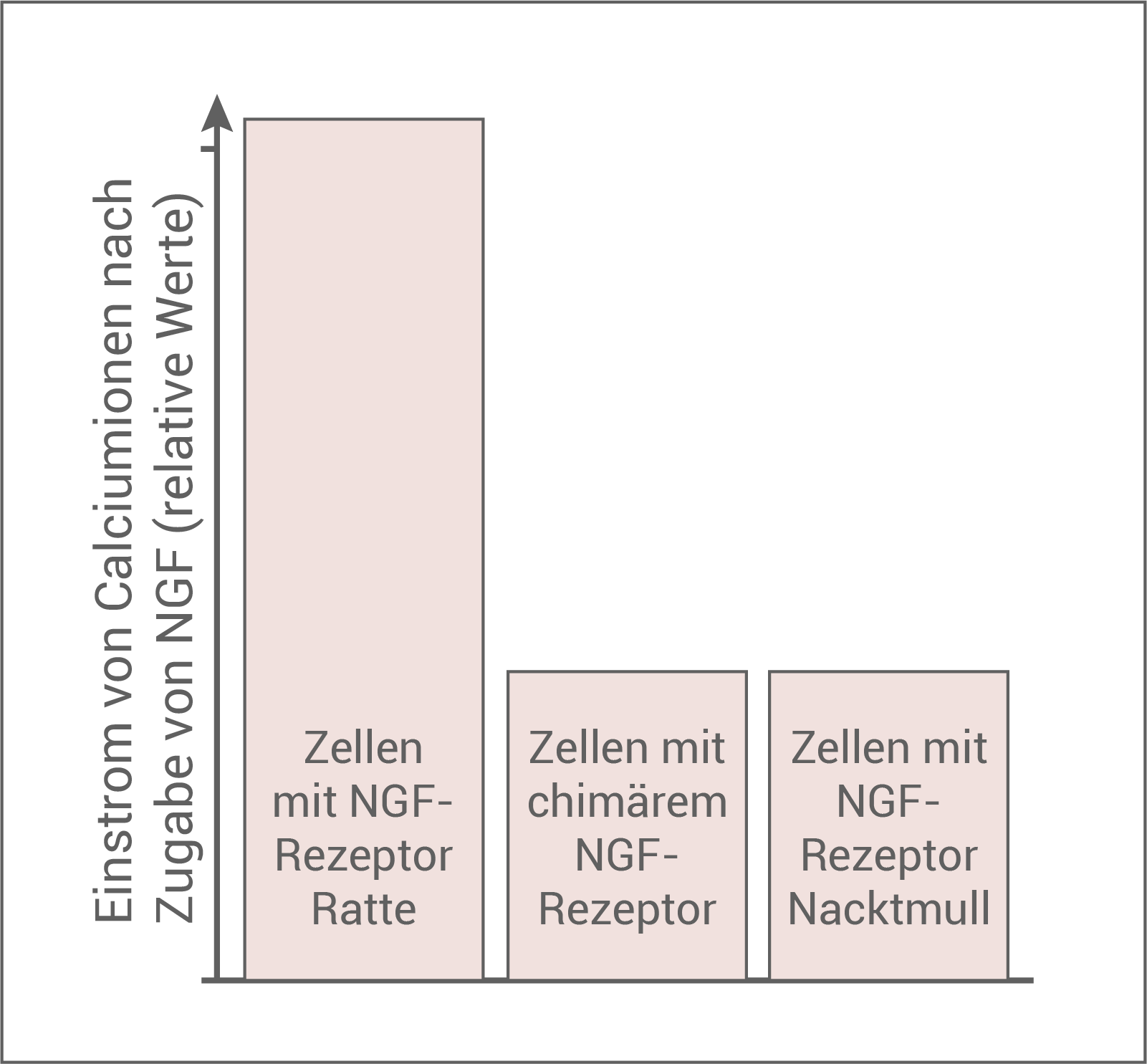
Abb. 5: Einstrom von Calciumionen in verschiedenartig manipulierte Zellen
4
Begründe anhand der Versuchsergebnisse (siehe Abb. 5), welches Modell zur Form des NGF-Rezeptors beim Nacktmull (siehe Abb. 4C) sicher widerlegt werden kann und inwieweit die Versuchsergebnisse für das andere Modell sprechen.
Kenntnisse über die Bedeutung von NGF und den zugehörigen Signalweg (siehe Abb. 4) bildeten eine Grundlage für die Entwicklung von Medikamenten zur Schmerzminderung bei Verletzungen und Entzündungen.
3 VP
5
Erläutere zwei Möglichkeiten, wie die Wirkung von NGF extrazellulär medikamentös unterbunden werden kann.
Bildnachweise [nach oben]
2 VP
20 VP
Ltshears - Trisha M Shears, Naked Mole Rat Eating, als gemeinfrei gekennzeichnet, Details auf Wikimedia Commons
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Beschreibung einer charakteristischen Angepasstheit (nur eine erforderlich):
Innerhalb einer unterirdisch lebenden Population entwickelten sich bei einigen Individuen durch Mutationen von Vorfahren des Nacktmulls neue Allele, deren Genprodukte zu einer geringen bzw. keiner Behaarung führten. Es entstand eine phänotypische Variabilität der Stärke der Fellausprägung durch Rekombination in der Population. Nacktmulle mit weniger Behaarung konnten sich in engen Gangsystemen, aufgrund von weniger Reibung, besser und schneller fortbewegen und waren somit für eine effiziente Nahrungssuche geeignet. Diese Individuen hatten damit einen Selektionsvorteil, da sie ihre Ressourcen besser nutzten und dadurch einen größeren Fortpflanzungserfolg (eine höhere reproduktive Fitness) erreichten. Diese betreffenden Allele häuften sich im laufen der Generationen im Genpool der Population an und die Allelhäufigkeit (Allelfrequenz) verschiebte sich in Richtung der Allele, die für die Ausprägung einer weitgehend unbeaahrten Haut verantwortlich waren.
- Kein oder stark reduziertes Fell, erkennbar sind nur Tasthaare. Aufgrund des unterirdischen Lebensraums ist ein schützendes Fell (vor Sonneneinstrahlung, Kälte) verzichtbar. Außerdem ist durch die Haarlosigkeit eine reibungsarme, verbesserte Fortbewegung in den engen Gängen möglich.
- Kaum ausgebildete Augen. Die Wahrnehmung visueller Reize ist im unterirdischen und lichtlosen Lebensraum unwichtig.
- Keine äußeren Ohrmuscheln. Die Ausbreitung akustischer Signale ist in engen Gangsystemen eingeschränkt. Die genaue Lokalisierung ist von geringer Bedeutung.
- Prägnante, nach vorne gebundene Nagezähne. Diese können als (Grab-)Werkzeuge in den unterirdischen Gängen verwendet werden.
Innerhalb einer unterirdisch lebenden Population entwickelten sich bei einigen Individuen durch Mutationen von Vorfahren des Nacktmulls neue Allele, deren Genprodukte zu einer geringen bzw. keiner Behaarung führten. Es entstand eine phänotypische Variabilität der Stärke der Fellausprägung durch Rekombination in der Population. Nacktmulle mit weniger Behaarung konnten sich in engen Gangsystemen, aufgrund von weniger Reibung, besser und schneller fortbewegen und waren somit für eine effiziente Nahrungssuche geeignet. Diese Individuen hatten damit einen Selektionsvorteil, da sie ihre Ressourcen besser nutzten und dadurch einen größeren Fortpflanzungserfolg (eine höhere reproduktive Fitness) erreichten. Diese betreffenden Allele häuften sich im laufen der Generationen im Genpool der Population an und die Allelhäufigkeit (Allelfrequenz) verschiebte sich in Richtung der Allele, die für die Ausprägung einer weitgehend unbeaahrten Haut verantwortlich waren.
2
Erklärung der Ausbildung eines Aktionspotenzials:
Aus Abb. 2 lässt sich entnehmen, dass kurz nach Einsetzen eines Reizes (mit konstanter Stärke) sich die Leitfähigkeit von -Ionen an den Schmerzsinneszellen von Säugern erhöht. Das wird verursacht durch die Öffnung der
-Ionen an den Schmerzsinneszellen von Säugern erhöht. Das wird verursacht durch die Öffnung der  -Ionenkanäle in der Dendritenmembran, woraufhin
-Ionenkanäle in der Dendritenmembran, woraufhin  -Ionen in das Zellplasma einströmen (entlang des Konzentrationsgradienten) und die Dendritenmembran depolarisieren. Es kommt zu einer elektrotonischen Ausbreitung der Erregung bis zum Axonhügel, wo bei Überschreitung des Schwellenwertes zur Entstehung von Aktionspotenzialen (AP) am Axon der Schmerzsinneszelle kommt.
Begründung der erwarteten Ergebnisse beim Nacktmull:
-Ionen in das Zellplasma einströmen (entlang des Konzentrationsgradienten) und die Dendritenmembran depolarisieren. Es kommt zu einer elektrotonischen Ausbreitung der Erregung bis zum Axonhügel, wo bei Überschreitung des Schwellenwertes zur Entstehung von Aktionspotenzialen (AP) am Axon der Schmerzsinneszelle kommt.
Begründung der erwarteten Ergebnisse beim Nacktmull:
Bei gleicher Reizstärke kommt es, aufgrund von z.B. weniger vorhandenen -Ionenkanälen in der Dendritemembran, zu einem schwächeren bzw. keinem
-Ionenkanälen in der Dendritemembran, zu einem schwächeren bzw. keinem  -Ioneneinstrom und dadurch zu einem geringeren Anstieg der
-Ioneneinstrom und dadurch zu einem geringeren Anstieg der  -Leitfähigkeit. Am Axonhügel der Schmerzsinneszelle wird darauffolgend eine geringe bzw. keine AP-Frequenz ausgelöst (bei unterschwelliger Depolarisation) und führt somit zu einer verminderten Schmerzempfindlichkeit. Vergleichbare AP-Frequenzen (also Schmerzempfindungen) von Sinneszellen anderer Säugetierarten würden beim Nacktmull so erst bei stärkeren Reizen erreicht werden.
-Leitfähigkeit. Am Axonhügel der Schmerzsinneszelle wird darauffolgend eine geringe bzw. keine AP-Frequenz ausgelöst (bei unterschwelliger Depolarisation) und führt somit zu einer verminderten Schmerzempfindlichkeit. Vergleichbare AP-Frequenzen (also Schmerzempfindungen) von Sinneszellen anderer Säugetierarten würden beim Nacktmull so erst bei stärkeren Reizen erreicht werden.
Aus Abb. 2 lässt sich entnehmen, dass kurz nach Einsetzen eines Reizes (mit konstanter Stärke) sich die Leitfähigkeit von
Bei gleicher Reizstärke kommt es, aufgrund von z.B. weniger vorhandenen
3.1
Erläuterung der NGF-Wirkung auf die Schmerzempfindlichkeit:
Nach dem Schlüssel-Schloss-Prinzip kommt es zur Anlagerung von NGF an den extrazellzlären Teil des NGF-Rezeptors (Transmembranprotein). Der intrazelluläre Teil bindet daraufhin eine Phosphatgruppe und überträgt diese auf ein Signalpeptid im Zellplasma. Diese phosphorylierte Form des Peptids wandert in den Zellkern und bewirkt die Aktivierung des Gens, das für den -Ionenkanal codiert. Daraus folgt eine verstärkte Bildung von
-Ionenkanal codiert. Daraus folgt eine verstärkte Bildung von  -Ionenkanälen, die in die Dendritenmembran der Schmerzsinneszellen eingebaut werden. Erfolgt eine Reizung strömen somit mehr
-Ionenkanälen, die in die Dendritenmembran der Schmerzsinneszellen eingebaut werden. Erfolgt eine Reizung strömen somit mehr  -Ionen in die Dendriten und führt zu einer stärkeren Depolarisation. Folglich kommt es zu einer höheren AP-Frequenz als ohne NGF-Einfluss. Also wird die Schmerzempfindlichkeit der Ratte durch die NGF-Wirkung erhöht.
-Ionen in die Dendriten und führt zu einer stärkeren Depolarisation. Folglich kommt es zu einer höheren AP-Frequenz als ohne NGF-Einfluss. Also wird die Schmerzempfindlichkeit der Ratte durch die NGF-Wirkung erhöht.
Nach dem Schlüssel-Schloss-Prinzip kommt es zur Anlagerung von NGF an den extrazellzlären Teil des NGF-Rezeptors (Transmembranprotein). Der intrazelluläre Teil bindet daraufhin eine Phosphatgruppe und überträgt diese auf ein Signalpeptid im Zellplasma. Diese phosphorylierte Form des Peptids wandert in den Zellkern und bewirkt die Aktivierung des Gens, das für den
3.2
Vergleich der Modelle mit dem NFG-Rezeptor der Ratte:
Beide Modelle des NGF-Rezeptors des Nacktmulls weisen jeweils eine andere Form der Molekülbindestelle als die vom NGF-Rezeptors der Ratte auf:
Eine mögliche Erklärung wäre ein unterbrochener oder ineffizienter Signaltransduktionsweg, der zur Ausprägung der -Ionenkanäle führt:
-Ionenkanäle führt:
 -Ionenkanalprotein codieren, vermindert werden oder nicht zustande kommen. Trotz der Anwesenehit von NGF wäre die Anzahl dieser Kanäle in der Dendritenmembran relativ gering.
-Ionenkanalprotein codieren, vermindert werden oder nicht zustande kommen. Trotz der Anwesenehit von NGF wäre die Anzahl dieser Kanäle in der Dendritenmembran relativ gering.
Beide Modelle des NGF-Rezeptors des Nacktmulls weisen jeweils eine andere Form der Molekülbindestelle als die vom NGF-Rezeptors der Ratte auf:
- Modell 1: Im Vergleich zum NGF-Rezeptors der Ratte ist die intrazelluläre Bindestelle für die Phosphatgruppe unverändert. Die extrazelluläre Bindestelle hat eine andere Form.
- Modell 2: Hier ist die extrazelluläre Bindestelle gleich und die intrazelluläre Phosphatbindestelle unterscheidet sich.
Eine mögliche Erklärung wäre ein unterbrochener oder ineffizienter Signaltransduktionsweg, der zur Ausprägung der
- Nach Modell 1 würde die räumlich veränderte extrazelluläre Bindestelle die Affinität des Rezeptors zu NGF herabsetzen oder die Bindung von NGF komplett verhindern.
- Nach Modell 2 könnte die Bindung der Phosphatgruppe an den intrazellulären Bereich des Rezeptors oder ihre Übertragung auf das Signalpeptid beeinträchtigt werden.
3.3
Ermittlung der wahrscheinlichsten DNA-Nukleotid-Sequenz:
 Begründung der Vermutung:
Begründung der Vermutung:
Die Aminosäure Serin ist redundant codiert (sechs mögliche Basentripletts). Dabei weisen zwei davon in der ersten Base und in der zweiten
und in der zweiten  auf, die anderen A und G. Die wahrscheinlichste Sequenz ist hier die mit der markierten Mutation in der zweiten Base von
auf, die anderen A und G. Die wahrscheinlichste Sequenz ist hier die mit der markierten Mutation in der zweiten Base von  nach
nach  da die Veränderung mit einer einzigen (Punkt)-Mutation erklärt werden kann. Die zweite Möglichkeit (Asn: 3' TTG/A 5'
da die Veränderung mit einer einzigen (Punkt)-Mutation erklärt werden kann. Die zweite Möglichkeit (Asn: 3' TTG/A 5'  Ser: 3' AGG/A 5') ist unwahrscheinlicher, da der Austausch zweier Nukleotide erforderlich wäre.
Ser: 3' AGG/A 5') ist unwahrscheinlicher, da der Austausch zweier Nukleotide erforderlich wäre.

Die Aminosäure Serin ist redundant codiert (sechs mögliche Basentripletts). Dabei weisen zwei davon in der ersten Base
4
Begründung der Interpretation der Versuchsergebnisse:
Es empfiehlt sich zunächst die Versuchsergebnisse aus Abb. 4 zu beschreiben. Nach NGF-Zugabe und Reizung ist der -Ioneneinstrom bei den Zellen mit dem Nacktmull-NGF-Rezeptor und dem chimären NGF-Rezeptor deutlich schwächer als der bei dem mit NGF-Rezeptor der Ratte.
-Ioneneinstrom bei den Zellen mit dem Nacktmull-NGF-Rezeptor und dem chimären NGF-Rezeptor deutlich schwächer als der bei dem mit NGF-Rezeptor der Ratte.
Modell 1 kann widerlegt werden, da der chimäre NGF-Rezeptor (Außenseite Rattenrezeptor, Innenseite Nacktmullrezeptor) nach NGF-Zugabe einen genauso geringen -Ioneneinstrom verursacht. In Modell 1 müsste der chimäre Rezeptor genau dem NGF-Rezeptor entsprechen, da ein gegenüber dem Rattenrezeptor unveränderter intrazellulärer Teil postuliert. Der
-Ioneneinstrom verursacht. In Modell 1 müsste der chimäre Rezeptor genau dem NGF-Rezeptor entsprechen, da ein gegenüber dem Rattenrezeptor unveränderter intrazellulärer Teil postuliert. Der  -Ioneneinstrom müsste daher dann genau gleich sein, was nicht der Fall ist und somit die Annahmen von Modell 2 stützt. Hier ist die Innenseite des Nacktmullrezeptors verändert, wodurch die Phosphatgruppe nicht gebunden und übertragen werden kann (also unterbrochener Signalweg) und es käme nur zu einem geringen
-Ioneneinstrom müsste daher dann genau gleich sein, was nicht der Fall ist und somit die Annahmen von Modell 2 stützt. Hier ist die Innenseite des Nacktmullrezeptors verändert, wodurch die Phosphatgruppe nicht gebunden und übertragen werden kann (also unterbrochener Signalweg) und es käme nur zu einem geringen  -Ioneneinstrom.
-Ioneneinstrom.
Es empfiehlt sich zunächst die Versuchsergebnisse aus Abb. 4 zu beschreiben. Nach NGF-Zugabe und Reizung ist der
Modell 1 kann widerlegt werden, da der chimäre NGF-Rezeptor (Außenseite Rattenrezeptor, Innenseite Nacktmullrezeptor) nach NGF-Zugabe einen genauso geringen
5
Erläuterung von Möglichkeiten, die Wirkung von NGF zu unterbinden (zwei erforderlich):
 -Ionenkanäle (in der Membran) wird also nicht erhöht, wodurch die schmerzauslösenden Reize nicht mehr zu einem erhöhten
-Ionenkanäle (in der Membran) wird also nicht erhöht, wodurch die schmerzauslösenden Reize nicht mehr zu einem erhöhten  -Ioneneinstrom, also zu einem geringeren Schmerzempfinden führen.
-Ioneneinstrom, also zu einem geringeren Schmerzempfinden führen.
- Kompetitiver Hemmstoff (NGF-ähnliche räumliche Struktur), welcher an die extrazellulären NGF-Bindestellen andockt und blockiert, ohne den Signalweg auszulösen.
- Anti-NGF-Antikörper, die spezifisch an NGF binden, wodurch NGF nicht mehr an den NGF-Rezeptor andocken kann.
- Enzym, welches NGF spaltet, wodurch keine Bindung von NGF an die NGF-Bindestelle des Rezeptors erfolgen kann.
- Wirkstoff, der an den NGF-Rezeptor bindet und dadurch die räumliche Struktur der extrazellulären NGF-Bindestelle verändert. Somit kann NGF nicht mehr binden.

