Aufgabe 3 – Stickstoffkreislauf
Für alle Organismen ist das Element Stickstoff lebensnotwendig. Obwohl die Luft aus etwa 78 % Stickstoff besteht, ist diese Stickstoffquelle für die meisten Pflanzen nicht nutzbar. Stickstoff wird von Pflanzen unter anderem in Form von Ammonium-Ionen  und Nitrat-Ionen
und Nitrat-Ionen  über die Wurzeln aufgenommen.
über die Wurzeln aufgenommen.
 aus, der als Bestandteil von Gülle als Dünger auf Felder ausgebracht wird. Bodenbakterien enthalten das Enzym Urease, das die Spaltung von Harnstoff in Ammoniak
aus, der als Bestandteil von Gülle als Dünger auf Felder ausgebracht wird. Bodenbakterien enthalten das Enzym Urease, das die Spaltung von Harnstoff in Ammoniak  und Kohlenstoffdioxid
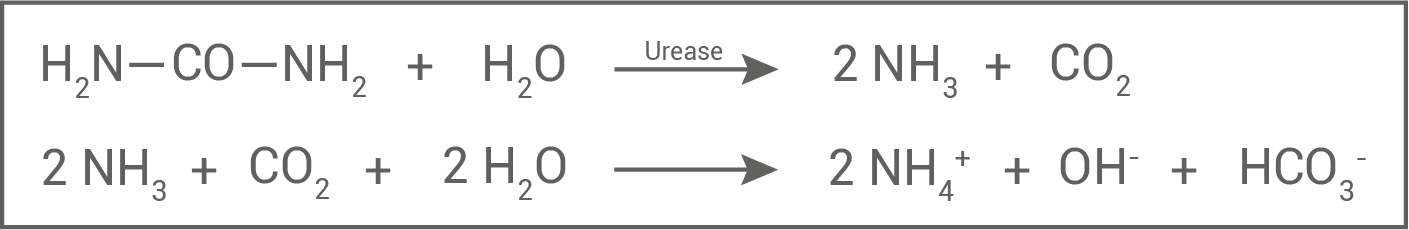
und Kohlenstoffdioxid  katalysiert. Diese Produkte reagieren in wässriger Lösung zu verschiedenen Ionen weiter (Abbildung 1) und machen so den Stickstoff für Pflanzen verfügbar.
katalysiert. Diese Produkte reagieren in wässriger Lösung zu verschiedenen Ionen weiter (Abbildung 1) und machen so den Stickstoff für Pflanzen verfügbar.
1
Nenne zwei stickstoffhaltige Biomoleküle und deren Funktion im pflanzlichen Organismus.
Säugetiere scheiden Stickstoff in Form von Harnstoff
2 VP

Abb. 1: Durch Urease katalysierte Umsetzung von Harnstoff und Reaktion der Produkte mit Wasser
2.1
Ordne das Enzym Urease einer Stoffklasse zu. Benenne die drei verschiedenen Strukturebenen des Ureasemoleküls und nenne die Bindungen bzw. Kräfte, durch welche diese Strukturen jeweils stabilisiert werden.
3 VP
2.2
Stelle den Ablauf der durch Urease katalysierten Reaktion in einer Abfolge beschrifteter Schemazeichnungen dar.
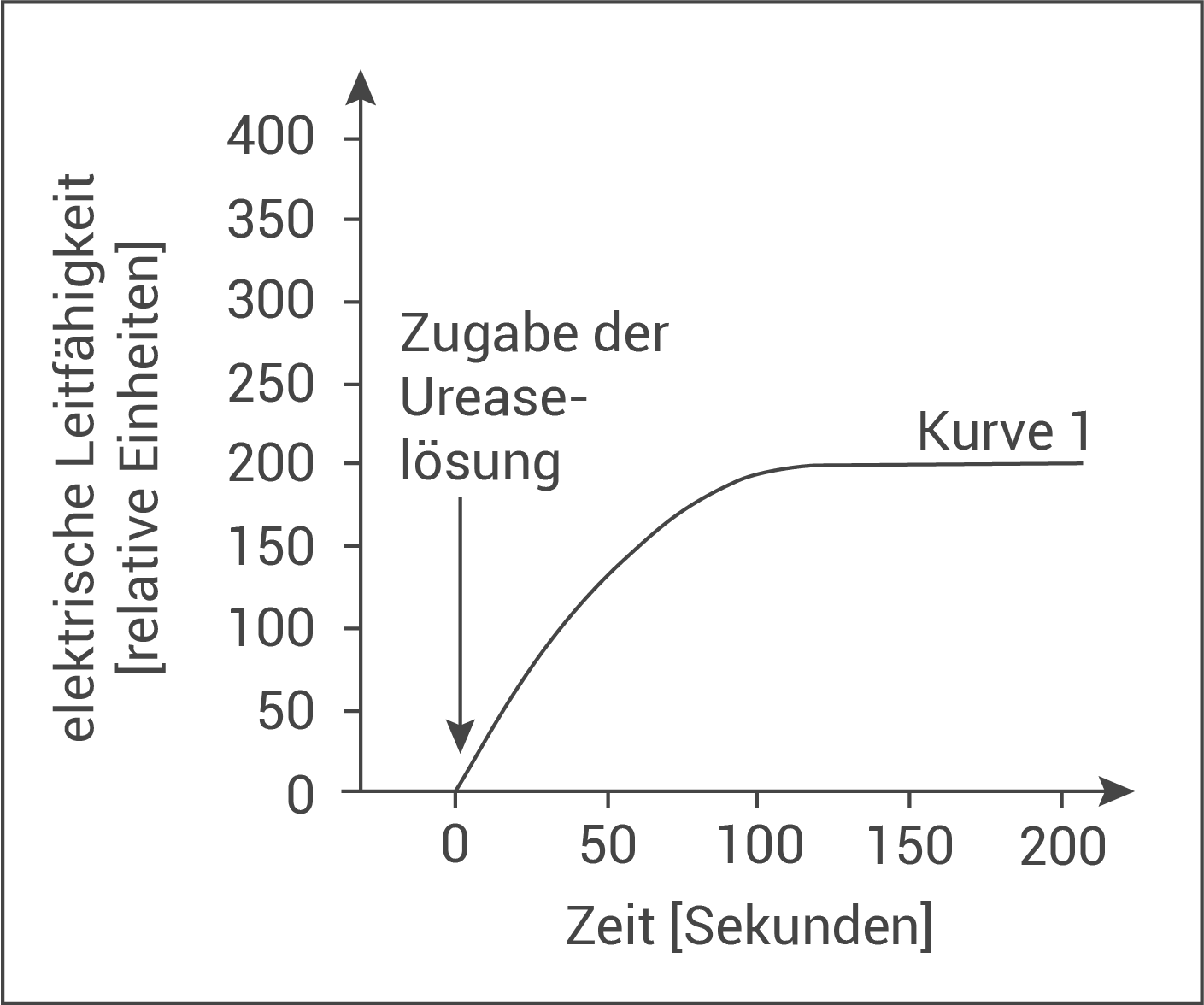
In einem Schülerpraktikum wird die Enzymaktivität der Urease bei verschiedenen Bedingungen untersucht. Dazu wird in drei Harnstofflösungen die elektrische Leitfähigkeit gemessen. Zum Zeitpunkt Null wird die Ureaselösung zugesetzt. Tabelle 1 zeigt die drei Versuchsansätze. Kurve 1 in Abbildung 2 zeigt die Ergebnisse der Leitfähigkeitsmessung bei Versuchsansatz A.
3 VP
| Versuchs- ansatz |
Harnstofflösung (50 mL) |
Ureaselösung (2 mL) |
|---|---|---|
Tab. 1: Versuchsansätze

Abb. 2: Verlauf der elektrischen Leitfähigkeit in Versuchsansatz (Kurve 1)
3.1
Erkläre, weshalb man durch Messung der elektrischen Leitfähigkeit der Lösungen der Versuchsansätze die Enzymaktivität der Urease untersuchen kann.
Beschreibe den Verlauf der Kurve 1 in Abbildung 2.
Erkläre die unterschiedliche Steigung der Kurve 1 in den drei Abschnitten 0 bis 30 Sekunden, 30 bis 100 Sekunden und ab 100 Sekunden.
Beschreibe den Verlauf der Kurve 1 in Abbildung 2.
Erkläre die unterschiedliche Steigung der Kurve 1 in den drei Abschnitten 0 bis 30 Sekunden, 30 bis 100 Sekunden und ab 100 Sekunden.
4 VP
3.2
Übertrage das Diagramm mit Kurve 1 aus Abbildung 2 in deine Reinschrift und zeichne in dieses Diagramm die zu erwartende Leitfähigkeitskurve für die beiden Versuchsansätze B und C ein. Begründe den jeweiligen Kurvenverlauf.
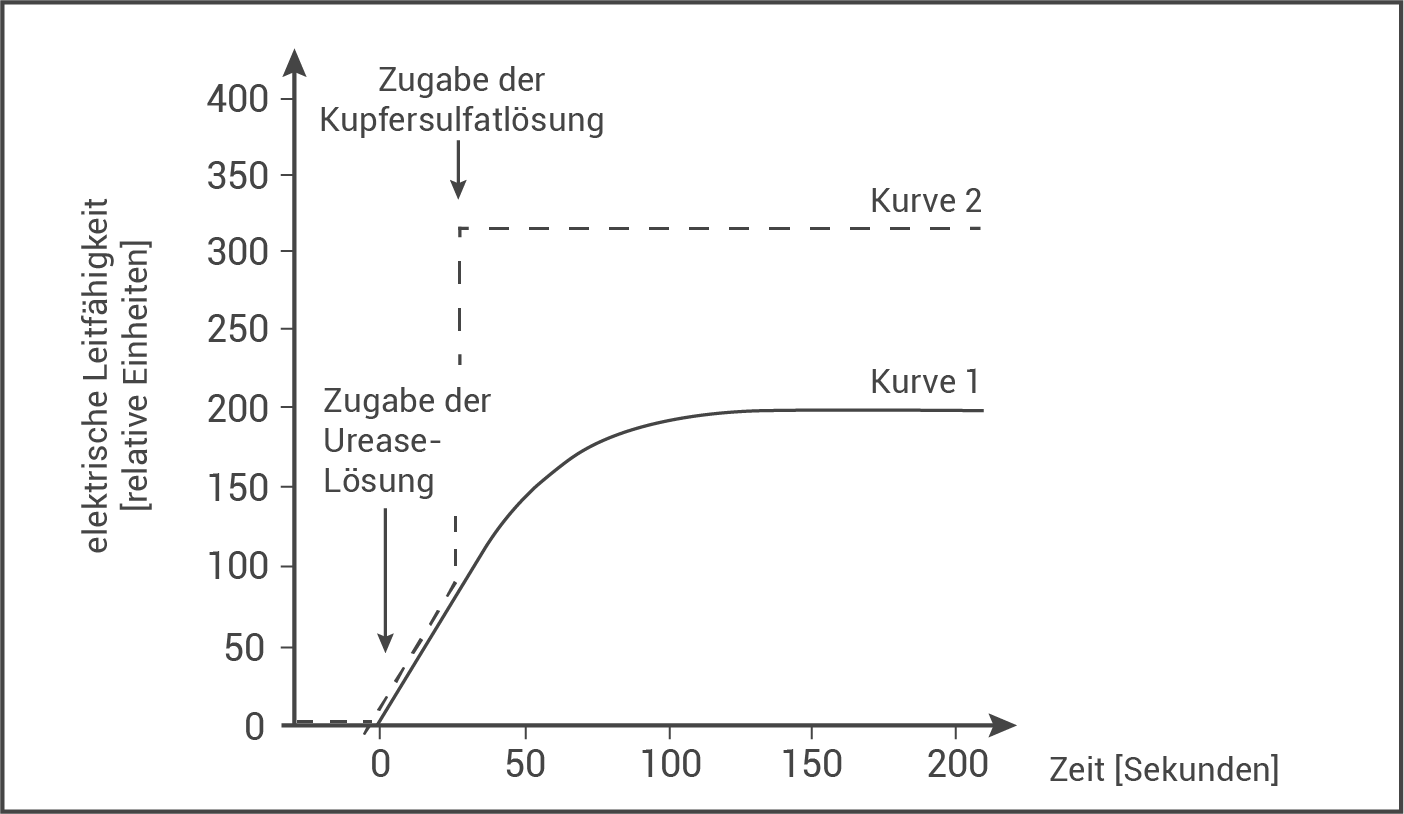
In einem weiteren Experiment wird Versuchsansatz A dahingehend modifiziert, dass nach 25 Sekunden Kupfersulfatlösung zugesetzt wird. Kurve 2 in Abbildung 3 zeigt den Verlauf der gemessenen Leitfähigkeit im Vergleich zu Kurve 1.
3 VP

Abb. 3: Verlauf der elektrischen Leitfähigkeit in Versuchsansatz A ohne und mit Zugabe von Kupfersulfatlösung
3.3
Beschreibe und erkläre den Verlauf der Kurve 2 in Abbildung 3.
Knöllchenbakterien können mithilfe des Enzyms Nitrogenase Luftstickstoff in für Pflanzen nutzbare Stickstoffverbindungen umwandeln. Ein Ziel der Pflanzenforschung ist es, das Nitrogenase-Gen der Knöllchenbakterien und damit die Fähigkeit zur Nutzung des Luftstickstoffs auf Pflanzen zu übertragen.
3 VP
4
Begründe, weshalb es schwieriger ist, transgene Pflanzen zu erzeugen, die dieses Nitrogenase-Gen enthalten, als transgene Bakterien (zwei Angaben).
2 VP
20 VP
1
Stickstoffhaltige Biomoleküle und ihre Funktion im pflanzlichen Organismus (zwei erforderlich):
- DNA: Speicherung des genetischen Codes
- tRNA: Transport der Aminosäuren
- mRNA: „Baupläne“ für Aminosäuresequenz
- ATP: Übertragung und kurzfristige Speicherung der Energie
- Protein: z. B. Funktion als Enzym (Katalyse)
- Chlorophyll: Absorption von Licht
- Vitamin B: Coenzym
2.1
Stoffklasse der Urease:
Die Urease lässt sich chemisch zur Stoffklasse der Proteine zuordnen. Strukturebenen des Ureasemoleküls und ihre Bindungen:
Die Urease lässt sich chemisch zur Stoffklasse der Proteine zuordnen. Strukturebenen des Ureasemoleküls und ihre Bindungen:
2.2
Schemazeichnungen der katalysierten Reaktion:
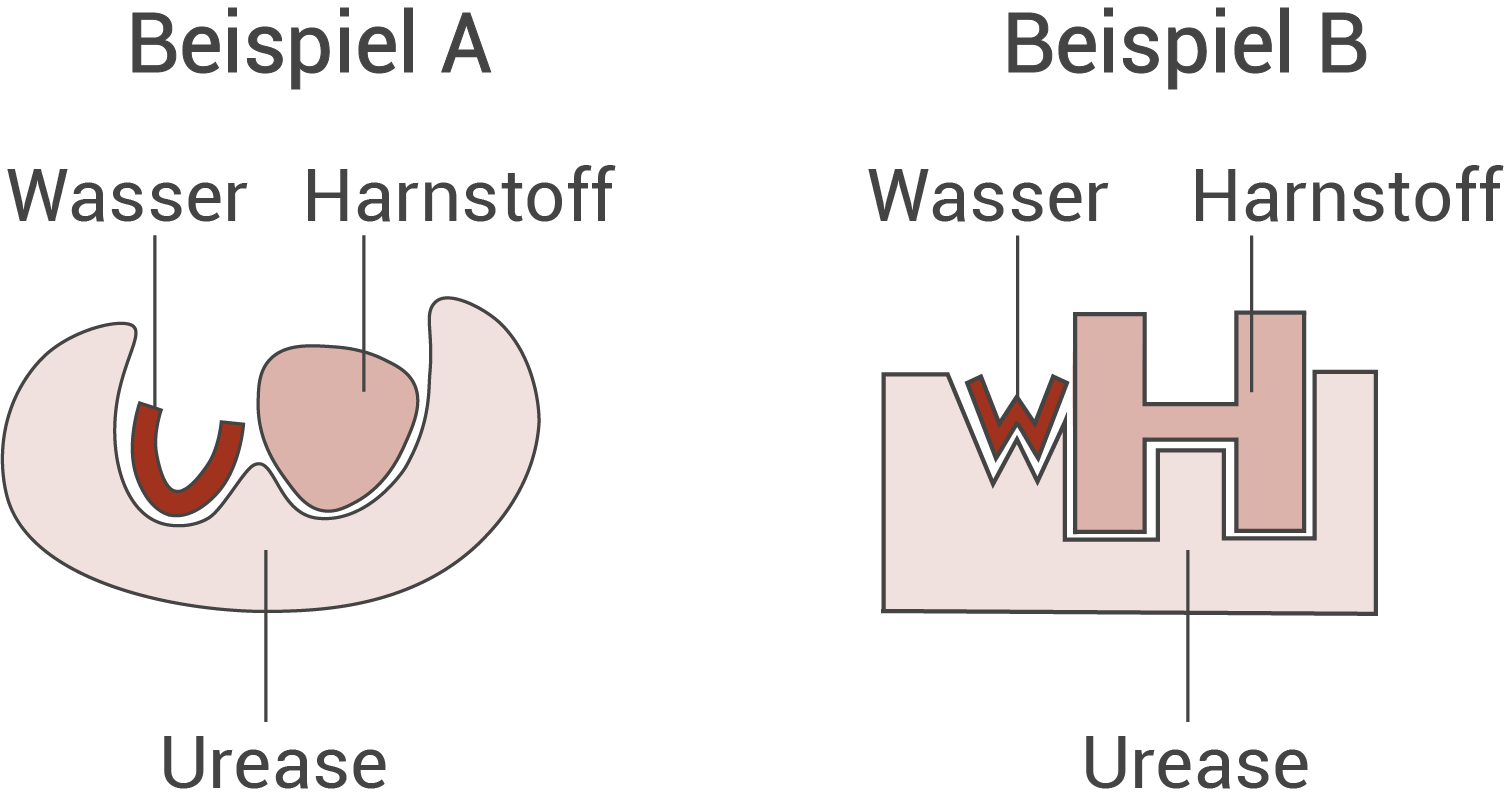
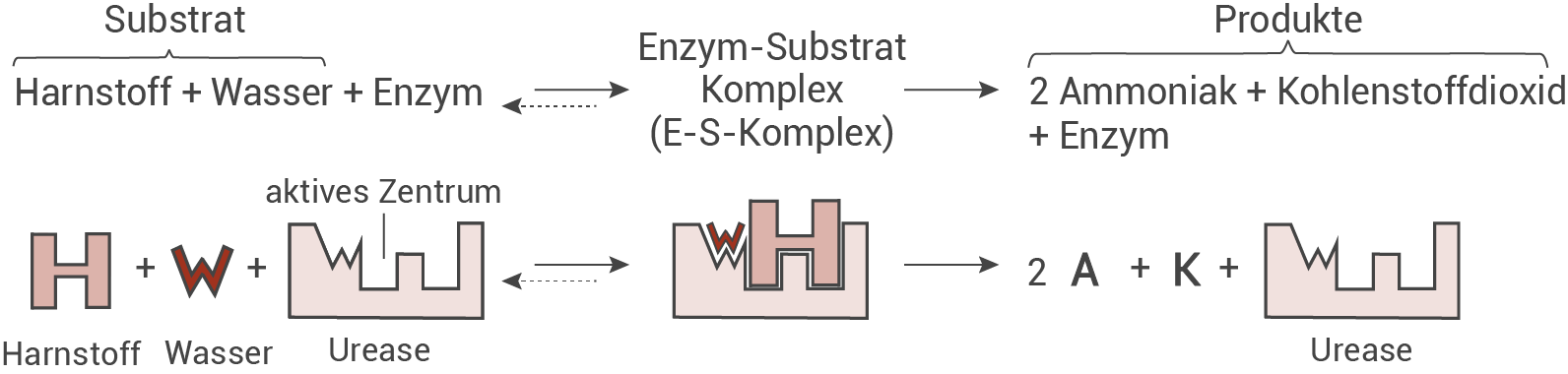 Da Wasser und Harnstoff gleichzeitig im aktiven Zentrum der Urease binden, wäre mit richtiger Begründung auch ein Schema nur mit Harnstoff als Substrat ausreichend.
Da Wasser und Harnstoff gleichzeitig im aktiven Zentrum der Urease binden, wäre mit richtiger Begründung auch ein Schema nur mit Harnstoff als Substrat ausreichend.
Beachte dass hier zwei Edukte (Substrate) im aktiven Zentrum binden. Du kannst die Symbole für das Enzym und die Substrate beliebig wählen. Hier siehst du zwei mögliche Beispiele:


3.1
Erklärung für die elektrische Leitfähigkeit:
Erst nachdem die Harnstoffspaltung bzw. die Folgereaktion stattgefunden haben, können Ionen entstehen, die für die elektrische Leitfähigkeit zuständig sind. Da das Wasser und die Harnstofflösung keinen Strom leiten, ist die Änderung der Leitfähigkeit pro Zeiteinheit ein Maß für die Enzymaktivität. Beschreibung des Kurvenverlaufs 1:
Erst nachdem die Harnstoffspaltung bzw. die Folgereaktion stattgefunden haben, können Ionen entstehen, die für die elektrische Leitfähigkeit zuständig sind. Da das Wasser und die Harnstofflösung keinen Strom leiten, ist die Änderung der Leitfähigkeit pro Zeiteinheit ein Maß für die Enzymaktivität. Beschreibung des Kurvenverlaufs 1:
- 0 - 30 s: Nachdem die Ureaselösung zugegeben wird, ist eine starke (lineare) Zunahme der Leitfähigkeit auf ca. 100 relative Einheiten zu beobachten.
- 30 - 100 s: Es ist eine weitere, aber langsamere, Zunahme auf ca. 200 relative Einheiten zu erkennen.
- 100 - 200 s: Bei ca. 200 relativen Einheiten nimmt die Leitfähigkeit nicht mehr zu, sondern bleibt konstant.
- 0 - 30 s: Zu Beginn des Experiments bewirkt die hohe Harnstoffkonzentration die Bindung aller Ureasemoleküle in E-S-Komplexe und die Aktivität mit maximaler Spaltungsrate. Daher nimmt die Ionenkonzentration, also die Leitfähigkeit, schnell zu.
- 30 - 100 s: Aufgrund der Substratumsetzung nimmt die Harnstoffkonzentration (Substratkonzentration) ab. Dadurch sind nicht mehr alle Ureasemoleküle in E-S-Komplexen gebunden, also "finden" nicht mehr alle Enzymmoleküle Harnstoffmoleküle. Die Ionenkonzentration nimmt pro Zeit weniger zu, daher steigt die Leitfähigkeit immer langsamer.
- 100 - 200 s: Es werden keine weiteren Ionen mehr gebildet, da alle Harnstoffmoleküle gespalten sind. Der Maximalwert der Leitfähigkeit ist erreicht und bleibt daher konstant.
3.2
Diagramm :
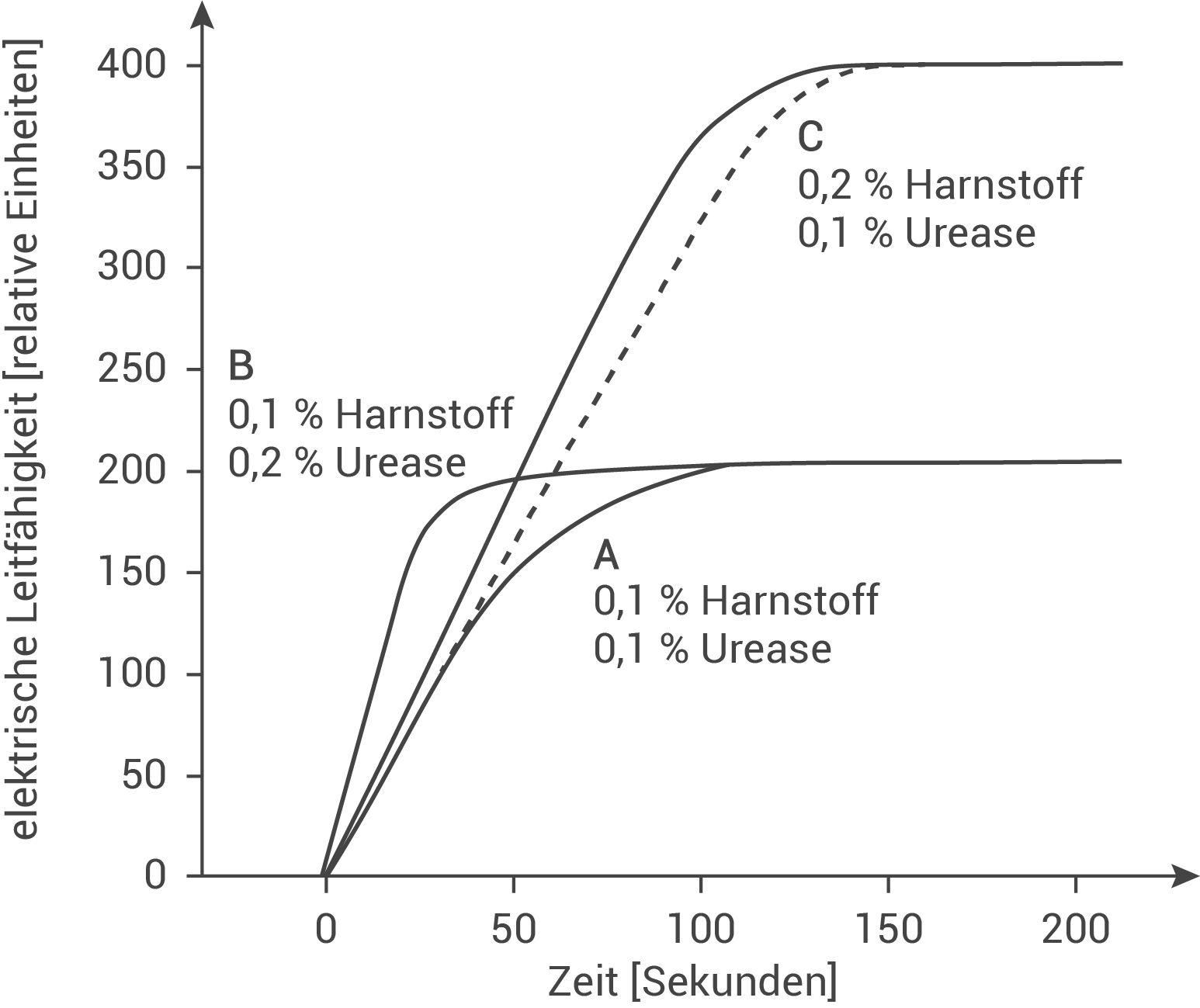 Begründung der Kurvenverläufe:
Begründung der Kurvenverläufe:
Versuchsansatz B: Durch die Verdopplung der Ureasekonzentration ist der Kurvenverlauf deutlich steiler als der gegenüber A. Pro Zeiteinheit sind viel mehr Ureasemoleküle aktiv (d.h. in E-S-Komplexen gebunden), weswegen die Spaltungsrate viel höher ist. Die Leitfähigkeit nimmt schneller zu, da pro Zeiteinheit mehr Harnstoffmoleküle gespalten werden und mehr Ionen entstehen. Die Harnstoffkonzentration ist im Ansatz A gleich groß, deswegen enstehen am Ende auch nicht mehr Ionen als im Ansatz A. Der Maximalwert der Leitfähigkeit gleich dem in Ansatz A.
Versuchsansatz C: Die Steigung ist etwas größer als bei Ansatz A, da die E-S-Komplexe durch die doppelte Substratkonzentration schneller gebildet werden. Enzym-und Substratmoleküle treffen zufällig aufeinander, deswegen bewirkt eine Erhöhung der Substratkonzentration, dass sich Enzym-und Substrat häufiger treffen.
Oder: Die Steigung entspricht der in Ansatz A, da bei einer Harnstoffkonzentration von 0,1 % alle aktiven Zentren der verfügbaren Ureasemoleküle besetzt waren und eine Erhöhung der Spaltungsrate durch mehr Harnstoff nicht möglich ist.
Bei vollständiger Umsetzung der doppelten Harnstoffkonzentration entsteht auch die doppelte Menge an Ionen, deswegen ist die maximale Leitfähigkeit etwa doppelt so groß wie die in Ansatz A und B.

Oder: Die Steigung entspricht der in Ansatz A, da bei einer Harnstoffkonzentration von 0,1 % alle aktiven Zentren der verfügbaren Ureasemoleküle besetzt waren und eine Erhöhung der Spaltungsrate durch mehr Harnstoff nicht möglich ist.
Bei vollständiger Umsetzung der doppelten Harnstoffkonzentration entsteht auch die doppelte Menge an Ionen, deswegen ist die maximale Leitfähigkeit etwa doppelt so groß wie die in Ansatz A und B.
3.3
Beschreibung Kurve 2:
Die Cu -Ionen (und Sulfationen), die in der zugegebenen Kupfersulfatlösung enthalten sind, bewirken einen sofortigen starken Anstieg der Leitfähigkeit. Die Harnstoffspaltung wird sofort gestoppt, weil die Kupferionen die Tertiärstruktur ändern und damit die katalytische Aktivität der Ureasemoleküle hemmen ("Vergiftung" durch Schwermetallionen). Die Leitfähigkeit bleibt konstant, da keine zusätzlichen Ionen durch Harnstoffspaltung mehr entstehen.
-Ionen (und Sulfationen), die in der zugegebenen Kupfersulfatlösung enthalten sind, bewirken einen sofortigen starken Anstieg der Leitfähigkeit. Die Harnstoffspaltung wird sofort gestoppt, weil die Kupferionen die Tertiärstruktur ändern und damit die katalytische Aktivität der Ureasemoleküle hemmen ("Vergiftung" durch Schwermetallionen). Die Leitfähigkeit bleibt konstant, da keine zusätzlichen Ionen durch Harnstoffspaltung mehr entstehen.
- 0 - 25 s: Nachdem die Ureaselösung zugegeben wurde, gleicht der Kurvenanstieg zunächst dem von Ansatz A.
- 25 - 200 s: Nach Zugabe der Kupfersulfatlösung steigt die Leitfähigkeit schlagartig an (unmittelbar auf ca. 320 realtive Einheiten) und bleibt dann konstant.
Die Cu
4
Begründung der Schwierigkeiten (zwei erforderlich):
- Die Zellwand der Pflanzen wirkt beim Einschleusen eines Fremdgens als Barriere.
- Das Genom bei eukaryotische Pflanzenzellen ist viel komplexer und hat viele Chromosomen.
- Pflanzenzellen haben keine Plasmide, weswegen kein Gentransfer (wie zwischen Bakterienzellen) möglich ist.
- Pflanzenzellen, die erfolgreich transformiert wurden, müssen erst zeitaufwändig zu einer vielzelligen Pflanze regeneriert werden.