Redox-Reaktionen
Ionen und Elektronen
Im Themengebiet Elektrochemie werden wir uns insbesondere mit Ionen und Elektronen beschäftigen. Aus diesem Grund wollen wir uns ganz zu Beginn noch einmal klar machen, was der Begriff der Ionen für Informationen beinhaltet, was Kationen und Anionen sind und welche Rolle die Elektronen dabei spielen.
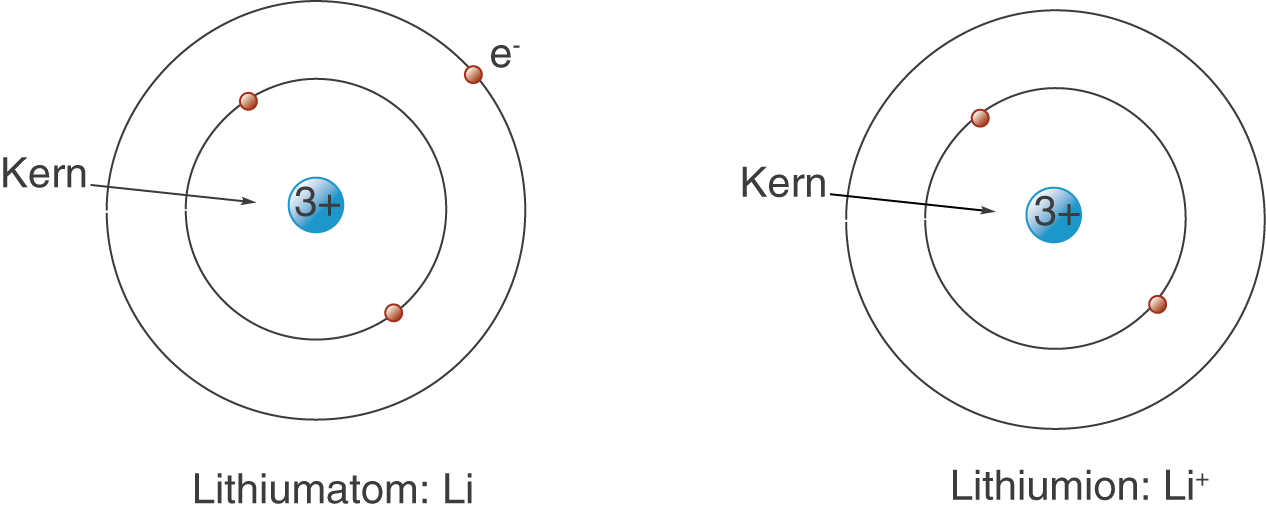
Als Beispiel wollen wir uns das Element Lithium anschauen, welches in der ersten Hauptgruppe (Alkalimetalle) steht und das drittleichteste Element des Periodensystems der Elemente (PSE) ist.
Wir sehen im linken Schaubild, dass Lithium aus einem Atomkern besteht, der drei positive Ladungen trägt (hier befinden sich drei Protonen, deshalb hat Lithium auch die Ordnungszahl 3). Damit diese drei positiven Ladungen ausgeglichen werden, befinden sich in der Elektronenhülle drei einfach negativ geladenen Elektronen , die auf ihren „Bahnen“ um den Kern kreisen. Damit ist das Element nach außen hin neutral, da die negativen Ladungen die positiven ausgleichen. Wenn wir nun einen gewissen Energiebetrag aufwenden (Ionisierungsenergie), dann können wir das äußerste Elektron aus der Elektronenhülle entfernen. Da die drei positiven Ladungen im Kern des Lithiums konstant bleiben, fehlt somit eine negative Ladung, um diese auszugleichen: Wir erhalten ein einfach geladenes Lithium-Ion
. Wie du siehst ist die Oktettregel somit erfüllt und dieses Ion ist stabil.
Anmerkung: Das hier verwendete Atommodell wird Bohr‘sches Atommodell genannt. Die einzelnen Bahnen, auf denen die Elektronen kreisen, sind die Schalen der Elektronenhülle. Dieses Modell ist sehr simpel, aber auch unheimlich hilfreich, da wir an ihm sehr viele Aspekte plausible erklären können. Wichtig ist, dass sich die Elektronen hier auf Bahnen aufhalten und nicht ungeordnet um den Atomkern herumfliegen. Bedenke immer, dass es sich hier nur um ein Modell handelt. Wir können diesem zwar sehr viele Informationen entnehmen, dennoch beschreibt es nicht die Realität.
Wir können das Besprochene folgendermaßen zusammenfassen:
- Atome bestehen aus negativ geladenen Elektronen und positiv geladenen Atomkernen
- Durch das Entfernen oder Hinzufügen von Elektronen erhalten wir Ionen
- Positiv geladene Ionen nennen wir Kationen, negativ geladene Anionen
Die Elektronen sind das zentrale Element dieses Konzepts. Erst durch die Änderung der Elektronenanzahl erhalten wir Ionen
Redox-Reaktionen
Wir wollen uns nun Reaktionen anschauen, bei welchen Elektronen übertragen werden: Redox-Reaktionen. Der Begriff „Redox“ ist dabei eine Kombination der beiden Begriffe Oxidation und Reduktion, die wir nun besprechen wollen.
Diese beiden Begriff bilden sowohl den Namen, als auch die wichtigste Grundlage der kompletten Redox-Chemie. Vergewissere dich also, dass du beide Begriffe und ihre Definition im Schlaf beherrschst.
Oxidation
Wir wollen an dieser Stelle wieder das Beispiel des Lithiums heranziehen. Wenn wir die Abgabe eines Elektrons als Reaktionsgleichung schreiben, dann sieht das so aus:
An diesem Beispiel können wir gleich zwei wichtige Merkmale einer solchen Reaktion erkennen: Die Abgabe des Elektrons, welches wir wie einen Reaktanden in die Reaktionsgleichung schreiben können, führt dazu, dass wir ein Lithium-Kation erhalten. Auf beiden Seiten des Reaktionspfeils haben wir die gleiche formale Ladungssituation: Neutral! Das atomare Lithium ist von Natur aus neutral und auf der rechten Seite negieren sich die beiden Ladungen gerade. Dieser Aspekt ist sehr wichtig, da wir diese Situation für alle Redox-Reaktion gewährleisten müssen.
- Die Abgabe von Elektronen ist mit einer Oxidation verbunden!
Wir werden in einem Kapitel weiter unten den Einsatz von Oxidationszahlen besprechen, mit deren Hilfe wir auch Redox-Reaktionen von Molekülen sehr gut nachvollziehen können. Was wir uns hier schon einmal merken können ist die Erhöhung der Ladung des Lithiums von 0 nach +1 und den Begriff der Oxidation, der in diesem Zuammenhang fällt.
Reduktion
Nun nehmen wir wieder das Beispiel des Lithiums zur Hand, um den Begriff der Reduktion zu erklären. Eine Reaktionsgleichung, die eine Reduktion veranschaulicht, würde folgendermaßen aussehen:
Das mag zunächst etwas seltsam aussehen, aber die Reduktion entspricht genau dem Gegenteil der Oxidation: Das Lithium-Kation nimmt ein Elektron auf und die Ladung wird um eins reduziert. Wieder können wir sehen, dass die Ladungen formal auf beiden Seiten ausgegelichen sind.
- Die Aufnahme von Elektronen ist mit einer Reduktion verbunden!
Im Bezug auf die bereits genannten Oxidationszahlen, können wir uns hier merken, dass die Erniedrigung der Ladung des Lithiums von +1 auf 0, durch die Aufnahme eines Elektrons mit dem Begriff der Reduktion verbunden ist.
Redox-Paare
Was wir im Zusammenhang mit den Begriffen der Oxidation und Reduktion an unserem Beispiel sehen konnten, ist das Auftreten von Lithium zusammen mit dem Lithium-Kation. An dieser Stelle wollen wir ein Konzept einführen, dass vom Prinzip her auch in der Säure-Base-Chemie eine zentrale Rolle spielt: Die Paarbildung. Während wir im Zusammenhang mit Säuren und Basen von Säure-Base-Paare sprechen, sprechen wir in diesem Kontext von Redox-Paaren. Ein Redox-Paar ist ein Paar, welches aus der reduzierten und der oxidierten Variante eines Elements besteht. Beispiele sind:
Wichtig ist hierbei, dass es sich immer um ein Paar handelt, welches die an einer Oxidation oder Reduktion beteiligten Formen des Elements beinhaltet. Das heißt, dass immer die reduzierte Form und die direkt zugehörige oxidierte Form ein Redox-Paar bilden.
Du siehst hier, dass Eisen (Fe) beispielsweise zwei oxidierte Formen besitzt. Die beiden Redox-Paare stehen dabei jeweils für beiden möglichen Redox-Reaktion. Die erste:
sowie die zweite mögliche Redox-Reaktion:
Eisen gibt also zuerst zwei Elektronen ab und wir erhalten ein -Kation und erst im nächsten Schritt wird dieses
-Kation zu einem
-Kation oxidiert. Wir werden verschiedene Redox-Paare im Themengebiet Elektrochemie kennen lernen und sehen, warum es notwendig ist auch hier immer Paare zu betrachten.
Oxidationszahlen
Oxidationszahlen sind ein sehr hilfreiches Werkzeug, welches wir verwenden können um die Redox-Chemie verschiedenster Verbindungen verstehen zu können. Ein zentrales Element dieses Werkzeugs ist die Eigenschaft der Elektronegativität. Diese gibt uns darüber Auskunft, wie stark ein Element Elektronenpaare in einer Verbindung an sich zieht. Je größer der Wert der Elektronegativität, desto stärker die Tendenz Elektronenpaare anzuziehen. Das heißt, dass du am besten das PSE verwendest, weil die Elektronegativität der einzelnen Elemente dort notiert ist.
Wir wollen für Oxidationszahlen römischen Ziffern verwenden. Es gibt ein paar Regeln, die für Oxidationszahlen gelten:
- Elemente haben immer die Oxidationszahl 0.
- Moleküle haben in der Summe die Oxidationszahl 0. Molekül-Ionen haben eine Oxidationszahl, die ihrer Ladung entspricht.
- Metall-Kationen haben immer positive Oxidationszahlen, die ihrer Ladung entsprechen.
- Wasserstoff hat in Verbindungen meistens die Oxidationszahl +I.
- Sauerstoff hat in Verbindungen meistens die Oxidationszahl -II.
- Bilden zwei identische Elemente eine chemische Bindung, werden die Elektronen geteilt.
Zwei weitere wichtige Aspekte sind, dass die Oxidationszahl maximal den Wert annehmen kann, der durch die Oktettregel möglich ist und das eine Verbindnung nach außen hin neutral sein muss. Wir wollen uns nun anhand von verschiedenen Beispielen die Anwendung von Oxidationszahlen klar machen.
(1) Salze
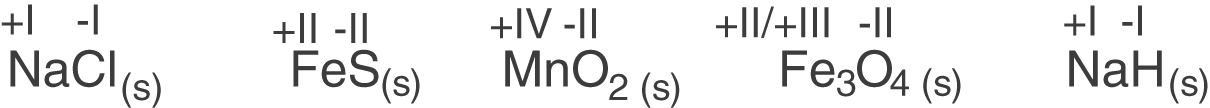
Wir betrachten diese Salze von links nach rechts. NaCl ist gewöhnliches Speisesalz. Das Natrium-Kation besitz als Alkalimetall eine Ladung von +1 und das Chlorid-Anion als Halogen eine Ladung von -1. Ionen besitzen gerade die Oxidationszahlen, die ihrer tatsächlichen Ladung entsprechen.
An zweiter Stelle steht Eisenmonosulfid FeS, bei welchem wir so vorgehen können: Schwefel steht in der sechsten Hauptgruppe und Metalle bilden generell Kationen. Dementsprechend muss die Ladung und damit auch die Oxidationszahl von Schwefel schon einmal negativ sein, so dass für das Salz elektrische Neutralität gilt. Damit die Oktettregel erfüllt ist, kann Schwefel noch zwei Elektronen aufnehmen. Folglich besitz Schwefel die Oxidationszahl -II. Da wie erwähnt die elektrische Neutraliät der Verbindung gelten muss, muss das Eisen-Kation die Oxidationszahl +II tragen.
Das dritte Beispiel ist Mangandioxid, welches auch als Braunstein bekannt ist. Hier haben wir zwei Sauerstoffatome, von denen wir wissen, dass sie immer die Oxidationszahl -II besitzen. Pro Sauerstoffatom gibt es hier also zwei negative Ladungen: Die Anzahl von Elementen in einer Verbindung wirkt sich auf die Summe der Ladungen aus, die durch die Oxidationszahlen beschrieben werden. Damit haben wir in der Summe eine negative Ladung von -IV. Da auch dieses Salz nach außen neutral sein muss, können wir folgern, dass Mangan (Mn) eine Oxidationszahl von +IV haben muss.
Die nächste Verbindung ist etwas trickreicher. Wieder sehen wir, dass Sauerstoff mit einer Oxidationszahl von -II beteiligt ist. Da vier Sauerstoffatome in der Verbindung vorkommen, kommen wir auf eine effektive negative Ladung von -VIII. Diese muss nun durch drei Eisen-Kationen ausgeglichen werden. Wir kennen hier sowohl das
-, als auch das
-Kation. Keines von beiden ist in dreifacher Ausführung in der Lage acht negative Ladungen zu kompensieren. Das wird erst dann möglich, wenn wir die beiden Oxidationstufen kombinieren. Diese besondere Verbindung trägt den Namen Magnetit, denn das gleichzeitige Vorkommen von einem
- und zwei
-Kationen führt neben einer kombinierten Oxidationszahl von +VIII zu magnetische Eigenschaften.
An letzter Stelle steht eine besondere Verbindung: NaH. Wenn wir uns Überlegen, dass Natrium ein Alkalimetall ist und ein Elektron abgibt, um die Oktettregel zu erfüllen, bekommen wir hier eine Oxidationszahl von +I. Um diese aber auszugleichen, müsste das Wasserstoff-Ion eine Oxidationszahl von -I aufweisen. Unseren Regeln nach, wäre das unmöglich. Hier bestätigt die Ausnahme die Regel: Es handelt sich um ein sogenanntes salzartiges Hydrid. In diesen Verbindungen besitzen Wasserstoff-Ionen eine negative Ladung und damit eine negative Oxidationszahl.
(2) Organische Verbindungen
Wir wollen am Beispiel der Aminosäure Leucin lernen, wie Oxidationszahlen von organischen Verbindungen bestimmt werden können.
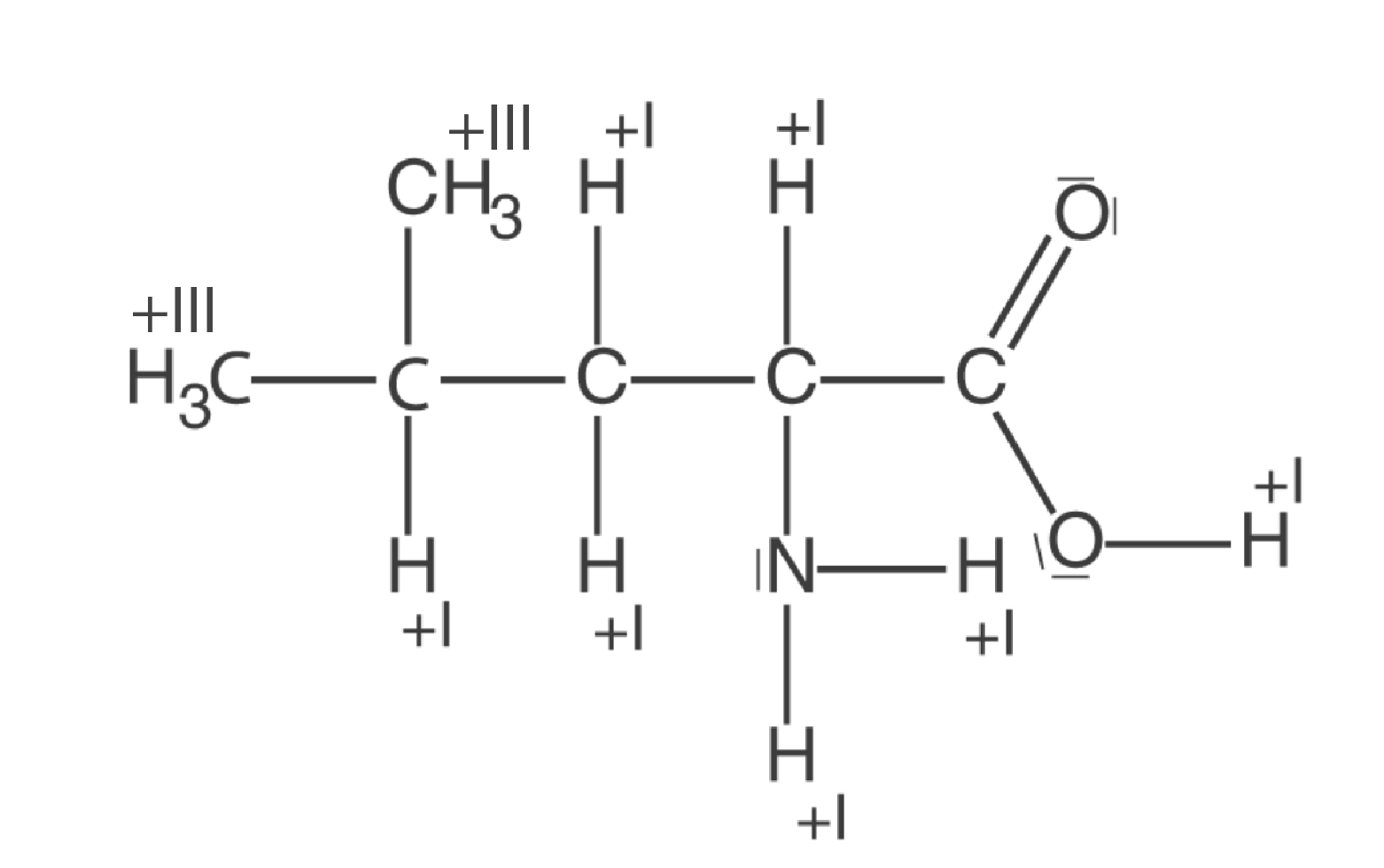
Wir haben in das Molekül die Oxidationszahlen (+I) des Wasserstoffs bereits eingezeichnet. Also beispielsweise zieht der einfach gebundene Sauerstoff der Carboxyl-Gruppe (C-O-Bindung) die Elektronen weg vom C- und vom H-Atom. Im nächsten Schritt kümmern wir uns um die Oxidationszahlen der O-Atome und des N-Atoms. Zur besseren Übersichtlichkeit entfernen wir die Oxidationszahlen der H-Atome wieder.
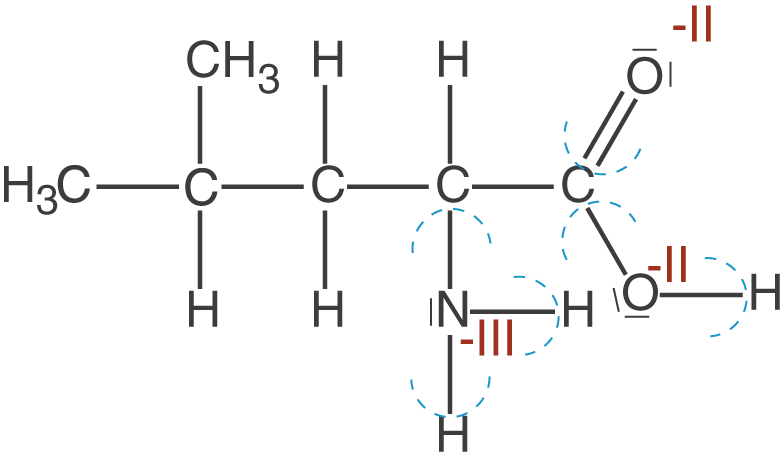
Der Stickstoff der Aminogruppe ist neben C- und H-Atomen das elektronegativste Element. Dementsprechend werden die Elektronen der Bindungen des Stickstoffs, zwei N-H-Bindungen und eine N-C-Bindung, zu diesem gezogen, was in einer Oxidationszahl von -III resultiert. Um diesen „Elektronenzug“ zu kennzeichnen, verwenden wir Halbkreise, die die betroffenen Elektronenpaare räumlich dem jeweiligen Atom zuordnen. Der Sauerstoff besitzt nach unseren Regeln die Oxidationszahl -II. Das entspricht dem Umstand, dass hier ebenfalls alle Elektronen der Bindungen zum Sauerstoff gezogen werden. In beiden Fällen ist die Oktettregel erfüllt worden. Abschließend wenden wir uns den C-Atomen zu:
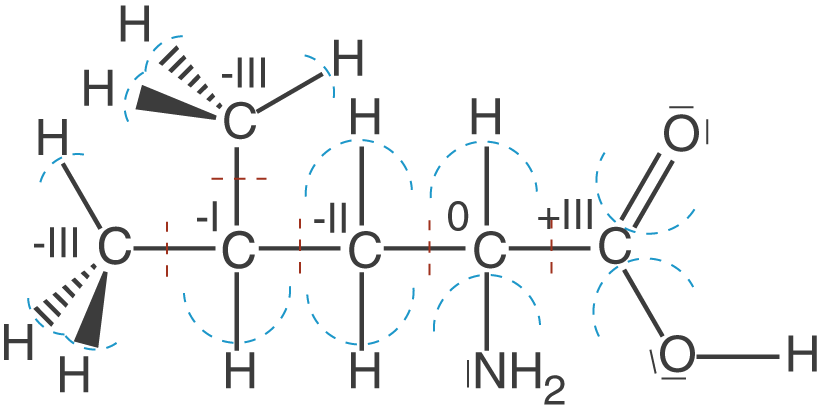
C-Atome sind elektronegativer als H-Atome, deshalb ziehen sie alle Elektronen einer C-H-Bindung zu sich. Im Falle einer C-C-Bindung wird das Elektronenpaar geteilt, was durch den roten Strich dargestellt wird. Wir fangen nun von links an die Oxidationszahlen zu bestimmen: Das erste C-Atom zieht sechs Elektronen der C-H-Bindungen zu sich (pro Bindung zwei Elektronen) und die Bindung zum nächsten C-Atom wird geteilt. Auf vier Elektronen, die normal wären (Kohlenstoff steht in der vierten Hauptgruppe), kommen hier sieben. Folglich eine Oxidationszahl von -III, weil formal ein Ladungsüberschuss von drei negativen Ladungen auftritt.
Das nächste C-Atom ist an drei C-C-Bindungen beteiligt: Diese Elektronen werden jeweils geteilt. Die vierte Bindung ist eine C-H-Bindung, ergo zwei Elektronen. In der Summe sind das dann fünf Elektronen an diesem C-Atom. Das macht eines mehr als normal und ergibt somit eine Oxidationszahl von -I. Das gleiche Prinzip gilt für die Methylgruppe am nächsten C-Atom.
C-Atom drei besitzt zwei C-H-Bindungen und zwei C-C-Bindungen. Das macht in der Summe vier Elektronen von den zwei C-H-Bindungen und je eines von den C-C-Bindungen, also sechs Elektronen. Damit beträgt die Oxidationszahl hier -II.
Das vierte C-Atom ist an zwei C-C-Bindungen, einer C-H-Bindung und einer C-N-Bindung beteiligt. Die beiden C-C-Bindungen tragen je ein Elektron bei, die C-H-Bindung zwei und die C-N-Bindung keines, da die Elektronegativität von Stickstoff größer ist als die von Kohlenstoff. Das macht in der Summe vier Elektronen und da vier normal sind, hat dieses C-Atom die Oxidationszahl 0.
Das letzte, an der Carboxylgruppe beteiligte C-Atom, besitzt eine C-C-Bindung und zwei C-O-Bindungen (wobei eine davon sogar eine Doppelbindung ist). Da Sauerstoff elektronegativer ist als Kohlenstoff, werden alle Elektronen der C-O-Bindungen zu ersterem gezogen. Die C-C-Bindung trägt ein Elektron bei. Das bedeutet, dass dieses C-Atom effektiv ein Elektron besitzt. Bei vier, die normal wären, fehlen also drei. Das macht dann eine Oxidationszahl von +III.
(3) Peroxide
Bevor wir dieses Kapitel abschließen wollen, werfen wir noch einen Blick auf die Stoffklasse der Peroxide und deren Oxidationszahl. Als Beispiel verwenden wir Wasserstoffperoxid .
Diese Verbindung gehört wieder zu den Ausnahmen, was unsere Regeln von oben betrifft. Da es aber eine der Ausnahmen ist, die auch in der Schule häufig angesprochen wird und ihre Verwendung findet, lohnt es sich sie hier gesondert zu betrachten.
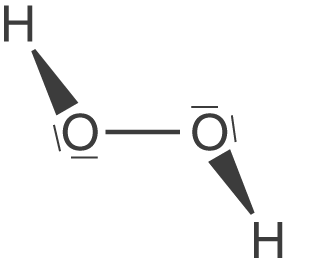
Die Strukurformel verdeutlicht schon die Verteilung der Elektronen im Molekül: Durch die höhere Elektronegativität von Sauerstoff, zieht dieser die Elektronen der O-H-Bindung zu sich. Das wird durch die keilförmigen Bindungsstriche veranschaulicht. Nun können wir dazu übergehen die Oxidationszahlen zu bestimmen. Die H-Atome besitzen formal gesehen keine Elektronen mehr, das heißt, dass sie die gewohnte Oxidationszahl von +I erhalten.
Wir betrachten jetzt den Sauerstoff, welcher die Peroxide so besonders macht. Die beiden O-Atome sind an je einer O-H-Bindung sowie an einer O-O-Bindung beteiligt. Diese letzte Bindung behandeln wir wie die C-C-Bindung im vorherigen Beispiel: Die Elektronen werden geteilt, da es keinen Unterschied in der Elektronegativität gibt. Beim Zusammenzählen der formalen Ladungen an den Sauerstoffatomen fällt folgendes auf: Ein Sauerstoffatom erhält beide Elektronen der O-H-Bindung und zusätzlich noch eines aus der O-O-Bindung. Dazu zählen wir noch je zwei Elektronen, der beiden freien Elektronenpaare. Damit kommen wir in der Summe auf sieben Elektronen, eines mehr als üblich wäre und folglich auf eine Oxidationszahl von -I am Sauerstoff.
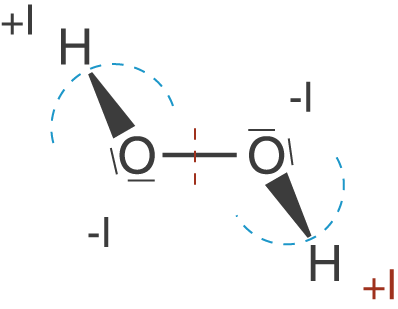
Diese Tatsache unterscheidet sich davon, dass O-Atome in Molekülen ansonsten sehr oft eine Oxidationszahl von -II aufweisen und stellt ein wichtiges Charakteristikum der Peroxide dar.
Anmerkung: Beim Aufstellen der Oxidationszahlen ist es wichtig einen kühlen Kopf zu bewahren. Es ist zunächst einmal völlig egal, wie komplex das Molekül ist, solange du bspw. H-Atome oder O-Atome siehst, kannst du diesen bereits ihre Oxidationszahlen zuordnen: +I und -II. O-O-Bindungen weißen auf ein Peroxid hin. Anschließend kannst du dich dann den restlichen Bestandteilen des Moleküls widmen. Denke immer daran: Das PSE ist dein Freund und Helfer! Hier stehen die Elektronegativitäten und du kannst ablesen, wieviele Elektronen ein Element auf der äußersten Schale normalerweise besitzt; gerade die Nummer seiner Hauptgruppe.
Das Aufstellen von Redox-Gleichungen
Wichtig:
Redox-Reaktionen sind eine zentrale Reaktionsklasse der Chemie. Du wirst sehr schnell merken, dass sich Redox-Reaktionen nicht nur auf anorganische Verbindungen beschränken, sonderen auch in der organischen Chemie verbreitet sind. Wir wollen diese Reaktionsklasse aus diesem Grund in diesem Kapitel ausführlich behandeln, damit du mit allen Begrifflichkeiten umzugehen lernst.
Redox-Reaktionen
Redox ist eine Kurzform für Reduktion-Oxidation. Bei Redox-Reaktionen handelt es sich demnach immer um eine Reduktion und eine Oxidation, welche miteinander kombiniert sind. Im allgemeinen handelt es sich bei diesem Reaktionstyp um eine Elektronenübertragungsreaktion. Wir wollen diesen Begriff an einem Beispiel genauer betrachten.
Die Oxidation von Magnesium mit Sauerstoff.
Anmerkung: Es scheint irgendwie so, wie wenn der Begriff der Oxidation irgendetwas mit der griechischen Bezeichung von Sauerstoff „Oxygenium“ zu tun hätte. Das ist eine geschichtliche Sache, da der französische Chemiker Antoine de Lavoisier mit diesem Begriff die Bildung von Oxiden beschreiben wollte. Heute ist der Begriff auf solche Reaktionen verallgemeinert, bei welchen Elektronen abgegeben werden und sich die Oxidationszahl des ehemaligen Besitzers erhöht.
(1) Halbreaktionen
Wir betrachten die Oxidation und die Reduktion in dieser Reaktion getrennt.
Oxidation
Magnesium ist ein Erdalkalimetall und steht folglich in der zweiten Hauptgruppe. Damit die Oktettregel erfüllt wird, werden zwei Elektronen abgegeben. Wir erhalten ein zweiwertiges Magnesium-Kation und formal zwei freie Elektronen. Die Oxidationszahl erhöht sich von null (elementares Magnesium) auf +II.
Reduktion
Sauerstoff ist in elementarer Form an dieser Reaktion beteiligt. Da Sauerstoff in der sechsten Hauptgruppe steht (Chalkogene), können hier pro O-Atom zwei Elektronen aufgenommen werden, so dass die Oktettregel erfüllt wird. Die Oxidationszahl wird pro O-Atom um zwei erniedrigt: von null auf -II.
(2) Gesamtreaktion
Wir wollen diese beiden Halbreaktionen nun zur Gesamtreaktion kombinieren. Dazu gehen wir so vor, wie wenn es sich bei diesen Reaktionsgleichungen um ein lineares Gleichungssystem handeln würde: Wir addieren die beiden Reaktionsgleichungen (I) und (II) aufeinander.
Vor der Addition der beiden Reaktionsgleichungen betrachten wir in beiden die Anzahl der Elektronen: Diese muss im Falle der Oxidation genau der Anzahl der Elektronen entsprechen, die für die Reduktion benötigt werden. Aus diesem Grund multiplizieren wir Reaktionsgleichung (I) mit zwei. Das heißt, dass in dieser Reaktion zwei Teile Magnesium oxidiert werden müssen. Damit einher geht die Reduktion der Verbindung, die die Elektronen aufnimmt, die beim Oxidationsprozess „freigesetzt“ wurden. Der zweite Schritt beinhaltet das Wegfallen der Elektronen aus der Gleichung:
In diesem Fall können wir die Elektronen ebenso aus der Gleichung herausrechnen, wie im Falle einer Gleichung aus der Mathematik: Wir ziehen auf beiden Seiten vier Elektronen ab. Damit erhalten wir unsere gesuchte Reaktion:
Nachdem wir gesehen haben, wie eine solche Reaktionsgleichung aufgestellt wird, gilt es einige Besonderheiten zu beachten und die Begriff des Oxidationsmittels und des Reduktionsmittels zu klären. Zunächst zu den Besonderheiten:
- Die Anzahl der Elektronen, die bei der Oxidation abgegeben werden, entspricht der Anzahl der Elektronen, die bei der Reduktion aufgenommen werden.
- Die Elektronen kürzen sich aus der finalen Reaktionsgleichung heraus.
- In jeder Reaktionsgleichung, die wir betrachtet haben, sind die Ladungen der Edukt- und Produktseite ausgeglichen!
Bevor wir uns insbesondere mit dem letzten Aspekt noch eingehender beschäftigen, wollen wir noch zwei wichtige Begrifflichkeiten einführen:
- Oxidationsmittel: Das Oxidationsmittel oxidiert andere Stoffe und wird selbst reduziert.
- Reduktionsmittel: Das Reduktionsmittel reduziert andere Stoffe und wird selbst oxidiert.
Der Name verdeutlich also die Aufgabe der Verbindung! Im Bezug auf die oben betrachtete Reaktion erhalten wir folgendes Ergebnis:
- Mg wird zu
oxidiert und liefert zwei Elektronen um elementaren Sauerstoff zu reduzieren: Elementares Magnesium ist für die Reduktion von Sauerstoff verantwortlich, ist also das Reduktionsmittel.
wird zu
reduziert und ermöglicht durch die Aufnahme von Elektronen, dass Magnesium oxidiert werden kann: Sauerstoff ist hier das Oxidationsmittel.
Nun wenden wir uns dem Ladungsausgleich für Redox-Reaktionen zu, die insbesondere im sauren oder alkalischen Milieu ablaufen: .
Redox-Reaktionen und Ladungsausgleich für 
Wir wollen uns beispielhaft die Reduktion von Permanganat () durch Fe(II) im sauren Milieu
anschauen. Dazu vergegenwärtigen wir uns zuerst die Teilreaktionen.
Nun bestimmen wird die Oxidationszahlen:
: +II, da die Oxidationszahl der Ladung des Kations entspricht.
: + III; die Oxidationszahl entspricht auch hier der Ladung des Kations.
: Die Oxidationszahl des Sauerstoffs mit -II kennen wir. Bei vier O-Atomen macht das -VIII. Da die effektive Ladung von Permanganat -I ist, muss das Mn-Atom sieben negative Ladungen durch sieben positive Ladungen kompensieren. Die Oxidationszahl von Mn beträgt hier also +VII.
: + II; wieder liegt ein Kation vor, also entrspricht die Oxidationszahl dessen Ladung.
Die Redox-Paare dieser Reaktion sehen dann so aus:
Nun wenden wir uns den Teilreaktionen zu.
Oxidation von EisenWenn wir die Ladungen auf beiden Seiten betrachten, kommen wir jeweils auf ein Ergebnis von +II. Damit können wir also zufrieden sein.
Reduktion von PermanganatVielleicht ist dir oben in der Reaktionsgleichung aufgefallen, dass, neben der unausgeglichenen Ladung, die Sauerstoffatome nicht auf der Produktseite auftauchen. Wir müssen also in beiden Fällen nacharbeiten. Folgende Reaktionsgleichung ist unser Ausgangspunkt:
Als nächstes betrachten wir den Ladungsausgleich. Auf der Eduktseite befinden sich formal sechs negative Ladungen, wohingegen sich auf der Produktseite zwei positive Ladungen befinden. Der Ladungsausgleich hängt nun direkt mit dem sauren Milieu zusammen, denn hier haben wirüberschüssige Oxonium-Ionen in der Lösung. Diese verwenden wir, um die überschüssigen negativen Ladungen auf der linken Seite auszugleichen:
Damit haben wir auf beiden Seiten in der Summe zwei positive Ladungen. Nun gleichen wir die Reaktionsgleichung noch im Bezug auf die beteiligten Elemente aus. Das lässt sich mit Wasser bewerkstelligen:
Jetzt kombinieren wir beide Teilreaktionen:
Da wir die erste Gleichung mit einem Faktor von fünf multipliziert haben, konnten wir die Elektronen aus der Gesamtreaktionsgleichung herauskürzen.
Dieses Beispiel bezog sich auf ein saures Milieu, in welchem wir Oxonium-Ionen als Träger positiver Ladungen verwenden können, um „überschüssige“ negative Ladungen auszugleichen. Wenden wir uns dem alkalischen Milieu zu, dann liegen uns mit Hydroxid-Ionen negative Ladungsträger vor. Diese können wir ebenso zum Ladungsausgleich verwenden. Der Unterschied ist hierbei aber, dass wir letztendlich mit negativen Ladungsträgern ausgleichen und nicht mit positiven.