Peptide und Proteine
Definition
Peptide sind die Polymere der Aminosäuren und die Bausteine der Proteine. Wir werden in diesem Skript zunächst einzelne Aminosäuren über die Peptidbindung verknüpfen, um im Anschluss Polypeptide und deren Struktur diskutieren zu können. Anschließend sind wir in der Lage eine Blick auf die Proteine zu werfen, die als zentraler Bestandteil vieler biochemischer Prozesse das Leben erst ermöglichen und die wir aus dem Alltag unter dem Begriff Eiweiße kennen.
Peptide - Polymere der Aminosäuren
Die Aminosäure als Monomer
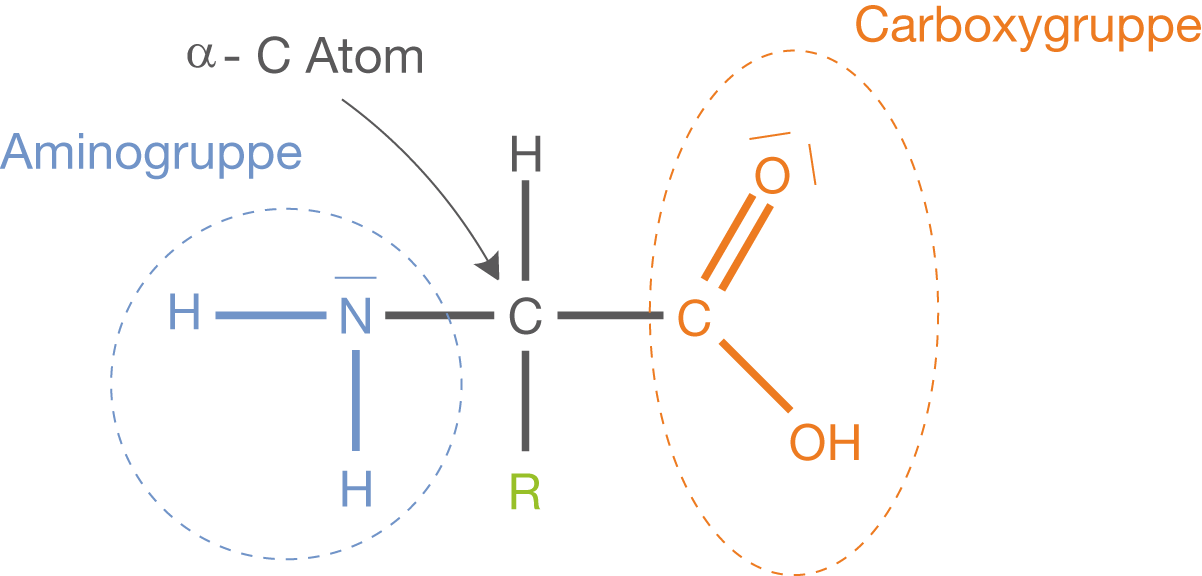
Aminosäuren sind die Monomere (Bausteine) der Peptide. Dementsprechend können wir Peptide als die Oligomere der Aminosäuren bezeichnen. Nimmt die Anzahl der Aminosäuren innerhalb eines Peptids zu, dann erhalten wir Polypeptide. Ausführliche Informationen zu den Grundlagen von Polymeren findest du auch im ChemieLV-Themengebiet Makromolekulare Chemie. An dieser Stelle ist es für uns wichtig, dass wir verschiedene Aminosäuren zuverlässig verknüpfen können, weshalb wir die relevanten funktionellen Gruppen der Aminosäuren betrachten (vgl. Abb. 2).
Jede Aminosäure weist eine Aminogruppe () und eine Carboxygruppe (
) auf. Diese beiden funktionellen Gruppen ermöglichen es Aminosäuren zu Peptiden zu verknüpfen. Des Weiteren werden wir sehen, dass die Anwesenheit zweier unterschiedlicher funktioneller Gruppen ausreicht, um Polypeptide aufzubauen.
Die Peptidbindung
Bildung durch Kondensation
| Anmerkung: | Theoretisch funktioniert die Peptidsynthese wie wir sie gerade besprochen haben. Praktisch gesehen ist die Synthese jedoch sehr viel komplizierter durchzuführen. Das Problem ist hierbei, dass du im Labor gerne eine bestimmte Anordnung der Aminosäuren in deinem Polypeptid möchtest. Wenn du jedoch einfach zwei Aminosäure in einem Gefäß zur Reaktion bringst, dann reagieren diese in irgendeiner Art und Weise ohne dass du Kontrolle darüber hättest. Die Kontrolle dieser Reaktion ist eine anspruchsvolle Aufgabe. |
Räumliche Struktur
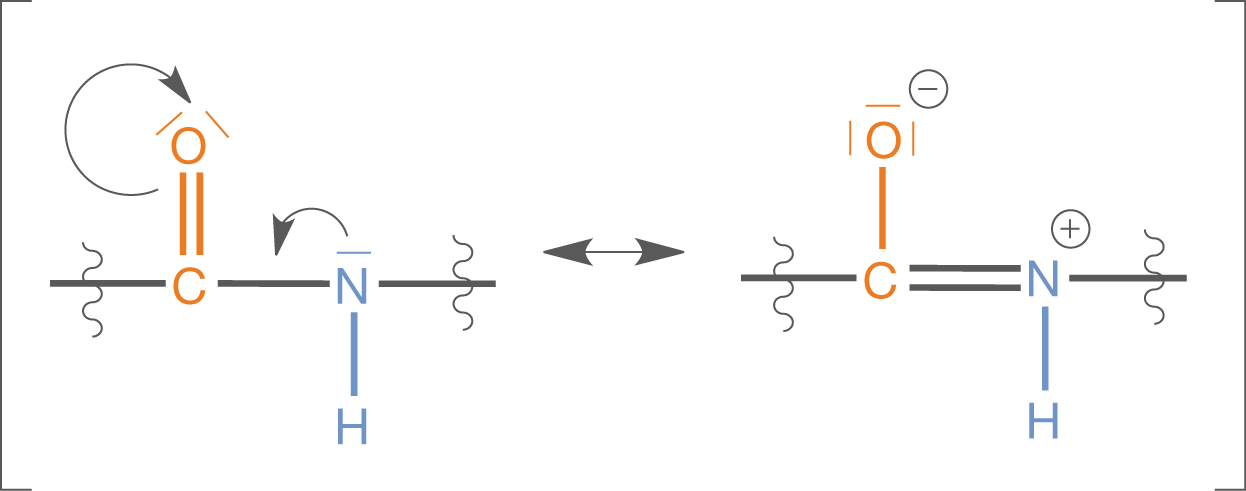
- Die Peptidbindung ist bei Raumtemperatur ziemlich starr, d.h es herrscht keine freie Drehbarkeit um die C-N-Bindungsachse.
- Der C-N-Bindungsabstand ist länger als der einer echten Doppelbindung, aber kürzer als der einer echten Einfachbindung.
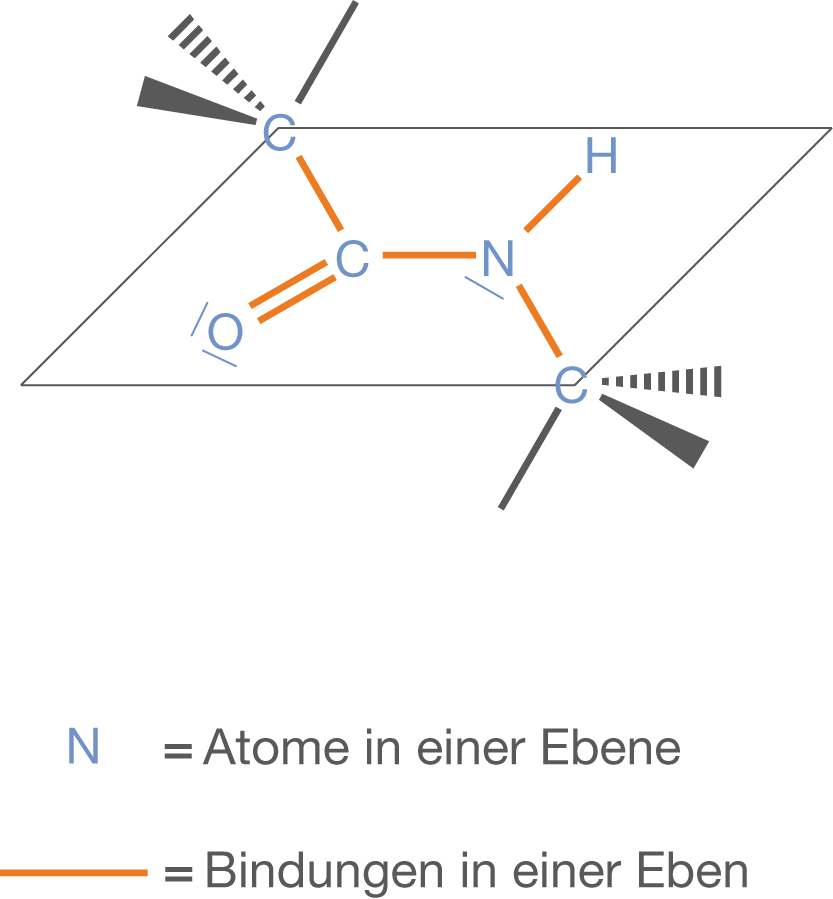
- Wichtig ist, dass die zur Peptidbindungen benachbarten Bindungen frei drehbar sind, womit verschiedene dreidimensionale Strukturen zustande kommen können (vgl. 3.1).
Polypeptide und die Aminosäuresequenz
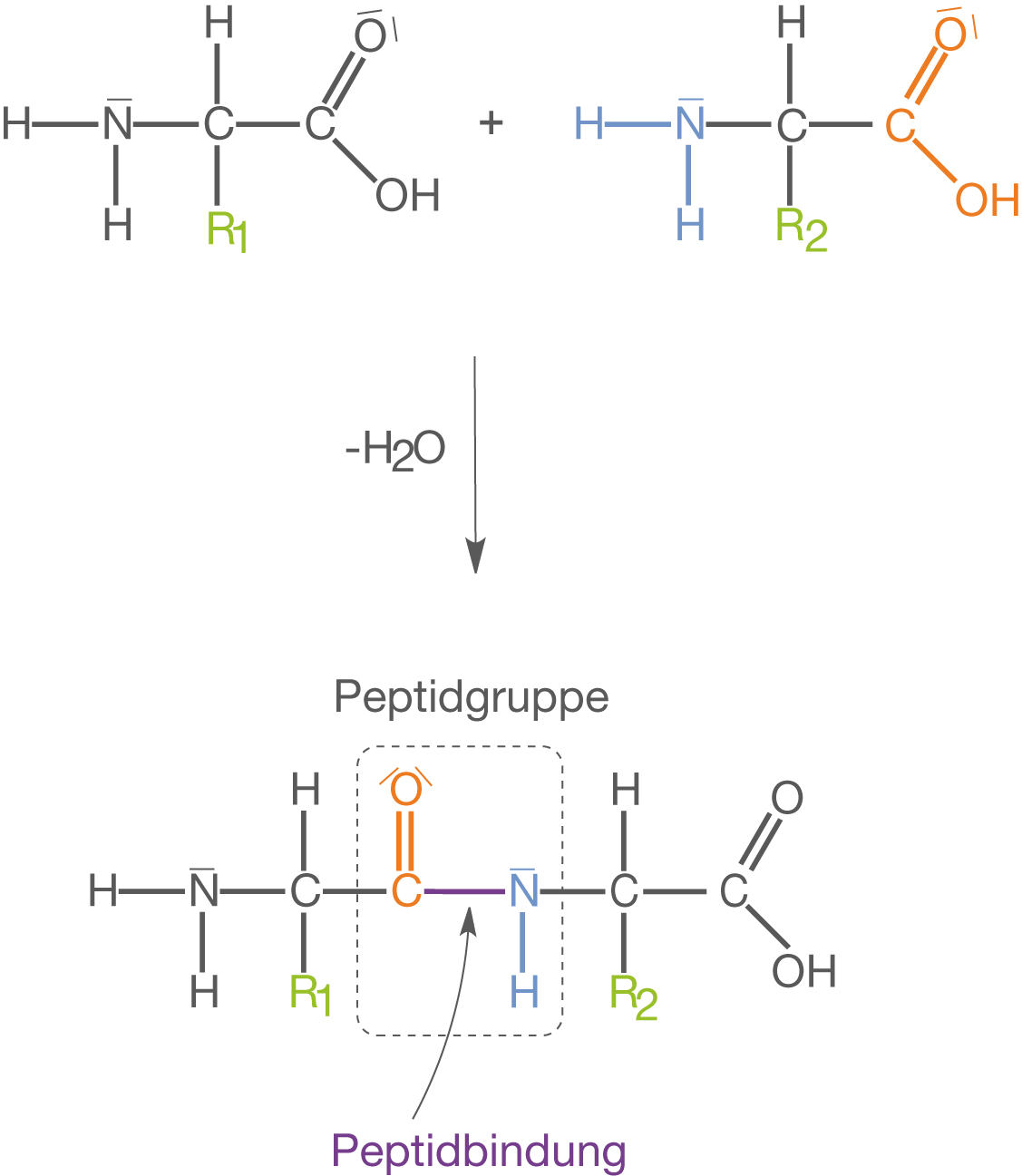
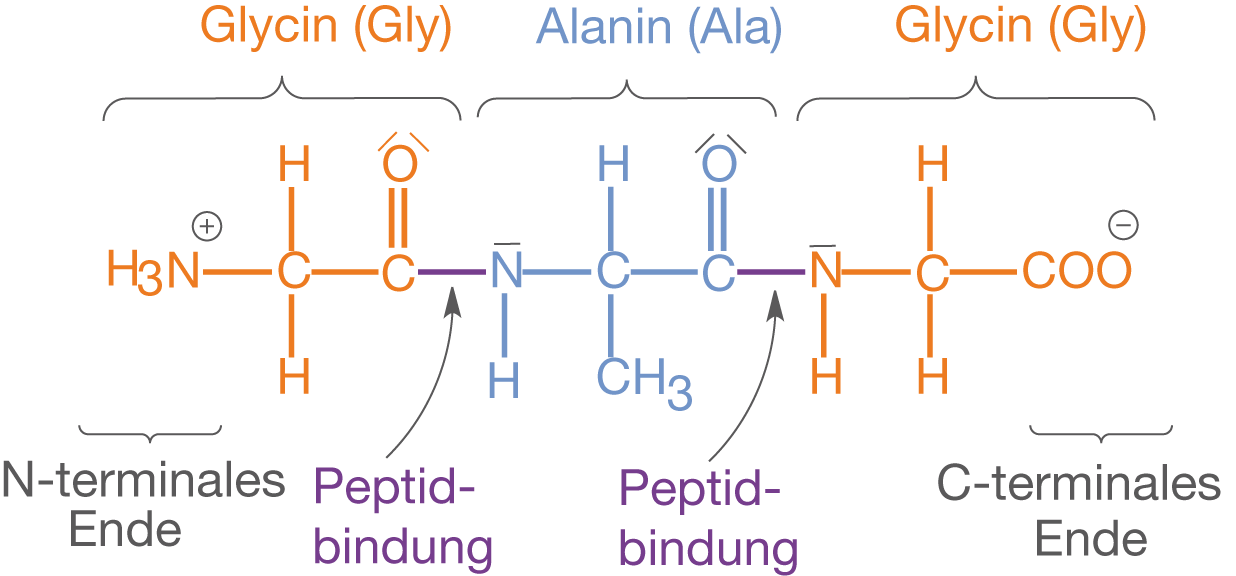
Durch mehrfache Kondensationsreaktionen werden verschiedene Aminosäuren unter Abspaltung von Wasser zu Polypeptiden verknüpft. Das charakteristische an diesen Polypeptiden ist die jeweilige Reihenfolge der Aminosäuren im Molekül. Man spricht in diesem Fall auch von der Aminosäuresequenz (vgl. Abb. 6). Die Aminosäuresequenz stellt die Primärstruktur eines Proteins dar.
Das in Abbildung 6 dargestellte Tripeptid bestehend aus Glycin und Alanin lässt sich nach dem Drei-Buchstaben-Code der beteiligten Aminosäuren benennen, indem die Kürzel der einzelnen Aminosäuren in der auftretenden Reihenfolge aneinander gehängt werden: Gly-Ala-Gly (vgl. ChemieLV-Skript Aminosäuren). Konventionell schreibt man die endständige Aminogruppe nach links und die endständige Carboxygruppe nach rechts. Im Fall der Aminogruppe spricht man vom N-terminalen Ende im Fall der Carboxygruppe vom C-terminalen Ende.
Proteine und deren Struktureigenschaften
Sekundärstruktur
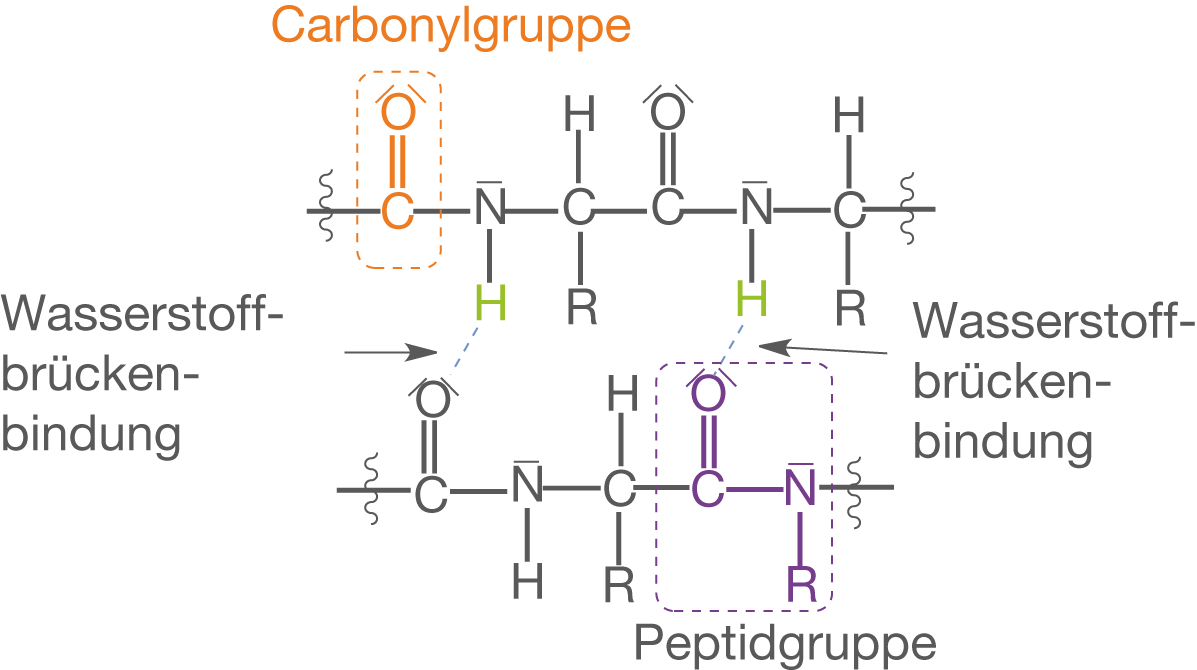
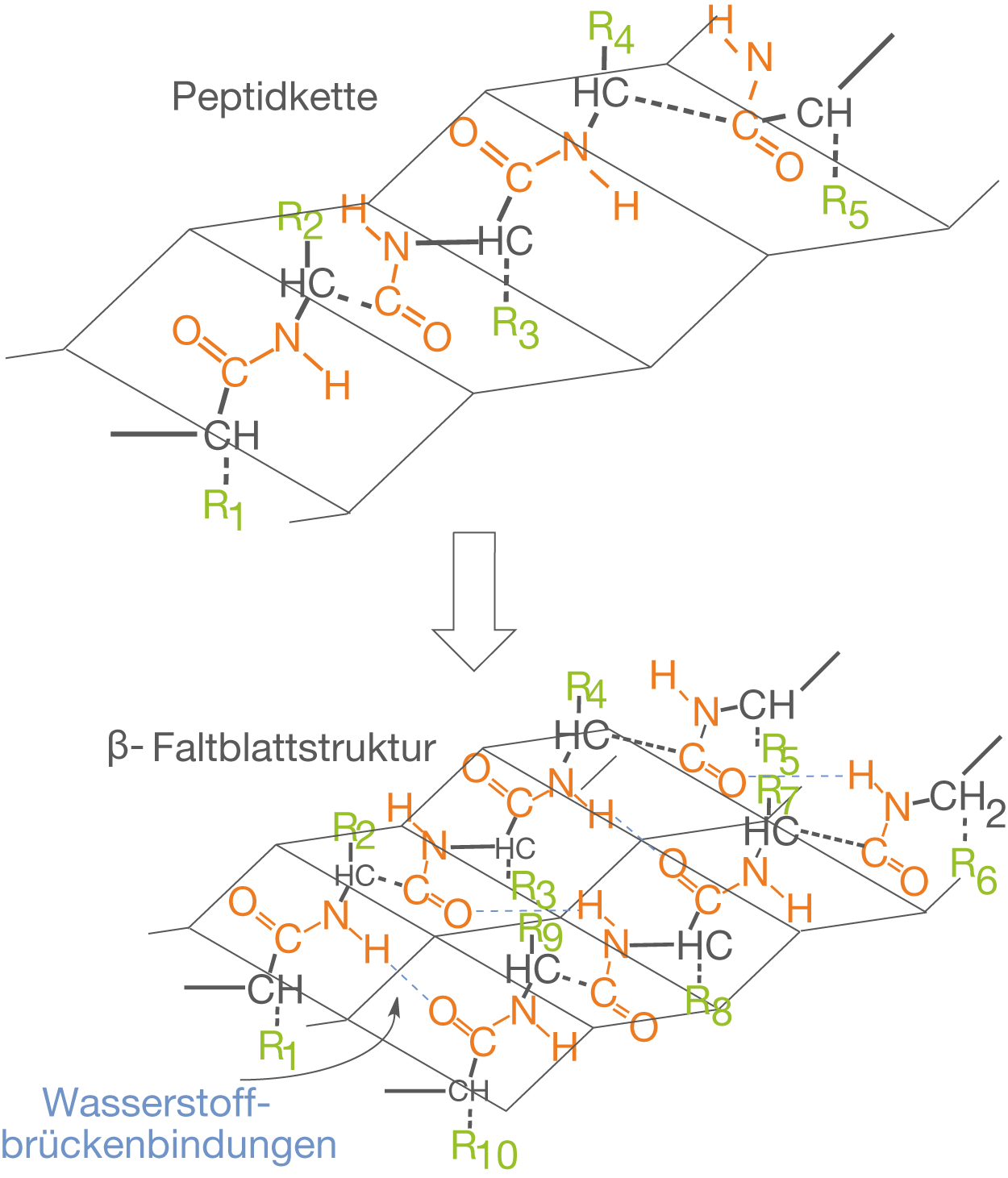
Die Sekundärstruktur eines Proteins bezieht sich auf die räumliche Orientierung einzelner benachbarter Polypeptidketten, sowie deren Anordnung in bestimmten Faltungsmustern. Grundlage für diese Sekundärstruktur ist auf der einen Seite die Starrheit der Peptidbindung und auf der anderen Seite das Bestreben der Kette mögliche Wasserstoffbrückenbindungen zu maximieren. Wasserstoffbrückenbindungen können sich bevorzugt zwischen dem H-Atom am Stickstoff der Peptidbindung und dem Carbonylsauerstoff innerhalb einer anderen Peptidgruppe ausbilden (vgl. Abb. 7).
In der Folge bilden sich zwei möglich Strukturen aus, die die Sekundärstruktur eines Proteins dominieren:
- die
- Helix
- die
- Faltblattstruktur
 - Helix
- Helix
Die
- Helix
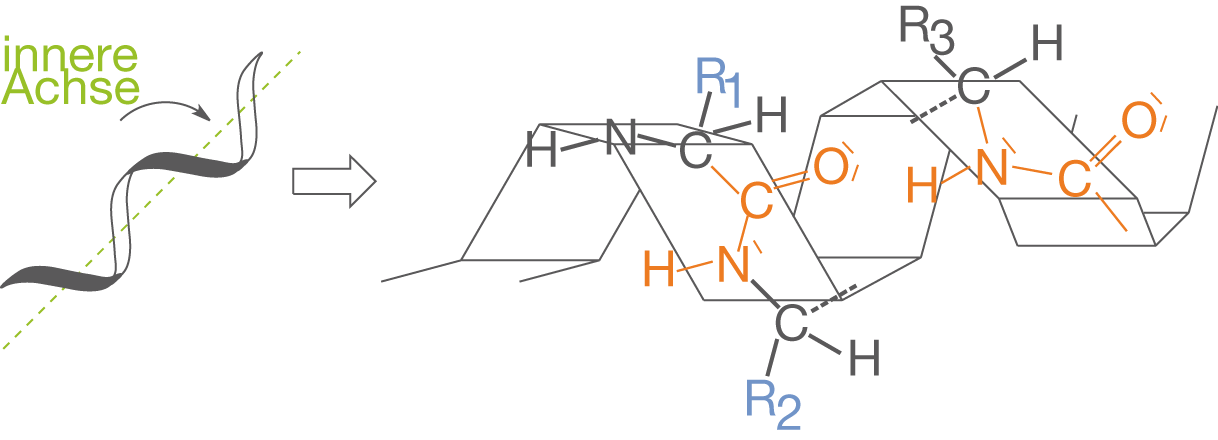
Die - Helix stellt eine Sekundärstruktur dar, die von einer einzigen Polypeptidkette aufgebaut wird. Hierbei sind insbesondere Aminosäuren enthalten, die verhältnismäßige große Reste aufweisen. Das Polypeptid ist im Fall einer Helix gleichsam um eine innere Achse gewunden (vgl. Abb. 8). Auf der rechten Seite in Abbildung 8 siehst du die Struktur einer Helix auf Grundlage der Peptidgruppe angedeutet. Jede dieser funktionellen Gruppen liegt wie bereits im Abschnitt „Räumliche Struktur“ diskutiert in einer Ebene, was auf die Mesomeriestabilisierung zurückzuführen ist. Die Reste
-
ragen von der Helix weg. Aus diesem Grund sind in diesem Fall große Reste auch kein Problem, da sie genügend Platz haben und sich nicht gegenseitig beeinflussen. Die Helixstruktur wird durch Wasserstoffbrückenbindungen innerhalb des Moleküls (intramolekular) stabilisiert.
Störungen durch Prolin
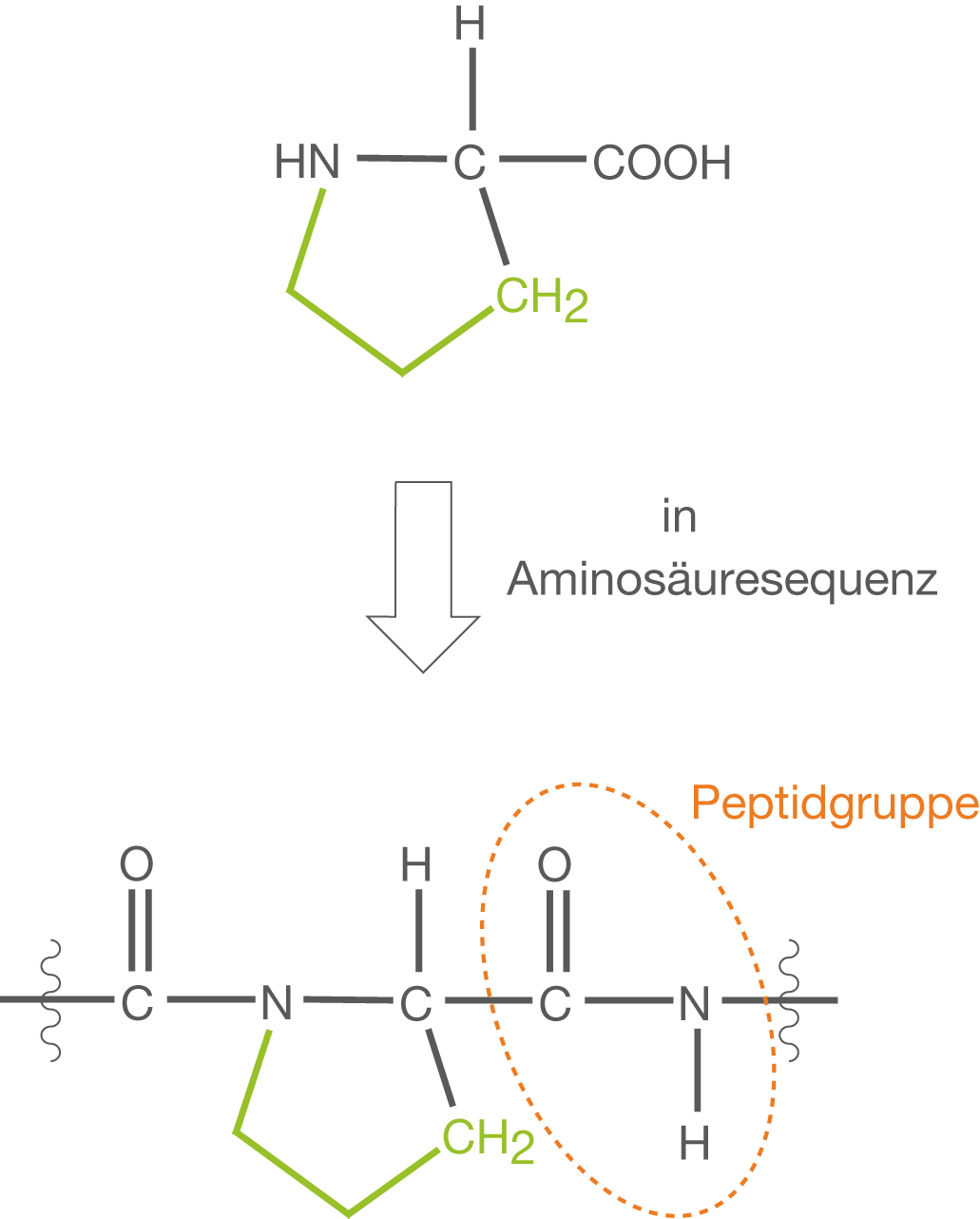
Eine Störung der -Helix wird durch Prolin herbeigeführt (vgl. Abb. 9).
Das Problem ist hierbei die cyclische Struktur des Rests von Prolin: Eine freie Drehung um die N-C-Bindungsachse ist nicht mehr gewährleistet, wie im Fall anderer Aminosäuren mit linearen Resten. Dies führt zur Störung der -Helix, indem beispielsweise Ecken ausgebildet werden.
 -Faltblatt
-Faltblatt
Neben der -Helix besteht ein zweiter Typ der Sekundärstruktur in Form der
-Faltblattstruktur. Diese Struktur weist eine plattige Form auf, die gefaltetem Papier ähnelt. Dabei stehen die Reste
-
der ehemaligen Aminosäuren in der Polypeptidkette nach oben und unten weg (vgl. Abb. 10) Die Peptidketten werden durch Wasserstoffbrückenbindungen stabilisiert. Beachte, dass es sich im Vergleich zur
- Helix hierbei um zwischenmolekulare (intermolekulare) Wechselwirkungen handelt. Die Anordnung der beiden Peptidketten kann noch weiter in parallel oder antiparallel unterschieden werden, je nachdem wie sie zueinander orientiert sind.
Tertiärstruktur
Die -Helix und die
-Faltblattstruktur sind sehr geordnete Strukturen. Im Fall von Proteinen ist es aber nicht der Fall, dass die Peptidketten immer so wohl geordnet vorliegen. Ein Beispiel haben wir schon im Fall von Prolin kennen gelernt, dass die Struktur der
- Helix aufbricht. Dementsprechend weist ein Protein Bereiche auf, die teilweise stark verknäult und gefaltet sind. Diese globulären Bereiche werden als Tertiärstruktur bezeichnet. Für ihrer Stabilität sind eine Reihe von Wechselwirkungen zuständig:
- Kovalente Disulfidbrücken
- Wechselwirkungen ionischer Reste
- Van-der-Waals-Kräfte
Von Disulfidbrücken und ionischen Resten
Disulfidbrücken
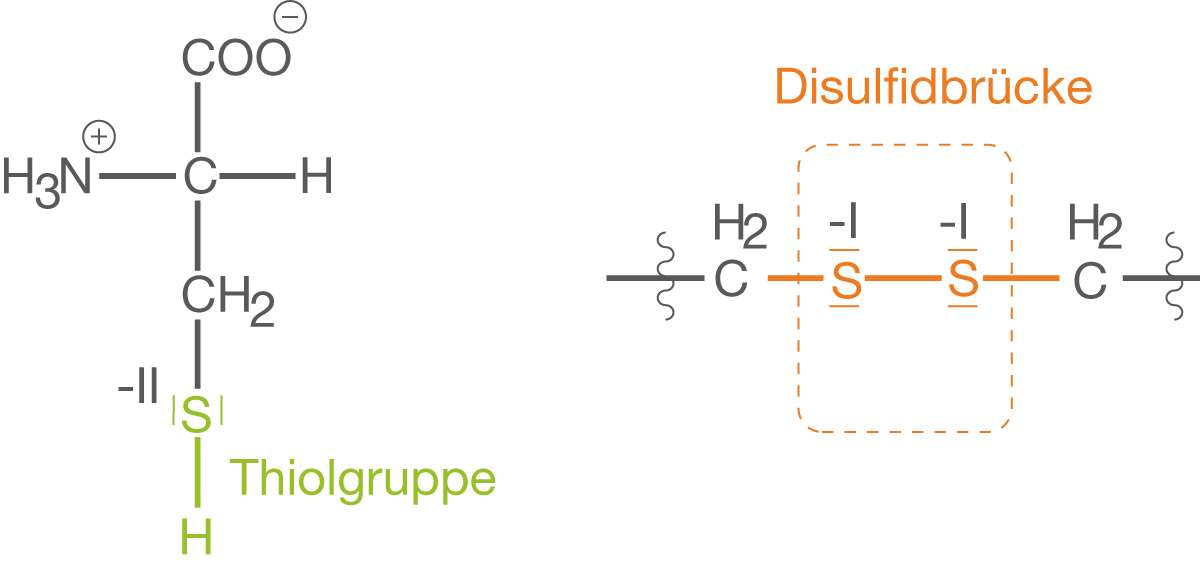
Disulfidbrücken gehen auf die Aminosäure Cystein zurück, die eine endständige Thiolgruppe (R-SH) aufweist (vgl. Abb. 11). Durch die Oxidation der Thiolgruppe entsteht die angesprochene Disulfidbrücke, eine kovalente Bindung zwischen den beiden Schwefelatomen.
Im Vergleich zu den Wasserstoffbrückenbindungen und anderen Wechselwirkungen, handelt es sich bei einer Disulfidbrücke effektiv um eine kovalente Bindung, was für ihre vergleichsweise hohe Stabilität spricht. Kommen nun in verschiedenen Peptidketten diese endständigen Thiolgruppen vor, so können die Ketten über Disulfidbrücken Bindungen miteinander eingehen, die zu einer erhöhten Stabilität beitragen. Dementsprechend wird die Tertiärstruktur so stabilisiert.
Ionische Wechselwirkungen
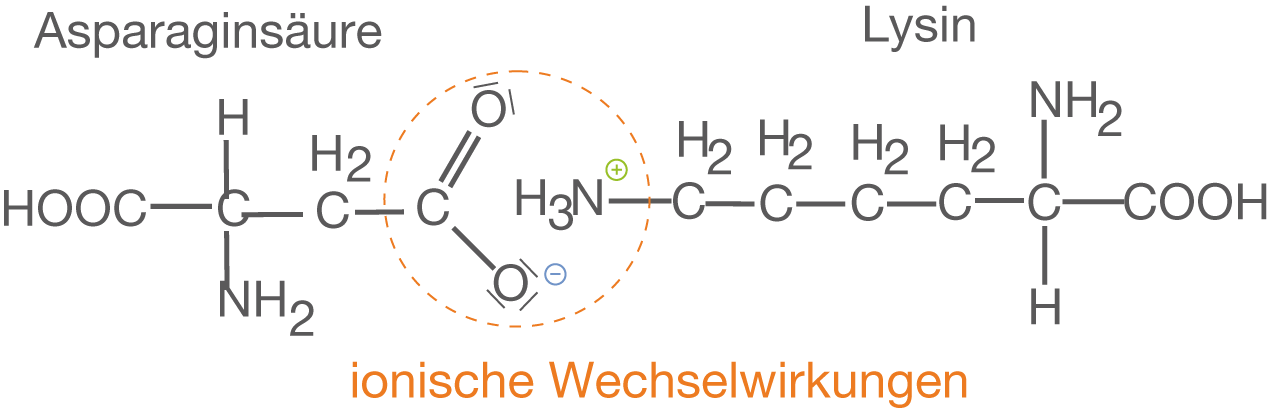
Ionische Wechselwirkungen zwischen oder innerhalb von Peptidketten sind auf die Säure-Base-Eigenschaften der funktionellen Gruppen von Polypeptiden zurückzuführen. Endständige Carboxy- und Aminogruppen reagieren in ähnlicher Weise, wie im Fall der Zwitterionen: Carboxygruppen werden deprotoniert, sodass sie eine negative Ladung tragen. Dahingegen werden die basischen Aminogruppen protoniert, was in einer positiven Ladung resultiert. Die Folgen sind in Abbildung 12 dargestellt.
Befinden sich diese beiden entgegengesetzt geladenen Reste nun in nächster Nähe zueinander, dann ziehen sich die beiden ungleichnamigen Ladungen an. Die ionische Wechselwirkung führt auf Grundlage anziehender elektrostatischer Kräfte zur Ausbildung einer Ionenbindung.
Das „Wunder“ der Dauerwelle
Das menschliche Haar ist aus einem Faserprotein namens Keratin aufgebaut. Keratin weist Cysteinreste in seiner Molekülstruktur auf, was dazu führt, dass hier Disulfidbrücken ausgebildet werden können. Diese Disulfidbrücken sind dafür verantwortlich, das die Dauerwelle eine Existenzberechtigung besitzt. Wir wollen uns nun kurz die entscheidenden Prozesse anschauen, die eine Dauerwelle so haltbar machen.
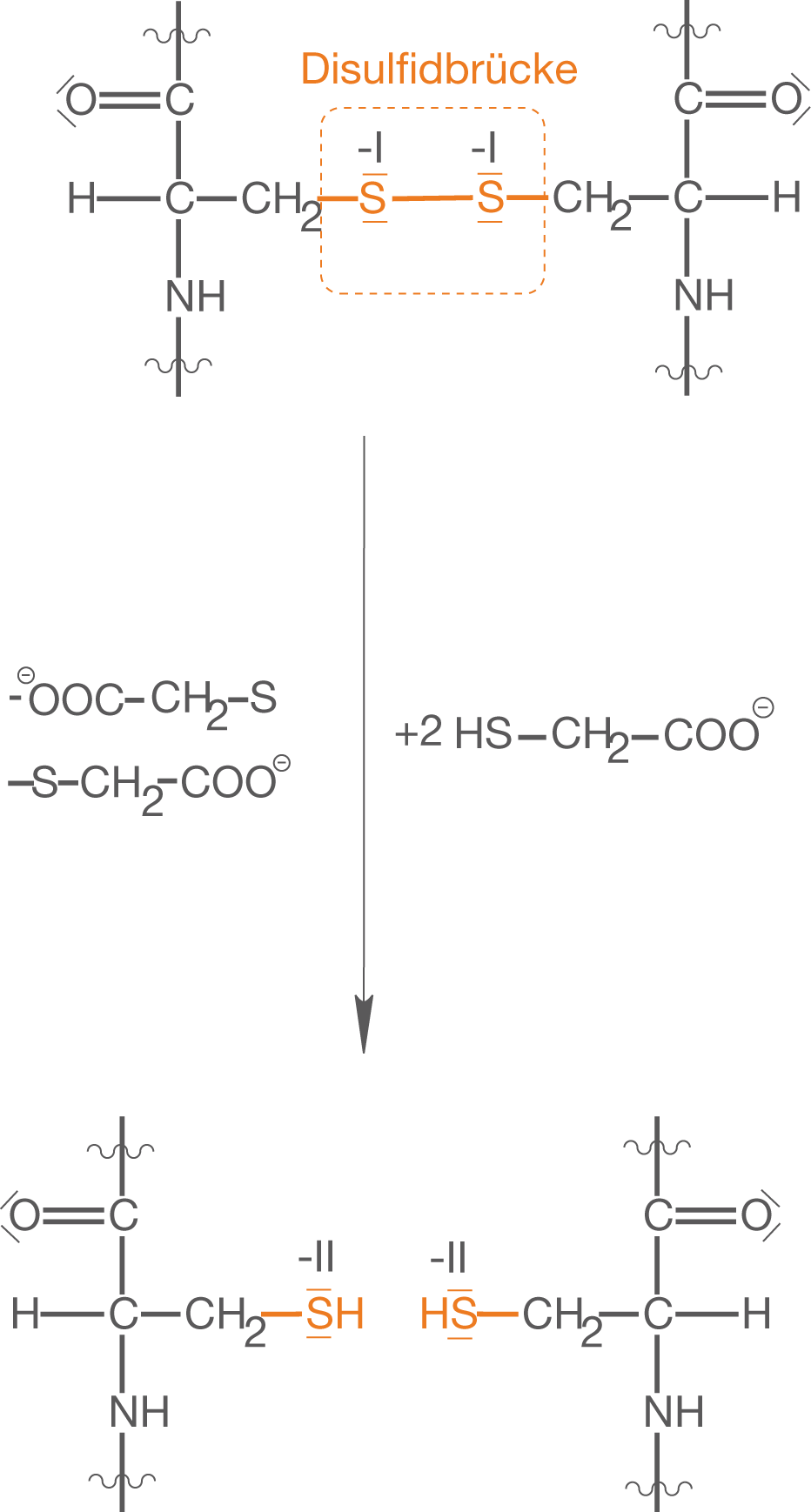
(1) Das Aufbrechen bestehender Disulfidbrücken
Zunächst wird das Haar mit dem Reduktionsmittel Thioglykolat (vgl. Abb. 13) behandelt (liegt eigentlich als Ammoniumthioglycolat vor), was eine Reduktion der Schwefelatome und somit eine Spaltung der Disulfidbrücke nach sich zieht. Das Produkt sind die endständigen Thiolgruppen von Cystein. Gleichzeitig wird das Thioglykolat oxidiert und somit über eine entsprechende Disulfidbrücke verknüpft.
(2) Neue Frisur und schließen der Disulfidbrücke
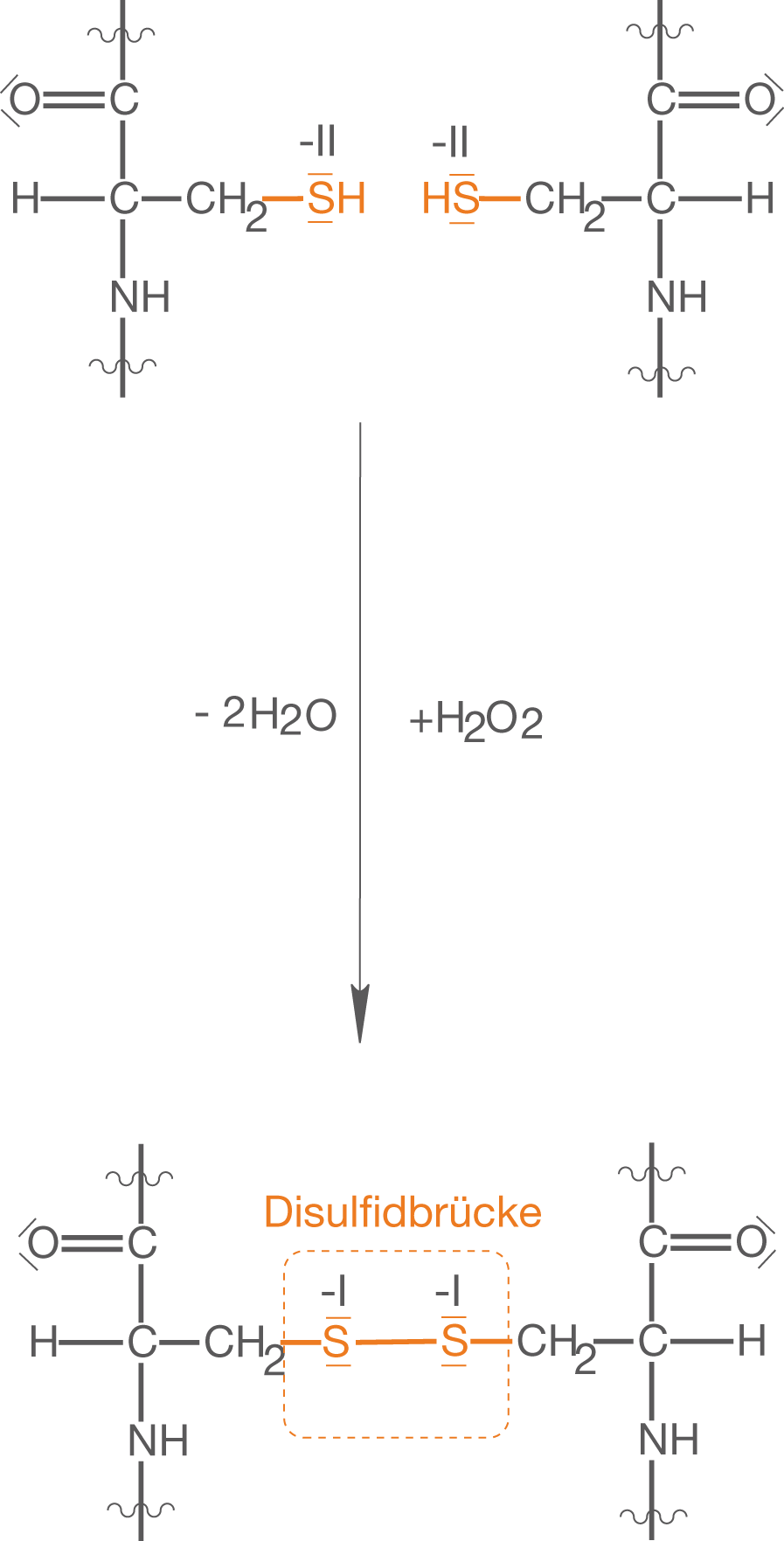
Nachdem die Haare in eine gewünschte Form gebracht werden, können die Disulfidbrücken wieder geschlossen werden, um für eine dauerhafte Stabilität zu sorgen. Du kannst sehen, dass diese Stabilität insbesondere darauf zurückzuführen ist, dass es sich hierbei um kovalente Bindungen handelt, die neu geknüpft werden. Um von den beiden Thiolgruppen wieder zur Disulfidbrücke zu gelangen, kommt mit Wasserstoffperoxid () ein relativ starkes Oxidationsmittel zum Einsatz (vgl. Abb. 14).
Wasserstoffperoxid oxidiert die beide endständigen Thiolgruppen zur Disulfidbrücke und wird selbst zu Wasser reduziert. Die fertige Dauerwelle ist nun stabil genug, um Wind und Wetter zu trotzen.
Quartärstruktur und Denaturierung
Die Quartärstruktur
Die Quartärstruktur stellt die oberste der hier besprochenen Strukturebenen eines Proteins dar. Ein Protein besteht meist nicht nur aus einem Polypeptid, sondern aus mehreren, die Zusammen eine funktionelle Einheit ergeben. Die Quartärstruktur beschreibt nun die gegenseitige Lage und räumliche Anordnung dieser Polypeptide im Gesamtprotein. Diese Anordnung führt letztendlich auch dazu, dass Proteine spezifische Aufgaben, beispielsweise in Form von Enzymen (Biokatalysatoren), erledigen. Wichtig ist, dass die Quartärstruktur bereits von der Primärstruktur der einzelnen Polypeptide entscheidend beeinflusst wird.
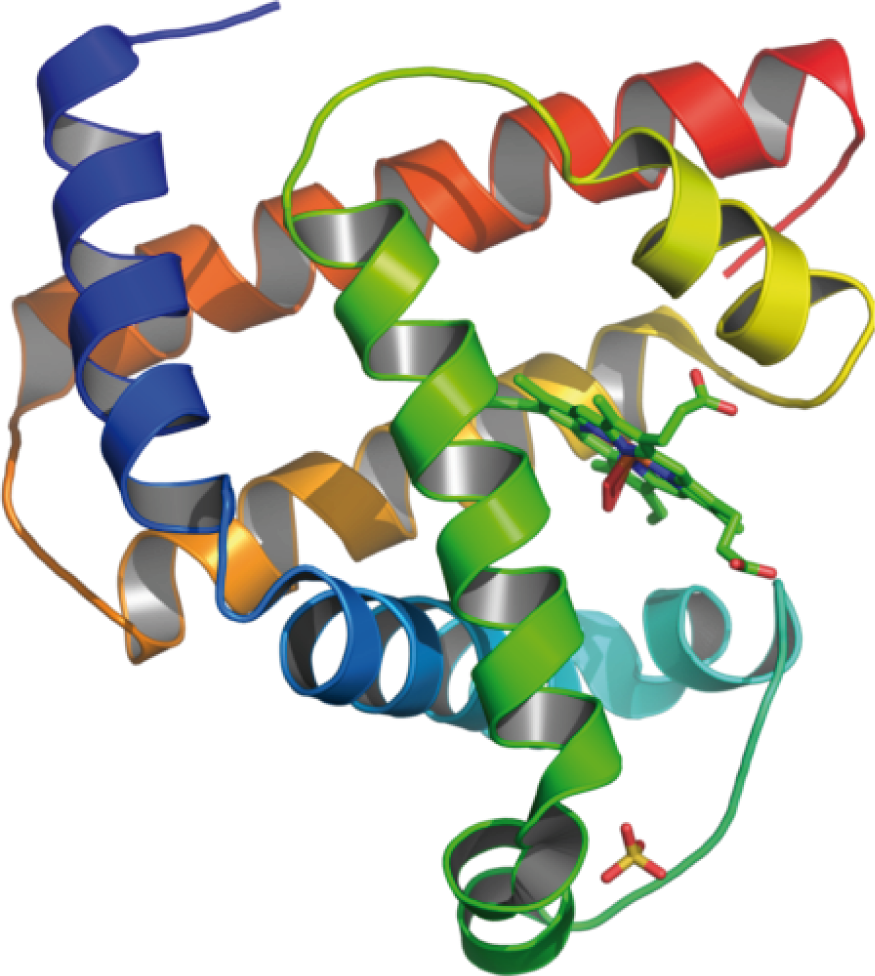
Ein Standardbeispiel für ein Protein mit einer Quartärstruktur ist das Hämoglobin, welches für den Sauerstofftransport verantwortlich ist (vgl. Abb. 15).
Denaturierung
Unter Denaturierung versteht man im Allgemeinen die räumliche Veränderung eines Proteins. Da die räumliche Orientierung in vielen Fällen einen funktionellen Einfluss hat, kann die Denaturierung auch als Schädigung der Proteinstruktur angesehen werden, die im Extremfall zu irreparablen Schäden führt. Da es sich um eine räumliche Veränderung handelt, wird die Primärstruktur in aller Regel nicht geschädigt. Die Denaturierung kann mehrere Ursachen haben, von denen vier an dieser Stelle beispielhaft genannt werden sollen: Änderungen des pH-Werts, Einfluss von Reduktionsmitteln, Hitze und Schwermetalle.
| pH-Wert-Änderung: | Der pH-Wert hat einen entscheidenden Einfluss auf die Ladungsverhältnisse innerhalb der Proteinstruktur. Durch Änderungen des pH-Werts kann es zum Verlust protonierter und deprotonierter funktioneller Gruppen kommen, was mit einem Verlust von Ladungen und somit von ionischen Wechselwirkungen einhergeht. Die Stabilität wird geschädigt. |
| Reduktionsmittel: | Bei Anwesenheit von Reduktionsmitteln werden eventuelle Disulfidbrücken durch Reduktion gespalten, was wiederum erhebliche Stabilitätseinbußen des Proteinmoleküls nach sich ziehen kann. |
| Hitze: | Hitze kann als externe Zufuhr von Wärmeenergie verstanden werden. Ist die zugeführte Energiemenge zu groß, kommt es zur Schädigungen von Bindungen und zwischenmolekularen Kräften. |
| Schwermetalle: | Schwermetallionen können in Wechselwirkung mit polaren Gruppen innerhalb des Proteins treten. Somit werden hier insbesondere ionische Bindungen stark abgeschwächt oder komplett aufgebrochen, da das Schwermetallkation beispielsweise den Platz der protonierten Aminogruppe einnimmt. |
Dennoch können wir auch von Denaturierungsprozessen profitieren, beispielsweise wenn wir uns unser Frühstücksei kochen oder wenn die Salzsäure im menschlichen Magen dabei hilft Fleisch zu verdauen.
Der Nachweis von Proteinen
Die Biuret-Probe
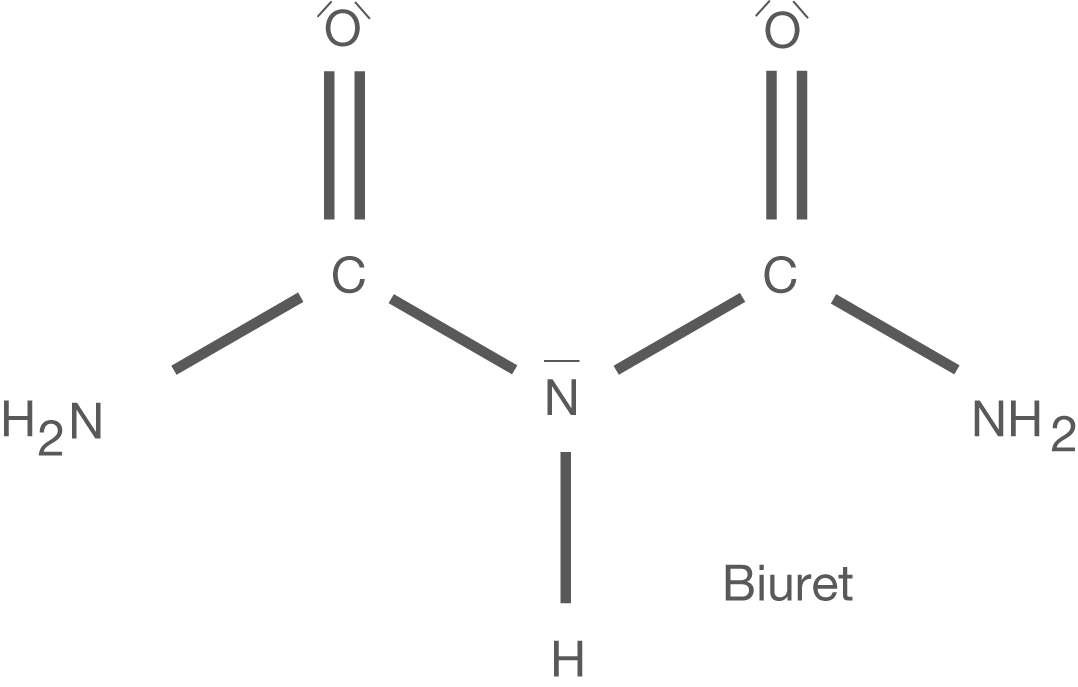
Die Biuret-Probe ermöglicht den Nachweis von Peptidbindungen in Proteinen. Diese Probe verdankt ihren Namen der Verbindung Biuret, die aber eigentlich gar nicht Bestandteil dieser Probe ist, sondern lediglich ebenfalls damit nachgewiesen werden kann. Die Biuret-Probe läuft mit Cu(II)-Ionen ab. Diese zweiwertigen Kationen () bilden in alkalischen Lösungen (
) und bei Anwesenheit von Peptidbindungen sogenannte Komplexverbindungen aus, die eine charakteristische violette Farbe aufweisen (vgl. Abb. 16).
Die Ninhydrinreaktion
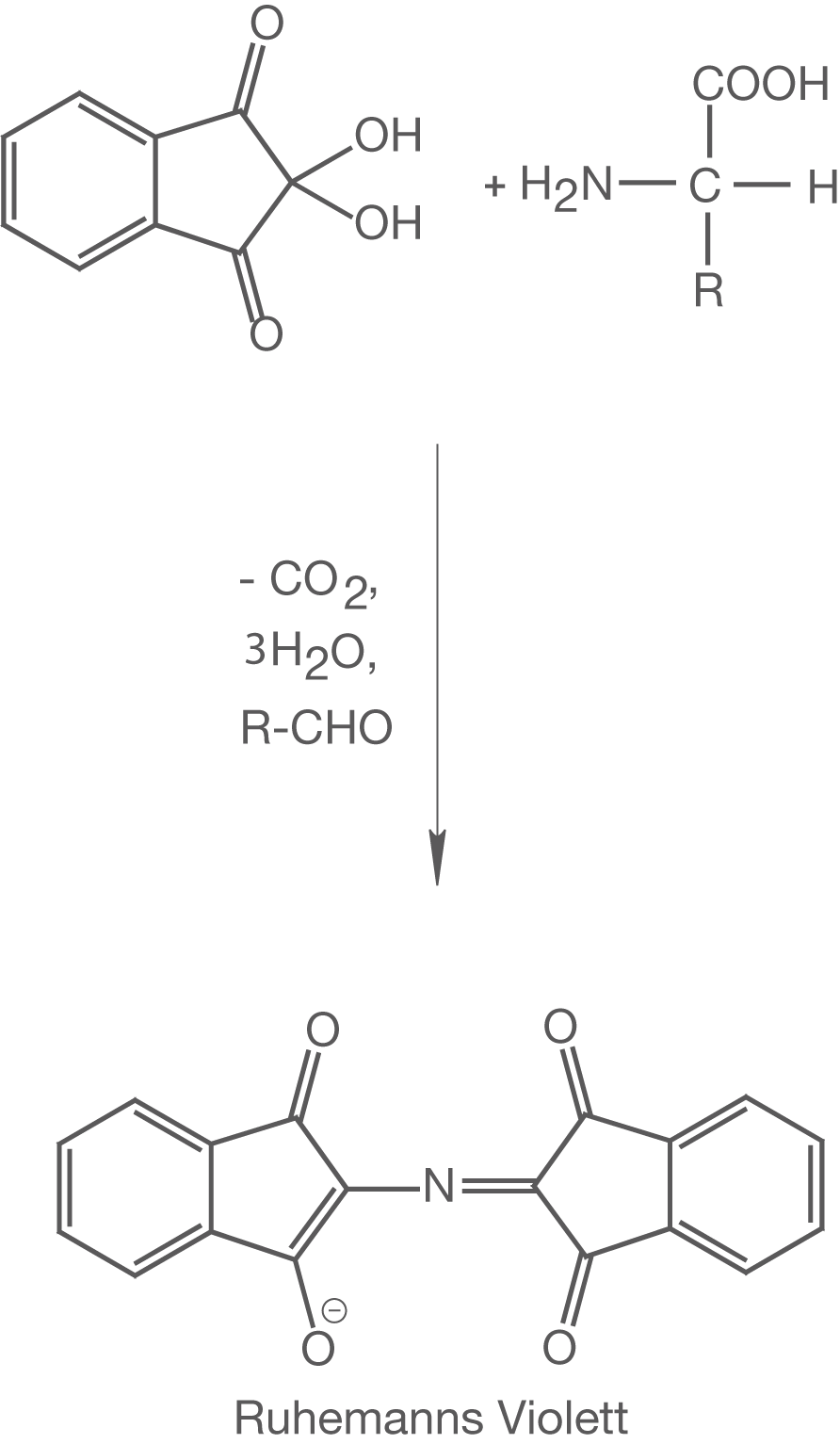
Im Gegensatz zur Biuret-Probe können mithilfe der Ninhydrinreaktion Aminogruppen nachgewiesen werden. Dementsprechend eignet sich dieser Nachweis vor allem für Aminosäuren (vgl. ChemieLV-Skript Aminosäuren) und kurzkettige Peptide (Oligopeptide) mit ungeschützten Aminogruppen. Im Falle dieses Nachweises reagiert das Molekül Ninhydrin mit einer -Aminosäure zu dem violetten Farbstoff Ruhemanns Violett (vgl. Abb. 17).
Zusammenfassung
- Aminosäuren sind die Monomere der Peptide: Je nach Kettenlänge werden Oligo- und Polypeptide unterschieden.
- Die Peptidgruppe
wird durch eine Kondensationsreaktion zwischen der Carboxy- und der Aminogruppe zweier Aminosäuren gebildet.
- Die Peptidgruppe ist mesomeriestabilisiert, womit die C-N-Bindung einen partiellen Doppelbindungscharakter aufweist. Dadurch ist die Rotation um diese Achse stark eingeschränkt und alle Atome und Bindungen, die an der Peptidgruppe beteiligt sind, liegen in einer Ebene.
- Die Reihenfolge in der Aminosäuren in einem Polypeptid verknüpft sind, nennt man Aminosäuresequenz. Diese legt die Primärstruktur von Proteinen fest.
- Polypeptide werden auf Grundlage des Drei-Buchstaben-Codes benannt.
- Die Sekundärstruktur bezieht sich auf die räumliche Orientierung von Polypeptiden und wird insbesondere durch die Maximierung der Anzahl eventueller Wasserstoffbrückenbindungen geprägt.
- Die
-Helix stellt ein gewundenes Polypeptidmolekül dar, welches durch intramolekulare Wasserstoffbrückenbindungen stabilisiert wird. Diese Struktur tritt im Fall von Polypeptiden mit großen Resten auf.
- Die
-Faltblattstruktur ähnelt gefaltetem Papier und wird durch intermolekulare Wasserstoffbrückenbindungen stabilisiert. Die Peptidketten sind hierbei entweder parallel oder antiparallel zueinander angeordnet.
- Bereiche eines Proteins, die stark verknäult vorliegen, werden als globulär bezeichnet und bilden die Tertiärstruktur des Proteins.
- Die Stabilität der Tertiärstruktur geht auf Disulfidbrücken zwischen Cysteinresten, auf ionische Wechselwirkungen endständiger geladener funktioneller Gruppen und auf van-der-Waals-Kräfte zurück.
- Im Fall der Dauerwelle werden Disulfidbrücken im Keratin der Haare genutzt, um eine stabile Frisur zu erreichen.
- Die Quartärstruktur eines Proteins beschreibt die gegenseitige räumliche Orientierung verschiedener Polypeptide, die in der Summe eine funktionelle Einheit bilden.
- Die Quartärstruktur wird bereits von der Primärstruktur beeinflusst.
- Unter Denaturierung versteht man die räumliche Veränderung der Proteinstruktur, was in aller Regel zu irreparablen Folgen führt. Auslöser sind beispielsweise Änderungen des pH-Werts, Hitzeeinfluss, die Anwesenheit von Reduktionsmitteln und die Anwesenheit von Schwermetallionen.
- Peptidgruppen können mithilfe der Biuret-Probe nachgewiesen werden.
- Freie Aminogruppen in Aminosäuren und Oligopeptiden werden mithilfe der Ninhydrin-reaktion nachgewiesen.