Aufgabe 5 – Salze der Salpetersäure
Die Salze der Salpetersäure kommen in unterschiedlichsten Anwendungen zum Einsatz. Ammoniumnitrat  wird z. B. in Kühlpacks bei Sportverletzungen eingesetzt. Kaliumnitrat
wird z. B. in Kühlpacks bei Sportverletzungen eingesetzt. Kaliumnitrat  wird als Oxidationsmittel in der Pyrotechnik verwendet.
wird als Oxidationsmittel in der Pyrotechnik verwendet.
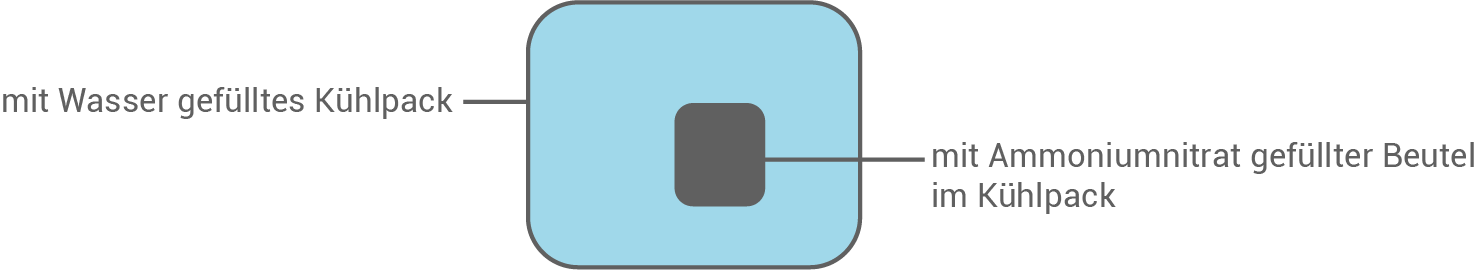

Abbildung 1: Schematische Darstellung eines Kühlpacks
1
Ammoniumnitrat löst sich unter Abkühlung in Wasser, daher wird es in sogenannten Kühlpacks (siehe Abb. 1) zur Schmerzlinderung bei Sportverletzungen eingesetzt. Um den Lösungsvorgang in Gang zu setzen, wird der innere Beutel zum Platzen gebracht und das darin befindliche Ammoniumnitrat löst sich im Wasser des äußeren Beutels.
1.1
Die Abkühlung beim Lösen von Ammoniumnitrat in Wasser soll in einem Modellversuch quantitativ untersucht werden.
- Beschreibe die Durchführung eines Modellversuchs mithilfe einer beschrifteten Skizze.
(3 VP)
1.2
In einem Experiment werden  Ammoniumnitrat in Wasser gelöst. Die Lösung
Ammoniumnitrat in Wasser gelöst. Die Lösung  ,
,  ) kühlt sich dabei von
) kühlt sich dabei von  auf
auf  ab.
Hinweis: In der verdünnten Lösung entspricht die Wärmekapazität in guter Näherung der spezifischen Wärmekapazität des Wassers
ab.
Hinweis: In der verdünnten Lösung entspricht die Wärmekapazität in guter Näherung der spezifischen Wärmekapazität des Wassers  , die Wärmekapazität der Versuchsanordnung kann vernachlässigt werden.
, die Wärmekapazität der Versuchsanordnung kann vernachlässigt werden.
- Berechne mit den experimentell bestimmten Daten die Enthalpieänderung beim Lösen von
Ammoniumnitrat
.
- Beurteile den Einfluss einer deutlichen Vergrößerung der Masse des zu lösenden Ammoniumnitrats auf die zu erwartende Genauigkeit der experimentellen Bestimmung der Lösungsenthalpie
bei gleichbleibendem Volumen des Wassers.
(3 VP)
1.3
Der Lösungsvorgang von Ammoniumnitrat kann mit folgender Reaktionsgleichung dargestellt werden:


 +
+ 
- Berechne die Entropieänderung des Lösungsvorgangs.
- Erkläre mithilfe der GIBBS-HELMHOLTZ-Gleichung, unter welcher Voraussetzung sich Salze unter Abkühlung (endotherm) in Wasser lösen können.
- Zeige durch eine Rechnung, dass diese Voraussetzung für das Lösen von Ammoniumnitrat bei Standardbedingungen erfüllt ist.
(5 VP)
1.4
Das Lösen von Salzen kann gedanklich vereinfacht in zwei Prozesse unterteilt werden:
a.
Die Trennung der Ionen aus dem Gitterverbund, wofür Energie benötigt wird.
b.
Die Anordnung der Wassermoleküle um die Ionen, bei der Energie frei wird.
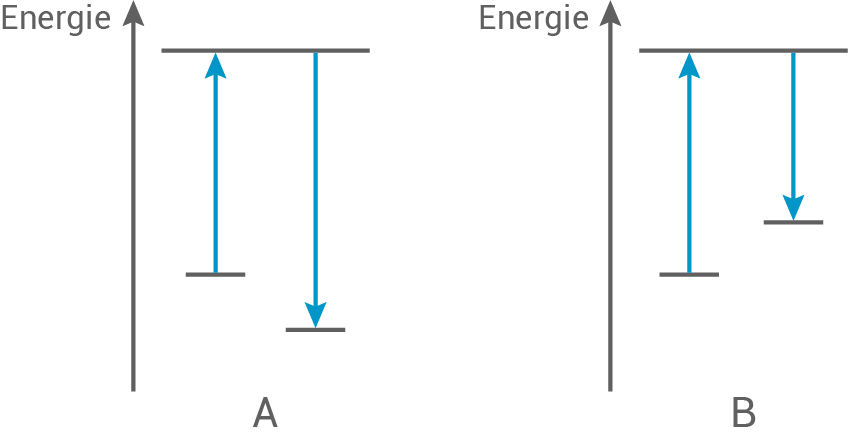
Abb. 2 zeigt schematisch einen exothermen und endothermen Lösungsvorgang, bei dem die beiden beschriebenen Prozesse dargestellt sind.

Abbildung 2: Energieschemata für einen exothermen und endothermen Lösungsvorgang
- Gib das Energieschemata an, das den Lösungsvorgang von Ammoniumnitrat qualitativ wiedergibt und begründe deine Angabe.
(2 VP)
2
Ammoniumnitrat zersetzt sich ab ca.  in Distickstoffoxid
in Distickstoffoxid  und Wasser. Bei höheren Temperaturen zerfällt es in Wasser, Stickstoff und Sauerstoff.
und Wasser. Bei höheren Temperaturen zerfällt es in Wasser, Stickstoff und Sauerstoff.
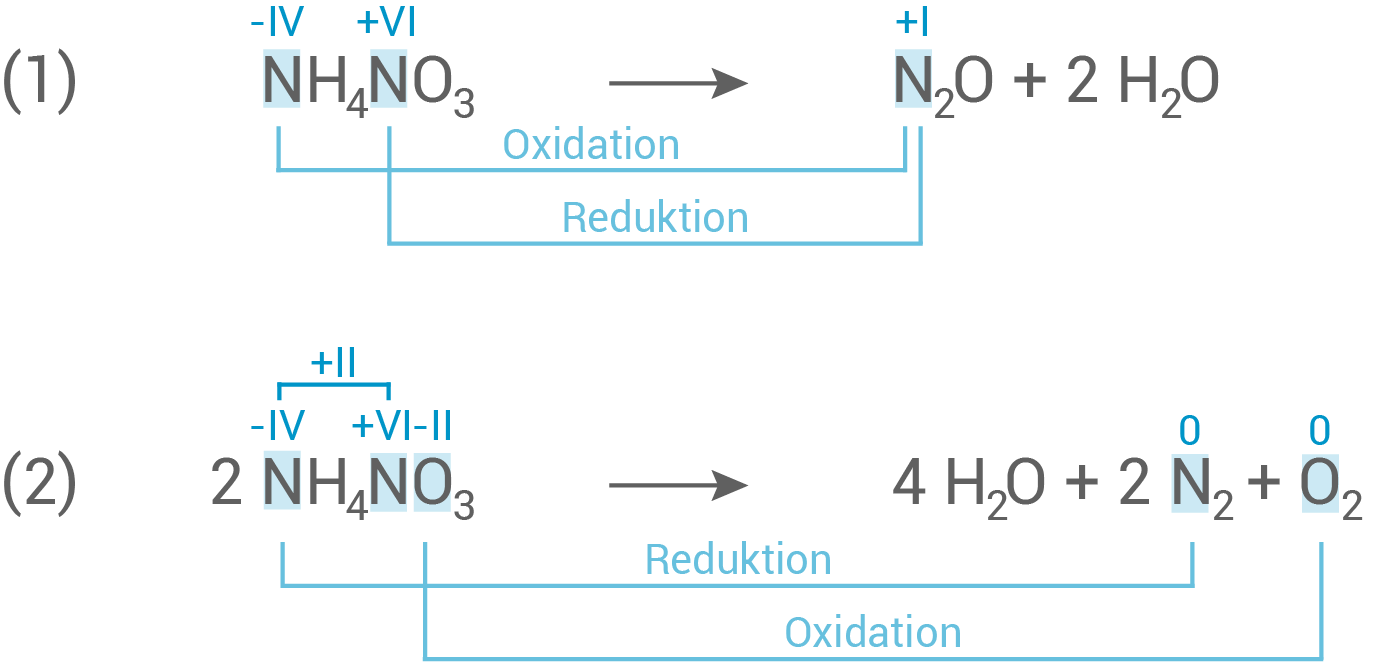
- Stelle für die beiden Zersetzungsreaktionen jeweils eine Reaktionsgleichung auf.
- Begründe, dass es sich jeweils um eine Redox-Reaktion handelt und kennzeichne in deinen Reaktionsgleichungen Oxidation und Reduktion.
(2 VP)
3
Kaliumnitrat wird in pyrotechnischen Produkten verwendet und ist als brandfördernd eingestuft. Vereinfacht kann für die Reaktion mit Kohlenstoff folgende Reaktionsgleichung formuliert werden:
 +
+ 

 +
+  Werden
Werden  Kaliumnitrat vollständig umgesetzt, wird eine Wärmemenge
Kaliumnitrat vollständig umgesetzt, wird eine Wärmemenge  frei.
frei.
- Erkläre die Einstufung von Kaliumnitrat als brandfördernder Stoff.
- Berechne mithilfe der obigen Wärmemenge und den thermodynamischen Daten aus dem Anhang die molare Standardbildungsenthalpie
für Kaliumnitrat.
(4 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Durchführung eines Modellsversuchs mit Skizze
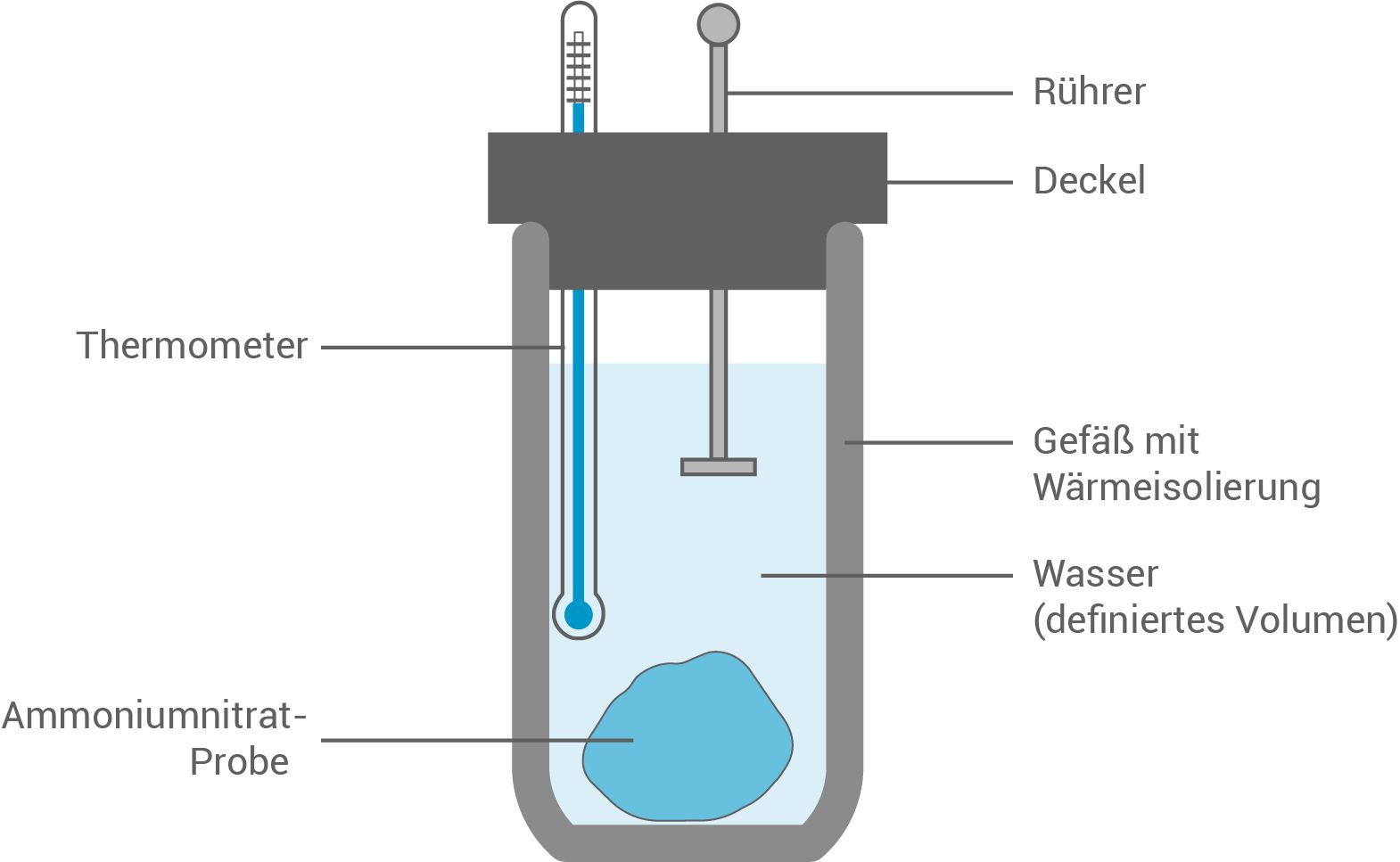 Zunächst wird eine definierte Menge an Wasser in das Kalorimeter eingefüllt. Wenn das Wasser und der Kalorimeter identisch sind, wird eine abgewogene des Ammoniumnitrats hinzugegeben und bis zur Auflösung verrührt. Wichtig ist regelmäßige Messung der Temperatur.
Zunächst wird eine definierte Menge an Wasser in das Kalorimeter eingefüllt. Wenn das Wasser und der Kalorimeter identisch sind, wird eine abgewogene des Ammoniumnitrats hinzugegeben und bis zur Auflösung verrührt. Wichtig ist regelmäßige Messung der Temperatur.

1.2
Berechnung der Enthalpieänderung
Da die Wärmekapazität der Versuchsanordnung vernachlässigt werden kann, lässt sich die beim Lösen umgesetzte Wärme  folgendermaßen berechnen:
Es handelt sich um einen endothermen Vorgang, deswegen behält die Lösungsenthalpie das positive Vorzeichen.
Beurteilung des Einflusses einer Massenvergrößerung
Wird die Masse an Ammoniumnitrat bei gleichbleibendem Wasservolumen vergrößert, ändert sich die Konzentration der Lösung
folgendermaßen berechnen:
Es handelt sich um einen endothermen Vorgang, deswegen behält die Lösungsenthalpie das positive Vorzeichen.
Beurteilung des Einflusses einer Massenvergrößerung
Wird die Masse an Ammoniumnitrat bei gleichbleibendem Wasservolumen vergrößert, ändert sich die Konzentration der Lösung  . Abweichungen sind demnach bei Verwendung der Wärmekapazität von reinem Wasser erkennbar. Die Vergrößerung der Masse könnte aber auch zur Überschreitung der Löslichkeit und damit zu Fehlern bei der Bestimmung der Lösungsenthalpie führen.
. Abweichungen sind demnach bei Verwendung der Wärmekapazität von reinem Wasser erkennbar. Die Vergrößerung der Masse könnte aber auch zur Überschreitung der Löslichkeit und damit zu Fehlern bei der Bestimmung der Lösungsenthalpie führen.
1.3
Entropieänderung des Lösungsvorgangs
Für die Berechnung der Entropie gilt:
Da  gilt:
gilt:
 Vorraussetzung für das Lösen der Salze
Als Grundlage dient die GIBBS-HELMHOLTZ-Gleichung:
Vorraussetzung für das Lösen der Salze
Als Grundlage dient die GIBBS-HELMHOLTZ-Gleichung:
 Damit eine Reaktion abläuft, also exergonisch ist, muss
Damit eine Reaktion abläuft, also exergonisch ist, muss  gelten.
gelten.
Bei einem endothermen Vorgang (Abkühlen) beträgt und daraus folgt als Bedingung für die Reaktion:
und daraus folgt als Bedingung für die Reaktion:
 Lösen von Ammoniumnitrat bei Standardbedingungen
Damit sich das Salz bei Standardbedingungen löst, muss
Lösen von Ammoniumnitrat bei Standardbedingungen
Damit sich das Salz bei Standardbedingungen löst, muss  sein. Mit den in den zuvor berechneten Werten für die Enthalpie (negativer Wert, da Abkühlung) und die Entropie lässt sich diese Tatsache mit der GIBBS-HELMHOLTZ-Gleichung überprüfen:
Alternative:
Berechnung der näherungsweisen Temperatur, ab der
sein. Mit den in den zuvor berechneten Werten für die Enthalpie (negativer Wert, da Abkühlung) und die Entropie lässt sich diese Tatsache mit der GIBBS-HELMHOLTZ-Gleichung überprüfen:
Alternative:
Berechnung der näherungsweisen Temperatur, ab der  gilt:
gilt:



Bei einem endothermen Vorgang (Abkühlen) beträgt
1.4
Angabe des passenden Energieschemata und Begründung
Das Lösen von Ammoniumnitrat ist endotherm. Folglich muss für die Entfernung der Ionen aus dem Gitter mehr Energie aufgebracht werden, als bei der Anordnung der Wassermoleküle um die Ionen frei wird.
Der Lösungsvorgang wird im Schema B dargestellt. Hier ist der Betrag des energieliefernden Vorgangs kleiner als der des Vorgangs der Energie benötigt.
Der Lösungsvorgang wird im Schema B dargestellt. Hier ist der Betrag des energieliefernden Vorgangs kleiner als der des Vorgangs der Energie benötigt.
2
Reaktionsgleichungen und Kennzeichnung von Oxidation und Reduktion

3
Einstufung von Kaliumnitrat
Um Kaliumnitrat einzustufen, wird die in der Aufgabenstellung dargestellte Reaktionsgleichung betrachtet.
Kaliumnitrat fungiert als Sauerstofflieferant für die Reaktion von Kohlenstoff zu Kohlenstoffdioxid
zu Kohlenstoffdioxid  . Der Stoff wird daher als brandfördernd eingestuft.
Berechnung der molaren Standardbildungsenthalpie
Für die Berechnung gilt:
Für
. Der Stoff wird daher als brandfördernd eingestuft.
Berechnung der molaren Standardbildungsenthalpie
Für die Berechnung gilt:
Für  wird die Gleichung umgestellt, die thermodynamischen Daten aus dem Anhang und die gegebene Wärmemenge eingesetzt:
wird die Gleichung umgestellt, die thermodynamischen Daten aus dem Anhang und die gegebene Wärmemenge eingesetzt:
Kaliumnitrat fungiert als Sauerstofflieferant für die Reaktion von Kohlenstoff