Aufgabe 4 – Edelmetalle
In Smartphones, Tablets sowie weiteren elektronischen Geräten sind u. a. Edelmetalle wie z.B. Gold, Kupfer und Silber in elektrisch leitenden Bauteilen enthalten. Deren Rückgewinnung ist sowohl unter ökologischen als auch unter wirtschaftlichen Gesichtspunkten sinnvoll.
1
Häufig werden diese Metalle nicht in reiner Form, sondern als metallische Legierungen in elektronischen Bauteilen verwendet.
1.1
Zur Rückgewinnung der Metalle werden die Legierungen mit Salpetersäure behandelt. Folgende Reaktionsgleichung gibt vereinfacht den Ablauf der Reaktion des in der Legierung vorkommenden Silbers mit Salpetersäure wieder:


 Hinweis: In Silbernitrat
Hinweis: In Silbernitrat  ist das Silber-Ion einfach positiv geladen.
ist das Silber-Ion einfach positiv geladen.
- Gib die in der Reaktionsgleichung fehlenden stöchiometrischen Koeffizienten a, b, c, d und e an.
- Erläutere, dass es sich hierbei um eine Redoxreaktion handelt.
- Begründe unter Verwendung der in Anlage 3 tabellierten Elektrodenpotenziale, ob eine Reaktion von Gold
und Kupfer
mit Salpetersäure zu erwarten ist.
(6 VP)
1.2
Eine metallische Legierungsprobe mit einer Masse von  enthält neben Silber ausschließlich Kupfer und Gold. Diese Probe wird mit Salpetersäure zur Reaktion gebracht.
enthält neben Silber ausschließlich Kupfer und Gold. Diese Probe wird mit Salpetersäure zur Reaktion gebracht.
Zur Bestimmung des Silberanteils in der Legierungsprobe wird die entstandene Metallsalz-Lösung neutralisiert und anschließend elektrolysiert. Hierbei wird an einer Elektrode ausschließlich elementares Silber abgeschieden. An der anderen Elektrode ist die Bildung eines Gases beobachtbar, mit dem die Glimmspanprobe positiv verläuft.
und anschließend elektrolysiert. Hierbei wird an einer Elektrode ausschließlich elementares Silber abgeschieden. An der anderen Elektrode ist die Bildung eines Gases beobachtbar, mit dem die Glimmspanprobe positiv verläuft.
Zur Bestimmung des Silberanteils in der Legierungsprobe wird die entstandene Metallsalz-Lösung neutralisiert
- Stelle jeweils eine Teilgleichung für die Reaktion auf, die bei der Elektrolyse an der jeweiligen Elektrode abläuft.
- Bestimme unter Verwendung der in Anlage 3 tabellierten Elektrodenpotenziale den Spannungsbereich, bei dem die Abscheidung von Silber stattfindet, ohne dass auch Kupfer abgeschieden wird.
- Beschreibe eine experimentelle Vorgehensweise zur Bestimmung der Masse an abgeschiedenem Silber.
- Berechne den Massenanteil
in
an Kupfer in der Legierungsprobe, wenn angenommen wird, dass
Gold enthalten sind und bei der Elektrolyse
Silber abgeschieden werden.
(6 VP)
2
In verschiedenen Experimenten wird das Elektrodenpotenzial einer Silber-Halbzelle gegenüber einer Wasserstoff-Halbzelle untersucht.
2.1
Zunächst soll das Standardpotenzial  einer Silber-Halbzelle mithilfe einer Standard-Wasserstoff-Halbzelle experimentell bestimmt werden.
einer Silber-Halbzelle mithilfe einer Standard-Wasserstoff-Halbzelle experimentell bestimmt werden.
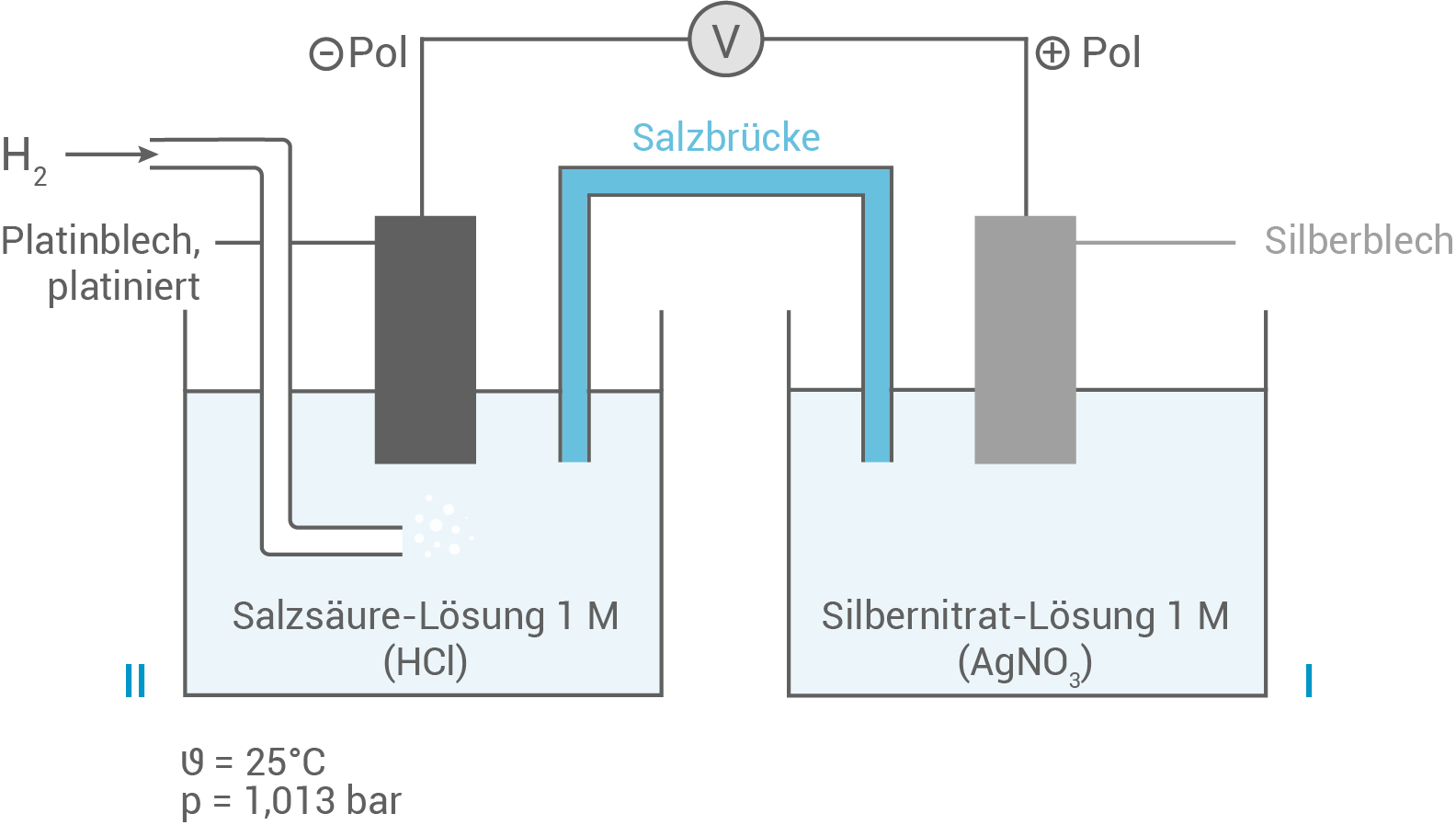
- Fertige für dieses Experiment eine beschriftete Skizze an.
- Erläutere mit Hilfe einer Berechnung die Vorgehensweise zur Herstellung von
der für das Experiment benötigten Silbernitrat-Lösung, wenn für das Experiment eine konzentrierte Silbernitrat-Lösung zur Verfügung steht, die in einem Liter
Silbernitrat enthält.
(5 VP)
2.2
In zwei weiteren Experimenten soll die Änderung des Elektrodenpotenzials bei Zugabe einiger Tropfen konzentrierter Salzsäure untersucht werden. Hierzu wird in einem Fall die Salzsäure in die Silber-Halbzelle gegeben, im anderen Fall in die Standard-Wasserstoff-Halbzelle. In beiden Fällen ist zu beobachten, dass die gemessene Spannung kleiner wird.
- Erläutere die bei beiden Experimenten gleiche Beobachtung unter Betrachtung der Veränderung der Elektrodenpotenziale.
(3 VP)
(20 VP)
1.1
Reaktionsgleichung mit den fehlenden stöchiometrischen Koeffizienten
 Begründung der Redoxreaktion
Die Oxidationszahlen zeigen eine Elektronenübertragung:
Begründung der Redoxreaktion
Die Oxidationszahlen zeigen eine Elektronenübertragung:
Das gibt ein Elektron ab und wird oxidiert und der Stickstoff nimmt drei Elektronen auf und wird reduziert. Alternative: Aufstellen von Teilgleichungen Reaktion von Gold und Kupfer mit Salpetersäure

Das gibt ein Elektron ab und wird oxidiert und der Stickstoff nimmt drei Elektronen auf und wird reduziert. Alternative: Aufstellen von Teilgleichungen Reaktion von Gold und Kupfer mit Salpetersäure
hat mit
ein positiveres Elektrodenpotenzial als das Potenzial der Reduktion von Salpetersäure (
). Elementares Gold wirkt daher nicht als Reduktionsmittel.
hat mit
ein negativeres Potenzial. Kupfer wird also von der Salpetersäure oxidiert.
1.2
Elektrodenteilgleichungen
Bestimmung der Spannungsbereiche
Mögliche Reaktionen am Minuspol (Kathode):
Mögliche Reaktionen am Pluspol (Anode):
Durch Kombination der möglichen Reaktionen ergeben sich folgende Spannungen:
Die Metallabscheidung erfolgt durch das Anlegen einer äußeren Spannung  .
.
Wenn ist, dann wird bei der Elektrolyse Silber am Minuspol abgeschieden.
Die Darstellung vernachlässigt die, durch die Abscheidung von Gasen auftretende, Überspannung.
Bestimmung der Silbermasse
Vor dem Experiment wird der Metallstab, an dem Silber abgeschieden wird (Minuspol), gewogen. Nach der Reaktion wird dieser vorsichtig getrocknet (ggf. mit Hilfe von leichtflüchtigen Lösungsmitteln wie Aceton) und erneut gewogen. Die Silbermasse ergibt sich nun aus der Massendifferenz.
Massenanteil von Silber in der Legierung
ist, dann wird bei der Elektrolyse Silber am Minuspol abgeschieden.
Die Darstellung vernachlässigt die, durch die Abscheidung von Gasen auftretende, Überspannung.
Bestimmung der Silbermasse
Vor dem Experiment wird der Metallstab, an dem Silber abgeschieden wird (Minuspol), gewogen. Nach der Reaktion wird dieser vorsichtig getrocknet (ggf. mit Hilfe von leichtflüchtigen Lösungsmitteln wie Aceton) und erneut gewogen. Die Silbermasse ergibt sich nun aus der Massendifferenz.
Massenanteil von Silber in der Legierung
![\(\begin{array}[t]{rll}
m_{Cu} &=& m\,_\text{Legierung} - m_{Ag} - m_{Au}& \\[5pt]
&=& 16,0 \,\text{g} - 0,300 \,\text{g} - 0,025 \,\text{g} & \\[5pt]
&=& 15,675 \,\text{g} & \\[10pt]
\omega_{Cu} &=& \dfrac{m_{Cu}}{m\,_\text{Legierung}} \cdot 100\,\% & \\[5pt]
&\approx& 98 \,\%
\end{array}\)](https://mathjax.schullv.de/6bf03e7dcd8a18ecd6aff609a468b4e10941e74ddec89ac4fd66d7e3af155744?color=5a5a5a)
| Abscheidung von Silber und Sauerstoff |
| Abscheidung von Kupfer und Sauerstoff |
| Wasserzersetzung |
Wenn
2.1
Versuchsaufbau zur Messung des Standardpotenzials der Silber-Halbzelle
 Vorgehensweise zur Herstellung der benötigten Silbernitrat-Lösung
Vorgehensweise zur Herstellung der benötigten Silbernitrat-Lösung
![\(\begin{array}[t]{rll}
M_{AgNO_3}&=& 169,9 \,\text{g} \cdot \text{mol}^{-1}& \\[5pt]
m_{AgNO_3}&=& 200\,\text{g}
\end{array}\)](https://mathjax.schullv.de/9b6b40e28a4627a109525577cbd984c35514da35a89eee9d1afe8886797a27ab?color=5a5a5a) Da eine einmolare Silbernitrat-Lösung benötigt wird, folgt:
Um eine einmolare Lösung für die Silber-Halbzelle zu erhalten, werden
Da eine einmolare Silbernitrat-Lösung benötigt wird, folgt:
Um eine einmolare Lösung für die Silber-Halbzelle zu erhalten, werden  konzentrierte Lösung im Messkolben auf einen Liter aufgefüllt.
konzentrierte Lösung im Messkolben auf einen Liter aufgefüllt.
Für das Experiment reicht es ca. auf
auf  aufzufüllen.
aufzufüllen.

Für das Experiment reicht es ca.
2.2
Erläuterung der gleichen Beobachtung anhand der Elektrodenpotenziale
Zugabe von Salzsäure zur Silber-Halbzelle:
Die Silber-und Chlorid-Ionen reagieren zu schwerlöslichem Silberchlorid.

 Das Potenzial der Halbzelle und die gemessene Spannung sinken, da die Konzentration der Silber-Ionen abnimmt.
Zugabe von Salzsäure zur Wasserstoff-Halbzelle:
Das Potenzial der Halbzelle und die gemessene Spannung sinken, da die Konzentration der Silber-Ionen abnimmt.
Zugabe von Salzsäure zur Wasserstoff-Halbzelle:
Wenn sich die - Ionenkonzentration erhöht, verschiebt sich das Gleichgewicht auf die rechte Seite und das Abscheidungspotenzial an der Platin-Elektrode erhöht sich.
- Ionenkonzentration erhöht, verschiebt sich das Gleichgewicht auf die rechte Seite und das Abscheidungspotenzial an der Platin-Elektrode erhöht sich.


 Das Potenzial der Wasserstoffelektrode wird positiver ("edler") und die Spannungsdifferenz im galvanischen Element kleiner.
Das Potenzial der Wasserstoffelektrode wird positiver ("edler") und die Spannungsdifferenz im galvanischen Element kleiner.
Die Silber-und Chlorid-Ionen reagieren zu schwerlöslichem Silberchlorid.
Wenn sich die