Aufgabe 3 – Kunststoff-Saiten der Ukulele
Für das hawaiianische Zupfinstrument Ukulele werden heutzutage kaum noch Saiten aus Naturdarm verwendet, sondern es stehen zahlreiche Kunststoff-Saiten zur Verfügung.
1
Ein Großteil der Ukulele-Saiten wird aus dem Kunststoff TYNEX (Polyamid 6.12) hergestellt.
(Polyamid 6.12) hergestellt.
1.1
Ein Ausschnitt aus der Strukturformel des verwendeten Kunststoffs ist in Abbildung 1 dargestellt.
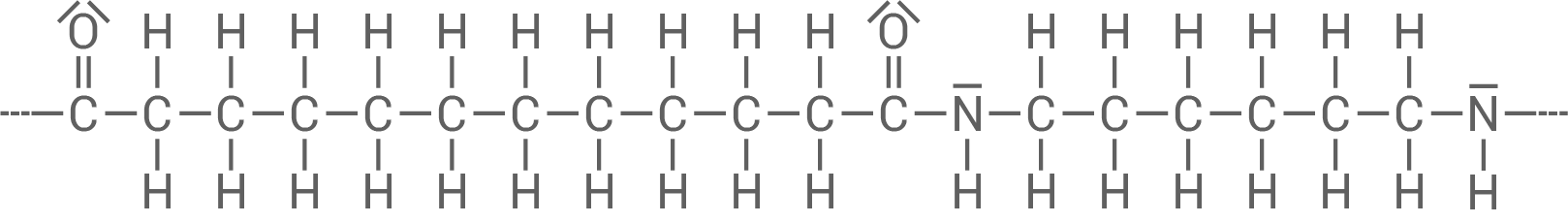

Abbildung 1: Strukturformelausschnitt aus einem Makromolekül des Kunststoffes TYNEX
- Zeichne je eine Strukturformel der beiden Monomer-Moleküle und gib von einem Monomer den systematischen Namen an.
- Beschreibe und erkläre das zu erwartende Verhalten dieses Kunststoffes beim Erwärmen.
(4 VP)
1.2
Eine TYNEX -Probe wird in einem Reagenzglas bis zur Zersetzung erhitzt. Ein befeuchtetes Universalindikatorpapier wird währenddessen über die Öffnung des Reagenzglases gehalten.
-Probe wird in einem Reagenzglas bis zur Zersetzung erhitzt. Ein befeuchtetes Universalindikatorpapier wird währenddessen über die Öffnung des Reagenzglases gehalten.
- Erkläre die zu erwartende Beobachtung am Universalindikatorpapier unter Verwendung einer Reaktionsgleichung.
(2 VP)
1.3
Der Klang von Saiten aus NYLGUT kommt dem von Naturdarmsaiten besonders nahe. NYLGUT
kommt dem von Naturdarmsaiten besonders nahe. NYLGUT wird aus Butan-1,4-diol und Benzol-1,4-dicarbonsäure synthetisiert.
wird aus Butan-1,4-diol und Benzol-1,4-dicarbonsäure synthetisiert.
- Zeichne einen Strukturformelausschnitt aus einem Makromolekül des Kunststoffes NYLGUT
, der mindestens drei Monomer-Bausteine enthält.
- Benenne den Reaktionstyp der Polyreaktion.
(3 VP)
2
Alternativ werden heute auch Saiten aus Fluorocarbon (Polydifluorethen) verwendet. Diese sind zwar härter und dünner, verstimmen sich aber nicht so schnell.
2.1
Ausgangsstoff für die Herstellung von Fluorocarbon ist 1,1-Difluorethen. Dieses wird aus Fluorwasserstoff (HF) und 1,1,1-Trichlorethan synthetisiert. Dabei entsteht neben 1,1-Difluorethen ein weiteres gasförmiges Produkt, welches beim Einleiten in Silbernitrat-Lösung einen weißen Niederschlag verursacht.
- Stelle die Reaktionsgleichung für die Synthese von 1,1-Difluorethen auf. Verwende hierbei Strukturformeln mit allen bindenden und nichtbindenden Elektronenpaaren.
(2 VP)
2.2
Der Kunststoff Polydifluorethen entsteht aus 1,1-Difluorethen durch eine Polyreaktion.
- Beschreibe einen Reaktionsmechanismus für die Synthese von Polydifluorethen unter Verwendung von geeigneten Formeldarstellungen und kurzen Texten.
(3 VP)
2.3
Polydifluorethen gehört zu der großen Gruppe der Fluorpolymere, bei deren Synthese unterschiedliche Fluorderivate des Ethens als Monomere verwendet werden.
| Strukturformel des Moleküls |
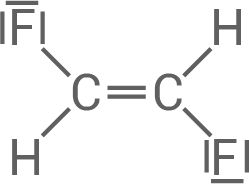
|
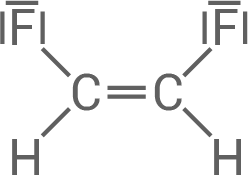
|
|---|---|---|
| Name | trans-1,2-Difluorethen | cis-1,2-Difluorethen |
| Siedetemperatur |
Tabelle 1: Siedetemperaturen der 1,2-Difluorethen-lsomere
- Erkläre die unterschiedlichen Siedetemperaturen der in der Tabelle 1 aufgeführten Difluorethen-Monomere.
(3 VP)
3
Für Bass-Ukulelen werden Saiten aus Polyurethan verwendet.
- Zeichne die Strukturformeln geeigneter Monomer-Moleküle mit bindenden und nichtbindenden Elektronenpaaren, aus denen ein von dir gewähltes Polyurethan hergestellt werden könnte.
- Benenne die funktionellen Gruppen in diesen Monomer-Molekülen und den Reaktionstyp der Polyreaktion.
(3 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Strukturformeln der Monomere
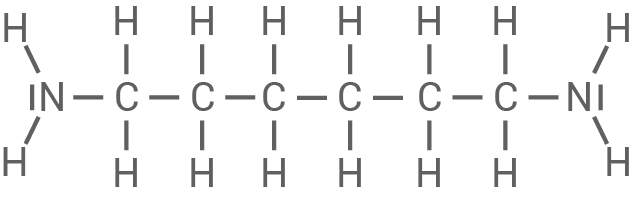
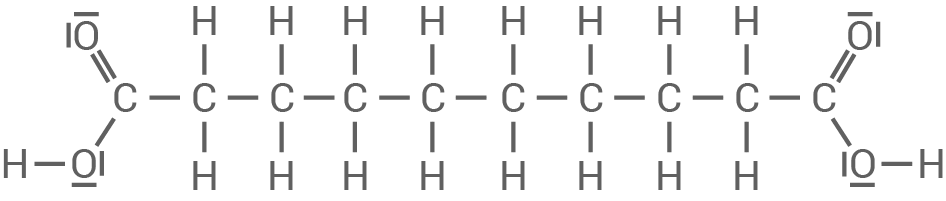 Verhalten von TYNEX
Verhalten von TYNEX beim Erwärmen
Es handelt sich um einen Thermoplasten, der beim Erhitzen schmilzt und sich anschließend zersetzt. Das ist auf die kettenförmige Struktur zurückzuführen. Die Van-der-Waals-Bindungen und Wasserstoffbrückenbindungen zwischen den Makromolekülen, also die intramolekularen Wechselwirkungen, werden beim Erwärmen überwunden, sodass sich die Ketten gegeneinander verschieben können.
beim Erwärmen
Es handelt sich um einen Thermoplasten, der beim Erhitzen schmilzt und sich anschließend zersetzt. Das ist auf die kettenförmige Struktur zurückzuführen. Die Van-der-Waals-Bindungen und Wasserstoffbrückenbindungen zwischen den Makromolekülen, also die intramolekularen Wechselwirkungen, werden beim Erwärmen überwunden, sodass sich die Ketten gegeneinander verschieben können.

1,6-Diaminohexan / Hexamethylendiamin

Dodecansäure
1.2
Beobachtung am Universalindikatorpapier
Zu Beobachten ist eine blaue Verfärbung des Universalindikatorpapiers (basisch). Grund dafür ist, dass beim Erhitzen gasförmiges Ammoniak gebildet wird. Dieses Gas reagiert unter Bildung von Hydroxid-Ionen mit Wasser.

1.3
Strukturformelausschnitt aus einem NYLGUTTYNEX - Makromolekül
- Makromolekül
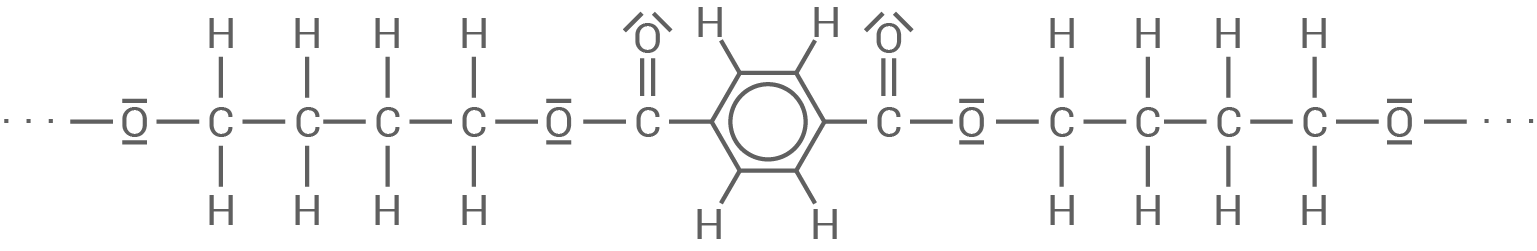 Reaktionstyp
Hierbei handelt es sich um eine vielfach ablaufende Kondensationsreaktion, also eine Polykondensation. Es werden dabei Wassermoleküle abgespalten.
Reaktionstyp
Hierbei handelt es sich um eine vielfach ablaufende Kondensationsreaktion, also eine Polykondensation. Es werden dabei Wassermoleküle abgespalten.

2.1
Reaktionsgleichung für die Synthese von 1,1-Difluorethen
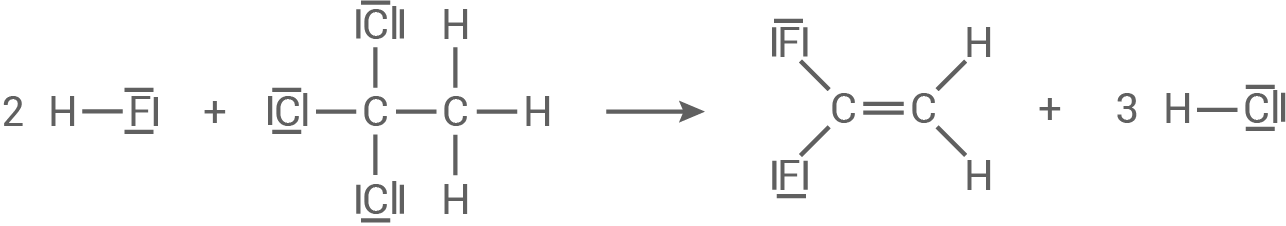

2.2
Reaktionsmechanismus für die Synthese von Polydifluorethen
Startreaktion (Radikalbildung):
Es wird ein Startradikal (z.B. aus Di-tert-Butylperoxid) unter Energiezufuhr (Wärme/Licht) gebildet.
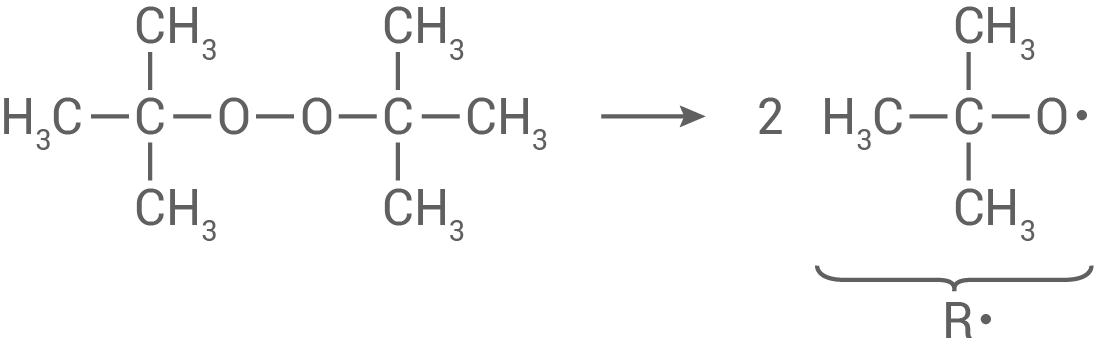 Kettenstart:
Das Startradikal greift die Doppebindung des 1,1-Difluorethens an und öffnet diese. Es wird eine Einfachbindung gebildet und es entsteht ein neues Radikal mit einem freien Elektron.
Kettenstart:
Das Startradikal greift die Doppebindung des 1,1-Difluorethens an und öffnet diese. Es wird eine Einfachbindung gebildet und es entsteht ein neues Radikal mit einem freien Elektron.
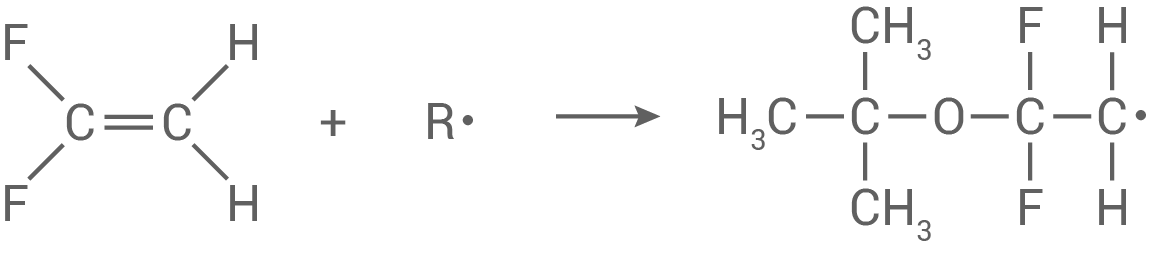 Kettenwachstum:
Das entstandene Radikal kann nun weiterreagieren und greift ein weiteres Molekül an, wodurch ein neues längeres Kettenradikal entsteht. Dieser Schritt kann n-mal wiederholt werden.
Kettenwachstum:
Das entstandene Radikal kann nun weiterreagieren und greift ein weiteres Molekül an, wodurch ein neues längeres Kettenradikal entsteht. Dieser Schritt kann n-mal wiederholt werden.
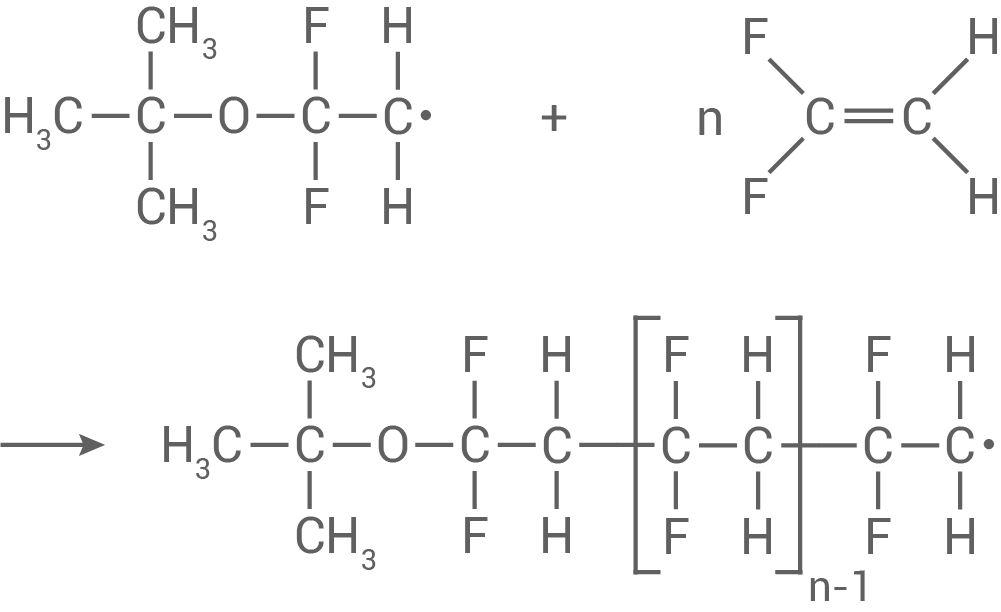 Kettenabbruch:
Eine Abbruchreaktion findet statt, wenn zwei Radikale miteinander reagieren.
Kettenabbruch:
Eine Abbruchreaktion findet statt, wenn zwei Radikale miteinander reagieren.
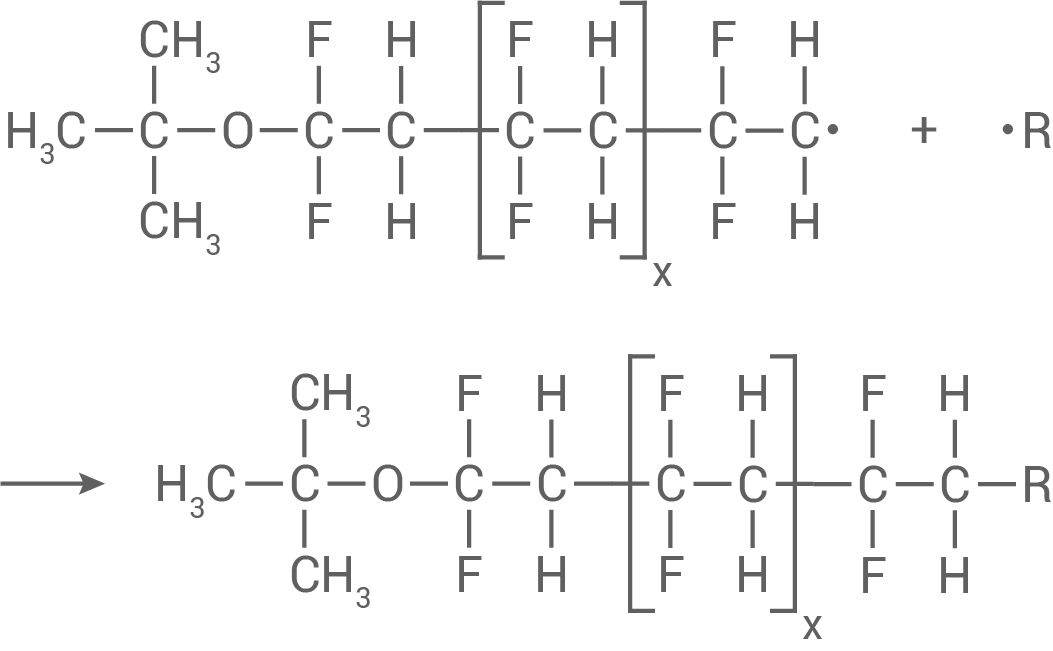




(eine von mehreren möglichen Beispielreaktionen)
2.3
Siedetemperaturen von trans-1,2-Difluorethen und cis-1,2-Difluorethen
Bei beiden Molekülen sind die  -Bindungen aufgrund der unterschiedlich großen Elektronegativitäten stark polarisiert. Dadurch ergeben sich negative und positive Partialladungen.
-Bindungen aufgrund der unterschiedlich großen Elektronegativitäten stark polarisiert. Dadurch ergeben sich negative und positive Partialladungen.
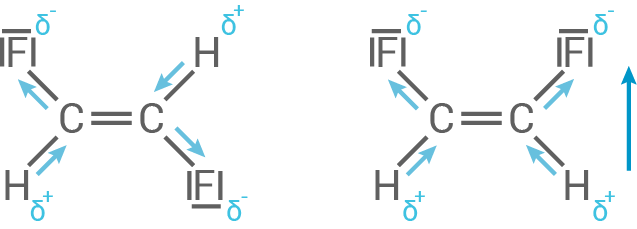 Es ergeben sich entlang der Bindungsachsen Dipolmomente.
Es ergeben sich entlang der Bindungsachsen Dipolmomente.
Bei trans-1,2-Difluorethen sind diese allerdings antiparallel ausgerichtet, wodurch sie sich aufheben (Vektoraddition).
Bei cis-1,2-Difluorethen sind diese parallel ausgerichtet und das Molekül besitzt ein Netto-Dipolmoment. Hat ein Molekül ein permanentes Dipolmoment ist eine stärkere Wechselwirkung möglich. Wird thermische Energie zugeführt, sind die Bindungen schwerer zu brechen als einfache VAN-DER-WAALS-Kräfte. Somit siedet das trans-Molekül bei niedrigeren Temperaturen als das cis-Molekül.

Bei trans-1,2-Difluorethen sind diese allerdings antiparallel ausgerichtet, wodurch sie sich aufheben (Vektoraddition).
Bei cis-1,2-Difluorethen sind diese parallel ausgerichtet und das Molekül besitzt ein Netto-Dipolmoment. Hat ein Molekül ein permanentes Dipolmoment ist eine stärkere Wechselwirkung möglich. Wird thermische Energie zugeführt, sind die Bindungen schwerer zu brechen als einfache VAN-DER-WAALS-Kräfte. Somit siedet das trans-Molekül bei niedrigeren Temperaturen als das cis-Molekül.
3
Monomere für ein Polyurethan
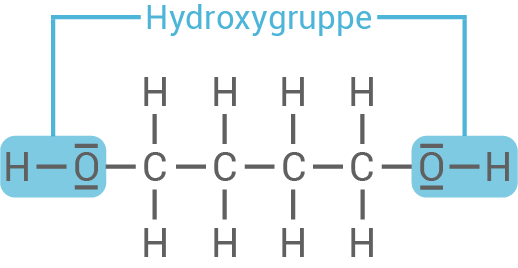
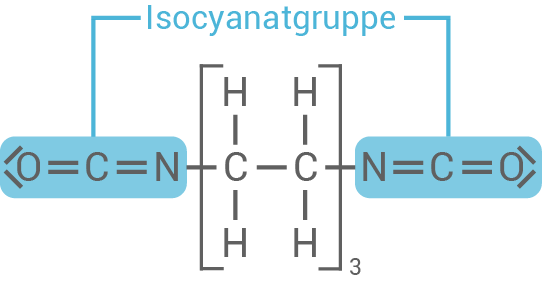 Funktionelle Gruppen und Reaktionstyp
Die funktionellen Gruppen sind Hydroxygruppen und Isocyanatgruppen.
Funktionelle Gruppen und Reaktionstyp
Die funktionellen Gruppen sind Hydroxygruppen und Isocyanatgruppen.
Die Reaktion folgt dem Mechanismus einer Polyaddition.
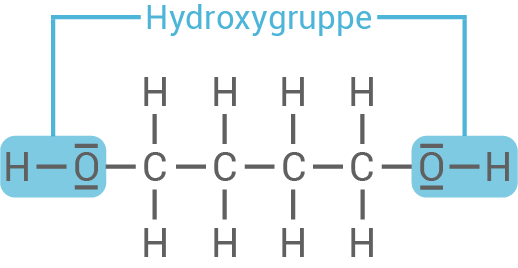
1,4-Butandiol

1,6-Hexandiisocyanat
Die Reaktion folgt dem Mechanismus einer Polyaddition.