Aufgabe 1 – Wasserdesinfektion in Schwimmbädern
Chlorgas wird zur Desinfektion von Wasser in Schwimmbädern verwendet. Beim Umgang mit diesem Gefahrstoff geschehen immer wieder Unfälle. So wurden im März 2018 in Bad Schönborn mehrere Personen durch einen Bedienungsfehler beim Füllen eines Chlortanks verletzt.
Ein Verfahren zur Herstellung von Chlor ist der DEACON-Prozess. Dabei werden Chlorwasserstoff und Sauerstoff in Gegenwart von Kupfer -chlorid bei
-chlorid bei  bis
bis  in einer Gleichgewichtsreaktion umgesetzt:
in einer Gleichgewichtsreaktion umgesetzt:
| Reaktion A: | |
1.1
Das in Reaktion A formulierte Gleichgewicht wird nun näher betrachtet.
- Stelle das Massenwirkungsgesetz für Reaktion A auf.
- Erkläre, wie durch Veränderung des Drucks einerseits und durch Veränderung der Temperatur andererseits die Chlorausbeute bei Reaktion A erhöht werden kann.
- Gib das Vorzeichen der Reaktionsentropie für Reaktion A an. Begründe deine Entscheidung.
(5 VP)
1.2
Das in Reaktion A formulierte Gleichgewicht ist stark temperaturabhängig. Eines der folgenden Diagramme stellt die Abhängigkeit der Chlorwasserstoff-Konzentration von der Temperatur qualitativ dar.
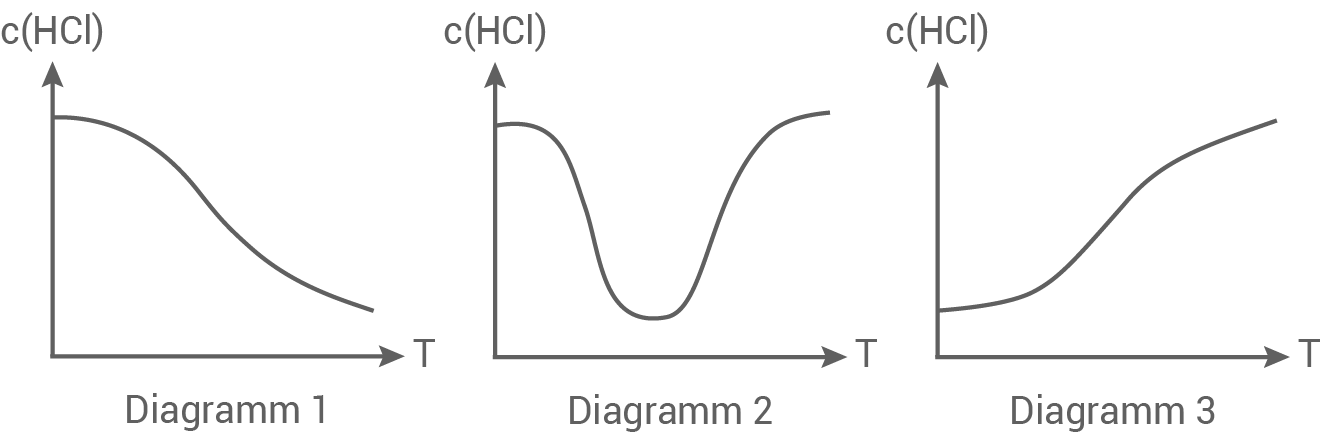

- Gib das Diagramm an, das für Reaktion A charakteristisch ist. Begründe deine Wahl.
(3 VP)
1.3
Tatsächlich läuft Reaktion A in zwei aufeinander folgenden Gleichgewichtsreaktionen ab:
| Reaktion B: | Kupfer |
| Reaktion C: | Kupfer |
- Stelle die Reaktionsgleichungen für die Reaktionen B und C auf.
- Zeige die Gültigkeit des Energieerhaltungssatzes durch Bilanzierung der Reaktionsenthalpien für die Reaktionen A, B und C. Hierfür eignen sich näherungsweise die thermodynamischen Daten aus Anlage 3.
- Begründe anhand der Reaktionsgleichungen, dass Kupfer
-chlorid als Katalysator wirkt.
(6 VP)
2.1
In kleineren Schwimmbecken wird das Wasser durch Zugabe von Natriumhypochlorit  desinfiziert. Dabei laufen nacheinander die folgenden beiden Gleichgewichtsreaktionen ab.
desinfiziert. Dabei laufen nacheinander die folgenden beiden Gleichgewichtsreaktionen ab.
| Reaktion D: | Hypochlorit-lonen reagieren dabei zunächst mit Wasser-Molekülen, wobei sich ein pH-Wert im alkalischen Bereich einstellt. |
| Reaktion E: | Nach einiger Zeit kommt es in der Lösung zu einer Folgereaktion. Dabei sinkt der pH-Wert und es bilden sich Chlorid-Ionen. Außerdem entsteht Sauerstoff, der desinfizierend wirkt. |
- Gib die chemische Formel von festem Natriumhypochlorit unter Verwendung aller bindenden und nichtbindenden Elektronenpaare an.
- Stelle die Reaktionsgleichungen für die Gleichgewichtsreaktionen D und E auf.
(3 VP)
2.2
In einem Schwimmbecken sind  Natriumhypochlorit in
Natriumhypochlorit in  Wasser gelöst.
Wasser gelöst.
- Berechne den pH-Wert in diesem Schwimmbecken unter der Annahme, dass Hypochlorit-lonen ausschließlich nach Reaktion D reagiert haben.
(3 VP)
(20 VP)
1.1
Massenwirkungsgesetz für Reaktion A
Für die Reaktion gilt:


 Daraus folgt:
Daraus folgt:

 Erhöhung der Chlorausbeute
Druckerhöhung:
Erhöhung der Chlorausbeute
Druckerhöhung:
Eine Druckerhöhung begünstigt nach LE CHATELIER die Reaktion, die unter Volumenabnahme verläuft.
An der Reaktionsgleichung sieht man, dass fünf Gasteilchen auf der linken Seite zu vier Gasteilchen reagieren. Da das Volumen abnimmt, führt eine Druckerhöhung zu einer Gleichgewichtsverschiebung zu den Produkten. Temperaturerniedrigung:
Durch eine Temperaturerniedrigung wird die exotherme Reaktion begünstigt. Da die Reaktion exotherm verläuft, liegt bei Neueinstellung des Gleichgewichts eine größere Konzentration von Chlorgas vor. Vorzeichen der Reaktionsentropie für Reaktion A Alle Reaktionsteilnehmer sind gasförmig, wodurch sich die Gesamtstoffmenge betrachten lässt. Die Reaktionslgeichung zeigt, dass die Anzahl der Gasteilchen von links nach rechts abnimm, womit die Entropie ein negatives Vorzeichen erhält.
Eine Druckerhöhung begünstigt nach LE CHATELIER die Reaktion, die unter Volumenabnahme verläuft.
An der Reaktionsgleichung sieht man, dass fünf Gasteilchen auf der linken Seite zu vier Gasteilchen reagieren. Da das Volumen abnimmt, führt eine Druckerhöhung zu einer Gleichgewichtsverschiebung zu den Produkten. Temperaturerniedrigung:
Durch eine Temperaturerniedrigung wird die exotherme Reaktion begünstigt. Da die Reaktion exotherm verläuft, liegt bei Neueinstellung des Gleichgewichts eine größere Konzentration von Chlorgas vor. Vorzeichen der Reaktionsentropie für Reaktion A Alle Reaktionsteilnehmer sind gasförmig, wodurch sich die Gesamtstoffmenge betrachten lässt. Die Reaktionslgeichung zeigt, dass die Anzahl der Gasteilchen von links nach rechts abnimm, womit die Entropie ein negatives Vorzeichen erhält.
1.2
Wahl eines Diagramms
Reaktion A ist exotherm, weswegen eine Temperaturerhöhung das Gleichgewicht auf Eduktseite verschiebt. Demnach kann nur Diagramm 3 in Frage kommen, da hier die Konzentration der Salzsäure steigt und nur hier diese Temperaturabhängigkeit dargestellt wird.
1.3
Reaktionsgleichungen für die Reaktionen B und C
Bilanzierung der Reaktionsenthalpien
Als Grundlage gilt der Satz von HESS, nachdem die Enthalpie einer Reaktion nur vom Anfangs- und Endzustand, nicht aber vom Weg zwischen beiden abhängig ist.
Reaktionen B und C können folglich aufsummiert werden, womit sich die Reaktion A als Summe der beiden Reaktionen ergibt:
Nach Kürzung ergibt sicher folgender Zusammenhang:
Für die Reaktionsenthalpien gilt:
Dies liefert für  den gleichen Wert wie in der Aufgabenstellung und zeigt die Gültigkeit des Energieerhaltungssatzes.
Katalysatorwirkung von Kupfer
den gleichen Wert wie in der Aufgabenstellung und zeigt die Gültigkeit des Energieerhaltungssatzes.
Katalysatorwirkung von Kupfer -chlorid
Ein Katalysator zielt darauf ab die Reaktionsgeschwindigkeit durch Senkung der Aktivierungsenergie zu erhöhen und unverändert aus der Reaktion hervorzugehen.
Kupfer
-chlorid
Ein Katalysator zielt darauf ab die Reaktionsgeschwindigkeit durch Senkung der Aktivierungsenergie zu erhöhen und unverändert aus der Reaktion hervorzugehen.
Kupfer -chlorid nimmt an Reaktion B teil, geht aber unverändert aus Reaktion C hervor. Es wirkt demnach als Katalysator.
-chlorid nimmt an Reaktion B teil, geht aber unverändert aus Reaktion C hervor. Es wirkt demnach als Katalysator.
| Reaktion B: | |
| Reaktion C: |
2.1
Chemische Formel von festem Natriumhypochlorit
 Reaktionsgleichungen für die Gleichgewichtsreaktionen D und E
Reaktionsgleichungen für die Gleichgewichtsreaktionen D und E

| Reaktion D: | |
| Reaktion E: |
2.2
pH-Wert im Schwimmbecken
![\(\begin{array}[t]{rll}
M(NaOCl)&=& 74,5\,\,\text{g}\cdot \text{mol}^{-1}
\end{array}\)](https://mathjax.schullv.de/58930d15a77a178a06e243ad001a73a7e8148b5ece9f7d10012e69f8bb27f9c0?color=5a5a5a)
![\(\begin{array}[t]{rll}
n(NaOCl) &=& \dfrac{m(NaOCl)}{M(NaOCl)}\\[5pt]
&=& \dfrac{148\,\,\text{g}}{74,5\,\,\text{g}\cdot \text{mol}^{-1} }\\[5pt]
&\approx& 1,99 \,\text{mol}
\end{array}\)](https://mathjax.schullv.de/905be55e97c69916d2f6a4e6d4a7dca803dc3f3f3e4ad321c6a22023f210ded3?color=5a5a5a)
![\(\begin{array}[t]{rll}
c(NaOCl)&=& \dfrac{n(NaOCl)}{V} \\[5pt]
&=&\dfrac{1,99 \,\text{mol} }{9000\,\text{l}} \\[5pt]
&\approx& 2,2 \cdot 10^{-4}\,\text{mol}\cdot \text{L}^{-1}
\end{array}\)](https://mathjax.schullv.de/71d889e084f0416cec318aedafa762e523efdf5c3705b774e822c06500d5f49a?color=5a5a5a) Für schwache Basen gilt:
Für schwache Basen gilt:
![\(\begin{array}[t]{rll}
pH&=& 14-pOH & \\[5pt]
&=& 14-5,06 & \\[5pt]
&=& 8,94
\end{array}\)](https://mathjax.schullv.de/68cd3548a606e0128c2b7d05a0c52d87625c6174c0c9e6169158511db77eea0c?color=5a5a5a) Nachdem Natriumhypochlorit dem Wasser zugesetzt wurde beträgt der pH-Wert
Nachdem Natriumhypochlorit dem Wasser zugesetzt wurde beträgt der pH-Wert 