Aufgabe 4 – Elemente Natrium und Chlor
Die Elemente Natrium und Chlor kommen in der Natur nicht elementar vor. Sie können großtechnisch durch elektrolytische Verfahren hergestellt werden.
1
Natrium wird hauptsächlich durch Schmelzflusselektrolyse von Natriumchlorid in einer DOWNS-Zelle hergestellt (siehe Abb. 1).
1.1
Für die Elektrolyse werden eine Graphit- und eine ringförmige Eisen-Elektrode verwendet. Die Eisen-Elektrode ist von einem engmaschigen Drahtnetz umgeben.
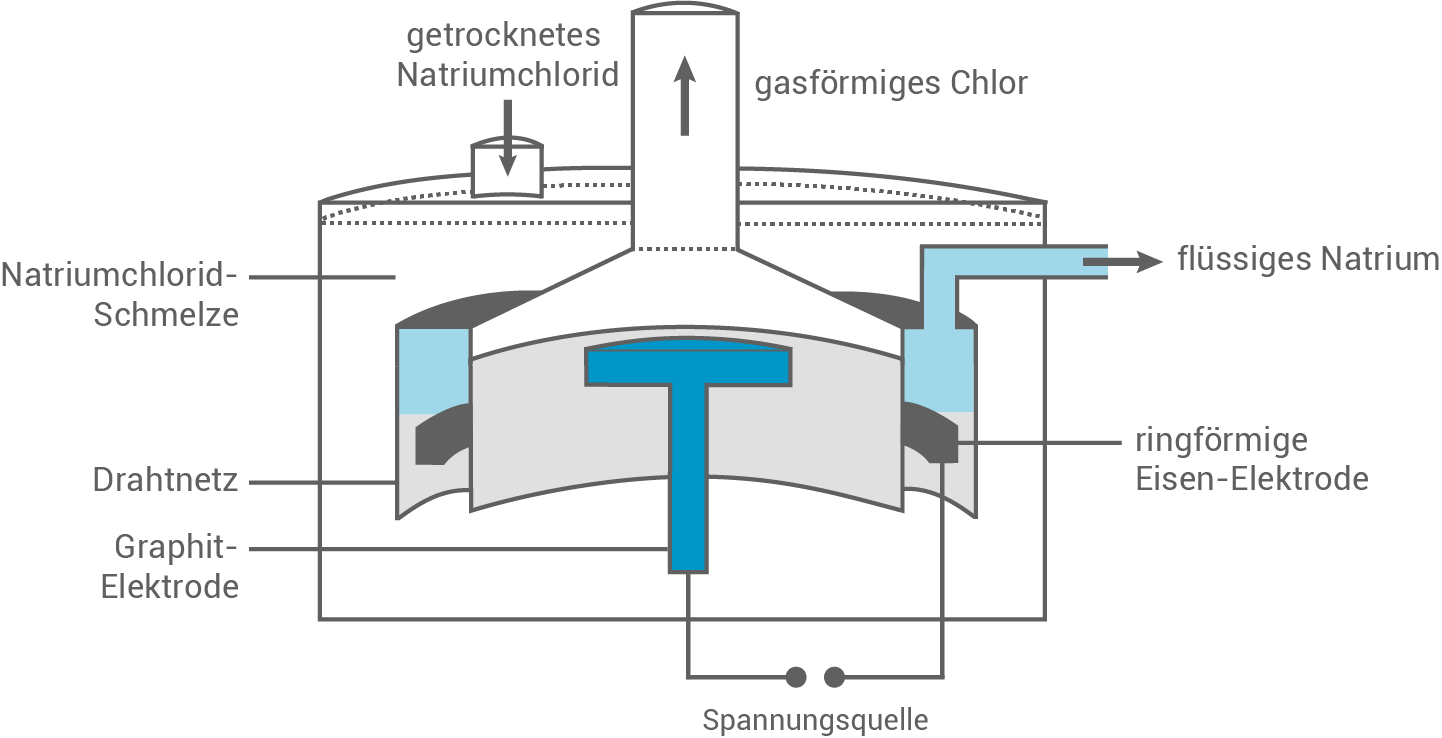

Abbildung 1: Schematische Darstellung einer DOWNS-Zelle
- Erläutere anhand von Abbildung 1 die in einer DOWNS-Zelle ablaufenden Prozesse von der Zufuhr des Edukts bis zur Entnahme der Produkte auf Stoffebene. Erkläre dabei auch die Bedeutung des Drahtnetzes.
- Beschreibe mit Hilfe von Teilgleichungen und einer Gesamtreaktionsgleichung die Vorgänge an den beiden Elektroden auf Teilchenebene.
(5 VP)
1.2
Die Temperatur, die zur Erzeugung der Natriumchlorid-Schmelze notwendig ist, wird durch Zugabe von Calciumchlorid auf  gesenkt, um Energie zu sparen. Beide Salze müssen dazu vorher getrocknet werden.
gesenkt, um Energie zu sparen. Beide Salze müssen dazu vorher getrocknet werden.
- Begründe die Notwendigkeit zur Trocknung der Salze anhand eines Aspekts.
- Erkläre, dass die Zugabe des Calciumchlorids nicht zu Nebenreaktionen an den Elektroden führt.
(4 VP)
1.3
Das bei der Schmelzflusselektrolyse gebildete, ebenfalls technisch wichtige Chlorgas wird aufgefangen und für weitere chemische Synthesen verwendet.
 gibt das Volumen der Stoffmengen
gibt das Volumen der Stoffmengen  eines Gases an.
eines Gases an.
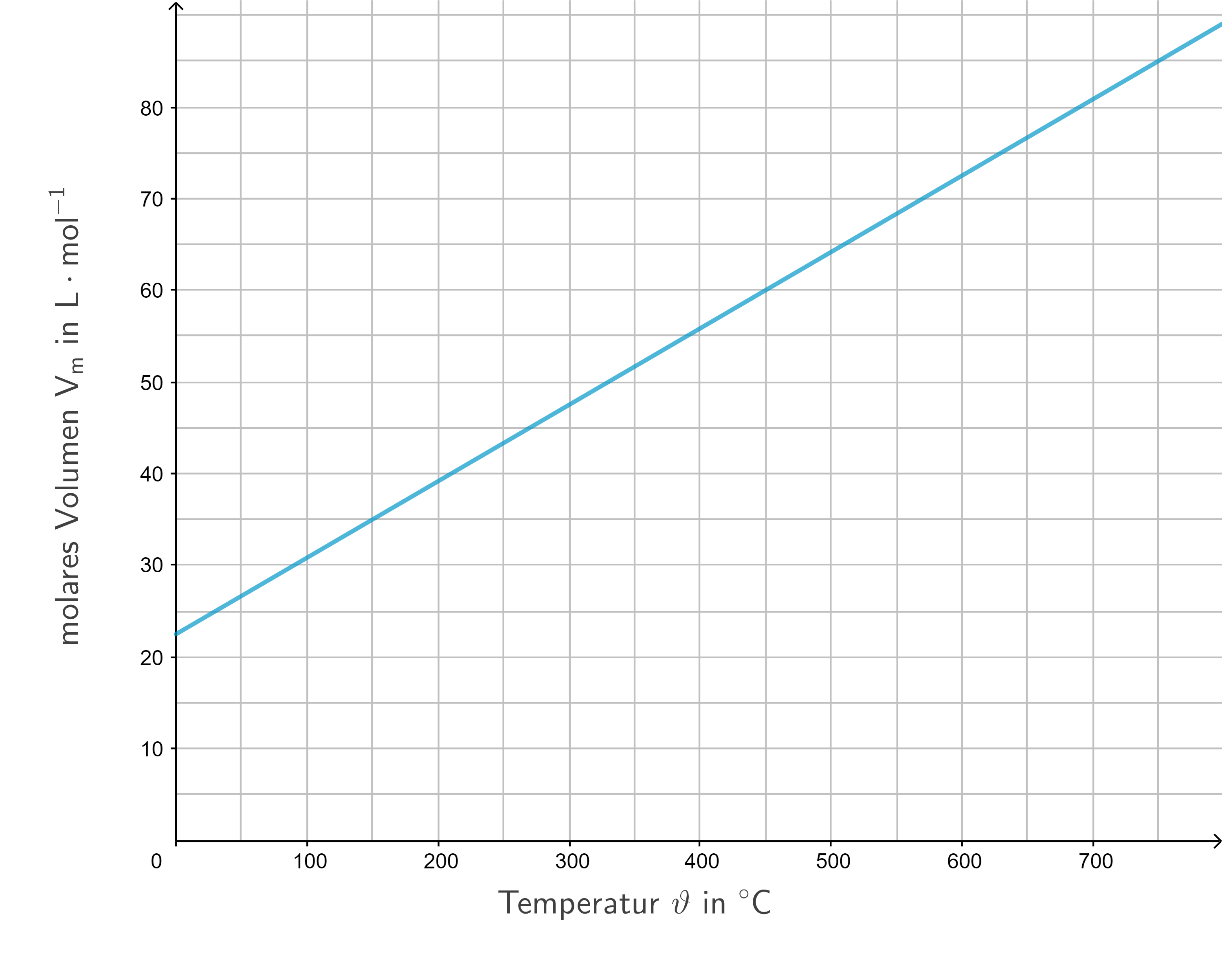
- Bestimme mithilfe von Abbildung 2 das Volumen an Chlorgas, das bei der vollständigen Elektrolyse von
Natriumchlorid bei einer Temperatur von
entsteht.

Abbildung 2: Temperaturabhängigkeit des molaren Volumens von Gasen bei Standarddruck
(3 VP)
2
In einem Modellversuch wird eine galvanische Zelle aus einer Chlor-Halbzelle und einer weiteren Halbzelle aufgebaut. Das Aufbauprinzip der Chlor-Halbzelle gleicht dem einer Wasserstoffhalbzelle.
2.1
Unter Standardbedingungen ergibt sich zwischen beiden Halbzellen die Potenzialdifferenz  .
.
- Bestimme das Elektrodenmaterial der weiteren Halbzelle.
- Erstelle eine beschriftete Skizze des Aufbaus dieser galvanischen Zelle. Gib dabei die Standardbedingungen an.
(4 VP)
2.2
Durch Veränderung der Reaktionsbedingungen an der Chlor-Halbzelle soll die Potenzialdifferenz dieser galvanischen Zelle erhöht werden.
- Erläutere zwei Möglichkeiten, um die Erhöhung der Potentialdifferenz zu erreichen.
(4 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Ablaufende Prozesse auf Stoffebene
In der Downs-Zelle wird getrocknetes Natriumchlorid geschmolzen und elektrolysiert. Eine ringförmige Eisen-Elektrode fungiert als Kathode, während ein feines Drahtnetz verhindert, dass das erzeugte Natrium in die Zelle zurückfließt. Kathode und Anode werden durch dieses Drahtnetz getrennt. Das Natrium (geringere Dichte) steigt in eine Rinne auf und fließt ab. Die Anode besteht aus Graphit und das entstehende Chlorgas entweicht durch eine Glocke, welche einem Trichter ähnelt (s. Abbildung).
Vorgänge an den Elektroden auf Teilchenebene
An der Eisen-Kathode wird das flüssige Natriumchlorid reduziert und an der Graphit-Anode oxidiert. Dabei entstehen elementares Natrium und elementares Chlor.
1.2
Notwendigkeit zur Trocknung der Salze
Durch nicht vollständig getrocknetes Salz könnte der Wasserdampf korrosiv auf die Stahl- und Eisenteile der DOWNS-Zelle wirken, besonders gemeinsam mit dem Chlorid-Ionen.
Zugabe des Calciumchlorids
Dass die Zugabe von Calciumchlorid nicht zu Nebenreaktionen an den Elektroden führt, kann mit den Zersetzungsspannungen erklärt werden, da bei einer Elektrolyse zunächst die Teilchen mit positivsten Elektrodenpotenzial umgesetzt werden:
![\(\begin{array}[t]{rll}
U_1&=& E^0 (2Cl^- / Cl_2) - E^0 (Na / Na^+)&\quad \scriptsize \; \\[5pt]
&=& 1,36 \,\text{V}- (-2,71 \,\text{V}) \\[5pt]
&=& 4,07 \,\text{V} \\[5pt]
\end{array}\)](https://mathjax.schullv.de/3d9cc8290d6513e9fe2248b6f087a1823b012598089a8143dc37980821490e47?color=5a5a5a)
![\(\begin{array}[t]{rll}
U_2&=& E^0 (2Cl^- / Cl_2) - E^0 (Ca / Ca^{2+}) \; \\[5pt]
&=& 1,36 \,\text{V}- (-2,87 \,\text{V}) &\quad \scriptsize \\[5pt]
&=& 4,23 \,\text{V} \\[5pt]
\end{array}\)](https://mathjax.schullv.de/61d48c927509dc40c80a4d4cffc3a38f4207f0e58ba77de10d0630f630f8727b?color=5a5a5a) Das Elektrodenpotenzial von Calcium ist kleiner als das von Natrium, deswegen findet an der Eisen-Elektrode keine Calcium-Abscheidung statt.
Das Elektrodenpotenzial von Calcium ist kleiner als das von Natrium, deswegen findet an der Eisen-Elektrode keine Calcium-Abscheidung statt.
1.3
Volumen des gewonnenem Chlorgases




![\(\begin{array}[t]{rll}
n(NaCl) &=&\dfrac{m(NaCl)}{M(NaCl)} &\quad \scriptsize \; \\[5pt]
&=& \dfrac{1000 \cdot 1000g}{58,5 \,\text{g} \cdot \,\text{mol}^{-1}} \\[5pt]
&\approx & 17 \ 094\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/3e0491903231fbdb6090c278c04c7441b8595564fa5f45fb3e86478b3fc99279?color=5a5a5a) Aus der Reaktionslgeichung folgt:
Aus der Reaktionslgeichung folgt:
![\(\begin{array}[t]{rll}
n(NaCl)&\mathrel{\widehat{=}}&n (Cl_2) &\quad \scriptsize \\[5pt]
n(Cl_2)&=& \dfrac{n (NaCl)}{2} \\[5pt]
&=& 8547 \,\text{mol} \\[10pt]
V (Cl_2) &=& V_m (Cl_2) \cdot n (Cl_2) \\[5pt]
&=& 72,5 \,\text{L} \cdot \,\text{mol}^{-1} \cdot 8547 \,\text{mol} \\[5pt]
&=& 619657,5 \,\text{L} \\[5pt]
\end{array}\)](https://mathjax.schullv.de/57f311528c79446131d10a23bf95bfd59058645b850f3c1414d30ec46eb75d3b?color=5a5a5a)
2.1
Potenzialdifferenz eines galvanisches Elements mit einer Chlor-Halbzelle
Ein galvanisches Element aus einer Chlor-Halbzelle und einer unbekannten Metall-Halbzelle besitzt eine Potenzialdifferenz von 
Die Chlor-Halbzelle kann entweder der Minus-oder der Pluspol sein: In der Tabelle der Elektrodenpotenziale (Anlage 3) findet sich nur der Wert von , weswegen es sich bei dem Anodenmaterial um Silber handelt.
Skizze des galvanischen Elements
, weswegen es sich bei dem Anodenmaterial um Silber handelt.
Skizze des galvanischen Elements
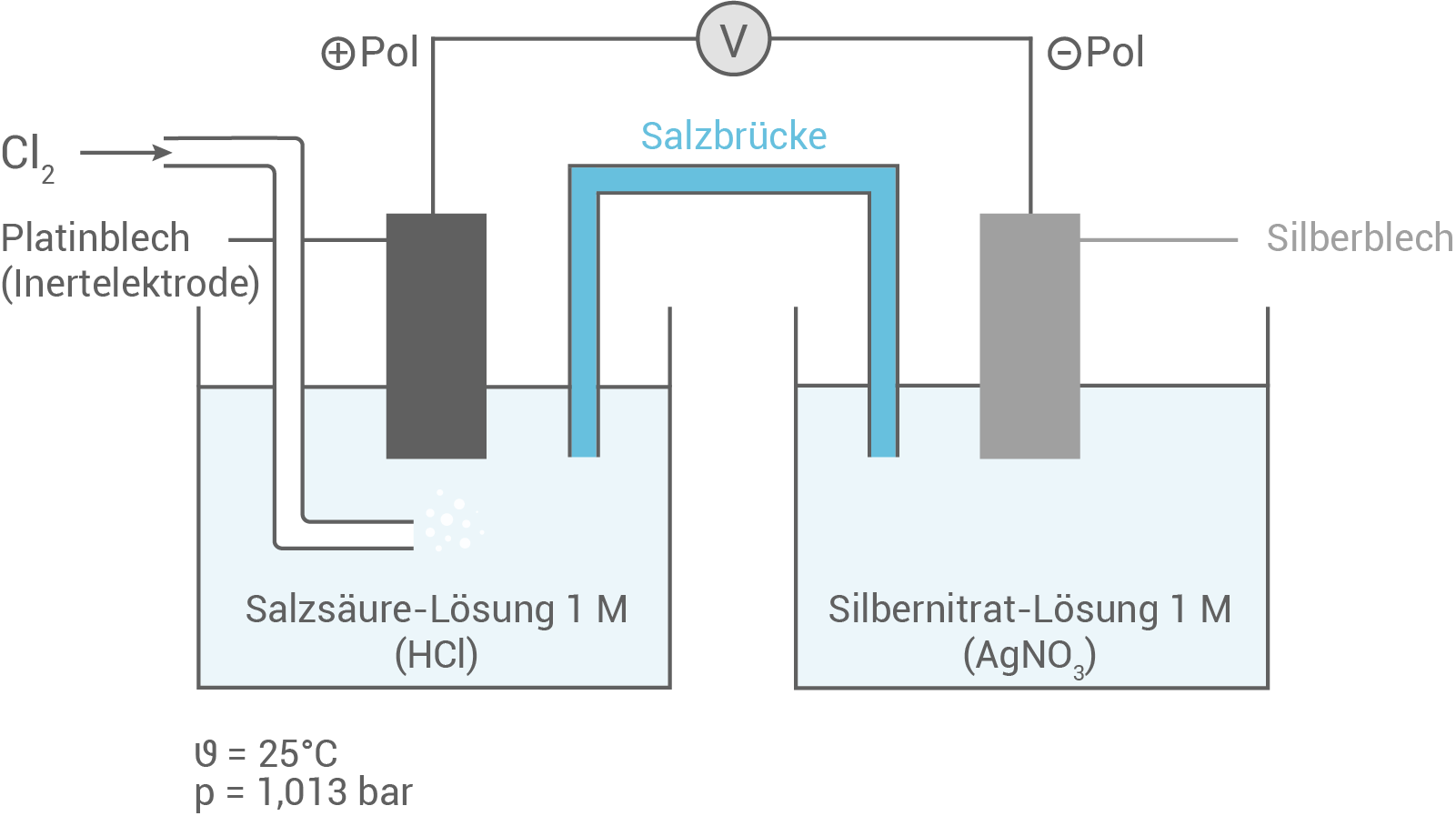
Die Chlor-Halbzelle kann entweder der Minus-oder der Pluspol sein: In der Tabelle der Elektrodenpotenziale (Anlage 3) findet sich nur der Wert von

2.2
Möglichkeiten zur Erhöhung des Elektrodenpotenzials der Chlor-Halbzelle
Allgemein werden Metallen nach NERNST Lösungstensionen in wässrigen Lösungen zugeordnet. Außerdem gilt, dass Metall-Kationen das Bestreben haben, sich an der Metall-Elektrode abzuscheiden (Abscheidungsbestreben). Beim Eintauchen einer Metall-Elektrode in ihre Salzlösung stellt sich dann zwischen der Lösungstension mit Metall-Kationen und dem Abscheidungsbestreben ein Gleichgewicht ein. Die Lage ist abhängig von der Metall-Art und der Konzentration der Metall-Ionenlösung.
Bei einer hohen Metall-Ionenkonzentration werden weniger Metall-Ionen die feste Phase verlassen und die Elektrode wird edler, also ihr Potenzial positiver. Das Umgekehrte gilt für eine niedrige Metall-Ionenkonzentration.
Bei der Chlor-Elektrode nehmen Chlor-Atome Elektronen an der Oberfläche des Platin-Bleches auf. Dabei entstehen Chlorid-Ionen und "positive Lücken". Die Chlorid-Ionen aus der Umgebung (Lösung) wirken dabei entgegen und es stellt sich ein elektrochemisches Gleichgewicht zwischen und
und  und ein bestimmtes Potenzial ein.
und ein bestimmtes Potenzial ein.
Bei der Chlor-Elektrode nehmen Chlor-Atome Elektronen an der Oberfläche des Platin-Bleches auf. Dabei entstehen Chlorid-Ionen und "positive Lücken". Die Chlorid-Ionen aus der Umgebung (Lösung) wirken dabei entgegen und es stellt sich ein elektrochemisches Gleichgewicht zwischen
- Erniedrigung der Chlorid-Ionen-Konzentration durch z.B. Verdünnen der Lösung
geringeres Abscheidungsbestreben der Chlorid-Lösung
- Erhöhung des Drucks
mehr positive Lücken auf dem Platinblech