Aufgabe 4 – ZEBRA-Batterie
Die sogenannte ZEBRA-Batterie (Zero Emission Battery Research Activity) kann vereinfacht als Natrium/Nickel-Zelle dargestellt werden. Ihren schematischen Aufbau zeigt Abb. 1. Im geladenen Zustand besteht eine Halbzelle aus Natrium (Schmelztemperatur:  , Siedetemperatur:
, Siedetemperatur:  ), die andere Halbzelle aus einem Gemisch aus Nickel(II)-chlorid
), die andere Halbzelle aus einem Gemisch aus Nickel(II)-chlorid  und Nickel (Schmelztemperatur:
und Nickel (Schmelztemperatur:  , Siedetemperatur
, Siedetemperatur  ). Die übliche Betriebstemperatur beträgt
). Die übliche Betriebstemperatur beträgt  . Der Separator ist bei dieser Temperatur durchlässig für Natrium-Kationen.
. Der Separator ist bei dieser Temperatur durchlässig für Natrium-Kationen.
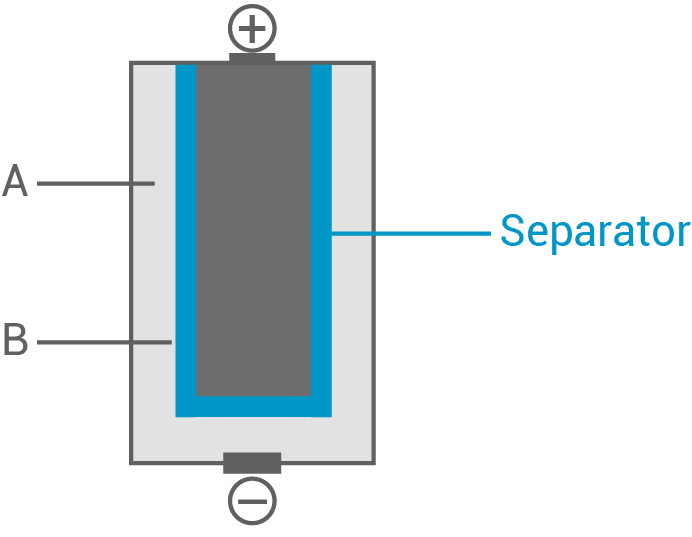
Abbildung 1: Schematische Darstellung einer ZEBRA-Batterie
1
Im Folgenden wird der Entladevorgang betrachtet, bei dem Natrium mit Nickelchlorid reagiert.
- Stelle die Teilgleichungen sowie die Gesamtreaktionsgleichung auf.
- Gib die Aggregatzustände der Elemente Natrium und Nickel im Betrieb an und begründe deine Angabe.
- Ordne die im Vortext genannten Stoffe den Batterieräumen A und B in Abb. 1 zu.
- Erkläre die Rolle des Separators und gib den Ladungsfluss innerhalb der Batterie an.
(6 VP)
2
Eine ZEBRA-Batterie liefert im Betrieb eine Spannung von  .
.
- Berechne die zu erwartende Spannung einer ZEBRA-Batterie unter Verwendung der Elektrodenpotenziale unter Standardbedingungen.
- Nenne zwei Gründe für die Abweichung der berechneten Spannung vom angegebenen Wert.
(3 VP)
3
In der Literatur wird die ZEBRA-Batterie häufig als Akkumulator bezeichnet.
- Erkläre das Prinzip eines Akkumulators am Beispiel der ZEBRA-Batterie.
(2 VP)
4
Für eines der am Redoxprozess der ZEBRA-Batterie beteiligten Metalle findet man die in Abb. 2 dargestellten GHS-Piktogramme. Zudem gelten u. a. folgende Gefahren-Sätze: "In Berührung mit Wasser entstehen entzündbare Gase, die sich spontan entzünden können." (H260) und "Verursacht schwere Verätzungen der Haut ..." (H314).


Abbildung 2: GHS-Piktogramm eines in der ZEBRA-Batterie verwendeten Metalls
- Ordne den Gefahren-Satz H260 einem der Metalle in der ZEBRA-Batterie zu und begründe deine Wahl mithilfe von Elektrodenpotenzialen.
- Erläutere ausgehend von einer Reaktionslgeichung die in den angegebenen H-Sätzen angeführten Gefahren.
(5 VP)
5
Das Redoxpaar Natrium-Atom/Natrium-Ion ist zentraler Bestandteil einer ZEBRA-Batterie.
- Beschreibe den Aufbau eines Natrium-Atoms sowie eines Natrium-Ions unter Verwendung von Informationen, die dem Periodensystem der Elemente entnommen werden können.
- Begründe den Größenunterschied der beiden Teilchen (Atom und Ion).
(4 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Teilgleichungen und Gesamtreaktionsgleichung
Oxidation:


 Reduktion:
Reduktion:


 Redoxgleichung:
Redoxgleichung:


 Gesamtgleichung:
Gesamtgleichung:


 Aggregatszustände und Begründung
Dem Informationstext lässt sich eine Betriebstemperatur von
Aggregatszustände und Begründung
Dem Informationstext lässt sich eine Betriebstemperatur von  entnehmen. Die Aggregatszustände der Elemente lassen sich demnach mit den gegebenen Schmelz-und Siedetemperaturen begründen:
entnehmen. Die Aggregatszustände der Elemente lassen sich demnach mit den gegebenen Schmelz-und Siedetemperaturen begründen:
 und
und  ist dem inneren Batterieraum B zuzuordnen, da hier die Reduktion stattfindet (siehe Reaktionsgleichung). Demnach findet sich das flüssige Natrium im äußeren Batterieraum A und wird oxidiert.
Rolle des Separators und Angabe des Ladungsflusses
Der Separator dient der Trennung des Oxidations und des Oxidations-und Reduktionsraums. Er ist durchlässig für
ist dem inneren Batterieraum B zuzuordnen, da hier die Reduktion stattfindet (siehe Reaktionsgleichung). Demnach findet sich das flüssige Natrium im äußeren Batterieraum A und wird oxidiert.
Rolle des Separators und Angabe des Ladungsflusses
Der Separator dient der Trennung des Oxidations und des Oxidations-und Reduktionsraums. Er ist durchlässig für  -Kationen und ermöglicht damit den Ladungsausgleich.
-Kationen und ermöglicht damit den Ladungsausgleich.
Da zu
zu  oxidiert wird, fließen die Natrium-Kationen von A nach B.
oxidiert wird, fließen die Natrium-Kationen von A nach B.
- Natrium: flüssig, da Smp.
Sdp.
- Nickel: fest, da Smp.
Sdp.
Da
2
Berechnung der zu erwartenden Spannung
Gründe für die Abweichung der berechneten Spannung
Die Elektrodenpotenziale beziehen sich auf Standardbedingungen:  , wässrige Lösungen,
, wässrige Lösungen,  . Die Betriebstemperatur beträgt allerdings weit über
. Die Betriebstemperatur beträgt allerdings weit über  und es liegen auch keine wässrigen Lösungen vor, deshalb kann es zu Abweichungen kommen.
und es liegen auch keine wässrigen Lösungen vor, deshalb kann es zu Abweichungen kommen.
3
Prinzip eines Akkumulators, am Beispiel der ZEBRA-Batterie
Ein Akkumulator ist ein galvanisches Element, welches durch umkehrbare Zellreaktionen wieder aufgeladen werden kann. Es handelt sich um eine reversible Redoxreaktion, weswegen das Laden dem umgekehrten Entladungsprozess entspricht. Nach Entladung kann durch Anlegen einer äußeren Spannung bei gleicher Polung der Akkumulatur wieder aufgeladen werden.
4
Zuordnung und Begründung des Gefahren-Satzes H260
Um den Gefahrensatz zuzuordnen, wird im Folgenden anhand der Elektrodenpotenziale beurteilt, ob das jeweilige Metall mit Wasser reagiert:
Da das Potenzial von Natrium negativer ist, reagiert es mit Wasser unter Bildung von Wasserstoff und Hydroxid-Ionen.
Nickel reagiert aufgrund des positiveren Potenzials nicht mit Wasser.
Damit ist der H-Satz dem Natrium zuzuordnen.
Erläuterung der Gefahren anhang einer Reaktionsgleichung


 Die Reaktionsgleichung zeigt, dass Wasserstoff entsteht, welches ein brennbares Gas ist. Außerdem bildet sich beim Mischen mit Sauerstoff ein Knallgas.
Die Reaktionsgleichung zeigt, dass Wasserstoff entsteht, welches ein brennbares Gas ist. Außerdem bildet sich beim Mischen mit Sauerstoff ein Knallgas.
Weiterhin entstehen Hydroxid-Ionen, durch die die Lösung alkalisch wird. Je nach Konzentration kann dies ätzend sein.
Weiterhin entstehen Hydroxid-Ionen, durch die die Lösung alkalisch wird. Je nach Konzentration kann dies ätzend sein.
5
Beschreibung des Aufbaus vom Atom und Ion
Natrium-Atom:
Aus dem Periodensystem kann entnommen werden, dass Natrium in der 1. Hauptgruppe steht und damit ein Alkalimetall ist. Natrium besitzt die Ordnungszahl 11, welche der Anzahl der Protonen im Atomkern entspricht. Bei einem neutral geladenen Atom ist die Anzahl der Elektronen in der Atomhülle gleich der Anzahl der Protonen im Atomkern. Die Anzahl der Neutronen im Atomkern ergibt sich als Differenz aus der Massenzahl und der Protonenzahl: .
Natrium-Ion:
.
Natrium-Ion:
Das Natrium-Atom besitzt 3 Schalen und ein Valenzelektron (1. Hauptgruppe). Damit die Edelgaskonfiguration (Neon) erreicht wird, muss ein Elektron abgegeben werden. Also besitzt das -Ion nur noch 10 Elektronen, aber weiterhin 11 Protonen. Die Anzahl der Neutronen bleibt ebenfalls gleich.
Begründung des Größenunterschieds
Das Natrium-Atom ist größer als das Natrium-Ion. Dies ist mit der Schalenbesetzung zu begründen. Um die Edelgaskonfiguration zu erreichen, gibt das Natrium-Ion ein Elektron ab. Demnach ist die äußerste Schale im Gegensatz zum neutralen Atom nicht mehr besetzt und kleiner.
-Ion nur noch 10 Elektronen, aber weiterhin 11 Protonen. Die Anzahl der Neutronen bleibt ebenfalls gleich.
Begründung des Größenunterschieds
Das Natrium-Atom ist größer als das Natrium-Ion. Dies ist mit der Schalenbesetzung zu begründen. Um die Edelgaskonfiguration zu erreichen, gibt das Natrium-Ion ein Elektron ab. Demnach ist die äußerste Schale im Gegensatz zum neutralen Atom nicht mehr besetzt und kleiner.
Aus dem Periodensystem kann entnommen werden, dass Natrium in der 1. Hauptgruppe steht und damit ein Alkalimetall ist. Natrium besitzt die Ordnungszahl 11, welche der Anzahl der Protonen im Atomkern entspricht. Bei einem neutral geladenen Atom ist die Anzahl der Elektronen in der Atomhülle gleich der Anzahl der Protonen im Atomkern. Die Anzahl der Neutronen im Atomkern ergibt sich als Differenz aus der Massenzahl und der Protonenzahl:
Das Natrium-Atom besitzt 3 Schalen und ein Valenzelektron (1. Hauptgruppe). Damit die Edelgaskonfiguration (Neon) erreicht wird, muss ein Elektron abgegeben werden. Also besitzt das