Aufgabe 2 – Anti-Aging-Produkte
Hyaluronsäure ist ein wichtiger Bestandteil unseres Bindegewebes, da sie in der Haut u. a. für Feuchtigkeitsspeicherung, Spannkraft und Elastizität sorgt.
Diese Eigenschaften führen dazu, dass Hyaluronsäure und deren Derivate in vielen kosmetischen Anti-Aging-Produkten zur Bekämpfung von Falten zu finden sind.
Diese Eigenschaften führen dazu, dass Hyaluronsäure und deren Derivate in vielen kosmetischen Anti-Aging-Produkten zur Bekämpfung von Falten zu finden sind.
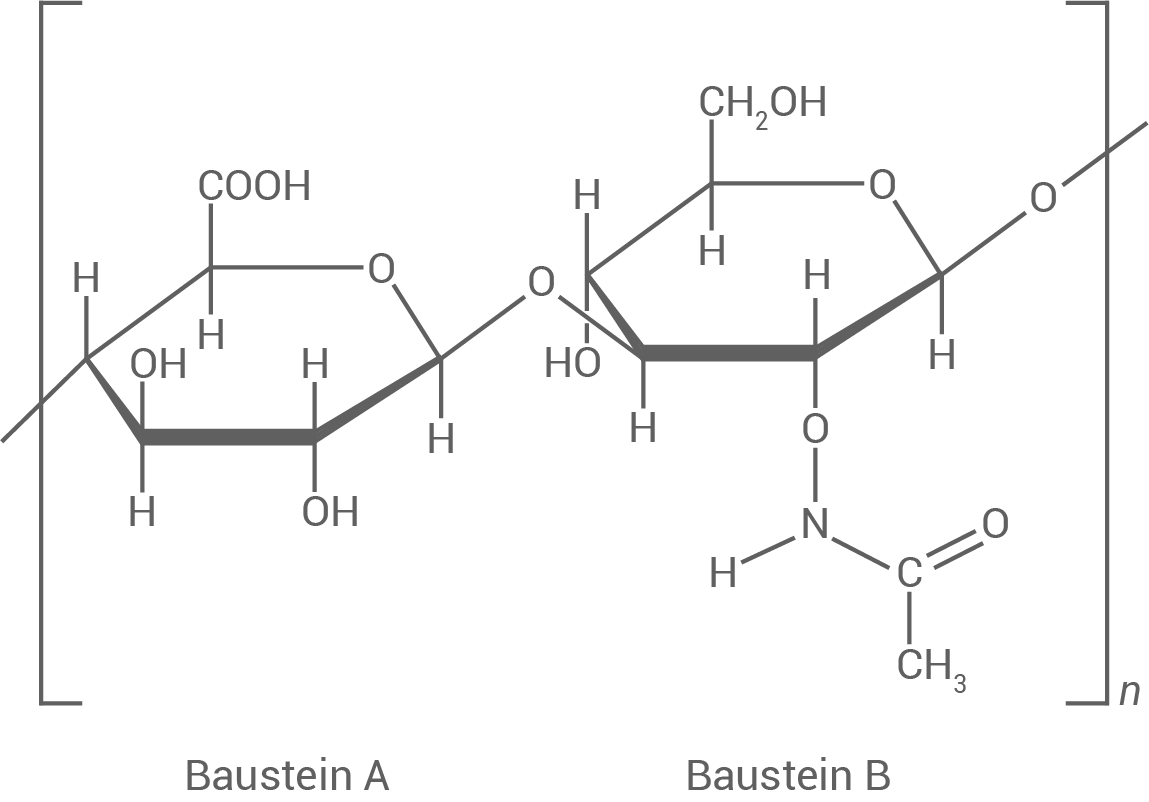
Abbildung 1: Strukturformelausschnitt eines Hyaluronsäure-Makromoleküls
1.1
Die Hyaluronsäure ist ein Polysaccharid, dessen Makromoleküle abwechselnd aus den Bausteinen A und B aufgebaut sind (Abb. 1). Bei dem Monomer-Molekül, welches dem Baustein A zugrunde liegt, handelt es sich um ein Glucuronsäure-Molekül.
- Zeichne die Strukturformeln der Monomer-Moleküle, die den Bausteinen A und B zugrunde liegen, in der HAWORTH-Projektion.
- Zeichne die Strukturformel des Monomer-Moleküls, das dem Baustein B zugrunde liegt, in FISCHER-Projektion.
- Kennzeichne in der FISCHER-Projektion alle asymmetrisch substituierten Kohlenstoff-Atome und gib an, ob es sich um die D- oder L-Form handelt. Begründe deine Entscheidung.
- Begründe ausgehend von geeigneten Strukturformeln und mithilfe von Oxidationszahlen, dass es sich bei Glucuronsäure um ein Oxidationsprodukt der Glucose handelt.
(6 VP)
1.2
Für die äußere Anwendung von kosmetischen Anti-Aging-Produkten sind zu lange Hyaluronsäure-Molekülketten ungeeignet, da sie nicht in tiefere Hautschichten eindringen können. Deshalb werden für die Herstellung von Hyaluronsäure-Produkten (z. B. Cremes, Gele) kürzere Hyaluronsäure-Molekülketten durch hydrolytische Spaltung erzeugt. Wird sehr lange hydrolysiert, erfolgt der Abbau bis zu Disaccharid-Molekülen mit der Abfolge A-B (s. Abb. 1). Ein weiterer Abbau zu Monosaccharid-Molekülen erfolgt nicht.
In einem Experiment wird eine Hyaluronsäure-Lösung sehr lange hydrolysiert.
Vor Beginn (Zeitpunkt 1) und am Ende der Hydrolyse (Zeitpunkt 2) werden jeweils wenige Milliliter der Lösung entnommen und die TOLLENS-Probe durchgeführt.
Vor Beginn (Zeitpunkt 1) und am Ende der Hydrolyse (Zeitpunkt 2) werden jeweils wenige Milliliter der Lösung entnommen und die TOLLENS-Probe durchgeführt.
- Begründe die zu erwartenden Ergebnisse der TOLLENS-Probe zu beiden Zeitpunkten auf molekularer Ebene.
- Zeichne eine Strukturformel des Disaccharid-Moleküls, welches nach der TOLLENS-Probe in der Lösung (Zeitpunkt 2) vorliegt.
- Benenne die Art der Verknüpfung zwischen den Bausteinen A und B.
(5 VP)
1.3
Um die feuchtigkeitsspendende Wirkung von hyaluronsäurehaltigen kosmetischen Produkten zu verbessern, lässt man einen Teil der Hyaluronsäure zu ihrem Natriumsalz (Natriumhyaluronat) reagieren. Dadurch erhöht sich die Wasseraufnahmefähigkeit des Produkts erheblich.
- Begründe anhand der Strukturmerkmale der Hyaluronsäure-Makromoleküle die grundsätzlich gute Wasseraufnahmefähigkeit der kosmetischen Produkte.
- Gib einen geeigneten Reaktionspartner der Hyaluronsäure an, der zur Synthese des Natriumsalzes der Hyaluronsäure eingesetzt werden kann.
- Gib eine mögliche Erklärung für die größere Wasseraufnahmefähigkeit von Natriumhyaluronat im Vergleich zur Hyaluronsäure an.
(5 VP)
2
Einige Anti-Aging-Cremes enthalten Methylparaben (4-Hydroxybenzoesäuremethylester) als Konservierungsmittel. Ein Ausgangsstoff für die Herstellung dieses Konservierungsmittels ist 4-Hydroxybenzoesäure. Der Synthese liegt eine Gleichgewichtsreaktion zugrunde.
- Stelle die zugehörige Reaktionsgleichung auf. Geben Sie dabei die Strukturformeln der beteiligten Stoffe an.
- Beschreibe ein Experiment, mit dem das Erreichen des chemischen Gleichgewichts beobachtet werden kann.
(4 VP)
(20 VP)
1.1
Strukturformeln der Monomer-Moleküle in HAWORTH-Projektion
Strukturformel des Monomer-Moleküls in FISCHER-Projektion
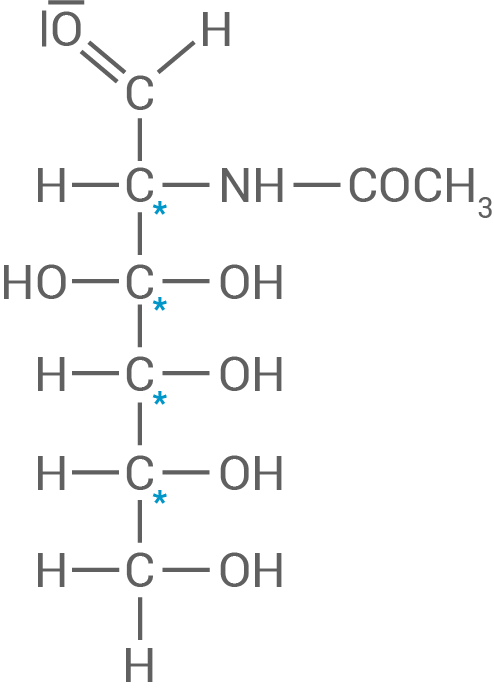 Asymmetrische
Asymmetrische  -atome und Entscheidung der Form
Die asymmetrisch substituierten Kohlenstoff-Atome sind mit
-atome und Entscheidung der Form
Die asymmetrisch substituierten Kohlenstoff-Atome sind mit  gekennzeichnet.
Die Lage der Hydroxylgruppe am untersten asymmetrischen Kohlenstoffatom bestimmt die Benennung nach D-oder L-Form. Da die Hydroxylgruppe rechts liegt, entspricht das Molekül der D-Form.
Begründung von Glucuronsäure als Oxidationsprodukt der Glucose
gekennzeichnet.
Die Lage der Hydroxylgruppe am untersten asymmetrischen Kohlenstoffatom bestimmt die Benennung nach D-oder L-Form. Da die Hydroxylgruppe rechts liegt, entspricht das Molekül der D-Form.
Begründung von Glucuronsäure als Oxidationsprodukt der Glucose
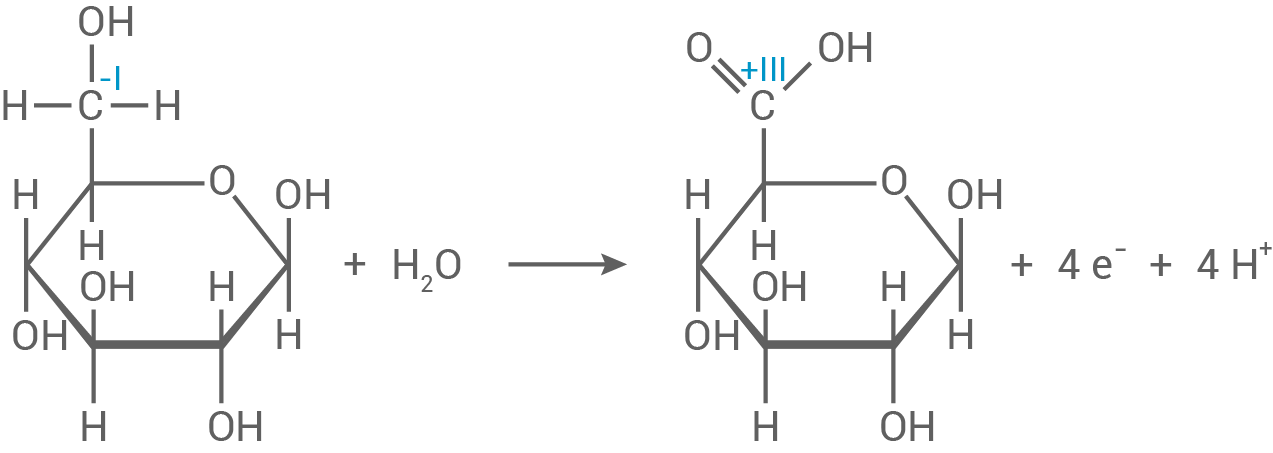 Die Oxidationszahl am sechsten Kohlenstoffatom des Glucose-Moleküls erhöht sich von -I zu +III. Das Kohlenstoffatom wird also oxidiert, wobei Glucuronsäure das Oxidationsprodukt der Glucose ist.
Die Oxidationszahl am sechsten Kohlenstoffatom des Glucose-Moleküls erhöht sich von -I zu +III. Das Kohlenstoffatom wird also oxidiert, wobei Glucuronsäure das Oxidationsprodukt der Glucose ist.
|
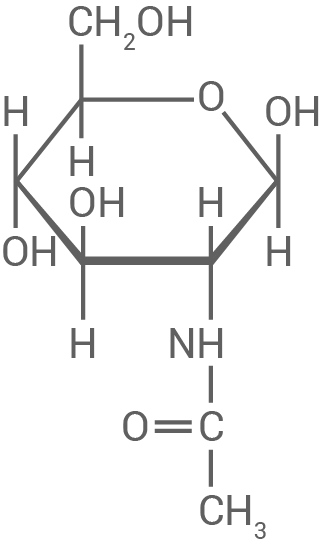
|
|
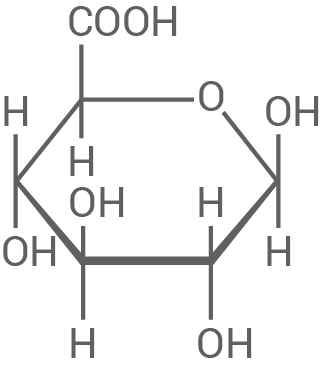
Monomer A
(D-Glucuronsäure) |
Monomer B
(N-Acetyl-D-Glucosamin) |


1.2
Ergebnisse der TOLLENS-Probe
Es liegen nur Polysaccharid Ketten vor, weswegen nur am Kettenende eine freie anomere  -Gruppe vorliegt. Demnach kann nur diese eine positive Reaktion zeigen.
Zu Zeitpunkt 1, also vor Beginn der Hydrolyse, ist eine negative Reaktion zu erwarten, da Hyaluronsäure-Lösung sich nicht-reduzierend verhält.
Zu Zeitpunkt 2, also am Ende der Hydrolyse, fällt die TOLLENS-Probe positiv aus, da die Lösung mit dem Dimeren A und B jeweils eine freie anomere Hydroxygruppe enthält. Die Lösung wirkt dann reduzierend.
Strukturformel des Disaccharid-Moleküls
-Gruppe vorliegt. Demnach kann nur diese eine positive Reaktion zeigen.
Zu Zeitpunkt 1, also vor Beginn der Hydrolyse, ist eine negative Reaktion zu erwarten, da Hyaluronsäure-Lösung sich nicht-reduzierend verhält.
Zu Zeitpunkt 2, also am Ende der Hydrolyse, fällt die TOLLENS-Probe positiv aus, da die Lösung mit dem Dimeren A und B jeweils eine freie anomere Hydroxygruppe enthält. Die Lösung wirkt dann reduzierend.
Strukturformel des Disaccharid-Moleküls
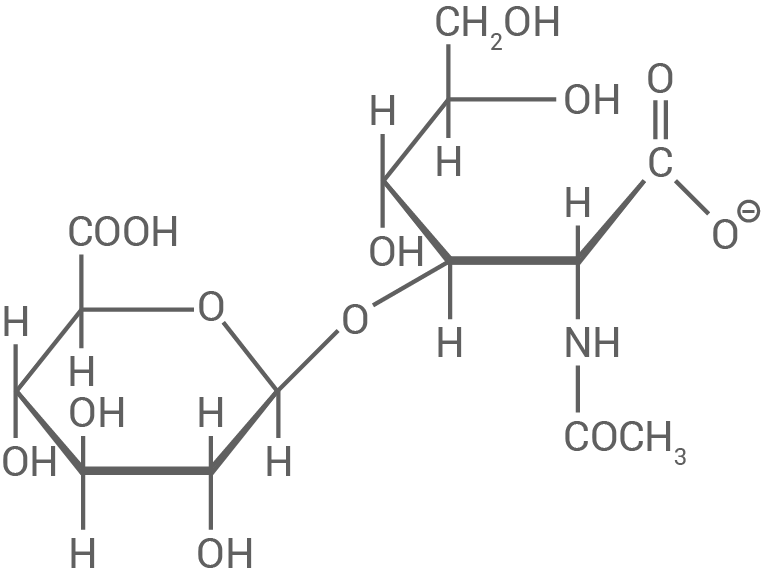 Verknüpfung zwischen den Bausteinen A und B
Es handelt sich um eine
Verknüpfung zwischen den Bausteinen A und B
Es handelt sich um eine  -1,3-glykosidische Bindung.
-1,3-glykosidische Bindung.

1.3
Begründung der guten Wasseraufnahmefähigkeit
Das Hyaluronsäure-Molekül weist eine große Anzahl an polaren Hydroxyl- und Carboxylgruppen auf. Diese erlauben die Ausbildung von inter- und intramolekularen Wasserstoffbrücken, woraus eine dreidimensionale Anordnung mit hydrophilen Lücken und Oberflächen aufweist. Folglich können sich viele Wassermoleküle ein- und anlagern, was die gute Wasseraufnahmefähigkeit erklärt.
Geeigneter Reaktionspartner der Hyaluronsäure
Die freien Carboxylgruppen der Hyaluronsäurekette können mit einer Base bzw. Lauge wie  Dabei werden diese zu Carboxylat
Dabei werden diese zu Carboxylat  umgesetzt.
Erklärung der größeren Wasseraufnahmefähigkeit von Natriumhyaluronat
Anstelle von Carboxylgruppen liegen Carboxylatgruppen vor und als Gegenionen befinden sich Natriumionen zwischen den Ketten. Dadurch entstehen starke elektrostatische Wechselwirkungen und diese ermöglichen die Einlagerung von mehr Wassermolekülen.
umgesetzt.
Erklärung der größeren Wasseraufnahmefähigkeit von Natriumhyaluronat
Anstelle von Carboxylgruppen liegen Carboxylatgruppen vor und als Gegenionen befinden sich Natriumionen zwischen den Ketten. Dadurch entstehen starke elektrostatische Wechselwirkungen und diese ermöglichen die Einlagerung von mehr Wassermolekülen.
2
Reaktionsgleichung der Estersynthese
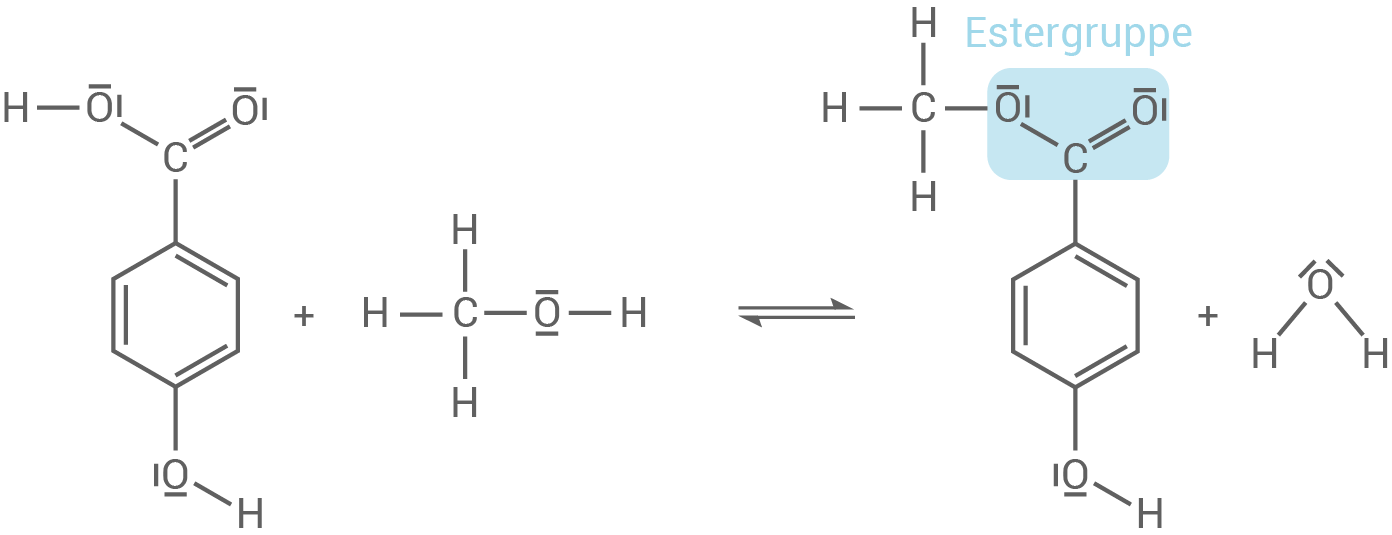 Experiment zum Erreichen des chemischen Gleichgewichts
4-Hydroxybenzoesäure (Paraben) wird mit Methanol (im Überschuss) und einer Säure (z.B. konzentrierte Schwefelsäure) verestert.
Experiment zum Erreichen des chemischen Gleichgewichts
4-Hydroxybenzoesäure (Paraben) wird mit Methanol (im Überschuss) und einer Säure (z.B. konzentrierte Schwefelsäure) verestert.
Die Säurekonzentration nimmt im Laufe der Reaktion ab, da die Carboxylgruppe in die Esterbindung eingeht. Im Gleichgewichtzustand ändert sich die Säurekonzentration nicht mehr.
Während des Experiments werden zu verschiedenen Zeitpunkten Proben entnommen und mit Natronlauge titriert. Als Indikator würde sich hierbei Bromthymolblau eignen. Sobald sich der Vebrauch an Natronlauge nicht mehr ändert, ist das Gleichgewicht erreicht.

Die Säurekonzentration nimmt im Laufe der Reaktion ab, da die Carboxylgruppe in die Esterbindung eingeht. Im Gleichgewichtzustand ändert sich die Säurekonzentration nicht mehr.
Während des Experiments werden zu verschiedenen Zeitpunkten Proben entnommen und mit Natronlauge titriert. Als Indikator würde sich hierbei Bromthymolblau eignen. Sobald sich der Vebrauch an Natronlauge nicht mehr ändert, ist das Gleichgewicht erreicht.