Aufgabe 4 – Zinn
Zinn  ist vermutlich seit ca. 3500 v.Chr. bekannt und wurde schon im Altertum wegen seiner guten Verformbarkeit zur Herstellung von Alltagsgegenständen benutzt. Es besitzt mit
ist vermutlich seit ca. 3500 v.Chr. bekannt und wurde schon im Altertum wegen seiner guten Verformbarkeit zur Herstellung von Alltagsgegenständen benutzt. Es besitzt mit  eine deutlich niedrigere Schmelztemperatur als andere Metalle wie Eisen und Kupfer und wird deshalb unter anderem auch zum Löten verwendet.
eine deutlich niedrigere Schmelztemperatur als andere Metalle wie Eisen und Kupfer und wird deshalb unter anderem auch zum Löten verwendet.
1.1
Zinn steht im Periodensystem der Elemente (PSE) in der vierten Hauptgruppe.
- Gib vier Informationen über den Aufbau eines Zinn-Atoms an, die aus dem PSE abgeleitet werden können.
- Begründe mithilfe des PSE, dass Zinn-Kationen in natürlich vorkommenden Salzen vorwiegend als
-lonen auftreten.
(3 VP)
1.2
Zinn lässt sich in einer Redoxreaktion aus Zinnstein (Zinn -oxid) gewinnen. Hierzu wird Zinnstein mit Kohlenstoff erhitzt, wobei sich neben dem Metall noch Kohlenstoffmonooxid bildet. Das so gewonnene Zinn ist noch durch andere Metalle wie z. B. Eisen verunreinigt. Um es zu reinigen, kann das Zinn in einem Flammofen (Abb. 1) auf ungefähr
-oxid) gewinnen. Hierzu wird Zinnstein mit Kohlenstoff erhitzt, wobei sich neben dem Metall noch Kohlenstoffmonooxid bildet. Das so gewonnene Zinn ist noch durch andere Metalle wie z. B. Eisen verunreinigt. Um es zu reinigen, kann das Zinn in einem Flammofen (Abb. 1) auf ungefähr  erhitzt werden.
erhitzt werden.
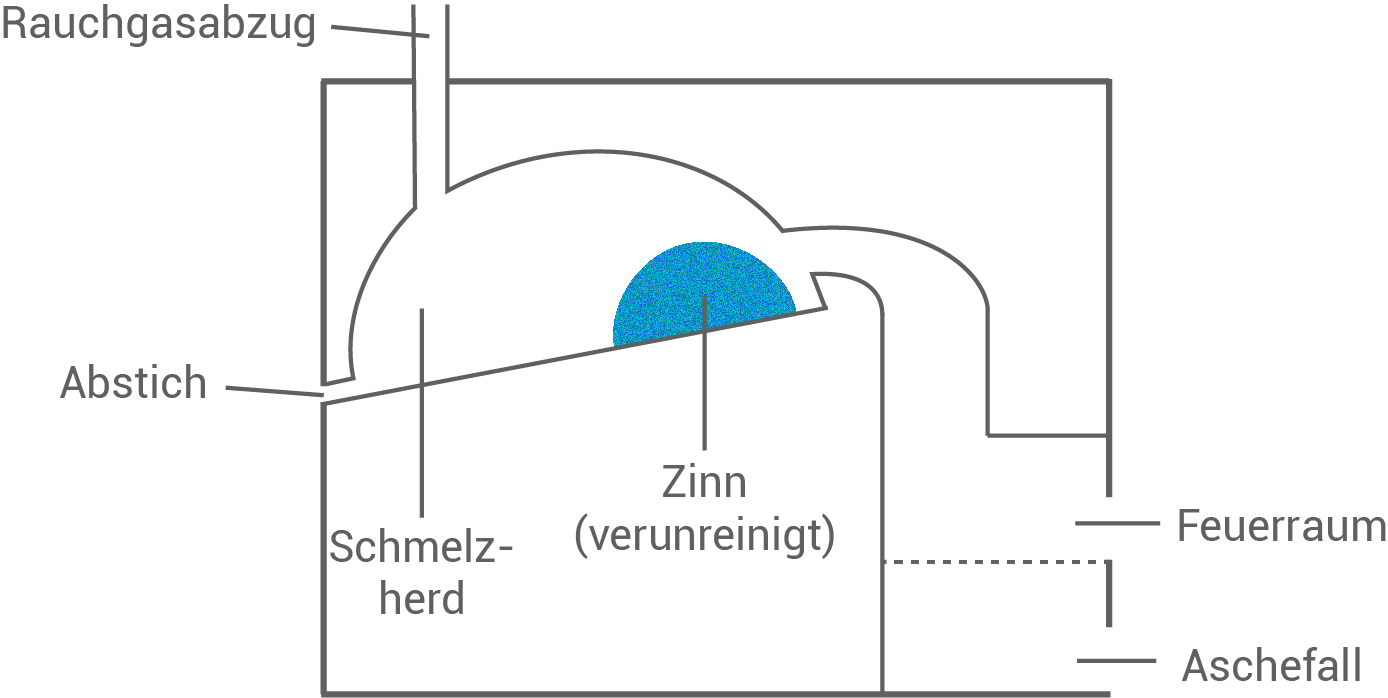

Abbildung 1: Flammofen (schematisch)
- Stelle eine Reaktionsgleichung für die Gewinnung von Zinn aus Zinnstein auf.
- Gib in der Reaktionsgleichung sämtliche Oxidationszahlen an und begründe, wo die Oxidation bzw. Reduktion stattfindet.
- Berechne die Masse an Zinnstein, die zur Herstellung von
Zinn notwendig ist.
- Erkläre das Prinzip der Reinigung des Zinns mithilfe von Abb. 1 und den Angaben im Text.
(7 VP)
2.1
Neben dem natürlich vorkommenden Zinn -oxid kann Zinn
-oxid kann Zinn -oxid synthetisch hergestellt werden. Diese metastabile Verbindung zerfällt unter bestimmten Bedingungen in elementares Zinn und Zinn
-oxid synthetisch hergestellt werden. Diese metastabile Verbindung zerfällt unter bestimmten Bedingungen in elementares Zinn und Zinn -oxid.
-oxid.
- Stelle die Reaktionsgleichung für den Zerfall von Zinn
-oxid auf.
- Erkläre an diesem Beispiel den Begriff metastabil.
(3 VP)
2.2
Das Redoxpaar  wird in zwei getrennten galvanischen Zellen untersucht. Die zweite Halbzelle besteht in einem Fall aus dem Redoxpaar
wird in zwei getrennten galvanischen Zellen untersucht. Die zweite Halbzelle besteht in einem Fall aus dem Redoxpaar  und im anderen Fall aus dem Redoxpaar
und im anderen Fall aus dem Redoxpaar  .
.
- Fertige von einer der beiden galvanischen Zellen eine beschriftete Skizze (unter Standardbedingungen) an.
- Stelle für die von dir gewählte galvanische Zelle die Teilgleichungen für die an Anode und Kathode ablaufenden elektrochemischen Prozesse auf, wenn mit der galvanischen Zelle ein Motor betrieben wird.
- Berechne die Spannung beider galvanischer Zellen unter Standardbedingungen.
- Erkläre die Änderung der Spannung in beiden galvanischen Zellen, wenn jeweils die Lösung in der Zinn-Halbzelle durch Zugabe von Wasser verdünnt wird.
(7 VP)
(20 VP)
1.1
Aufbau eines Zinn-Atoms an
![\([Kr]\,4d^{10}\)](https://mathjax.schullv.de/30f043e0f9ab74d8eca2bbb07cece419fc336755f6bb13eee5019d7e7bcccff1?color=5a5a5a) zu erreichen. Deshalb treten überwiegend
zu erreichen. Deshalb treten überwiegend  -Ionen auf.
Es müssen dabei oxidative Bedingungen herrschen.
-Ionen auf.
Es müssen dabei oxidative Bedingungen herrschen.
- Ordnungszahl
Protonen
- Protonenzahl = Elektronenzahl
Elektronen
- Elektronenkonfiguration:
- Element der
Hauptgruppe
vier Valenzelektronen; Elemente zwei- oder vierwertig
- relative Atommasse:
kein Reinelement und besitzt mehrere Isotope
1.2
Reaktionsgleichung für die Zinngewinnung aus Zinnstein


 Oxidationszahlen und Redoxreaktion
Oxidationszahlen und Redoxreaktion
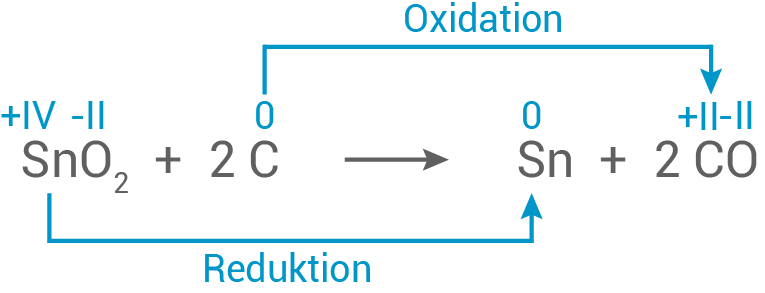 Die Zinn
Die Zinn -Ionen werden zu Zinn reduziert und Kohlenstoff wird zu Kohlenstoffmonoxid oxidiert.
Masse an Zinnstein für die Herstellung von
-Ionen werden zu Zinn reduziert und Kohlenstoff wird zu Kohlenstoffmonoxid oxidiert.
Masse an Zinnstein für die Herstellung von  Zinn
Mit der gegebenen Masse und der molaren Masse lässt sich zunächst die benötigte Stoffmenge berechnen:
Zinn
Mit der gegebenen Masse und der molaren Masse lässt sich zunächst die benötigte Stoffmenge berechnen:
![\(\begin{array}[t]{rll}
M(Sn)&= & 118,7\,\text{g} \cdot \text{mol}^{-1} \\[5pt]
n(Sn)&=& \dfrac{m(Sn)}{M(Sn)} \\[5pt]
&=& \dfrac{100\ 000\,\text{g}}{118,7\,\text{g}\cdot \text{mol}^{-1}} \\[5pt]
&\approx&842\,\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/d6afac2b10c1c131f33ab1505fc2bf1c2dd698d49a32553931b7ebb007293bc5?color=5a5a5a) Weiterhin gilt:
Weiterhin gilt:
![\(\begin{array}[t]{rll}
n(Sn)&=& n(SnO_2) \\[5pt]
\end{array}\)](https://mathjax.schullv.de/1d33dc69e4eb0a3e34dc03071214bde64afdfed360ff5a473350872e79d17d62?color=5a5a5a) Mit der molaren Masse von Zinnstein kann nun die Masse berechnet werden:
Mit der molaren Masse von Zinnstein kann nun die Masse berechnet werden:
![\(\begin{array}[t]{rll}
M(SnO_2)&=& 150,7\,\text{g}\cdot \,\text{mol}^{-1} \\[5pt]
m(SnO_2)&=& n(SnO_2)\cdot M(SnO_2) \\[5pt]
&=& 842\,\text{mol} \cdot 150,7\,\text{g}\cdot \,\text{mol}^{-1} \\[5pt]
&\approx& 127 \,000\,\text{g} \\[5pt]
&\approx& 127 \,\text{kg}
\end{array}\)](https://mathjax.schullv.de/c804c694fafe631cc61d3ae241267cd002ca38a98c0d5607799c3e70320b64da?color=5a5a5a) Für
Für  Zinn werden ca.
Zinn werden ca.  Zinnstein benötigt.
Prinzip der Reinigung
Die Konstruktion des Ofens vermeidet den direkten Kontakt zwischen Zinn und der Flamme. Dieser wird nämlich nur durch die heißen Gase geschmolzen, wodurch mögliche Verunreinigungen vermieden werden sollen und die Temperatur besser kontrolliert werden kann.
Zinn schmilzt bei
Zinnstein benötigt.
Prinzip der Reinigung
Die Konstruktion des Ofens vermeidet den direkten Kontakt zwischen Zinn und der Flamme. Dieser wird nämlich nur durch die heißen Gase geschmolzen, wodurch mögliche Verunreinigungen vermieden werden sollen und die Temperatur besser kontrolliert werden kann.
Zinn schmilzt bei  Die im Rohzinn enthaltenen Metalle schmelzen allerdings erst bei höheren Temperaturen. Das geschmolzene Reinzinn kann somit im abgeschrägten Schmelzherd zum Abstich abfließen und die festen anderen Metalle bleiben im Ofen zurück.
Die im Rohzinn enthaltenen Metalle schmelzen allerdings erst bei höheren Temperaturen. Das geschmolzene Reinzinn kann somit im abgeschrägten Schmelzherd zum Abstich abfließen und die festen anderen Metalle bleiben im Ofen zurück.

2.1
Reaktionsgleichung für den Zerfall von Zinn -oxid
-oxid


 Erklärung von Metastabilität
Ist ein Stoff metastabil wären Zerfalls- oder Umwandlungsreaktionen bei Raumtemperatur bzw. bei den gegebenen Bedingungen thermodynamisch möglich, laufen aber aufgrund einer kinetischen Hemmung nicht ab.
Erklärung von Metastabilität
Ist ein Stoff metastabil wären Zerfalls- oder Umwandlungsreaktionen bei Raumtemperatur bzw. bei den gegebenen Bedingungen thermodynamisch möglich, laufen aber aufgrund einer kinetischen Hemmung nicht ab.
Für den Zerfall von Zinn -oxid bedeutet dies, dass es über lange Zeit gelagert werden kann ohne durch entstandenes Zinn oder Zinn
-oxid bedeutet dies, dass es über lange Zeit gelagert werden kann ohne durch entstandenes Zinn oder Zinn -oxid verunreinigt zu werden.
-oxid verunreinigt zu werden.
Für den Zerfall von Zinn
2.2
Skizze einer galvanischen Zelle aus Zinn und Silber
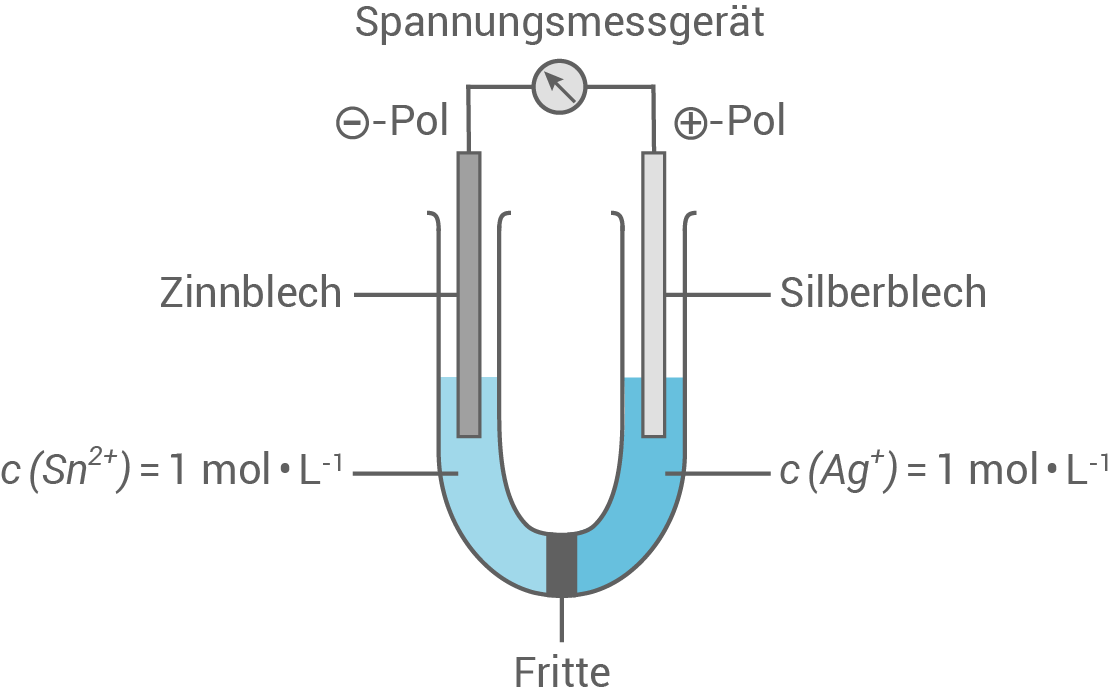 Alternativ: Eisen-Halbzelle anstelle Silber-Halbzelle
Elektrochemischen Prozesse bei einem Motor
Spannungsberechnung
Allgemein gilt:
Alternativ: Eisen-Halbzelle anstelle Silber-Halbzelle
Elektrochemischen Prozesse bei einem Motor
Spannungsberechnung
Allgemein gilt:
 Daraus folgt für die Elemente:
Daraus folgt für die Elemente:
![\(\begin{array}[t]{rll}
U_1 &=& E^0(Ag/Ag^{+})-E^0(Sn/Sn^{2+}) \\[5pt]
&=& 0,80\,\,\text{V}-(-0,14\,\,\text{V}) \\[5pt]
&=& 0,94\,\,\text{V}
\end{array}\)](https://mathjax.schullv.de/810826fc4aeed69aa72002002b87280f95a50ada43d91970d645b35eee39b52b?color=5a5a5a) oder:
oder:
![\(\begin{array}[t]{rll}
U_2 &=& E^0(Sn/Sn^{2+})-E^0(Fe/Fe^{2+}) \\[5pt]
&=& -0,14\,\,\text{V}-(-0,44\,\,\text{V}) \\[5pt]
&=& 0,30\,\,\text{V}
\end{array}\)](https://mathjax.schullv.de/5b1502a55b3eff45f1a60e11431d64f6daea8d59ed84031d46cbad671933b339?color=5a5a5a) Spannungsänderung durch Verdünnung
Nach der NERNST'schen Gleichung kann einem Metall in einer wässrigen Lösung eine Lösungsspannung zugeordnet werden. Enthält die Lösung Metallkationen, besteht bei diesen das Bestreben, sich an der Metallelektrode abzuscheiden, was als "Abscheidungsbestreben" bezeichnet wird. Beim Eintauchen einer Metallelektrode in ihre Salzlösung stellt sich ein elektrochemisches Gleichgewicht ein, dessen Position von der Metallart (Lösungsspannung) und der Konzentration der Metallionenlösung (Abscheidungsbestreben) abhängt.
Spannungsänderung durch Verdünnung
Nach der NERNST'schen Gleichung kann einem Metall in einer wässrigen Lösung eine Lösungsspannung zugeordnet werden. Enthält die Lösung Metallkationen, besteht bei diesen das Bestreben, sich an der Metallelektrode abzuscheiden, was als "Abscheidungsbestreben" bezeichnet wird. Beim Eintauchen einer Metallelektrode in ihre Salzlösung stellt sich ein elektrochemisches Gleichgewicht ein, dessen Position von der Metallart (Lösungsspannung) und der Konzentration der Metallionenlösung (Abscheidungsbestreben) abhängt.
Ist die Metallionenkonzentration in der Lösung niedrig, verlassen viele Metallionen die feste Phase, und die Elektrode wird "unedler". Das Gegenteil gilt für eine hohe Metallionenkonzentration. Das elektrochemische Gleichgewicht einer Elektrode aus Metall/Metallsalzlösung kann durch die Messung ihres Elektrodenpotenzials gegen die Normalwasserstoffelektrode (Elektrodenpotenzial = bestimmt werden.
Durch die Verringerung der Zinnionenkonzentration unter
bestimmt werden.
Durch die Verringerung der Zinnionenkonzentration unter  in einer Zinn-Halbzelle wird ihr Elektrodenpotenzial kleiner als
in einer Zinn-Halbzelle wird ihr Elektrodenpotenzial kleiner als  und die Zinn-Elektrode wird "unedler".
und die Zinn-Elektrode wird "unedler".
Im Zinn-Silber-Element fungiert die Zinn-Halbzelle als Anode und die Silber-Halbzelle als Kathode. Eine Verdünnung der Lösung auf der Zinnseite führt zu einer größeren Spannungsmessung ohne Stromfluss im Vergleich zum Zinn-Silber-Element unter Standardbedingungen. Hierbei muss das Elektrodenpotenzial in die Berechnung einfließen, da in der Zinn-Halbzelle Zinn oxidiert wird (Anodenreaktion). Beispiel:
![\(\begin{array}[t]{rll}
U&=& E^0\,\text{(Kathode)} - E\,\text{(Anode)}& \\[5pt]
&=& 0,80 \,\text{V} - (-0,20 \,\text{V}) & \\[5pt]
&=& 1,00 \,\text{V}
\end{array}\)](https://mathjax.schullv.de/9673d365174c1d744213967e62c233ea4129e6403f0fd705dd6eafb86b7dac1e?color=5a5a5a) Im Zinn-Eisen-Element fungiert die Zinn-Halbzelle als Kathode und die Eisen-Halbzelle als Anode. Bei einer Verringerung der Zinnionenkonzentration unter
Im Zinn-Eisen-Element fungiert die Zinn-Halbzelle als Kathode und die Eisen-Halbzelle als Anode. Bei einer Verringerung der Zinnionenkonzentration unter  in diesem Element muss für die Betrachtung der Spannung ein Wert
in diesem Element muss für die Betrachtung der Spannung ein Wert  für das Elektrodenpotenzial angenommen werden (da die Zinn-Halbzelle in diesem Fall die Kathode ist).
Beispiel:
für das Elektrodenpotenzial angenommen werden (da die Zinn-Halbzelle in diesem Fall die Kathode ist).
Beispiel:

![\(\begin{array}[t]{rll}
U&=& E\,\text{(Kathode)} - E^0\,\text{(Anode)}& \\[5pt]
&=& -0,20 \,\text{V} - (-0,44 \,\text{V}) & \\[5pt]
&=& 0,24 \,\text{V}
\end{array}\)](https://mathjax.schullv.de/a81adfc6ac8ec5db82fea8b906bc3c372faffdae17538a3b3a6c8638d7c68357?color=5a5a5a)

Ist die Metallionenkonzentration in der Lösung niedrig, verlassen viele Metallionen die feste Phase, und die Elektrode wird "unedler". Das Gegenteil gilt für eine hohe Metallionenkonzentration. Das elektrochemische Gleichgewicht einer Elektrode aus Metall/Metallsalzlösung kann durch die Messung ihres Elektrodenpotenzials gegen die Normalwasserstoffelektrode (Elektrodenpotenzial =
Im Zinn-Silber-Element fungiert die Zinn-Halbzelle als Anode und die Silber-Halbzelle als Kathode. Eine Verdünnung der Lösung auf der Zinnseite führt zu einer größeren Spannungsmessung ohne Stromfluss im Vergleich zum Zinn-Silber-Element unter Standardbedingungen. Hierbei muss das Elektrodenpotenzial in die Berechnung einfließen, da in der Zinn-Halbzelle Zinn oxidiert wird (Anodenreaktion). Beispiel: