Aufgabe 1 – Pikrinsäure
Die Beeinflussung eines chemischen Gleichgewichts kann am Beispiel des Anthracen-Pikrinsäure-Gleichgewichts experimentell untersucht werden. Dazu werden Lösungen von Anthracen und Pikrinsäure zusammengegeben. Es stellt sich folgendes Gleichgewicht ein:
1
Zur Untersuchung des Gleichgewichts werden folgende Versuche durchgeführt:
| Versuch A: | Es wird weiteres Anthracen gelöst. |
| Versuch B: | Es wird zusätzlich Pikrinsäure gelöst. Dabei wird eine Intensivierung der Rotfärbung beobachtet. |
| Versuch C: | Das Stoffgemisch wird erhitzt. Dabei wird eine Abschwächung der Rotfärbung beobachtet. |
- Nenne die zu erwartende Beobachtung bei Versuch A.
- Stelle das Massenwirkungsgesetz für diese Gleichgewichtsreaktion auf und begründe damit die Beobachtung in Versuch B.
- Beschreibe das Prinzip von LE CHATELIER und erläutere davon ausgehend die Beobachtung in Versuch C.
(6 VP)
2
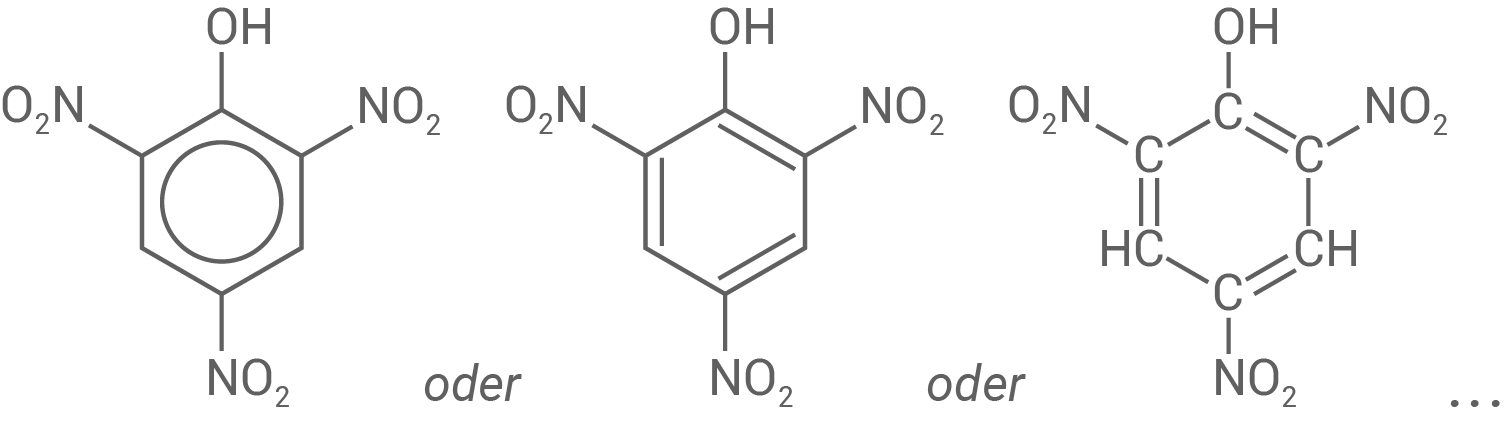
Bei Pikrinsäure handelt es sich um 2,4,6-Trinitrophenol (auch 1-Hydroxy-2,4,6-Trinitrobenzol). Für die Nitrogruppe  werden die in Abbildung 1 gezeigten Strukturformel-Darstellungen vorgeschlagen.
werden die in Abbildung 1 gezeigten Strukturformel-Darstellungen vorgeschlagen.
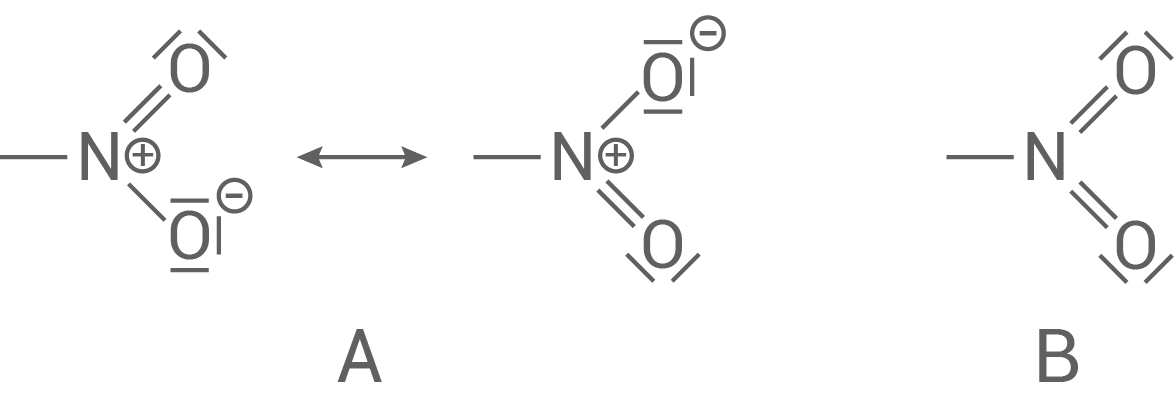

Abbildung 1: Unterschiedliche Strukturformel-Darstellungen für die Nitrogruppe
- Erkläre die Bedeutung des Pfeils in Darstellung A.
- Begründe, dass die Darstellung B problematisch ist.
- Zeichne eine Strukturformel des Pikrinsäure-Moleküls.
- Beschreibe den räumlichen Bau des aromatischen Rings im Pikrinsäure-Molekül.
(5 VP)
3
Pikrinsäure darf an Schulen nicht mehr verwendet oder gelagert werden, da sie sich bereits bei geringen thermischen oder mechanischen Belastungen schlagartig zersetzen kann. Bei der Zersetzung von Pikrinsäure entstehen Kohlenstoff, Wasserdampf und die Gase Kohlenstoffmonooxid und Stickstoff. Auf Gefäßen, in denen Pikrinsäure gelagert wird, sind folgende Gefahrenpiktogramme zu finden.


Abbildung 2: Gefahrenpiktogramme für Pikrinsäure
- Stelle eine Reaktionsgleichung für die Zersetzung von Pikrinsäure mit Hilfe von Molekülformeln (Summenformeln) auf.
- Gib die Gefahren an, auf die die Gefahrenpiktogramme in Abbildung 2 hinweisen.
- Begründe die Kennzeichnung von Pikrinsäure mit dem Gefahrenpiktogramm A unter Einbeziehung der Reaktionsgleichung.
(4 VP)
4
Der prozentuale Massenanteil  von Pikrinsäure in einer wässrigen Pikrinsäure-Lösung soll ermittelt werden. Dazu werden
von Pikrinsäure in einer wässrigen Pikrinsäure-Lösung soll ermittelt werden. Dazu werden  der Lösung mit Wasser auf ca.
der Lösung mit Wasser auf ca.  aufgefüllt.
aufgefüllt.
Bei der anschließenden Titration mit Natronlauge werden bis zum Äquivalenzpunkt
werden bis zum Äquivalenzpunkt  der eingesetzten Natronlauge verbraucht. Bei der Titration läuft folgende chemische Reaktion ab:
der eingesetzten Natronlauge verbraucht. Bei der Titration läuft folgende chemische Reaktion ab:



Bei der anschließenden Titration mit Natronlauge
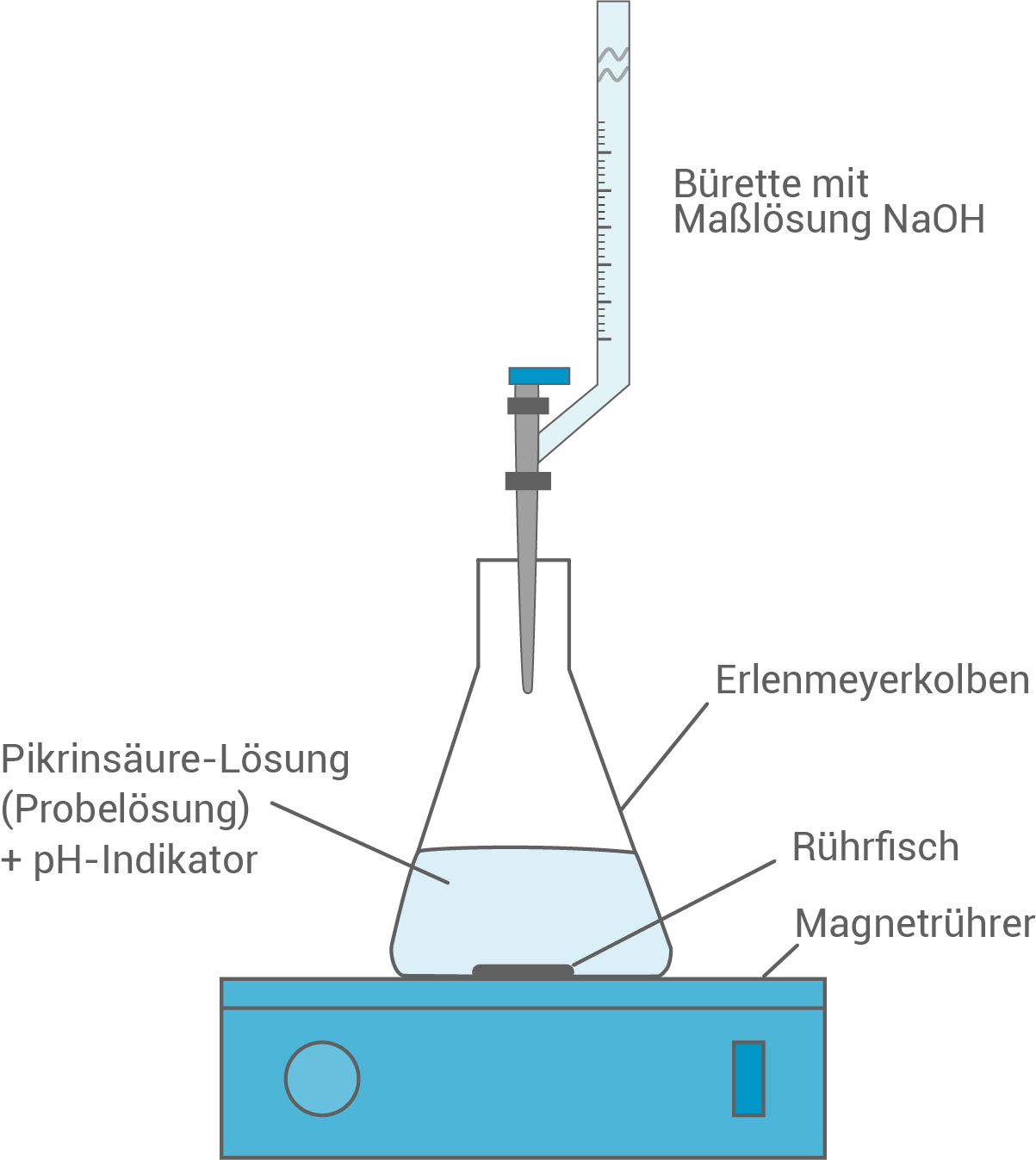
- Zeichne einen vollständig beschrifteten Versuchsaufbau für die Durchführung dieser Titration.
- Berechne den prozentualen Massenanteil
an Pikrinsäure in der wässrigen Pikrinsäure-Lösung.
(5 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Beobachtung Versuch A
Die Rotfärbung intensiviert sich.
Aufstellen des Massenwirkungsgesetzes (MWG)
 Begründung der Beobachtung in B
Zusätzliches Lösen von Pikrinsäure, bewirkt eine Erhöhung derer Stoffmengenkonzentration
Begründung der Beobachtung in B
Zusätzliches Lösen von Pikrinsäure, bewirkt eine Erhöhung derer Stoffmengenkonzentration  welche das chemische Gleichgewicht verschiebt. Aus dem MWG folgt, dass für einen Ausgleich die Stoffmengenkonzentration von Anthracenpikrat erhöht werden muss, damit das Verhältnis von Zähler und Nenner wieder stimmt. Folglich bleibt so
welche das chemische Gleichgewicht verschiebt. Aus dem MWG folgt, dass für einen Ausgleich die Stoffmengenkonzentration von Anthracenpikrat erhöht werden muss, damit das Verhältnis von Zähler und Nenner wieder stimmt. Folglich bleibt so  konstant.
konstant.
Die Erhöhung von ist der Grund für die Intensivierung der Rotfärbung.
Prinzip von LE CHATELIER und Beobachtungen in Versuch C
Das Prinzip von LE CHATELIER besagt, dass wenn auf ein sich im Gleichgewicht befindlichen System, ein äußerer Zwang ausgeübt wird, sich die Lage des Gleichgewichts so verschiebt, dass die Wirkung des Zwanges minimal wird.
ist der Grund für die Intensivierung der Rotfärbung.
Prinzip von LE CHATELIER und Beobachtungen in Versuch C
Das Prinzip von LE CHATELIER besagt, dass wenn auf ein sich im Gleichgewicht befindlichen System, ein äußerer Zwang ausgeübt wird, sich die Lage des Gleichgewichts so verschiebt, dass die Wirkung des Zwanges minimal wird.
Bei einer Temperaturerhöhung (hier durch Erhitzen des Stoffgemischs) wird die endotherme Reaktion bevorzugt. Das Gleichgewicht verschiebt sich folglich auf die Seite der Edukte (Anthracen und Pikrinsäure), wodurch sich die Rotfärbung abschwächt.
Die Erhöhung von
Bei einer Temperaturerhöhung (hier durch Erhitzen des Stoffgemischs) wird die endotherme Reaktion bevorzugt. Das Gleichgewicht verschiebt sich folglich auf die Seite der Edukte (Anthracen und Pikrinsäure), wodurch sich die Rotfärbung abschwächt.
2
Bedeutung des Pfeils
In Darstellung A ist ein Mesomeriepfeil abgebildet. Dieser stellt die mesomeren Grenzformeln der Nitrogruppe dar und zeigt, dass die tatsächlichen Bindungsverhältnisse in keinem von beiden korrekt bzw. real sind (unterschiedliche Verteilung der Elektronen).
Problematik der Darstellung B
Darstellung B ist problematisch, da hier die Edelgasregel, also die Oktettregel, für das Stickstoff-Atom nicht erfüllt ist.
Strukturformel von Pikrinsäure (nur eine erforderlich)
 Räumlicher Bau des aromatischen Rings
Der aromatische Ring in Pikrinsäure wird aus sechs
Räumlicher Bau des aromatischen Rings
Der aromatische Ring in Pikrinsäure wird aus sechs  -Atomen mit gleichlangen Bindungen und gleich großen Bindungswinkeln gebildet. Dieses gleichseitige Sechseck ist eine planare Struktur.
-Atomen mit gleichlangen Bindungen und gleich großen Bindungswinkeln gebildet. Dieses gleichseitige Sechseck ist eine planare Struktur.

3
Reaktionsgleichung für die Zersetzung von Pikrinsäure


 Gefahrenhinweise
Gefahrenhinweise
Begründung der Kennzeichnung
Die Reaktionsgleichung zeigt die Bildung von Wasserdampf, Kohlenstoffmonooxid und Stickstoff. Das sind alles gasförmige Produkte, die sich schlagartig bilden können.
| A: | explosiv / explosionsgefährlich |
| B: | giftig |
4
Versuchsaufbau für die Titration
 Berechnung des prozentualen Masseanteils an Pikrinsäure
Für die Berechnung wird zunächst die Stoffmenge der verbrauchten Maßlösung bestimmt:
Berechnung des prozentualen Masseanteils an Pikrinsäure
Für die Berechnung wird zunächst die Stoffmenge der verbrauchten Maßlösung bestimmt:
![\(\begin{array}[t]{rll}
n(NaOH)&=& c \cdot V& \\[5pt]
&=& 0,010\,\text{mol} \cdot \text{L}^{-1} \cdot 0,014\,\text{L} & \\[5pt]
&=& 0,00014 \,\text{mol} & \\[5pt]
&=& 0,14\,\text{mmol}
\end{array}\)](https://mathjax.schullv.de/631b8a428ad97bb6c753b9a39485c21dfe886ec91dac81ca7680242b2ac85de7?color=5a5a5a) Weiterhin gilt:
Weiterhin gilt:
 Mit der molaren Masse
Mit der molaren Masse  kann nun daraus der Massenanteil bestimmt werden:
kann nun daraus der Massenanteil bestimmt werden:
 Der prozentuale Massenanteil an Pikrinsäure in der wässrigen Pikrinsäure-Lösung beträgt also
Der prozentuale Massenanteil an Pikrinsäure in der wässrigen Pikrinsäure-Lösung beträgt also 
