Aufgabe 4 – Aluminium
Das Metall Aluminium wird in der Automobilindustrie aufgrund seiner geringen Dichte und guten Verformbarkeit (Duktilität) als Werkstoff verwendet. Ebenso wird die Nutzung von Aluminium in Batterien von Elektroautos erprobt.
1
Aluminium wird durch Schmelzflusselektrolyse von Aluminiumoxid gewonnen (Abbildung 1). Hierbei befindet sich - vereinfacht betrachtet - geschmolzenes Aluminiumoxid in einer mit Kohle beschichteten Wanne, in die Kohlestäbe tauchen. Das Aluminiumoxid reagiert während der Elektrolyse zunächst zu Aluminium und elementarem Sauerstoff. Der bei der Elektrolyse entstehende Sauerstoff reagiert in einer Folgereaktion mit dem Kohlenstoff der Kohlestäbe zu Kohlenstoffdioxid.
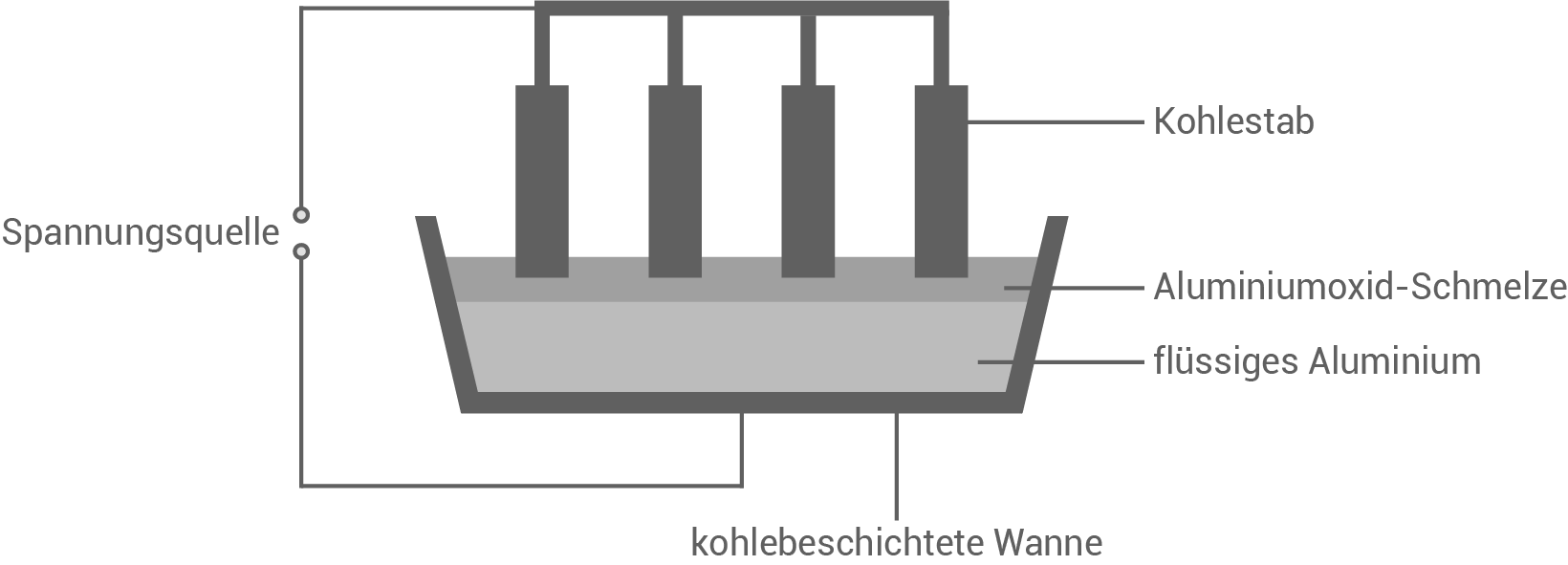

Abbildung 1: Schematische Darstellung der Schmelzflusselektrolyse von Aluminiumoxid
- Stelle die Teilgleichungen für die an den Elektroden ablaufenden Vorgänge auf.
- Ordne den Elektroden die Begriffe Pluspol, Minuspol, Anode, Kathode, Oxidation und Reduktion zu.
- Stelle die Gesamtreaktionsgleichung aus Elektrolyse und Folgereaktion auf.
(9 BE)
2
Manche Metalle lassen sich durch Elektrolyse aus ihren wässrigen Salz-Lösungen herstellen.
- Erkläre, dass die Gewinnung von Aluminium aus einer wässrigen Aluminiumsalz-Lösung durch Elektrolyse unter Standardbedingungen jedoch nicht möglich ist.
(3 BE)
3
Im Automobilbau wird Aluminium vor allem für die tragenden Karosserieteile verwendet. Für den Bau eines Elektroautos werden  Aluminium benötigt.
Aluminium benötigt.
- Berechne die Masse an Aluminiumoxid, die für die Herstellung dieses Elektroautos mindestens benötigt wird.
- Erkläre die Duktilität des Aluminiums mithilfe einer Modellvorstellung.
(8 BE)
4
Aluminium-Luft-Batterien werden in der Forschung als mögliche Energiespeicher für den Antrieb von Elektroautos untersucht. In diesen Batterien dienen Aluminium und Sauerstoff als Ausgangsstoffe.
4.1
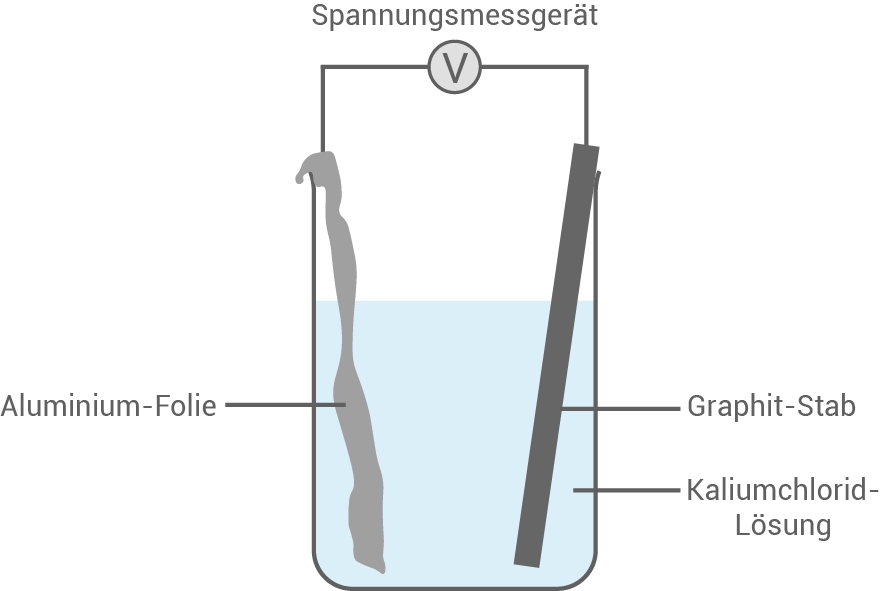
In einem Modellversuch soll die Spannung einer Aluminium-Luft-Batterie gemessen werden. Für den Versuch stehen unter anderem folgende Materialien zur Verfügung: Graphit-Stab, Aluminiumfolie, wässrige Kaliumchlorid-Lösung 
- Zeichne einen beschrifteten Aufbau dieses Modellversuchs.
- Erkläre eine Funktion der Kaliumchlorid-Lösung.
- Stelle die Teilgleichungen für Oxidation und Reduktion sowie die Gesamtgleichung auf, wenn die beiden Elektroden leitend miteinander verbunden sind.
- Berechne die zu erwartende Spannung der Batterie unter Verwendung der Elektrodenpotenziale aus Anlage 3.
(11 BE)
4.2
In einem Internet-Forum sind zur Aluminium-Luft-Batterie folgende Aussagen zu lesen:
I
„Der Ladezustand der Batterie kann durch Wiegen bestimmt werden.“
II
„Die Spannung der Batterie ist größer, wenn die Graphit-Elektrode mit Sauerstoff umspült wird.“
III
„Die Spannung der Batterie ist bei Verwendung von Zink anstelle von Aluminium größer.“
- Beurteile diese Aussagen.
(9 BE)
(40 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Teilgleichungen für die Elektrodenvorgänge
Kathode (kohlebeschichtete Wanne): 

 Anode (Kohlestäbe):
Anode (Kohlestäbe): 

 Zuordnung der Begriffe
Die kohlebeschichtete Wanne stellt die Kathode und damit den Minuspol dar. Hier erfolgt die Reduktion.
An den Kohlestäben erfolgt die Oxidation und stellt demnach die Anode und den Pluspol dar.
Gesamtreaktionsgleichung
Zuordnung der Begriffe
Die kohlebeschichtete Wanne stellt die Kathode und damit den Minuspol dar. Hier erfolgt die Reduktion.
An den Kohlestäben erfolgt die Oxidation und stellt demnach die Anode und den Pluspol dar.
Gesamtreaktionsgleichung
2
Erklärung zur Unmöglichkeit der Aluminiumgewinnung aus wässriger Aluminiumsalz-Lösung
Zur Erklärung werden die Standardelektrodenpotenziale betrachtet und der Wert für die Reduktion von Wasser mit der von  verglichen:
verglichen:
Das Potenzial des Redoxpaares  ist negativer als das des Redoxpaares
ist negativer als das des Redoxpaares  wodurch das Wasser zuerst reduziert werden würde. Somit wäre die Elektrolyse ineffizient und würde nicht bevorzugt Aluminium, sondern Wasserstoffgas produzieren.
wodurch das Wasser zuerst reduziert werden würde. Somit wäre die Elektrolyse ineffizient und würde nicht bevorzugt Aluminium, sondern Wasserstoffgas produzieren.
3
Berechnung der benötigten Aluminiumoxid-Masse
Mit der gegebenen Masse und der molaren Masse von Aluminium wird zunächst berechnet, welche Stoffmenge benötigt wird:
![\(\begin{array}[t]{rll}
n (Al)&=& \dfrac{m}{M}& \\[5pt]
&=& \dfrac{600\,\text{kg}}{27\,\text{g}\cdot\text{mol}^{-1}} & \\[5pt]
&=& \dfrac{600 \ 000\,\text{g}}{27\,\text{g}\cdot\text{mol}^{-1}} & \\[5pt]
&\approx & 22200\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/10cf661f1a1825284f7aa3aeaf60ecd9519ddcad78f26ee913d9b6a04283abbe?color=5a5a5a) Aus der Reaktionsgleichung folgen die Stoffmengenverhältnisse:
Aus der Reaktionsgleichung folgen die Stoffmengenverhältnisse:
 Daraus folgt:
Daraus folgt:
![\(\begin{array}[t]{rll}
m(Al_2O_3)&=& n \cdot M & \\[5pt]
&=& 0,5 \cdot n(Al) \cdot M (Al_2O_3) & \\[5pt]
&\approx& 11100 \,\text{mol} \cdot 102\,\text{g}\cdot\text{mol}^{-1} & \\[5pt]
&\approx& 1132200 \,\text{g} = 1132,200\,\text{kg}
\end{array}\)](https://mathjax.schullv.de/40d749cc72a6e79c413c4376d954124596da4a8d577ba9b3b28830a827c93c9b?color=5a5a5a) Erklärung der Duktilität von Aluminium
Die Duktilität von Aluminium lässt sich durch das Elektronengas-Modell erklären. In Metallen wie Aluminium sind die Außenelektronen der Metall-Atome frei beweglich und nicht fest an einzelne Atomrümpfe gebunden. Stattdessen bilden sie ein sogenanntes Elektronengas, das sich frei zwischen den Atomrümpfen bewegen kann. Verschieben sich die Atomrümpfe durch äußere Einwirkung, kommt es daher nicht zur Abstoßung der positiven Ladungen; die Metallbindung bleibt erhalten.
Erklärung der Duktilität von Aluminium
Die Duktilität von Aluminium lässt sich durch das Elektronengas-Modell erklären. In Metallen wie Aluminium sind die Außenelektronen der Metall-Atome frei beweglich und nicht fest an einzelne Atomrümpfe gebunden. Stattdessen bilden sie ein sogenanntes Elektronengas, das sich frei zwischen den Atomrümpfen bewegen kann. Verschieben sich die Atomrümpfe durch äußere Einwirkung, kommt es daher nicht zur Abstoßung der positiven Ladungen; die Metallbindung bleibt erhalten.
4.1
Beschrifteter Aufbau des Modellversuchs
 Funktion der Kaliumchlorid-Lösung
Die frei beweglichen Ionen in der Kaliumchlorid-Lösung bewirken die elektrische Leitfähigkeit der Lösung. Erst dadurch kann die Reaktion stattfinden. Teilgleichungen und Gesamtgleichung
Berechnung der Spannung
Es gilt:
Funktion der Kaliumchlorid-Lösung
Die frei beweglichen Ionen in der Kaliumchlorid-Lösung bewirken die elektrische Leitfähigkeit der Lösung. Erst dadurch kann die Reaktion stattfinden. Teilgleichungen und Gesamtgleichung
Berechnung der Spannung
Es gilt:
![\(\begin{array}[t]{rll}
U &=& E^0 (OH^-/O_2) - E^0(Al/Al^{3+}) & \\[5pt]
&=& 0,82\,\text{V} - (-1,86\,\text{V}) & \\[5pt]
&=& 2,50\,\text{V}
\end{array}\)](https://mathjax.schullv.de/69aa90f7a80bc78e8b445f157767fe7908f0fa2bcd760ad8d13c1947c3c0ffb0?color=5a5a5a)

4.2
Beurteilung der Aussagen
I
„Der Ladezustand der Batterie kann durch Wiegen bestimmt werden.“
Die Aussage ist korrekt, da beim Entladen der Batterie Sauerstoff aus der Luft aufgenommen wird, was zu einer Zunahme der Batteriemasse führt.
II
„Die Spannung der Batterie ist größer, wenn die Graphit-Elektrode mit Sauerstoff umspült wird.“
Hier bewirkt das Umspülen eine Erhöhung der Sauerstoffkonzentration und somit ein positiveres Potenzial des  -Paares. Die Konzentration des
-Paares. Die Konzentration des  -Paares verändert sich jedoch nicht, wodurch die Gesamtspannung der Batterie größer wird. Die Aussage ist daher korrekt.
-Paares verändert sich jedoch nicht, wodurch die Gesamtspannung der Batterie größer wird. Die Aussage ist daher korrekt.
III
„Die Spannung der Batterie ist bei Verwendung von Zink anstelle von Aluminium größer.“
Diese Aussage ist falsch, da das Elektrodenpotenzial von  positiver als das von
positiver als das von  ist und die Spannung somit geringer.
ist und die Spannung somit geringer.