Aufgabe 2 – Ribose
Ribose  ist eine in der Natur häufig vorkommende Aldopentose. Sie kommt als Baustein in zahlreichen für den Organismus wichtigen, komplexen Verbindungen vor. Beispielhaft sind hier der Energieträger Adenosinmonophosphat (AMP), der sekundäre Botenstoff cAMP (cyclisches AMP) oder auch die Ribonucleinsäure (RNA) zu nennen.
ist eine in der Natur häufig vorkommende Aldopentose. Sie kommt als Baustein in zahlreichen für den Organismus wichtigen, komplexen Verbindungen vor. Beispielhaft sind hier der Energieträger Adenosinmonophosphat (AMP), der sekundäre Botenstoff cAMP (cyclisches AMP) oder auch die Ribonucleinsäure (RNA) zu nennen.
1
Abbildung 1 zeigt eine Strukturformel eines Ribose-Moleküls.
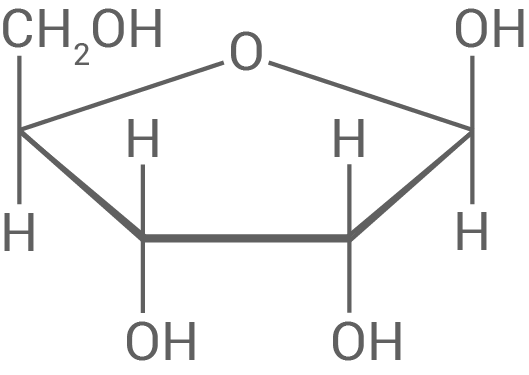

Abbildung 1: Strukturformel eines Ribose-Moleküls
1.1
Das Ribose-Molekül kann in wässriger Lösung als Fünfring, Sechsring oder in offenkettiger Form vorliegen.
- Zeichne die offenkettige Form des Ribose-Moleküls in FISCHER-Projektion und eine Sechsring-Form in HAWORTH-Projektion.
- Erkläre anhand der gezeichneten Strukturen die bei der Benennung von Kohlenhydrat-Molekülen üblichen Bezeichnungen D- und L-Form sowie
- und
-Form.
- Begründe die unterschiedliche Anzahl an asymmetrisch substituierten Kohlenstoff-Atomen in der offenkettigen Form und einer Ringform.
(6 VP)
1.2
Der Zuckergehalt einer wässrigen Ribose-Lösung kann mit einer Fällungsreaktion bestimmt werden. Dabei wird die Lösung mit einer alkalischen,  -lonen enthaltenden Lösung versetzt. Es fällt rotes Kupfer(l)-oxid
-lonen enthaltenden Lösung versetzt. Es fällt rotes Kupfer(l)-oxid  aus. Bei der Reaktion entsteht aus der Aldehydgruppe des Ribose-Moleküls eine Carboxylatgruppe
aus. Bei der Reaktion entsteht aus der Aldehydgruppe des Ribose-Moleküls eine Carboxylatgruppe  .
.
- Stelle eine zugehörige Reaktionsgleichung auf.
- Begründe, dass es sich um eine Redoxreaktion handelt.
- Überprüfe folgende Aussage: „Bei vollständigem Reaktionsumsatz ist die Masse des ausfallenden Kupfer(l)-oxids nahezu identisch mit der Masse der eingesetzten Ribose.“
(5 VP)
2
Adenosinmonophosphat (AMP) und cyclisches Adenosinmonophosphat (cAMP) (siehe Abb. 2) können mit Hilfe der Papierchromatographie getrennt werden. Die Trennung beruht auf unterschiedlich starken Wechselwirkungen zwischen dem Cellulose-Papier und den beiden Substanzen. Dabei treten bei AMP stärkere Wechselwirkungen als bei cAMP auf.
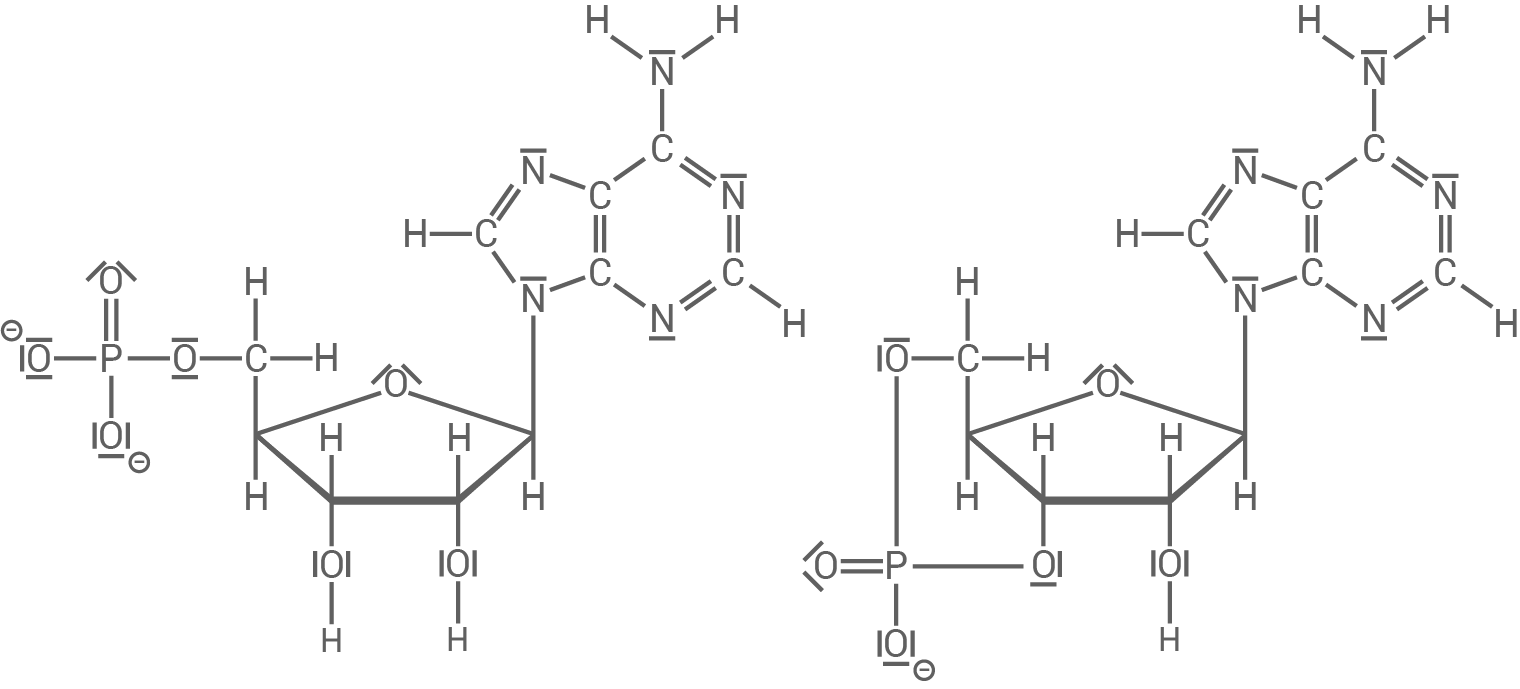

Abbildung 2: Strukturformel eines AMP-Ions (links) und eines cAMP-Ions (rechts)
- Vergleiche die Struktur des AMP-lons mit der des cAMP-lons.
- Erkläre die unterschiedlich starken Wechselwirkungen zwischen Cellulose und AMP bzw. Cellulose und cAMP.
(3 VP)
3
Die RNA spielt eine zentrale Rolle bei der Proteinbiosynthese, dem Prozess zum Aufbau von Proteinen aus Aminosäuren.
Folgende Liste zeigt typische Reste proteinogener Aminosäuren:
Die Funktionalität von Proteinen ist im Wesentlichen durch ihren räumlichen Bau bestimmt. Es lassen sich vier verschiedene Strukturebenen unterscheiden.
Folgende Liste zeigt typische Reste proteinogener Aminosäuren:
| A | |
|---|---|
| B | |
| C | |
| D | |
| E | |
| F | |
| G |
- Beschreibe die charakteristische Wechselwirkung, die die Sekundärstruktur von Proteinen stabilisiert.
- Gib unter Verwendung der oben aufgelisteten Aminosäure-Reste (Mehrfachverwendung ist möglich) drei verschiedene Paare an, die zur Stabilisierung von Tertiär- oder Quartärstrukturen beitragen.
- Benenne die Wechselwirkungen oder Bindungen zwischen den ausgewählten Aminosäureresten.
(6 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Ribose-Molekül
Bezeichnungen bei der Benennung von Kohlenhydrat-Molekülen
Unterschiedliche Anzahl asymmetrisch substituierter  -Atome
Durch die Ringbildung bzw. die Halbacetalbildung sind am
-Atome
Durch die Ringbildung bzw. die Halbacetalbildung sind am  -Atom vier unterschiedliche Substituenten gebunden. Somit sind in der Ringform
-Atom vier unterschiedliche Substituenten gebunden. Somit sind in der Ringform  ,
,  und
und  asymmetrisch substituierte
asymmetrisch substituierte  -Atome.
-Atome.
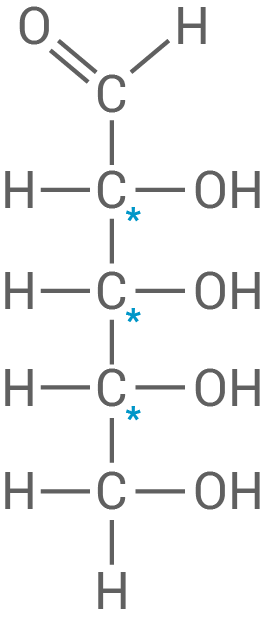
|
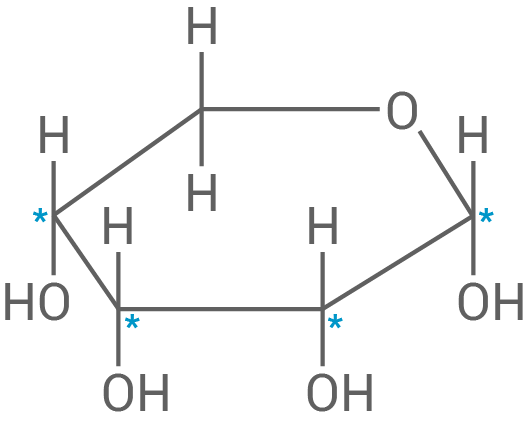
|
|
Fischer-Projektion
|
Haworth-Projektion
|
| D-und L-Form (FISCHER-Projektion): | Steht die |
| Die cyclische (Halbacetal-) Form des D-Ribose-Moleküls, in der die |
1.2
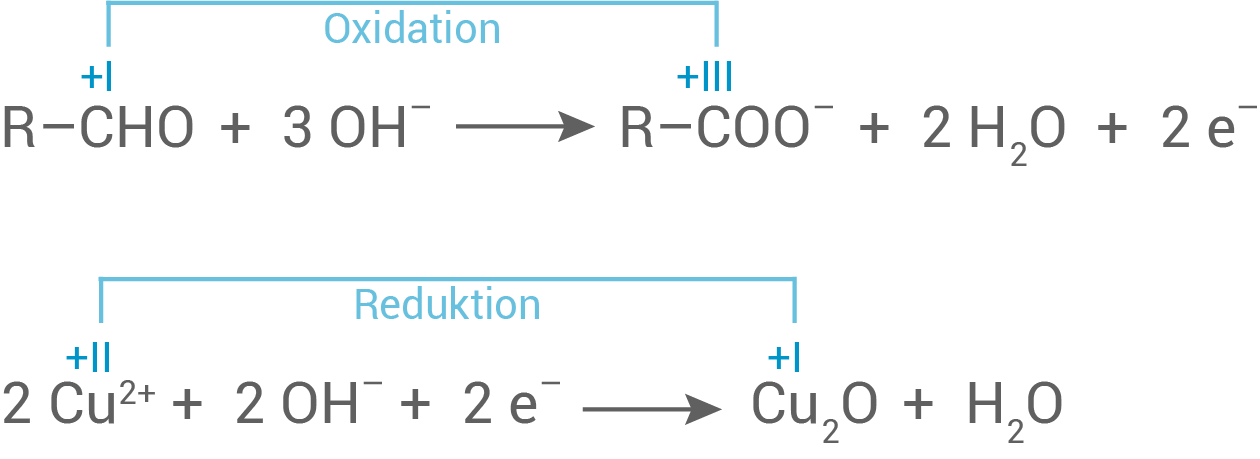
Zugehörige Reaktionsgleichung


 Begründung der Redoxreaktion (über Oxidationszahlen)
Begründung der Redoxreaktion (über Oxidationszahlen)
 Überprüfung der Aussage
Es gilt
Überprüfung der Aussage
Es gilt  (Ribose) =
(Ribose) =  (Kupferoxid), deshalb genügt ein Vergleich der molaren Massen:
(Kupferoxid), deshalb genügt ein Vergleich der molaren Massen:
Die molaren Massen unterscheiden sich um nahezu  und sind damit nicht "nahezu identisch". Die Aussage kann damit nicht bestätigt werden.
und sind damit nicht "nahezu identisch". Die Aussage kann damit nicht bestätigt werden.

2
Vergleich der Struktur des AMP-lons mit der des cAMP-lons
Unterschiedlich starke Wechselwirkungen
Der Ribosebaustein des AMP-Ions besitzt zwei negative Ladungen am Phosphat-Rest und zwei Hydroxy-Gruppen. Dadurch sind die Wechselwirkungen mit den Hydroxy-Gruppen der Cellulose stärker als die des cAMP-Ions mit Cellulose.
| Gemeinsamkeiten |
|
|---|---|
| Unterschiede |
|
3
Proteinbiosynthese
Stabilisierung der Sekundärstruktur von Proteinen:
Zwischen den Peptidgruppen werden Wasserstoffbrücken ausgebildet. Hierbei wechselwirkt das H-Atom einer Peptidbindung mit dem O-Atom einer weiteren. Diese intramolekularen Kräfte stabiisieren die Sekundärstruktur. Aminosäure-Paare, Benennung der Wechselwirkungen: Zwischen zwei Thiol-Gruppen wie in A sind kovalente S-S-Bindungen (Disulfidbrücken) möglich.
In E und F sind hydrophobe Reste vorhanden, die Van-der-Waals-Kräfte ausbilden können.
Bei geladenen Resten, wie in den Seitenketten von C und D, kommt es im Protein zu starken ionischen Wechselwirkungen.
Polaren Seitenketten wie in B und G wechselwirken über Wasserstoffbrückenbindungen.
Zwischen den Peptidgruppen werden Wasserstoffbrücken ausgebildet. Hierbei wechselwirkt das H-Atom einer Peptidbindung mit dem O-Atom einer weiteren. Diese intramolekularen Kräfte stabiisieren die Sekundärstruktur. Aminosäure-Paare, Benennung der Wechselwirkungen: Zwischen zwei Thiol-Gruppen wie in A sind kovalente S-S-Bindungen (Disulfidbrücken) möglich.
In E und F sind hydrophobe Reste vorhanden, die Van-der-Waals-Kräfte ausbilden können.
Bei geladenen Resten, wie in den Seitenketten von C und D, kommt es im Protein zu starken ionischen Wechselwirkungen.
Polaren Seitenketten wie in B und G wechselwirken über Wasserstoffbrückenbindungen.