Aufgabe 5 – Wasserstoff
Jedes Jahr werden weltweit mehr als 600 Milliarden Kubikmeter Wasserstoff für zahllose Anwendungen in Industrie, Technik und Labor gewonnen.
1
Im Labor können kleinere Mengen Wasserstoff gewonnen werden, indem man eine saure Lösung mit einem unedlen Metall wie z.B. Zink umsetzt. Dabei läuft folgende exotherme Reaktion ab:



1.1
In einem Experiment wird Wasserstoff aus Zinkblech und verdünnter Salzsäure hergestellt.
- Beschreibe ein experimentelles Vorgehen, mit dem nachgewiesen werden kann, dass bei diesem Experiment Wasserstoff entsteht.
- Berechne die Masse an Zink, die zur Erzeugung von
Wasserstoff bei Raumbedingungen mindestens eingesetzt werden muss.
Hinweis: Bei Raumbedingungen nimmteines Gases das Volumen
ein.
- Begründe zwei Maßnahmen, durch die die Wasserstoffentwicklung beschleunigt werden könnte.
(6 VP)
1.2
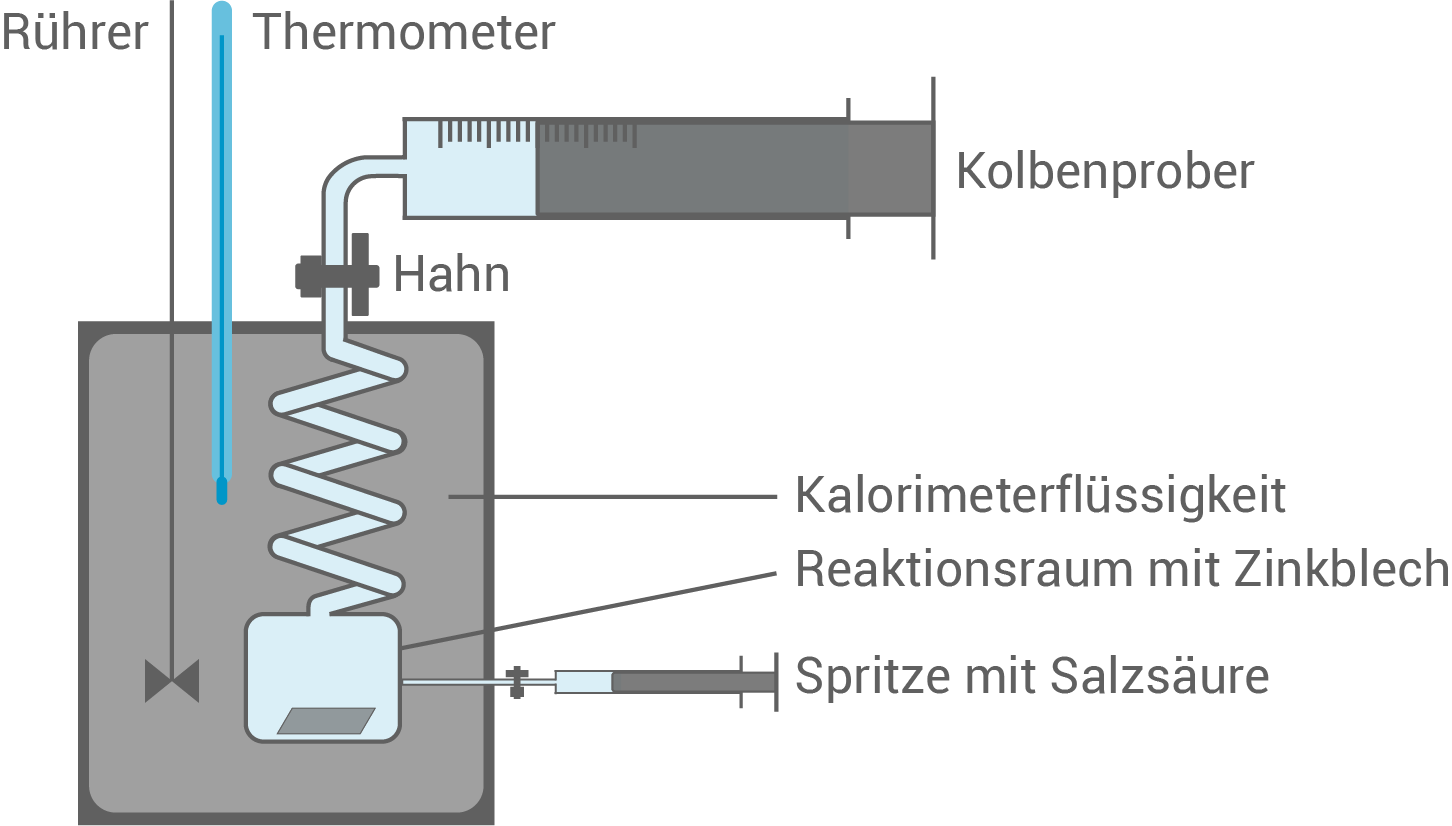
Zur Bestimmung der Reaktionsenthalpie soll diese Reaktion in der in Abbildung 1 dargestellten Versuchsapparatur durchgeführt werden, wobei die Spritze direkt nach der Zugabe von Salzsäure verschlossen wird.
Die Reaktion wird einmal bei geöffnetem Hahn (Fall A) und einmal bei geschlossenem Hahn (Fall B) am Kolbenprober durchgeführt.
Die Reaktion wird einmal bei geöffnetem Hahn (Fall A) und einmal bei geschlossenem Hahn (Fall B) am Kolbenprober durchgeführt.
- Nenne für beide Fälle zu erwartende Beobachtungen, gehe dabei auch auf die Vorgänge im Reaktionsraum ein.
- Begründe, ob die Reaktionsenthalpie über Fall A oder Fall B bestimmt werden muss.

Abbildung 1: Schematische Darstellung der Versuchsapparatur
(4 VP)
1.3
Die Reaktionsenthalpie wird mit Hilfe eines Kalorimeters ermittelt. Das Kalorimeter (Wärmekapazität des Kalorimeters  ) wird dazu mit
) wird dazu mit  Wasser (spez. Wärmekapazität
Wasser (spez. Wärmekapazität  ) befüllt und
) befüllt und  Zink werden vollständig umgesetzt.
Zink werden vollständig umgesetzt.
Die Wassertemperatur wird in regelmäßigen Abständen gemessen. Man erhält die in Tabelle 1 angegebenen Messwerte. Tabelle 1: Temperaturverlauf bei der Reaktion von Zink mit Salzsäure
Die Wassertemperatur wird in regelmäßigen Abständen gemessen. Man erhält die in Tabelle 1 angegebenen Messwerte. Tabelle 1: Temperaturverlauf bei der Reaktion von Zink mit Salzsäure
| Messpunkt | Temperatur ϑ |
|---|---|
- Stelle die Daten aus Tabelle 1 in einem Diagramm dar.
- Berechne die Reaktionsenthalpie für die Reaktion der Stoffmenge
- Ermittle die molare Standardbildungsenthalpie von hydratisierten Zink-Ionen.
(5 VP)
2
Großtechnisch kann Wasserstoff über die sogenannte Dampfreformierung gewonnen werden. Dabei wird in einer endothermen Reaktion Methan mit Wasserdampf an einem Nickelkatalysator zu Kohlenstoffmonooxid und Wasserstoff umgesetzt.
- Stelle eine Reaktionsgleichung für diesen Prozess auf.
- Begründe das Vorzeichen der Reaktionsentropie.
- Erläutere die Funktion des Katalysators mit Hilfe eines Enthalpiediagramms.
(5 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Experimentelles Vorgehen
Wasserstoff kann mit der Knallgasprobe nachgewiesen werden:
Das entstandene Gas wird aufgefangen (z.B. mit einem Reagenzglas) und an eine offene Flamme gehalten
 Ein Zünden zeigt Wasserstoff an.
Berechnung der Masse an Zink
Mit dem Hinweis kann zunächst die Stoffmenge berechnet werden:
Ein Zünden zeigt Wasserstoff an.
Berechnung der Masse an Zink
Mit dem Hinweis kann zunächst die Stoffmenge berechnet werden:




![\(\begin{array}{rcl}
24\,\text{L} & \mathrel{\widehat{=}}& 1\,\text{mol}\\[5pt]
1\,\text{L}& \mathrel{\widehat{=}}& 0,042\,\text{mol} \\[5pt]
0,1\,\text{L} & \mathrel{\widehat{=}}& 0,0042\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/e5fe428be1ba503ff37ee82623d0e3a47ea1d43cc2ee6298784dd1f1735b2f58?color=5a5a5a)



 Weiterhin gilt:
Weiterhin gilt:
 Daraus folgt die Masse:
Daraus folgt die Masse:
![\(\begin{array}[t]{rll}
m (Zn)&=& n \cdot M & \\[5pt]
&=& 0,0042\,\text{mol} \cdot 65 \,\text{g}\cdot \text{mol}^{-1} & \\[5pt]
&=& 0,27 \,\text{g}
\end{array}\)](https://mathjax.schullv.de/a30ab45e5b73a99605aab8d14c612048a101100276cbf0581588d01cda1b36c3?color=5a5a5a) Es müssen mindestens
Es müssen mindestens  Zink eingesetzt, um
Zink eingesetzt, um  Wasserstoff zu erzeugen.
Maßnahmen zur Beschleunigung der Wasserstoffentwicklung
Wasserstoff zu erzeugen.
Maßnahmen zur Beschleunigung der Wasserstoffentwicklung
Das entstandene Gas wird aufgefangen (z.B. mit einem Reagenzglas) und an eine offene Flamme gehalten
- Verwendung von Zinkpulver: Erhöhung des Zerteilungsgrad von Zink
- Erhöhung der Salzsäurekonzentration: Erhöhung der Anzahl an potenziellen Reaktionspartnern
1.2
Beobachtungen
Bestimmung der Reaktionsenthalpie
Die Reaktionsenthalpie erfolgt über Fall A, da der Druck konstant bleiben muss.
| Im Reaktionsraum: | Gasentwicklung, Abbau des Zinkblechs |
| Fall A: | Stempel des Kolbenprobers wird herausgedrückt, Temperatursteigung |
| Fall B: | Temperatursteigung |
1.3
Diagramm zu Tabelle 1
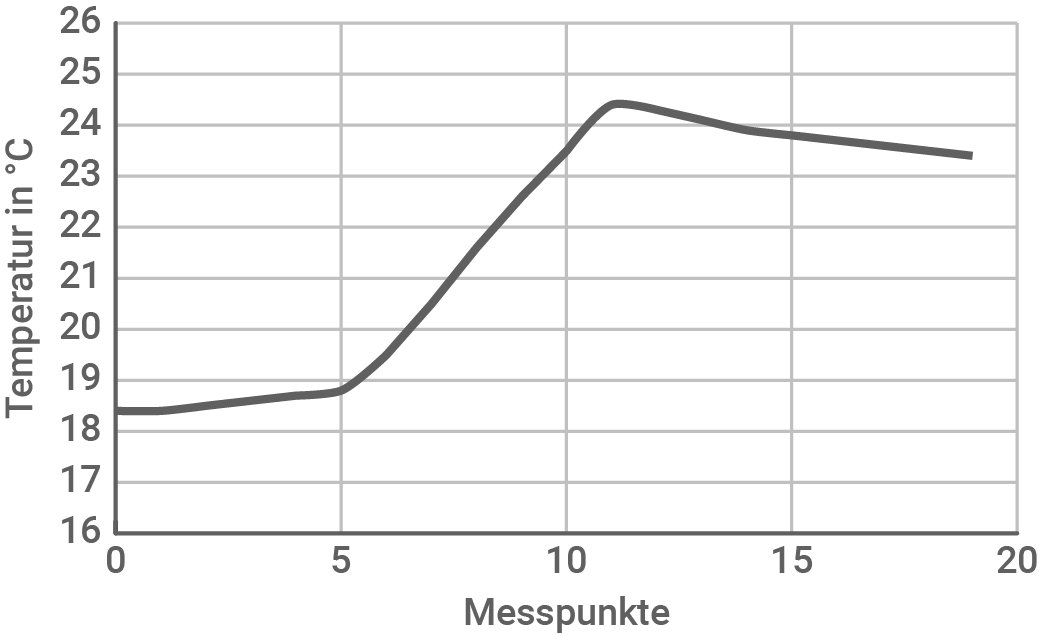 Berechnung der Reaktionsenthalpie
Aus dem Diagramm kann durch Extrapolation die Temperaturdifferenz ermittelt werden:
Berechnung der Reaktionsenthalpie
Aus dem Diagramm kann durch Extrapolation die Temperaturdifferenz ermittelt werden:
 Daraus folgt:
Dies gilt jedoch nur für:
Daraus folgt:
Dies gilt jedoch nur für:
 Für
Für  Zink ergibt sich:
Zink ergibt sich:




![\(\begin{array}{rcl}
0,076\,\text{mol}& \mathrel{\widehat{=}}& 11700 \,\text{J} \\[5pt]
0,001\,\text{mol}& \mathrel{\widehat{=}}& 153,9\,\text{J} \\[5pt]
1 \,\text{mol}& \mathrel{\widehat{=}}& 153,9\,\text{kJ}
\end{array}\)](https://mathjax.schullv.de/4763d03cdc63177a8715e2a0b9ad159af7493df3241795fd355695daacc08e02?color=5a5a5a)



 Die Reaktionsenthalpie für die gegebene Zinkstoffmenge beträgt ca.
Die Reaktionsenthalpie für die gegebene Zinkstoffmenge beträgt ca.  Das Vorzeichen ist negativ, da es sich um eine exotherme Reaktion handelt.
Ermittlung der molaren Standardbildungsenthalpie von hydratisierten Zink-Ionen
Aus der Reaktionsgleichung ergibt sich:
Das Vorzeichen ist negativ, da es sich um eine exotherme Reaktion handelt.
Ermittlung der molaren Standardbildungsenthalpie von hydratisierten Zink-Ionen
Aus der Reaktionsgleichung ergibt sich:
![\(\begin{array}[t]{rll}
n(Zn^{2+}\,_\text{(aq)})&=& n(Zn)& \\[5pt]
\Delta_fH_m^0 (Zn^{2+}\,_\text{(aq)})&\approx& -153,9\,\text{kJ}
\end{array}\)](https://mathjax.schullv.de/166529d5c70708679672f8da19a59d8cace612d555f5d9f1ffa1417c314e53fa?color=5a5a5a) Damit beträgt die molare Standardbildungsenthalpie von hydratisierten Zink-Ionen ebenfalls ca.
Damit beträgt die molare Standardbildungsenthalpie von hydratisierten Zink-Ionen ebenfalls ca. 

2
Reaktionsgleichung für den Prozess


 Begründung des Entropievorzeichens
Die Entropie beschreibt den Grad der 'Unordnung' in einem chemischen System. Da in diesem Prozess nur gasförmige Stoffe beteiligt sind, können die Stoffmengen direkt verglichen werden.
Begründung des Entropievorzeichens
Die Entropie beschreibt den Grad der 'Unordnung' in einem chemischen System. Da in diesem Prozess nur gasförmige Stoffe beteiligt sind, können die Stoffmengen direkt verglichen werden.
Auf der Eduktseite befinden sich , auf der Produktseite
, auf der Produktseite  d.h. die Anzahl der Teilchen nimmt zu und es wird 'ungeordneter'.
d.h. die Anzahl der Teilchen nimmt zu und es wird 'ungeordneter'.
Die Entropie nimmt folglich auch zu und besitzt ein positives Vorzeichen: Funktion des Katalysators
Funktion des Katalysators
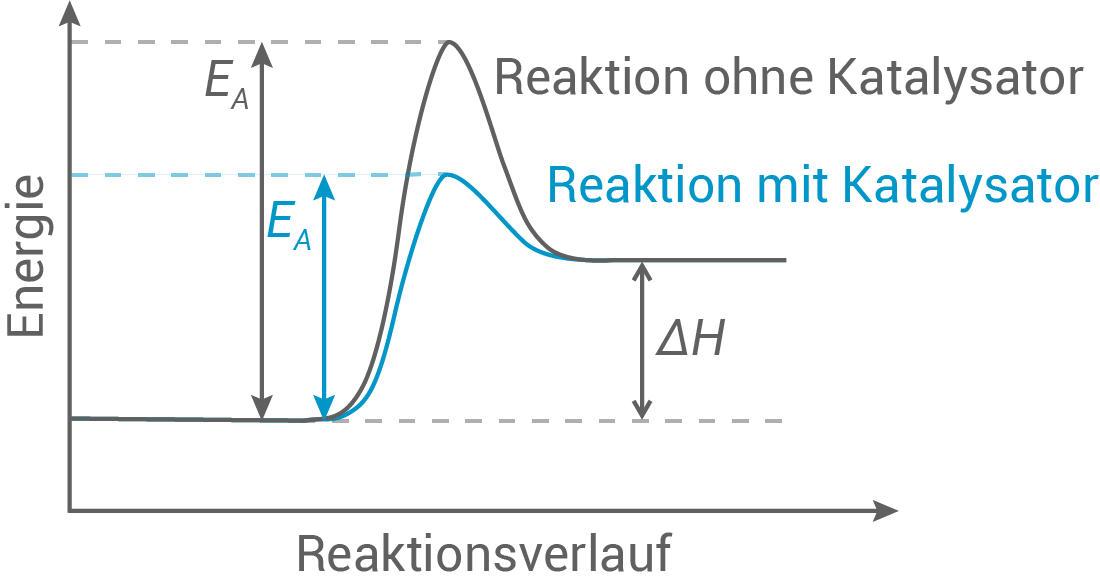 Aus Diagramm ergibt sich, dass ein Katalysator eingesetzt wird, um die Aktivierungsenergie abzusenken.
Aus Diagramm ergibt sich, dass ein Katalysator eingesetzt wird, um die Aktivierungsenergie abzusenken.
Auf der Eduktseite befinden sich
Die Entropie nimmt folglich auch zu und besitzt ein positives Vorzeichen:
