Aufgabe 2 – Gifte
Stoffe, die schädigend auf Organismen wirken, werden als Gifte bezeichnet. Zahlreiche anorganische und organische Verbindungen wirken als Gift. Die Giftwirkung beruht im Allgemeinen auf der Störung von Stoffwechselprozessen. Störungen können zum Beispiel durch Digitoxin (Abb. 1a) und Apamin (Abb. 1b) ausgelöst werden.
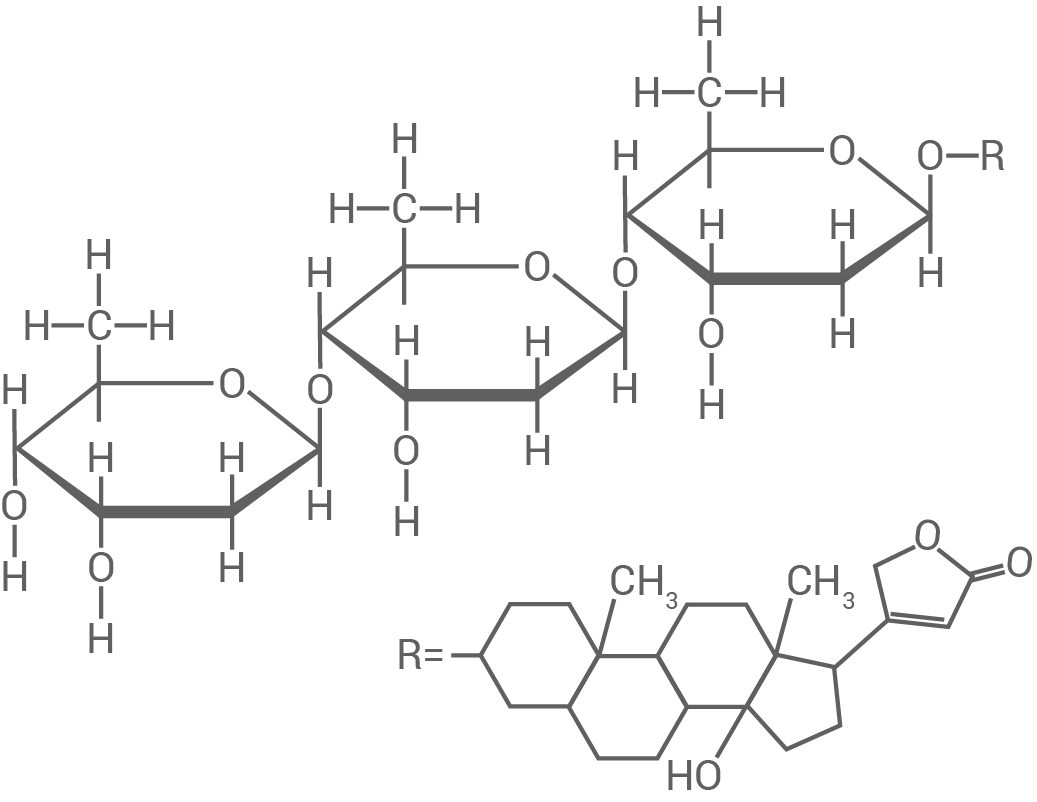
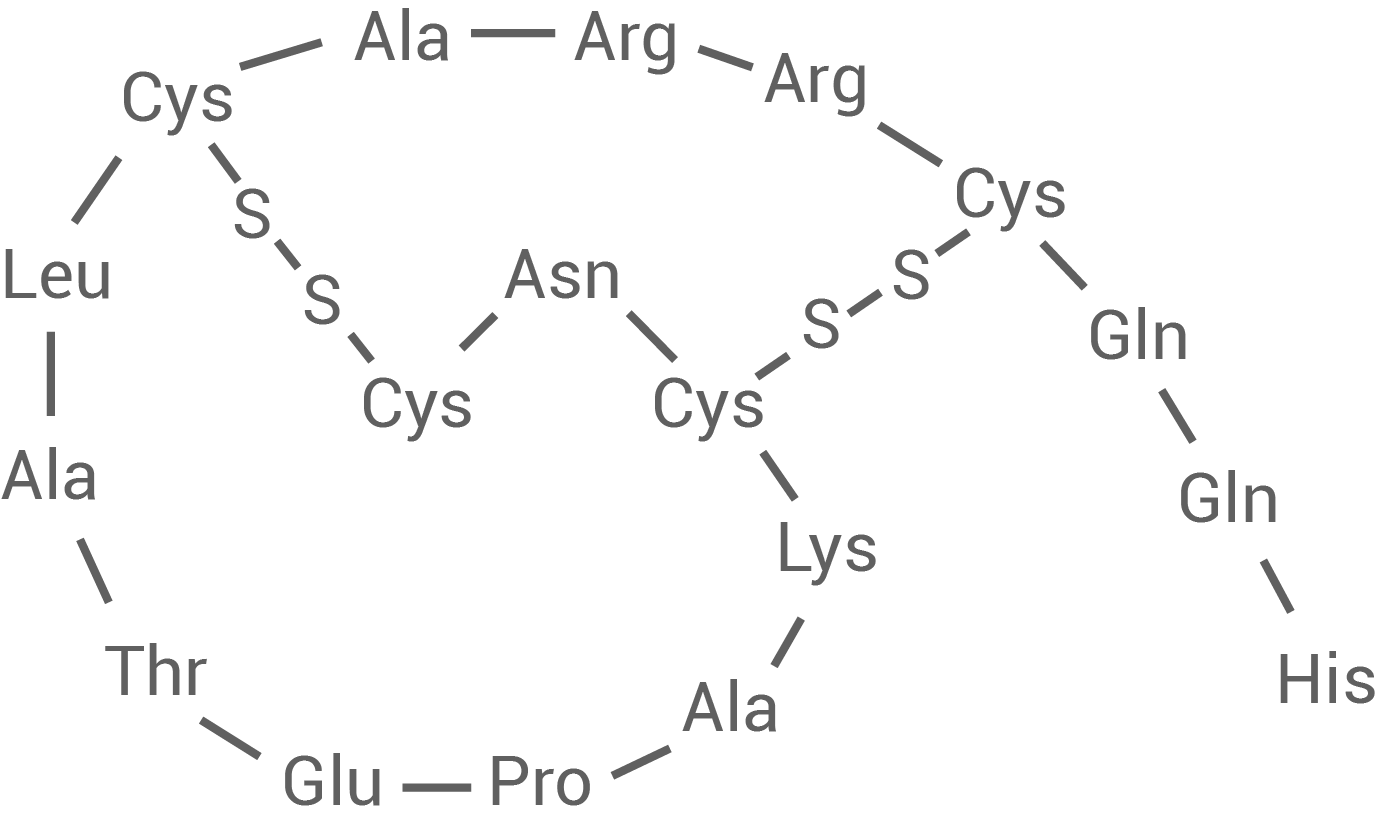

Abbildung 1a: Vereinfachte Strukturformel des Digitoxin-Moleküls

Abbildung 1b: Vereinfachte Struktur des Apamin-Moleküls
1
Digitoxin kommt in den Blättern des Roten Fingerhutes vor und beeinflusst die Herzmuskelkontraktion. Es ist ein sogenanntes Glycosid, dessen Moleküle aus drei identischen Monosaccharid-Bausteinen und einem Steroid-Baustein aufgebaut sind.
- Zeichne ein D-Glucose-Molekül und einen Monosaccharid-Baustein des Digitoxin-Moleküls in der FISCHER-Projektion und kennzeichnen Sie jeweils die asymmetrischen Kohlenstoff-Atome.
- Vergleiche die beiden Strukturen.
- Benenne die glycosidische Bindung zwischen zwei Monosaccharid-Bausteinen im Digitoxin-Molekül eindeutig.
- Beschreibe die experimentelle Durchführung und die zu erwartende Beobachtung der TOLLENS-Probe mit dem Monosaccharid aus Digitoxin.
(7 VP)
2
Apamin ist der Bienengiftbestandteil mit der höchsten Toxizität. Sein Anteil im Bienengift beträgt 
- Gib drei Informationen über den Aufbau eines Apamin-Moleküls an, die aus Abbildung 1 b abgeleitet werden können.
- Zeichne unter Verwendung von Tabelle 1 einen Strukturformelausschnitt des Apamin-Moleküls, der drei Aminosäuren umfasst, und kennzeichnen Sie das verknüpfende Strukturelement. Hinweis: Histidin bildet das N-terminale Ende.
- Erkläre das Prinzip einer Kondensationsreaktion am Beispiel der Verknüpfung zweier Aminosäuren.
(6 VP)
3
Mellitin ist mit  der Hauptbestandteil des Bienengifts. Abbildung 2 a veranschaulicht die Struktur eines Mellitin-Moleküls, in dessen Primärstruktur die Aminosäure Prolin vorkommt. Aufgrund seines Einflusses auf die Struktur eines Peptids wird Prolin als „Helixbrecher“ bezeichnet.
der Hauptbestandteil des Bienengifts. Abbildung 2 a veranschaulicht die Struktur eines Mellitin-Moleküls, in dessen Primärstruktur die Aminosäure Prolin vorkommt. Aufgrund seines Einflusses auf die Struktur eines Peptids wird Prolin als „Helixbrecher“ bezeichnet.
|
|
|
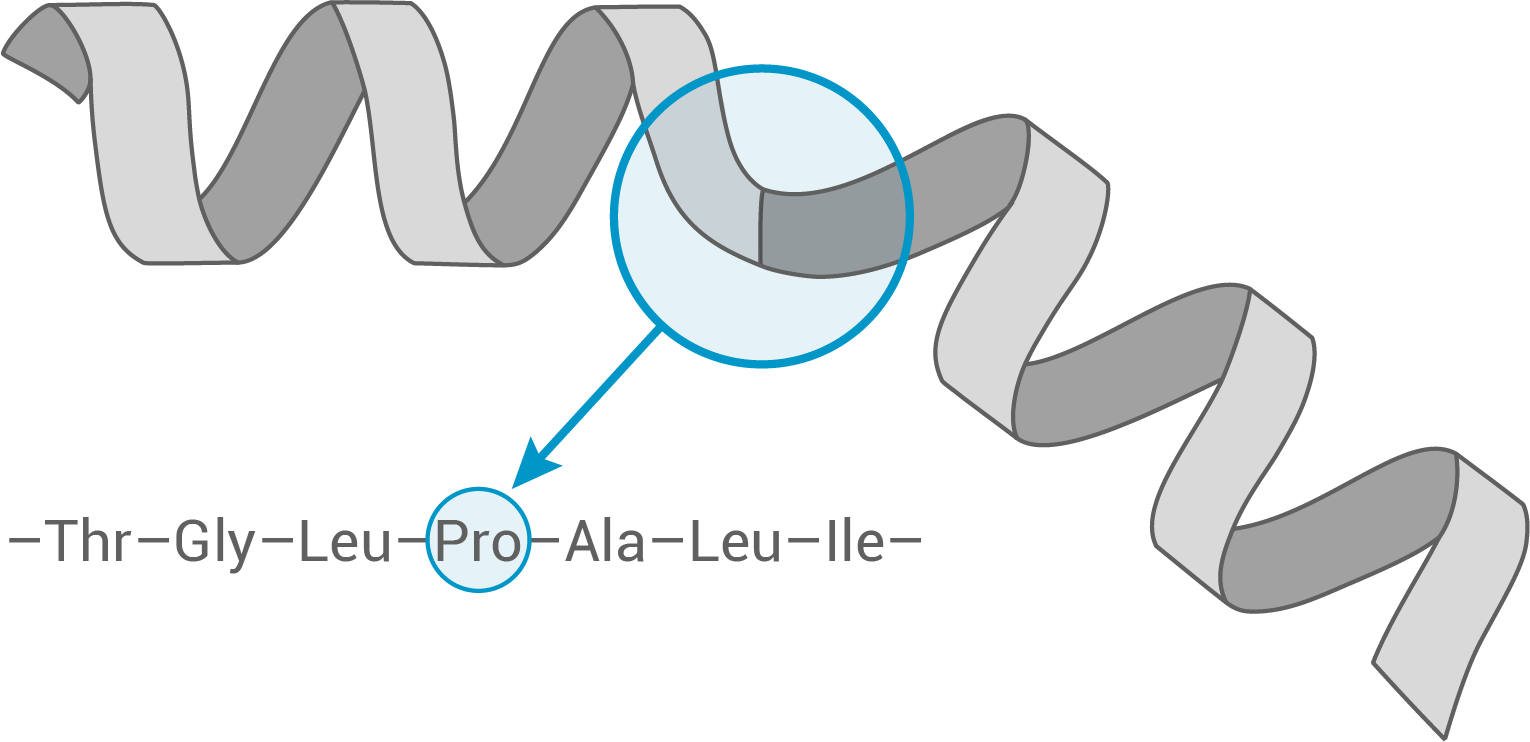
Abbildung 2a: Dreidimensionale Darstellung eines Mellitin-Moleküls
|
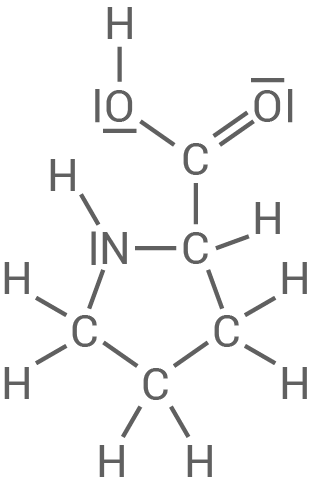
Abbildung 2b: Strukturformel des Prolin-Moleküls
|
- Beschreibe die Stabilisierung der
-Helixstruktur im Mellitin-Molekül.
- Erkläre anhand von Abbildung 2 a den Begriff „Helixbrecher“.
- Gib eine mögliche Erklärung für die Wirkung des Prolin-Moleküls (Abb. 2 b) als „Helixbrecher“.
(5 VP)
4
Um die Giftwirkung von Bienengift zu lindern kann bite away ein elektronisches Gerät in Form eines Stiftes, angewendet werden. Der Hersteller gibt zur Anwendung u. a. folgende Hinweise:
ein elektronisches Gerät in Form eines Stiftes, angewendet werden. Der Hersteller gibt zur Anwendung u. a. folgende Hinweise:
„bite away wird mit der keramischen Kontaktfläche auf dem Stich oder Biss platziert und leicht angedrückt. Anschließend wählt man zwischen den beiden Behandlungszeiten:
wird mit der keramischen Kontaktfläche auf dem Stich oder Biss platziert und leicht angedrückt. Anschließend wählt man zwischen den beiden Behandlungszeiten:
 Sobald diese Temperatur erreicht ist, leuchtet eine LED auf. Sie erlischt, nachdem sich das Gerät nach der gewählten Anwendungsdauer automatisch abschaltet."
Sobald diese Temperatur erreicht ist, leuchtet eine LED auf. Sie erlischt, nachdem sich das Gerät nach der gewählten Anwendungsdauer automatisch abschaltet."
- 3 Sekunden (linker Schalter) bei Erstanwendung und für empfindliche Personen
- 6 Sekunden (rechter Schalter) für eine reguläre Anwendung
bite away : Gebrauchsanweisung, RIEMSER Pharma GmbH (2017)
: Gebrauchsanweisung, RIEMSER Pharma GmbH (2017)
- Erkläre die lindernde Wirkungsweise des Medizinprodukts bite away
(2 VP)
(20 VP)
1
Molekül und Monosaccharid-Baustein
 asymmetrische Kohlenstoff-Atome
Vergleich der beiden Strukturen
asymmetrische Kohlenstoff-Atome
Vergleich der beiden Strukturen
Glycosidische Bindung im Digitoxin-Molekül
Die  -Gruppen an
-Gruppen an  der Zuckerbausteine liegen jeweils oberhalb der Ringebene (vgl. Abbildung). Zwei Monosaccharid-Bausteine sind jeweils über
der Zuckerbausteine liegen jeweils oberhalb der Ringebene (vgl. Abbildung). Zwei Monosaccharid-Bausteine sind jeweils über  und
und  und damit
und damit  -1,4-glycosidisch verknüpft.
TOLLENS-Probe mit dem Monosaccharid-Baustein
Bei der Tollens-Reaktion wird eine Silbernitrat-Lösung mit konzentrierter Ammoniak-Lösung versetzt. Dabei bildet sich ein Niederschlag, der sich bei weiterer Versetzung wieder "auflöst". Das Tollens-Reagenz wird mit einer geringen Menge des gelösten Monosaccharids vermischt und anschließend erhitzt (Wasserbad/Gasbrenner). Bildet sich ein braunschwarzer Niederschlag von kolloidalem Silber bzw. ein Silberspiegel ist der Nachweis für ein reduzierendes Monosaccharid positiv.
Die Tollens-Probe verläuft für das Digitoxin-Monosaccharid positiv, da sich der Pyranose-Ring im Alkalischen öffnet und die dann freiliegende Aldehydgruppe oxidiert werden kann.
-1,4-glycosidisch verknüpft.
TOLLENS-Probe mit dem Monosaccharid-Baustein
Bei der Tollens-Reaktion wird eine Silbernitrat-Lösung mit konzentrierter Ammoniak-Lösung versetzt. Dabei bildet sich ein Niederschlag, der sich bei weiterer Versetzung wieder "auflöst". Das Tollens-Reagenz wird mit einer geringen Menge des gelösten Monosaccharids vermischt und anschließend erhitzt (Wasserbad/Gasbrenner). Bildet sich ein braunschwarzer Niederschlag von kolloidalem Silber bzw. ein Silberspiegel ist der Nachweis für ein reduzierendes Monosaccharid positiv.
Die Tollens-Probe verläuft für das Digitoxin-Monosaccharid positiv, da sich der Pyranose-Ring im Alkalischen öffnet und die dann freiliegende Aldehydgruppe oxidiert werden kann.

|

|
|
D-Glucose
|
Monosaccharid-Baustein von Digitoxin (=Digitoxose)
|
| D-Glucose | Digitoxose |
|---|---|
|
|
|
|
2
Aufbau eines Apamin-Moleküls
Apamin besitzt elf verschiedene Aminosäuren und insgesamt  wodurch es sich um einen Oligopeptid handelt. Weiterhin sind der Abbildung zwei Disulfid-Brücken zu entnehmen und die Primärstruktur (AS-Sequenz) kann abgelesen werden.
Mögliche Strukturformelausschnitte des Apamin-Moleküls
wodurch es sich um einen Oligopeptid handelt. Weiterhin sind der Abbildung zwei Disulfid-Brücken zu entnehmen und die Primärstruktur (AS-Sequenz) kann abgelesen werden.
Mögliche Strukturformelausschnitte des Apamin-Moleküls

 Prinzip einer Kondensationsreaktion
Bei der Verknüpfung zweier Aminosäuren in einer Kondensationsreaktion, wird unter Abspaltung von Wasser ein Peptid gebildet. Durch die Reaktion einer Aminogruppe und einer Säuregruppe wird eine Säureamidbindung, also eine Peptidbindung gebildet.
Verknüpfung Beispiel von Alanin (nicht verlangt):
Prinzip einer Kondensationsreaktion
Bei der Verknüpfung zweier Aminosäuren in einer Kondensationsreaktion, wird unter Abspaltung von Wasser ein Peptid gebildet. Durch die Reaktion einer Aminogruppe und einer Säuregruppe wird eine Säureamidbindung, also eine Peptidbindung gebildet.
Verknüpfung Beispiel von Alanin (nicht verlangt):


Leu – Ala – Thr

Ala – Thr – Glu

3
Stabilisierung der  -Helixstruktur im Mellitin-Molekül
In Peptiden oder Proteinen sind
-Helixstruktur im Mellitin-Molekül
In Peptiden oder Proteinen sind  -Helices Sekundärstrukturelemente, bei denen die Aminosäure-Kette als rechtsgängige Helix angeordnet ist (ca.
-Helices Sekundärstrukturelemente, bei denen die Aminosäure-Kette als rechtsgängige Helix angeordnet ist (ca.  AS pro Windung). Die Stabilisierung erfolgt über Wasserstoffbrückenbindungen, die sich zwischen den übereinander liegenden Peptidbindungen ausbilden.
AS pro Windung). Die Stabilisierung erfolgt über Wasserstoffbrückenbindungen, die sich zwischen den übereinander liegenden Peptidbindungen ausbilden.
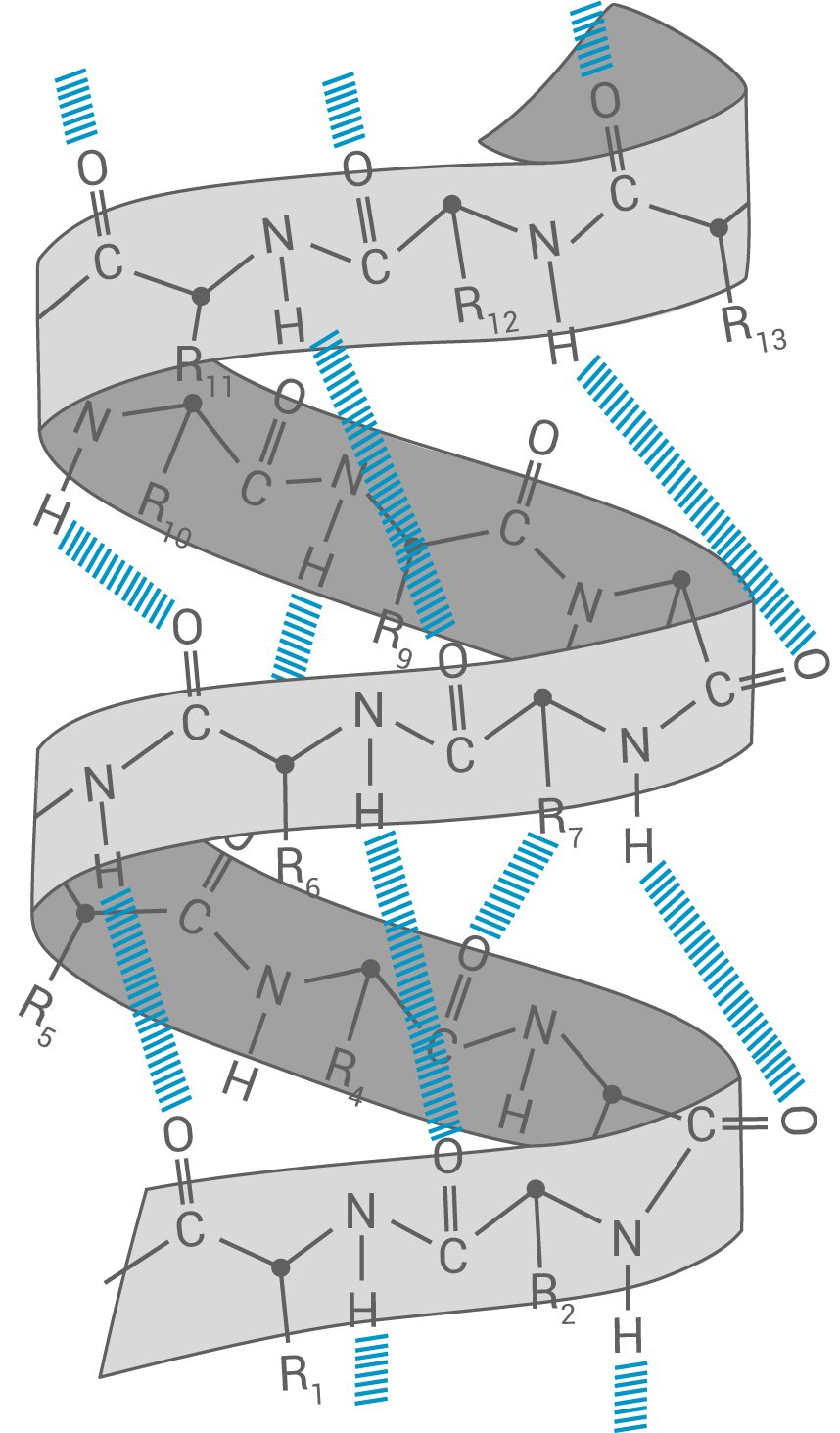 Erklärung des Begriffs „Helixbrecher“
Die Abbildung zeigt eine Unterbrechung der Helix-Struktur an der Postiton des Prolins. Hier ist die Aminosäure-Kette nicht aufgewunden.
Wirkung des Prolin-Moleküls als „Helixbrecher“
Die Atome -
Erklärung des Begriffs „Helixbrecher“
Die Abbildung zeigt eine Unterbrechung der Helix-Struktur an der Postiton des Prolins. Hier ist die Aminosäure-Kette nicht aufgewunden.
Wirkung des Prolin-Moleküls als „Helixbrecher“
Die Atome - - liegen in einer Ebene, da die Peptidbindung planar ist. Um die Bindungen zwischen den
- liegen in einer Ebene, da die Peptidbindung planar ist. Um die Bindungen zwischen den  -
- -Atomen und den
-Atomen und den  -Atomen der Peptidbindungen bzw. zwischen den
-Atomen der Peptidbindungen bzw. zwischen den  -
- -Atomen und den
-Atomen und den  -Atomen der Peptidbindungen kann eine Rotation um einen bestimmen Winkel
-Atomen der Peptidbindungen kann eine Rotation um einen bestimmen Winkel  bzw.
bzw.  stattfinden. Da die Aminogruppe des Prolins Bestandteil eines Fünfringes ist, ist der Winkel
stattfinden. Da die Aminogruppe des Prolins Bestandteil eines Fünfringes ist, ist der Winkel  an der Stelle stark eingeschränkt. An dieser Stelle können außerdem keine Wasserstoffbrückenbindungen gebildet werden. Die eingeschränkte Rotationsmöglichkeit und fehlende Wasserstoffbrückenbindungen führen zu einer Unterbrechung der Helix-Struktur.
an der Stelle stark eingeschränkt. An dieser Stelle können außerdem keine Wasserstoffbrückenbindungen gebildet werden. Die eingeschränkte Rotationsmöglichkeit und fehlende Wasserstoffbrückenbindungen führen zu einer Unterbrechung der Helix-Struktur.
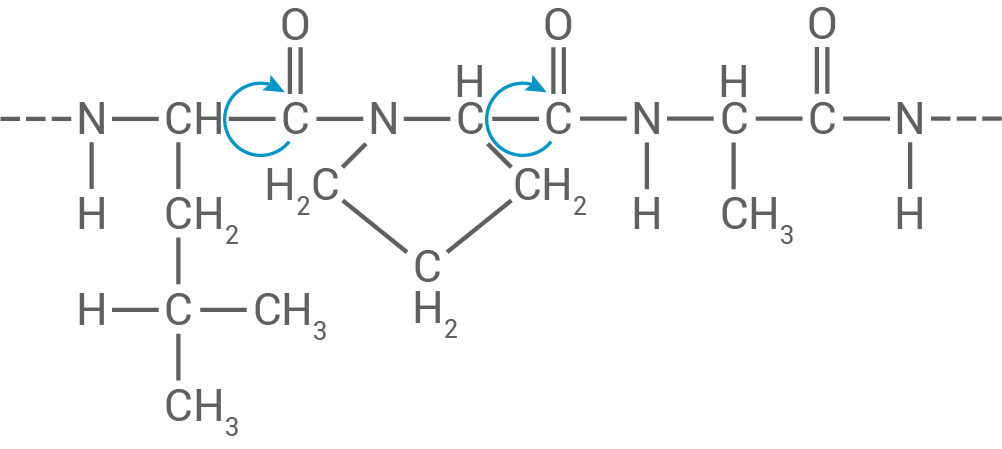
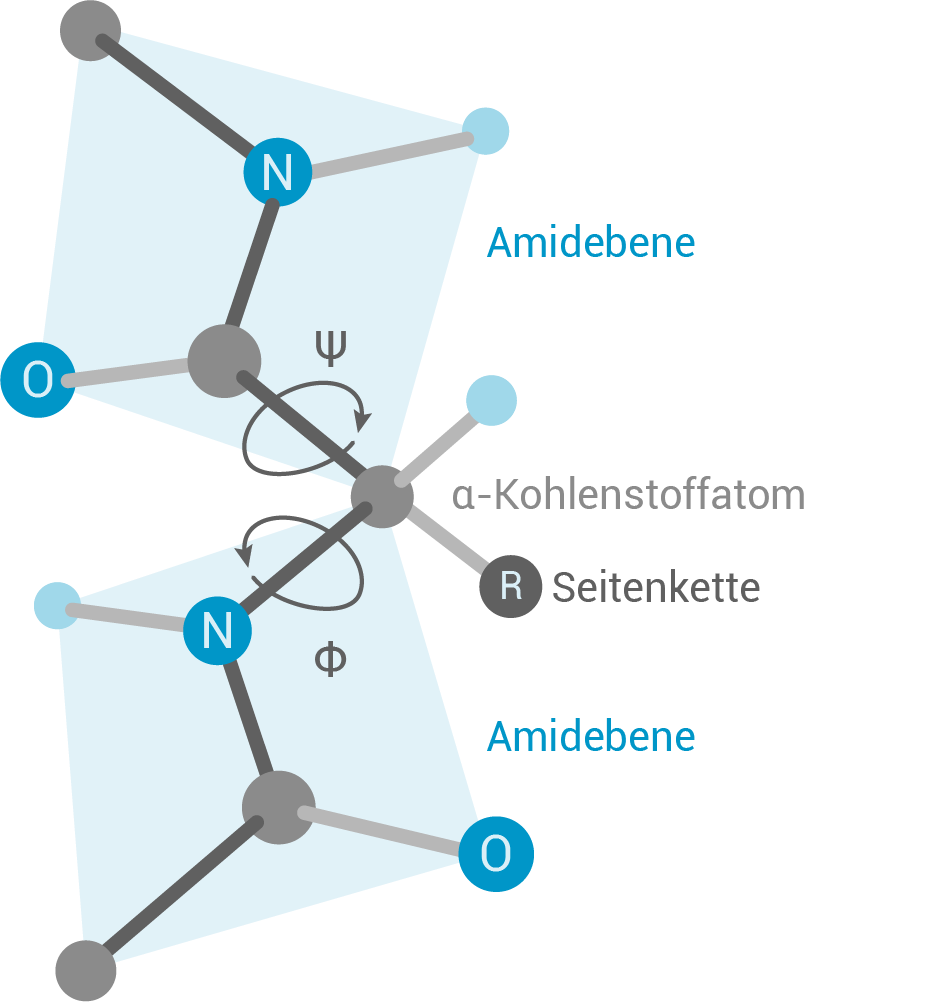

(nicht verlangt)


(nicht verlangt)
4
Wirkungsweise von bite away Bei der Anwendung wird die Stich-/ Bissstelle erhitzt, wobei die zugeführte Wärme eine lokale Anregung der Moleküle bewirkt. Dadurch werden stabilisierende Wechselwirkungen (Wasserstoffbrückenbindungen) an dieser Stelle aufgebrochen und die Proteine und Peptide verändern ihre dreidimensionale Struktur.
Bei der Anwendung wird die Stich-/ Bissstelle erhitzt, wobei die zugeführte Wärme eine lokale Anregung der Moleküle bewirkt. Dadurch werden stabilisierende Wechselwirkungen (Wasserstoffbrückenbindungen) an dieser Stelle aufgebrochen und die Proteine und Peptide verändern ihre dreidimensionale Struktur.
Ist die Wärmemenge groß genug, kommt es zu einer irreversiblen Hitzedenaturierung. Die Konformationsänderungen können die Giftwirkung mindern und dabei kann die physiologische Reaktion auf den Stich, durch Veränderung der Proteine in der Haut, weniger stark ausfallen.
Ist die Wärmemenge groß genug, kommt es zu einer irreversiblen Hitzedenaturierung. Die Konformationsänderungen können die Giftwirkung mindern und dabei kann die physiologische Reaktion auf den Stich, durch Veränderung der Proteine in der Haut, weniger stark ausfallen.