Aufgabe 3 – Kunststoffe im Tischtennis
Der Tischtennissport ist ohne den Einsatz von Kunststoffen heutzutage nicht mehr denkbar. Bei der Herstellung der Tischtennisschläger, Bälle, Netze und bei der Beschichtung der Tischtennisplatte werden Kunststoffe eingesetzt.
1
Die Beschichtung einer Tischtennisplatte erfolgt häufig in zwei Schritten.
1.1
In Schritt 1 wird ein Polyester aus Butendisäure und Ethan-1,2-diol hergestellt.
- Stelle eine vollständige Reaktionsgleichung zur Herstellung des Polyesters unter Verwendung der entsprechenden Strukturformeln mit allen bindenden und nichtbindenden Elektronenpaaren auf.
(3 VP)
1.2
In Schritt 2 wird dieser Polyester durch Zugabe von Styrol (Phenylethen) gehärtet.
- Zeichne einen möglichen Strukturformelausschnitt des auf diese Weise gehärteten Polyesters.
- Erkläre die zu erwartenden unterschiedlichen thermischen Eigenschaften des ungehärteten und des gehärteten Polyesters.
(4 VP)
2.1
Für das Tischtennisspiel im Outdoor-Bereich werden häufig Tischtennisnetze verwendet, die aus Polyethen (PE) bestehen. PE kann durch radikalische Polymerisation gewonnen werden.
- Formuliere den vollständigen Reaktionsmechanismus für die Herstellung von Polyethen unter Verwendung von Strukturformeln.
- Beschreibe die Wirkungsweise der Radikale bei den einzelnen Reaktionsschritten.
(4 VP)
2.2
Polyethen wird meist aus Mineralölprodukten hergestellt. Inzwischen ist es jedoch auch möglich, bei der PE-Synthese von nachwachsenden Rohstoffen auszugehen. Dafür wird zunächst Zucker zu Ethanol vergoren, welches anschließend unter Abspaltung von Wasser zu gasförmigem Ethen umgesetzt wird.
- Stelle eine Reaktionsgleichung für die Umsetzung von Ethanol zu Ethen unter Verwendung von Strukturformeln mit allen bindenden und nichtbindenden Elektronenpaaren auf.
- Beschreibe die Durchführung und die Beobachtung eines Experiments zum Nachweis der
-
-Doppelbindung.
(3 VP)
3.1
Seit 2017 werden Tischtennisbälle aus dem Kunststoff ABS hergestellt. Dieser wird aus den Monomeren Acrylnitril, Buta-1,3-dien und Styrol (Phenylethen) synthetisiert.
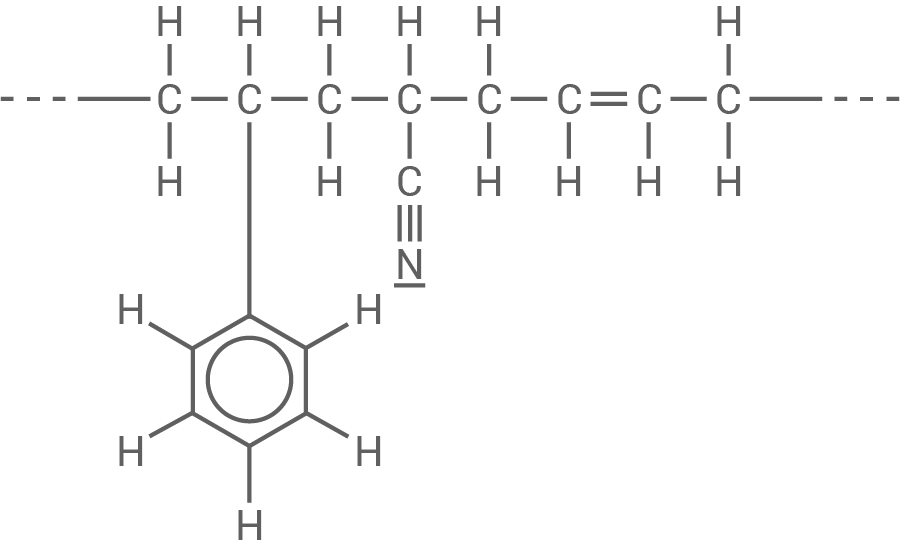

Abbildung 1: Strukturformelausschnitt aus einem ABS-Molekül
- Gib die Strukturformeln der Monomere von
an.
- Ordne die im Text genannten Namen der Monomere den jeweiligen Strukturformeln zu.
(3 VP)
3.2
In einer Werkhalle  lang,
lang,  breit,
breit,  hoch
hoch in der
in der  -Kunststoffe produziert werden, kommt es im Verlauf des Syntheseprozesses zu einem Zwischenfall, bei dem
-Kunststoffe produziert werden, kommt es im Verlauf des Syntheseprozesses zu einem Zwischenfall, bei dem  Liter flüssiges Styrol
Liter flüssiges Styrol  Dichte
Dichte  verdampfen und in die Halle freigesetzt werden. Der am Arbeitsplatz maximal zulässige Grenzwert (kurz AGW-Wert) für die Konzentration an Styrol in der Luft beträgt
verdampfen und in die Halle freigesetzt werden. Der am Arbeitsplatz maximal zulässige Grenzwert (kurz AGW-Wert) für die Konzentration an Styrol in der Luft beträgt  .
.
- Berechne, ob dieser Grenzwert nach dem Zwischenfall in der Werkhalle überschritten wird.
(3 VP)
(20 VP)
1.1
Reaktionsgleichung zur Herstellung des Polyesters
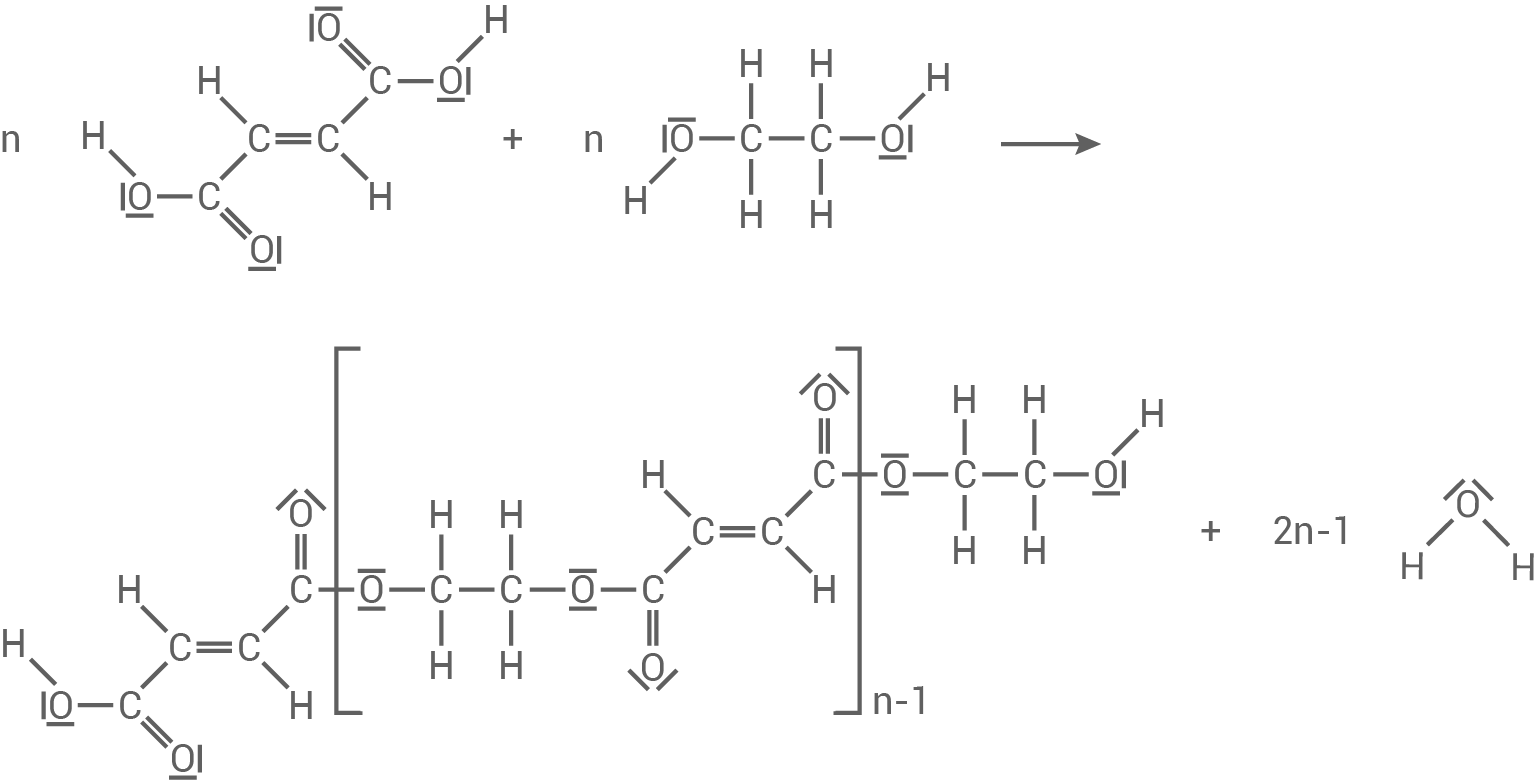

1.2
Möglicher Strukturformelausschnitt
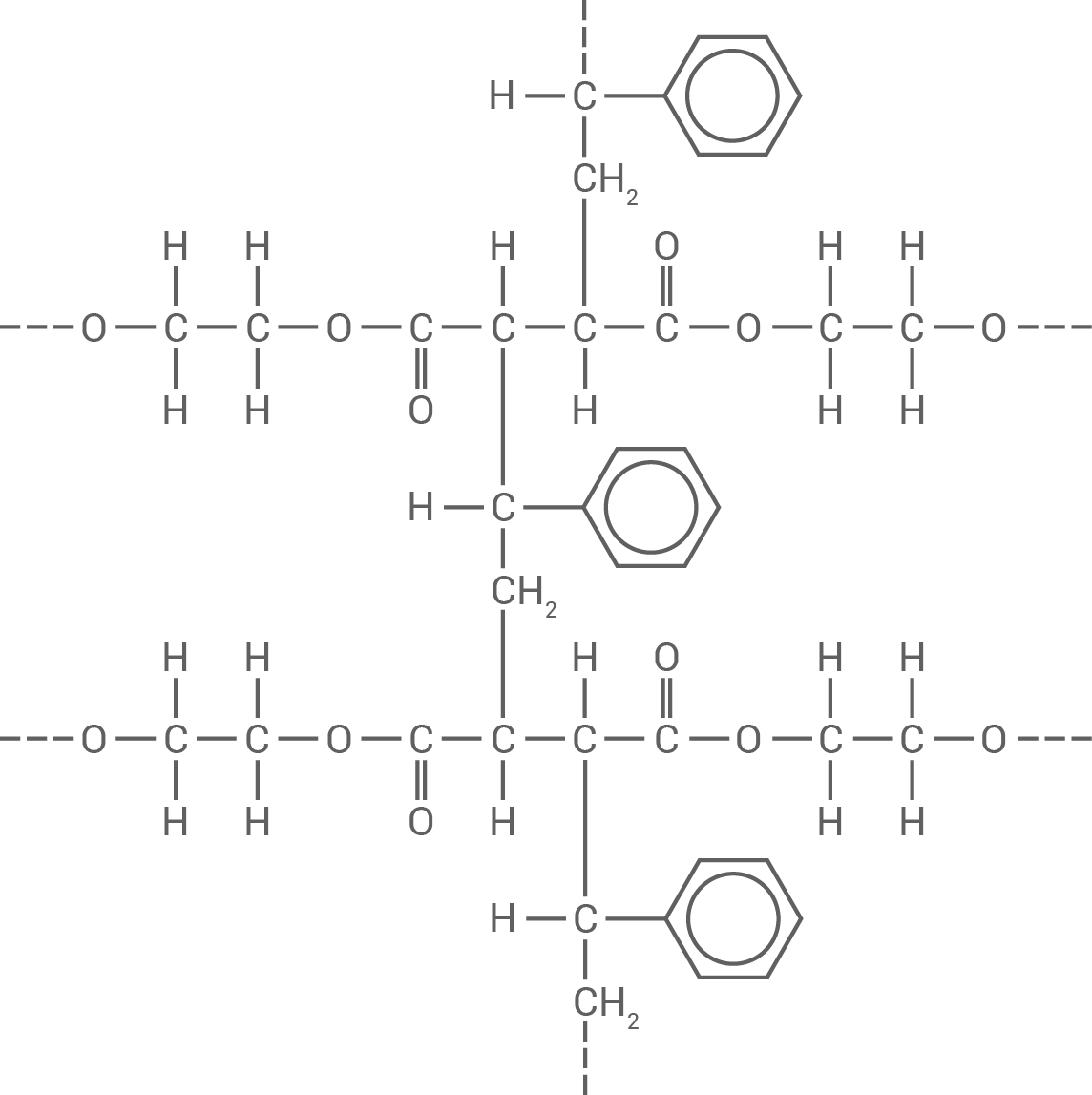 Unterschiedliche thermische Eigenschaften
Unterschiedliche thermische Eigenschaften

Ungehärtet:
- thermoplastische Eigenschaften
- geringe intermolekulare Kräfte, wodurch die Ketten sich unter Wärmezufuhr gegeinander verschieben
- das Material erweicht oder schmilzt und kann verformt werden
- duroplastische Eigenschaften
- dreidimensionale Vernetzung, wodurch die Makromoleküle unter Wärmezufuhr weniger beweglich sind
- lässt sich über einen weiten Temperaturbereich nicht verformen und zersetzt sich bei sehr hohen Temperaturen
2.1
Reaktionsmechanismus für die Herstellung von Polyethen
Radikalbildung (z.B. aus Dibenzoylperoxid):
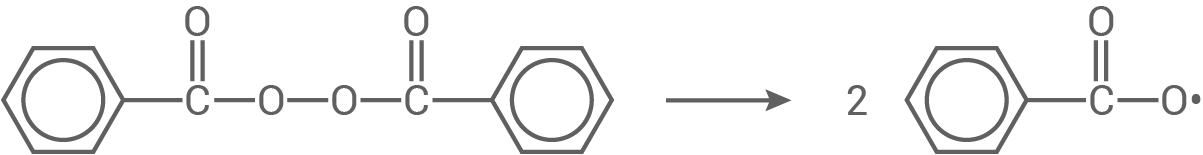 Kettenstart:
Kettenstart:
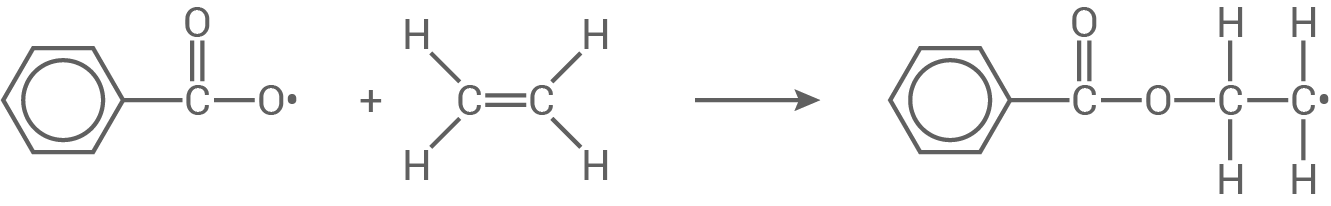 Kettenwachstum:
Kettenwachstum:
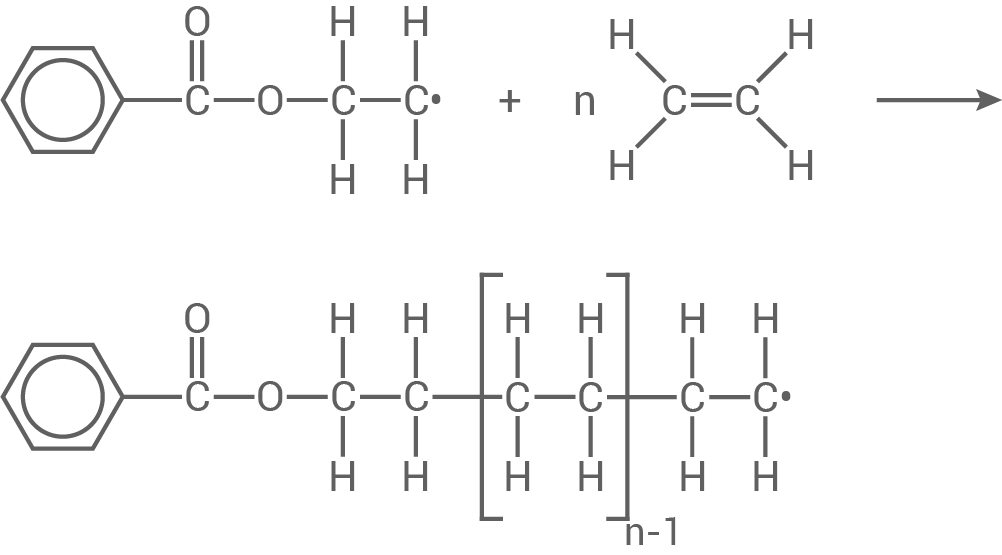 Mögliche Abbruchreaktionen
Reaktion zweier Radikale:
Mögliche Abbruchreaktionen
Reaktion zweier Radikale:
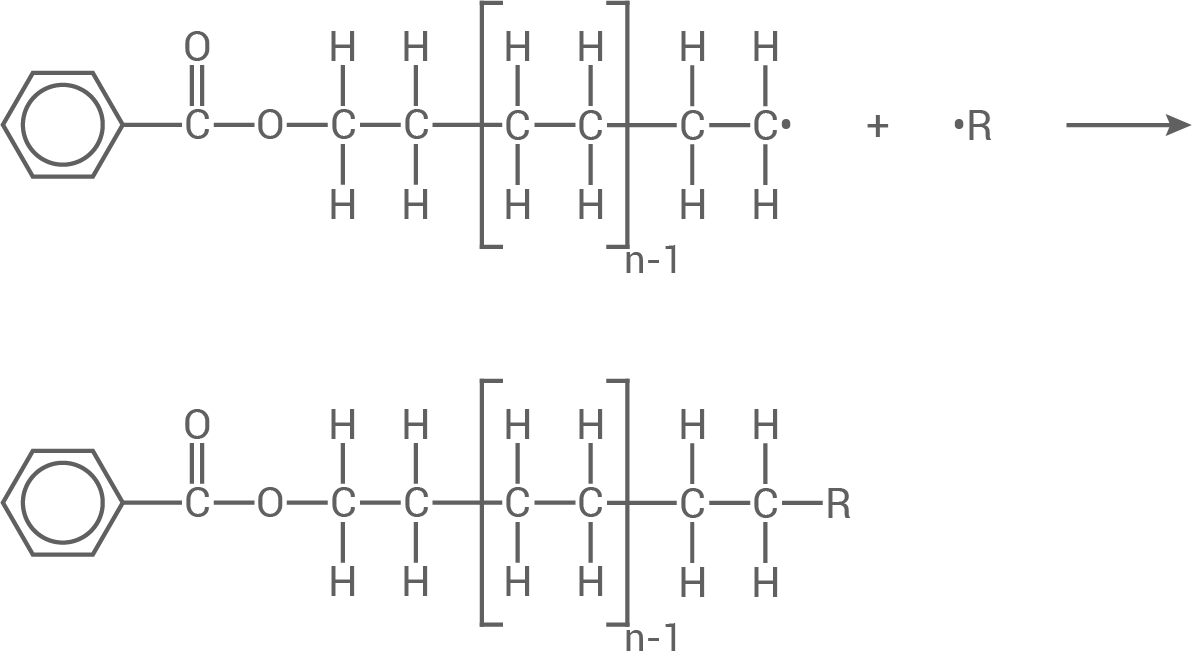 Disproportionierung:
Disproportionierung:
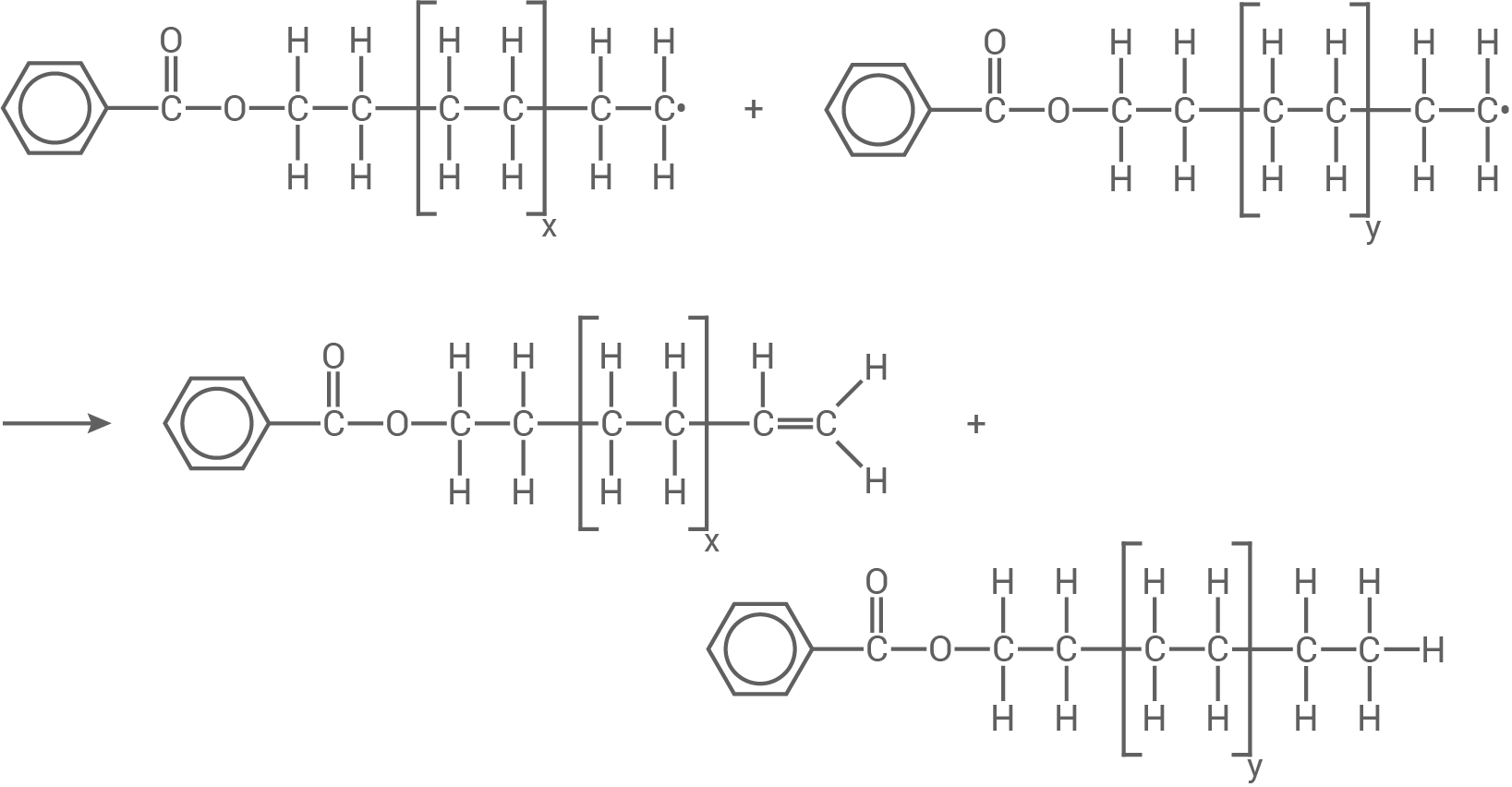 Wirkungsweise der Radikale
Durch die Wechselwirkung der ungepaarten Elektronen des Starterradikals mit den
Wirkungsweise der Radikale
Durch die Wechselwirkung der ungepaarten Elektronen des Starterradikals mit den  -Elektronen des Ethens, bildet sich eine neue kovalente Bindung aus. Am Ethen bleibt nun ein ungepaartes Elektron übrig, welches mit einem weiteren Ethen-Molekül reagiert.
-Elektronen des Ethens, bildet sich eine neue kovalente Bindung aus. Am Ethen bleibt nun ein ungepaartes Elektron übrig, welches mit einem weiteren Ethen-Molekül reagiert.
Bei der Kettenvereinigung kommt es zur Wechselwirkung zweier ungepaarter Elektronen, die eine -
- -Einfachbindung bilden.
-Einfachbindung bilden.
Bei der Disproportionierung reagieren zwei Polymerradikale, indem eine Kette A ein -Atom einer zweiten Kette B abstrahiert. An A entsteht nun eine
-Atom einer zweiten Kette B abstrahiert. An A entsteht nun eine  -
- -Bindung und an B eine Doppelbindung.
-Bindung und an B eine Doppelbindung.





Bei der Kettenvereinigung kommt es zur Wechselwirkung zweier ungepaarter Elektronen, die eine
Bei der Disproportionierung reagieren zwei Polymerradikale, indem eine Kette A ein
2.2
Umsetzung von Ethanol zu Ethen
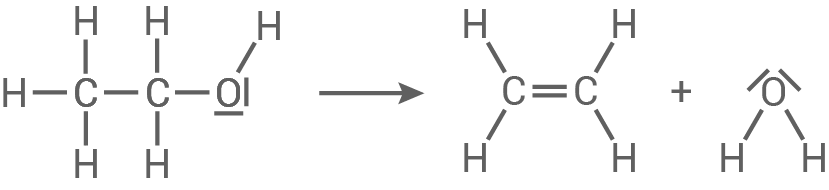 Experiment zum Nachweis der Doppelbindung
Der Nachweis einer Doppelbindung erfolgt durch die Reaktion mit einer Brom-Lösung, bei der sich das Brom an die Doppelbindung addiert. Dabei entfärbt sich die Lösung und zeigt einen positiven Nachweis an.
Hier: das gasförmiges Ethen wird durch die Brom-Lösung geleitet. Nach kurzer Zeit kann eine Entfärbung beobachtet werden.
Experiment zum Nachweis der Doppelbindung
Der Nachweis einer Doppelbindung erfolgt durch die Reaktion mit einer Brom-Lösung, bei der sich das Brom an die Doppelbindung addiert. Dabei entfärbt sich die Lösung und zeigt einen positiven Nachweis an.
Hier: das gasförmiges Ethen wird durch die Brom-Lösung geleitet. Nach kurzer Zeit kann eine Entfärbung beobachtet werden.

3.1
Strukturformeln und Namen der Monomere
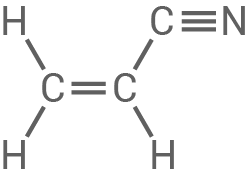
|
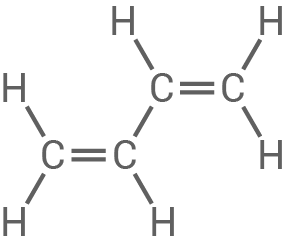
|
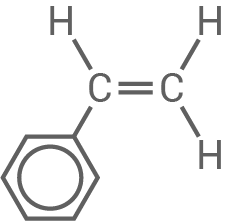
|
|
Acrylnitril
|
Buta-1,3-dien
|
Styrol
|
3.2
Berechnung des Grenzwertes
![\(\begin{array}[t]{rll}
M\,_\text{Sty} &=& 104 \,\text{g} \cdot \text{mol}^{-1}& \\[5pt]
V\,_\text{Sty} &=& 5000 \,\text{mL} & \\[5pt]
\rho\,_\text{Sty}&=& 0,91 \,\text{g} \cdot \,\text{mL}^{-1}
\end{array}\)](https://mathjax.schullv.de/f748c682649b6317fbdb5cd23726259b3705ca52d01ddd2945996eb372ee0221?color=5a5a5a)



![\(\begin{array}[t]{rll}
m\,_\text{Sty}&=& 0,91 \,\text{g} \cdot \text{mL}^{-1} \cdot 5000 \,\text{mL} &\quad \scriptsize \; \\[5pt]
&=& 4550 \,\text{g} \\[5pt]
&=& 4,55 \cdot 10^6 \,\text{mg} \\[5pt]
\end{array}\)](https://mathjax.schullv.de/7ca74a2b528257d6fbe6210fae03bbb9e7669bea89ab75f0fcfcc2455622400d?color=5a5a5a)
![\(\begin{array}[t]{rll}
V\,_\text{Werkhalle}&=& \,\text{Länge} \cdot \,\text{Breite} \cdot \,\text{Höhe} &\quad \scriptsize
\; \\[5pt]
&=& 50 \cdot 15 \cdot 12 \,\text{m}^3 \\[5pt]
&=& 9000 \,\text{m}^3 \\[5pt]
\end{array}\)](https://mathjax.schullv.de/ba42a3a20d1bc72e0e2882a3f0705087f067a7cada1236fd60e16f4472afb947?color=5a5a5a) Konzentration des Styrols in der Werkhallen-Luft:
Konzentration des Styrols in der Werkhallen-Luft:
![\(\begin{array}[t]{rll}
c\,_\text{Styrol}&=& \dfrac{m\,_\text{Styrol}}{V\,_\text{Styrol}} & \\[5pt]
&=& \dfrac{4,55 \cdot 10 ^6 \,\text{mg}}{9000 \,\text{m}^{3}} \\[5pt]
&\approx & 505,6 \,\text{mg} \cdot \text{m}^{-3} \\[5pt]
\end{array}\)](https://mathjax.schullv.de/44ecf0320b9136e444ed6bc3bb4f1362b09633b9af7ad33ca9543258f66e786c?color=5a5a5a) Der Arbeitsplatzgrenzwert für das Styrol wird um fast das Sechsfache überschritten.
Der Arbeitsplatzgrenzwert für das Styrol wird um fast das Sechsfache überschritten.