Aufgabe 4 – Alkali- und Erdalkalimetalle
Zur Gewinnung von Alkali- und Erdalkalimetallen sind deren im Meerwasser enthaltenen Ionen in das Interesse der Forschung gerückt.
1
Lithium ist aufgrund seiner Verwendung in Akkumulatoren ein wichtiges Gebrauchsmetall. Ziel eines Forschungsprojekts ist es, Lithium elektrolytisch direkt aus Meerwasser zu gewinnen.
1.1
In einem Experiment wird eine wässrige Lithiumchlorid-Lösung  elektrolysiert.
elektrolysiert.
- Gib alle in der Lösung enthaltenen Ionen sowie ihre Konzentrationen an.
- Stelle für alle theoretisch möglichen Elektroden-Vorgänge eine Teilgleichung auf.
- Begründe mit Hilfe der Elektrodenpotenziale die tatsächlich ablaufenden Elektroden-Reaktionen und berechne damit die zur Elektrolyse notwendige Spannung.
Hinweis: Mögliche Überspannungen sind nicht zu berücksichtigen.
(7 VP)
1.2
Eine Idee zur technischen Umsetzung der Gewinnung von Lithium aus Meerwasser zeigt Abbildung 1.
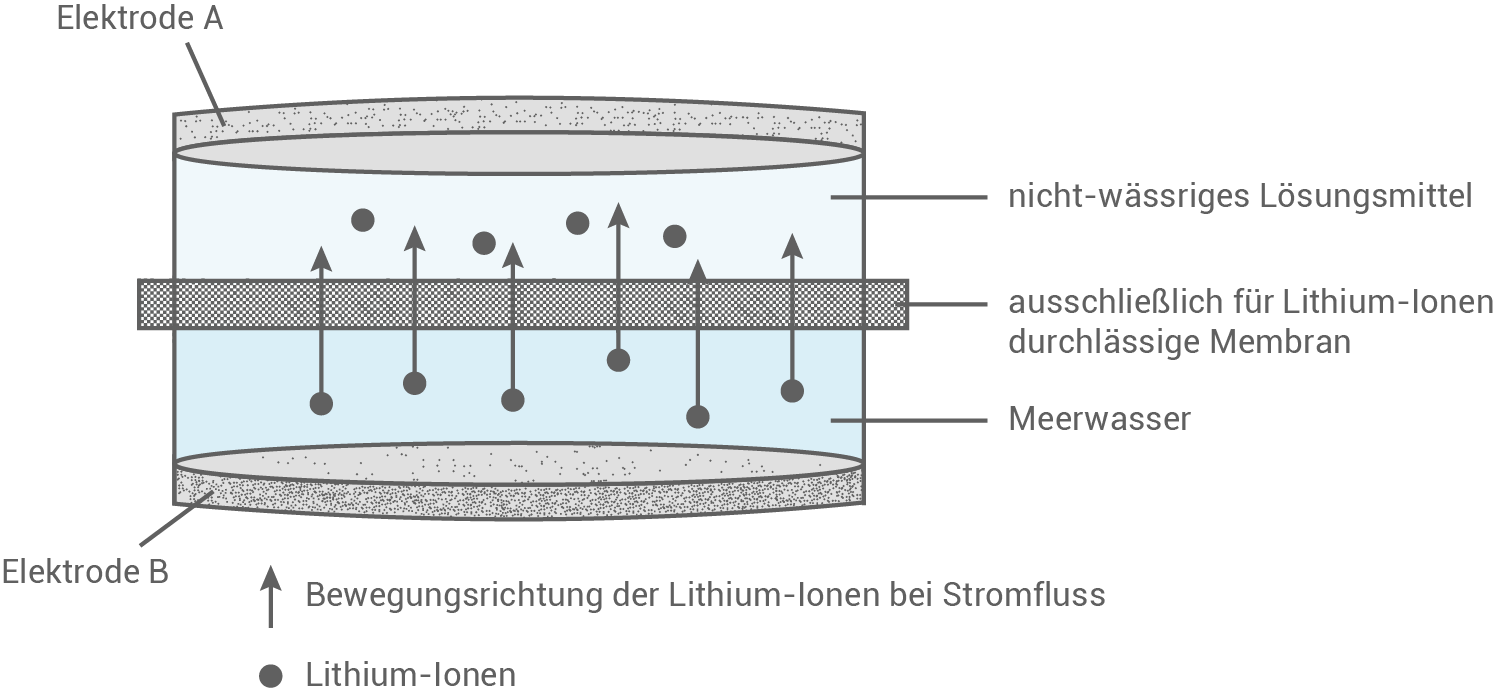

Abbildung 1: Schematische Darstellung einer Elektrolyse-Apparatur zur Gewinnung von Lithium aus Meerwasser
- Ordne den Elektroden A und B die Begriffe Anode und Kathode sowie Minus- und Pluspol zu.
- Begründe zwei Funktionen der Membran.
(4 VP)
2
Meerwasser wird zur Gewinnung von Magnesiumchlorid in wässriger Lösung verwendet.
2.1
Die Gewinnung von Magnesiumchlorid erfolgt in zwei Schritten:
| (A) | Zunächst wird Calciumhydroxid-Pulver zu Meerwasser gegeben, wodurch sich schwerlösliches Magnesiumhydroxid bildet. |
| (B) | Das reine Magnesiumhydroxid wird mit Salzsäure versetzt, wobei sich unter anderem Magnesiumchlorid bildet. |
- Gib für (B) eine Reaktionsgleichung an.
- Gib den Reaktionstyp an und begründe deine Angabe.
(3 VP)
2.2
Die Konzentration von Magnesium-Ionen in einer wässrigen Magnesiumchlorid-Lösung kann mit Hilfe einer Leitfähigkeitstitration ermittelt werden. Dabei läuft folgender Prozess ab:


 Bei der Titration werden
Bei der Titration werden  der Magnesiumchlorid-Lösung unbekannter Konzentration mit einer Calciumhydroxid-Lösung der Konzentration
der Magnesiumchlorid-Lösung unbekannter Konzentration mit einer Calciumhydroxid-Lösung der Konzentration  titriert. Dabei wird die Leitfähigkeit in Abhängigkeit des zugegebenen Volumens an Calciumhydroxid-Lösung ermittelt. Man erhält das in Abbildung 2 dargestellte Diagramm.
titriert. Dabei wird die Leitfähigkeit in Abhängigkeit des zugegebenen Volumens an Calciumhydroxid-Lösung ermittelt. Man erhält das in Abbildung 2 dargestellte Diagramm.
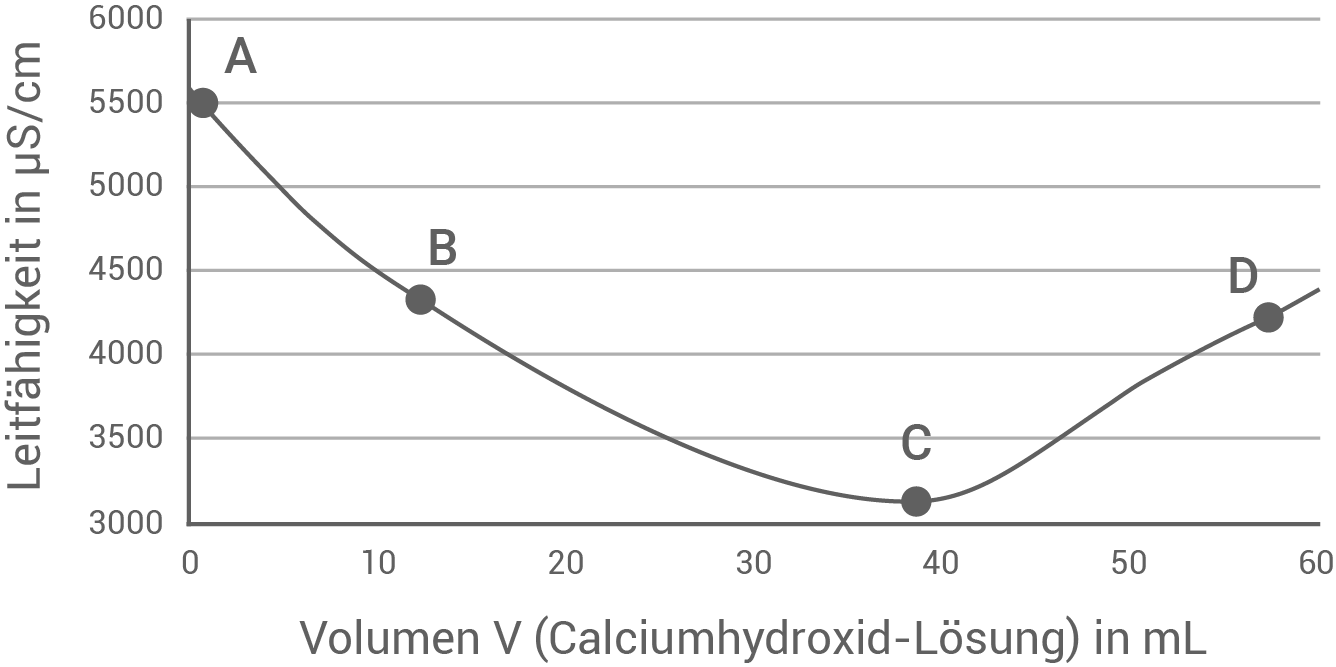

Abbildung 2: Diagramm der durchgeführten Leitfähigkeitstitration
- Gib für die Punkte A, B, C und D die Ionen an, die in der Lösung vorliegen und die Leitfähigkeit maßgeblich beeinflussen.
Hinweis: Magnesiumhydroxid kann als unlöslich betrachtet werden. - Berechne die Konzentration der Magnesium-Ionen in der vorgelegten Lösung.
- Begründe den Anstieg der Leitfähigkeit nach Punkt C.
(6 VP)
(20 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Ionen in der Lösung
![\(\begin{array}[t]{rll}
c(Li^+)&=& c(Cl^-) & \\[5pt]
&=& 1\,\text{mol} \cdot \text{L}^{-1} & ,\\[10pt]
c(H_3O^+)&=& c(OH^-) & \\[5pt]
&=& 10^{-7} \,\text{mol} \cdot \text{L}^{-1} & \\[5pt]
\end{array}\)](https://mathjax.schullv.de/fe7c6e0cbff03c154e538df13c9f555e99ad39dcd292b46f913baf48bf498019?color=5a5a5a) Theoretisch mögliche Elektroden-Vorgänge
Tatsächlich ablaufende Elektroden-Reaktionen
Um die tatsächlich ablaufende Reaktion zu ermitteln, müssen die Zersetzungsspannungen für die vier verschiedenen Kombinationen der Reaktionen berechnet werden:
Die geringste Zersetzungsspannung ergibt sich also für die Elektrolyse von Wasser. Es laufen
Theoretisch mögliche Elektroden-Vorgänge
Tatsächlich ablaufende Elektroden-Reaktionen
Um die tatsächlich ablaufende Reaktion zu ermitteln, müssen die Zersetzungsspannungen für die vier verschiedenen Kombinationen der Reaktionen berechnet werden:
Die geringste Zersetzungsspannung ergibt sich also für die Elektrolyse von Wasser. Es laufen  und
und  mit einer Spannung von
mit einer Spannung von  statt.
statt.
1.2
Zuordnung der Begriffe
Funktionen der Membran (zwei erforderlich)
| Elektrode A: | Minuspol, Kathode |
| Elektrode B: | Pluspol, Anode |
- Trennung von Anoden- und Kathodenraum: die gebildeten Stoffe kommen in keinen direkten Kontakt
- Ladungsausgleich: es wird keine Gegenspannung aufgebaut
- Stromfluss: der Stromkreis ist geschlossen
- Trennung von Lithium und Wasser: so wird eine Reaktion und damit die Bildung von Wasserstoff verhindert
2.1
Reaktionsgleichung für (B)


 Reaktionstyp
Aus der Reaktionsgleichung lässt sich entnehmen, dass die Oxonium-Ionen
Reaktionstyp
Aus der Reaktionsgleichung lässt sich entnehmen, dass die Oxonium-Ionen  ihre Protonen abgeben und die Hydroxid-Ionen
ihre Protonen abgeben und die Hydroxid-Ionen  welche aufnehmen. Es findet daher eine Säure-Base-Reaktion statt.
welche aufnehmen. Es findet daher eine Säure-Base-Reaktion statt.
2.2
Ionen in der Lösung
Berechnung der Magnesium-Ionenkonzentration
Der Verbrauch an Calciumhydroxid-Lösung wird an Punkt C im Diagramm abgelesen:
 Daraus kann nun die Stoffmenge berechnet werden, woraus die Berechnung der Magnesium-Ionenkonzentration folgt:
Daraus kann nun die Stoffmenge berechnet werden, woraus die Berechnung der Magnesium-Ionenkonzentration folgt:
![\(\begin{array}[t]{rll}
c(Mg^{2+})&=& \dfrac{n}{V}& \\[5pt]
&=& \dfrac{0,00038\,\text{mol}}{0,05\,\text{L}} & \\[5pt]
&=& 0,0076\,\text{mol}\cdot\text{L}^{-1}
\end{array}\)](https://mathjax.schullv.de/bafa16bf938e83c736efa4698076f866e87e30c6b8c79644d096ff7a3ea08277?color=5a5a5a) Die Konzentration der Magnesium-Ionen in der vorgelegten Lösung beträgt
Die Konzentration der Magnesium-Ionen in der vorgelegten Lösung beträgt  Begründung der ansteigenden Leitfähigkeit
An Punkt C ist ein Anstieg der Leitfähigkeit beobachtbar, da an Punkt C eine Calciumchlorid-Lösung vorliegt und durch die Zugabe der Calciumhydroxid-Lösung die Leitfähigkeit größer wird.
Begründung der ansteigenden Leitfähigkeit
An Punkt C ist ein Anstieg der Leitfähigkeit beobachtbar, da an Punkt C eine Calciumchlorid-Lösung vorliegt und durch die Zugabe der Calciumhydroxid-Lösung die Leitfähigkeit größer wird.
| A: | |
| B: | |
| C: | |
| D: |