Aufgabe 1 – Kohlenstoffdioxid
Bei der Verbrennung fossiler Energieträger entsteht unter anderem das Treibhausgas Kohlenstoffdioxid. Um einen weiteren Temperaturanstieg der Atmosphäre zu vermeiden, sollten diese Kohlenstoffdioxidemissionen verringert werden. In einem Forschungsprojekt wird aus Kohlenstoffdioxid Kohlenstoffmonooxid hergestellt, welches zur Synthese von Treibstoffen verwendet wird. Ein weiteres Forschungsprojekt untersucht eine Methode zur Speicherung von Kohlenstoffdioxid in tiefen Gesteinsschichten.
1.1
In einer Gleichgewichtsreaktion reagiert Kohlenstoff mit Kohlenstoffdioxid unter Bildung von Kohlenstoffmonooxid (BOUDOUARD-Gleichgewicht).
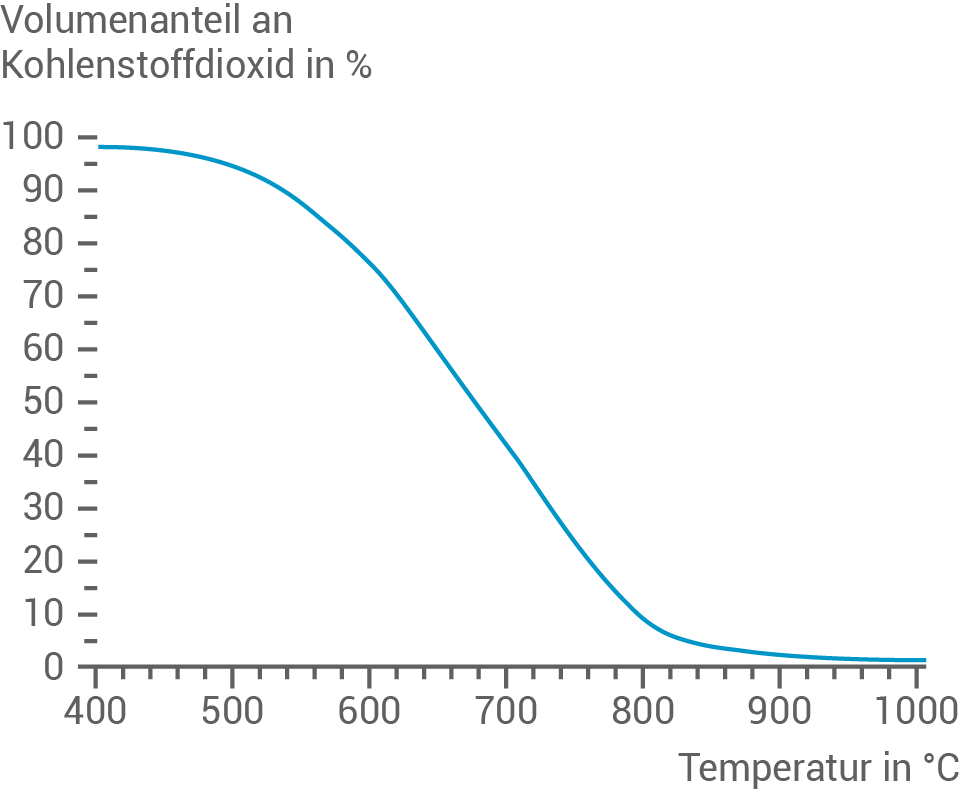

Abbildung 1: Temperaturabhängigkeit des BOUDOUARD-Gleichgewichts
- Gib für das BOUDOUARD-Gleichgewicht eine Reaktionsgleichung an und stelle das Massenwirkungsgesetz auf. Hinweis: Der Feststoff wird im Massenwirkungsgesetz nicht berücksichtigt.
- Gib die Temperatur an, bei der das Gasgemisch einen Volumenanteil von
Kohlenstoffdioxid enthält.
- Begründe das Vorzeichen der Reaktionsenthalpie
für die Bildung von Kohlenstoffmonooxid mit dem Prinzip von LE CHATELIER.
- Gib den Einfluss einer Druckänderung bei konstanter Temperatur auf die Gleichgewichtslage an und begründe diesen.
(7 VP)
1.2
Bei der FISCHER-TROPSCH-Synthese reagieren Kohlenstoffmonooxid und Wasserstoff bei  an Katalysatoren zu gasförmigen Alkanen und Wasserdampf.
an Katalysatoren zu gasförmigen Alkanen und Wasserdampf.
- Gib für die Synthese von Octan eine Reaktionsgleichung an.
- Berechne die Reaktionsenthalpie
für die Bildung von
Octan unter Berücksichtigung der Aggregatzustände der Stoffe.
- Begründe das Vorzeichen der Reaktionsentropie
anhand der Reaktionsgleichung.
- Treffe eine Aussage über den freiwilligen Ablauf der Reaktion in Abhängigkeit von der Temperatur und begründe.
(6 VP)
2
Dem isländischen Forschungsprojekt CarbFix ist es gelungen, in Kraftwerken anfallendes Kohlenstoffdioxid in Gesteinsschichten dauerhaft zu speichern. Dazu wird eine Kohlenstoffdioxid-Lösung in ca.  Tiefe in poröse Gesteinsschichten gepresst. Dabei entsteht unter anderem Kalk
Tiefe in poröse Gesteinsschichten gepresst. Dabei entsteht unter anderem Kalk  .
.
Die Kalkbildung wird in einem vereinfachten Modellexperiment nachvollzogen:
Ein Erlenmeyerkolben wird mit einer ausreichenden Menge gesättigter Calciumhydroxid-Lösung befüllt. Anschließend wird Kohlenstoffdioxid-Lösung zugegeben und der Erlenmeyerkolben verschlossen.
Die Kalkbildung wird in einem vereinfachten Modellexperiment nachvollzogen:
Ein Erlenmeyerkolben wird mit einer ausreichenden Menge gesättigter Calciumhydroxid-Lösung befüllt. Anschließend wird Kohlenstoffdioxid-Lösung zugegeben und der Erlenmeyerkolben verschlossen.
- Erkläre die saure Eigenschaft einer Kohlenstoffdioxid-Lösung anhand einer Reaktionsgleichung.
- Erkläre anhand einer Reaktionsgleichung, dass es sich bei der im Modellexperiment beschriebenen Kalkbildung um eine Säure-Base-Reaktion nach BRØNSTED handelt.
- Beschreibe ein experimentelles Vorgehen und dessen Auswertung.
(7 VP)
(20 VP)
1.1
Reaktionsgleichung des BOUDOUARD-Gleichgewichts


 Massenwirkungsgesetz
Massenwirkungsgesetz
 Temperaturbestimmung
Das Schaubild zeigt, dass die Temperatur, bei der das Gasgemisch einen Volumenanteil von
Temperaturbestimmung
Das Schaubild zeigt, dass die Temperatur, bei der das Gasgemisch einen Volumenanteil von  Kohlenstoffdioxid enthält, ca.
Kohlenstoffdioxid enthält, ca.  beträgt.
Vorzeichen der Reaktionsenthalpie
Das Schaubild zeigt die Temperaturabhängigkeit des BOUDOUARD-Gleichgewichts. Mit steigender Temperatur nimmt der Volumenanteil an
beträgt.
Vorzeichen der Reaktionsenthalpie
Das Schaubild zeigt die Temperaturabhängigkeit des BOUDOUARD-Gleichgewichts. Mit steigender Temperatur nimmt der Volumenanteil an  ab. Daran sieht man, dass hohe Temperaturen die Hinreaktion begünstigen.
ab. Daran sieht man, dass hohe Temperaturen die Hinreaktion begünstigen.
Nach dem Prinzip von LE CHATELIER wird bei Wärmezufuhr die endotherme Reaktion (Wärme verbrauchend) begünstigt – andersrum wird die exotherme Reaktion bei einer Temperaturerniedrigung bevorzugt. Da beim BOUDOUARD-Gleichgewicht die Reaktion durch Temperaturerhöhung bevorzugt wird, ist die Reaktion endotherm und die Reaktionsenthalpie positiv: Einfluss einer Druckänderung bei konstanter Temperatur
Beim BOUDOUARD-Gleichgewicht nimmt die Anzahl der Gasteilchen in Reaktionsrichtung zu. Aus einem gasförmigen Molekül
Einfluss einer Druckänderung bei konstanter Temperatur
Beim BOUDOUARD-Gleichgewicht nimmt die Anzahl der Gasteilchen in Reaktionsrichtung zu. Aus einem gasförmigen Molekül  entstehen zwei gasförmige Moleküle
entstehen zwei gasförmige Moleküle 
Nach dem Prinzip von LE CHATELIER weicht das System, bei Druckerhöhung so aus, dass die volumenverkleinernde Reaktion gefördert wird. Dadurch wird dem Zwang ausgewichen. Das Gleichgewicht verschiebt sich auf die Seite der Reaktion, auf der weniger Teilchen in der Gasphase sind, also auf die Seite der Edukte.
Nach dem Prinzip von LE CHATELIER wird bei Wärmezufuhr die endotherme Reaktion (Wärme verbrauchend) begünstigt – andersrum wird die exotherme Reaktion bei einer Temperaturerniedrigung bevorzugt. Da beim BOUDOUARD-Gleichgewicht die Reaktion durch Temperaturerhöhung bevorzugt wird, ist die Reaktion endotherm und die Reaktionsenthalpie positiv:
Nach dem Prinzip von LE CHATELIER weicht das System, bei Druckerhöhung so aus, dass die volumenverkleinernde Reaktion gefördert wird. Dadurch wird dem Zwang ausgewichen. Das Gleichgewicht verschiebt sich auf die Seite der Reaktion, auf der weniger Teilchen in der Gasphase sind, also auf die Seite der Edukte.
1.2
Reaktionsgleichung der Octansynthese


 Berechnung der Reaktionsenthalpie
Es gilt:
Die Reaktionsenthalpie beträgt für die Bildung von
Berechnung der Reaktionsenthalpie
Es gilt:
Die Reaktionsenthalpie beträgt für die Bildung von  Octan
Octan  Vorzeichen der Reaktionsentropie
Die Reaktionsgleichung zeigt
Vorzeichen der Reaktionsentropie
Die Reaktionsgleichung zeigt  gasförmige Teilchen auf der Eduktseite
gasförmige Teilchen auf der Eduktseite  und
und  auf der Produktseite
auf der Produktseite 
Die Abnahme der Zahl der Gasteilchen bedeuten einen Übergang in einen geordneteren Zustand. Die Entropie nimmt ab, deshalb besitzt die Reaktionsentropie ein negatives Vorzeichen. Temperaturabhängigkeit der Freien Enthalpie Ob die Reaktion freiwillig abläuft, zeigt die Freie Enthalpie. Dafür wird zunächst die Entropie berechnet: Mithilfe der GIBBS-HELMHOLTZ-Gleichung kann nun weitergerechnet werden: Das negative Vorzeichen zeigt, dass das Gleichgewicht stark auf der Produktseite liegt und die Reaktion freiwillig abläuft.
Die Abnahme der Zahl der Gasteilchen bedeuten einen Übergang in einen geordneteren Zustand. Die Entropie nimmt ab, deshalb besitzt die Reaktionsentropie ein negatives Vorzeichen. Temperaturabhängigkeit der Freien Enthalpie Ob die Reaktion freiwillig abläuft, zeigt die Freie Enthalpie. Dafür wird zunächst die Entropie berechnet: Mithilfe der GIBBS-HELMHOLTZ-Gleichung kann nun weitergerechnet werden: Das negative Vorzeichen zeigt, dass das Gleichgewicht stark auf der Produktseite liegt und die Reaktion freiwillig abläuft.
2
Saure Eigenschaft einer Kohlenstoffdioxid-Lösung


 Bei der Reaktion von Kohlenstoffdioxid mit Wasser entstehen die Ionen der Kohlensäure
Bei der Reaktion von Kohlenstoffdioxid mit Wasser entstehen die Ionen der Kohlensäure  Die Oxonium-Ionen
Die Oxonium-Ionen sorgen für die saure Eigenschaft der Kohlenstoffdioxid-Lösung.
Reaktionsgleichung der Kalkbildung
Eine Säure-Base-Reaktion nach BRØNSTED ist eine Reaktion, bei der eine Säure ein Proton (
sorgen für die saure Eigenschaft der Kohlenstoffdioxid-Lösung.
Reaktionsgleichung der Kalkbildung
Eine Säure-Base-Reaktion nach BRØNSTED ist eine Reaktion, bei der eine Säure ein Proton ( ) an einen Reaktionspartner überträgt.
) an einen Reaktionspartner überträgt.


 Es findet eine Protonenübertragung statt. Die Ionen der Kohlensäure
Es findet eine Protonenübertragung statt. Die Ionen der Kohlensäure  wirken hierbei als Säure (Protonendonator) und
wirken hierbei als Säure (Protonendonator) und  als Base (Protonenakzeptor), womit eine Säure-Base-Reaktion nach BRØNSTED stattfindet.
Experimentelles Vorgehen und Auswertung
Es wird eine Calciumcarbonat-Lösung mit einer Kohlenstoffdioxid-Lösung zusammengegeben und die dabei gebildete Calciumcarbonatmenge bestimmt.
als Base (Protonenakzeptor), womit eine Säure-Base-Reaktion nach BRØNSTED stattfindet.
Experimentelles Vorgehen und Auswertung
Es wird eine Calciumcarbonat-Lösung mit einer Kohlenstoffdioxid-Lösung zusammengegeben und die dabei gebildete Calciumcarbonatmenge bestimmt.
Bei der Reaktion entsteht eine Suspension an Calciumcarbonat, welche abfiltriert wird. Der Rückstand im Filter wird getrocknet und gewogen.
wird getrocknet und gewogen.
Nun kann mit der Masse an Calciumcarbonat auf die Masse des gebundenen Kohlenstoffdioxids zurückgerechnet werden. Aus den Reaktionsgleichungen folgt:

 Weiterhin folgt:
Alternativ kann die Masse an
Weiterhin folgt:
Alternativ kann die Masse an  über die Änderung der Stoffmenge an Hydroxid-Ionen durch eine Titration bestimmt werden.
über die Änderung der Stoffmenge an Hydroxid-Ionen durch eine Titration bestimmt werden.
Bei der Reaktion entsteht eine Suspension an Calciumcarbonat, welche abfiltriert wird. Der Rückstand im Filter
Nun kann mit der Masse an Calciumcarbonat auf die Masse des gebundenen Kohlenstoffdioxids zurückgerechnet werden. Aus den Reaktionsgleichungen folgt: