Aufgabe 4 – Brom
Brom wurde erstmals 1826 durch den französischen Chemiker ANTOINE-JÉRÔME BALARD aus Meeresalgen gewonnen. Die industrielle Produktion begann 1860. Auch heute wird Brom in Labor und Technik in vielfältiger Weise verwendet.
1
Beim Arbeiten mit leicht flüchtigem, stark giftigem Brom sollte aus Sicherheitsgründen stets eine geeignete Chemikalie bereitstehen, um austretendes Brom unschädlich machen zu können.
1.1
In der Praxis verwendet man dazu häufig eine wässrige Natriumthiosulfat- Lösung  die mit Brom unter Bildung von Natriumbromid, Schwefel und Schwefelsäure reagiert.
die mit Brom unter Bildung von Natriumbromid, Schwefel und Schwefelsäure reagiert.
- Stelle eine Reaktionsgleichung für die beschriebene Reaktion auf.
- Begründe, dass es sich um eine Redoxreaktion handelt.
(4 VP)
1.2
Eine gängige Lösung enthält  Massenprozent Natriumthiosulfat.
Massenprozent Natriumthiosulfat.
- Beschreibe die Herstellung von
der angegebenen Natriumthiosulfatlösung.
- Überprüfe, ob damit
Brom unschädlich gemacht werden könnte.
(4 VP)
1.3
Brom besitzt mit  im Vergleich zu Wasser eine relativ niedrige Siedetemperatur.
im Vergleich zu Wasser eine relativ niedrige Siedetemperatur.
- Erkläre diesen Sachverhalt.
(2 VP)
2
Eine technische Anwendung von Brom stellen sogenannte Redox-Flow-Akkumulatoren dar. Deren Besonderheit ist, dass die Elektrolyte außerhalb der Zelle in separaten Tanks (Elektrolytspeicher) gelagert werden und nur zum Zeitpunkt der Ladung oder Entladung durch die Zelle gepumpt werden. Durch die daraus resultierende hohe Speicherkapazität sind sie besonders geeignet zur Zwischenspeicherung elektrischer Energie aus regenerativen Quellen in Zeiten eines Überangebots. Diese Energie kann später im Bedarfsfall passgenau abgerufen werden.
2.1
Die in einem Zink-Brom-Redox-Flow-Akkumulator ablaufenden elektrochemischen Vorgänge können zunächst an einer einfachen Galvanischen Zelle theoretisch betrachtet werden.
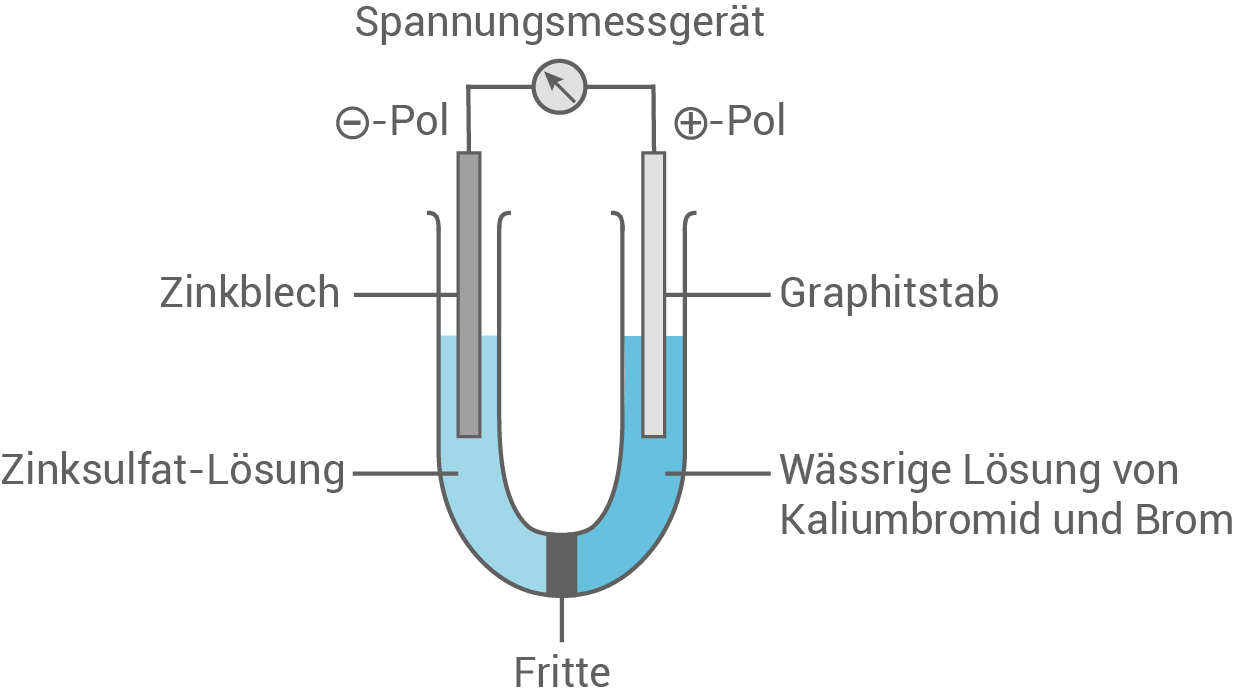
- Zeichne und beschrifte eine einfache Zink-Brom-Zelle.Dazu werden folgende Chemikalien verwendet: Zinkblech, Graphitstab, Brom, Zink
-sulfat, Kaliumbromid und Wasser.
- Stelle die Gleichungen der Teilreaktionen beim Lade- und Entladevorgang auf. Hinweis: Eine Zersetzung von Wasser findet nicht statt.
- Berechne die unter Standardbedingungen zu erwartende Spannung.
(6 VP)
2.2
Im Zink-Brom-Redox-Flow-Akkumulator wird in beiden Halbzellen Zink -bromidlösung eingesetzt.
-bromidlösung eingesetzt.
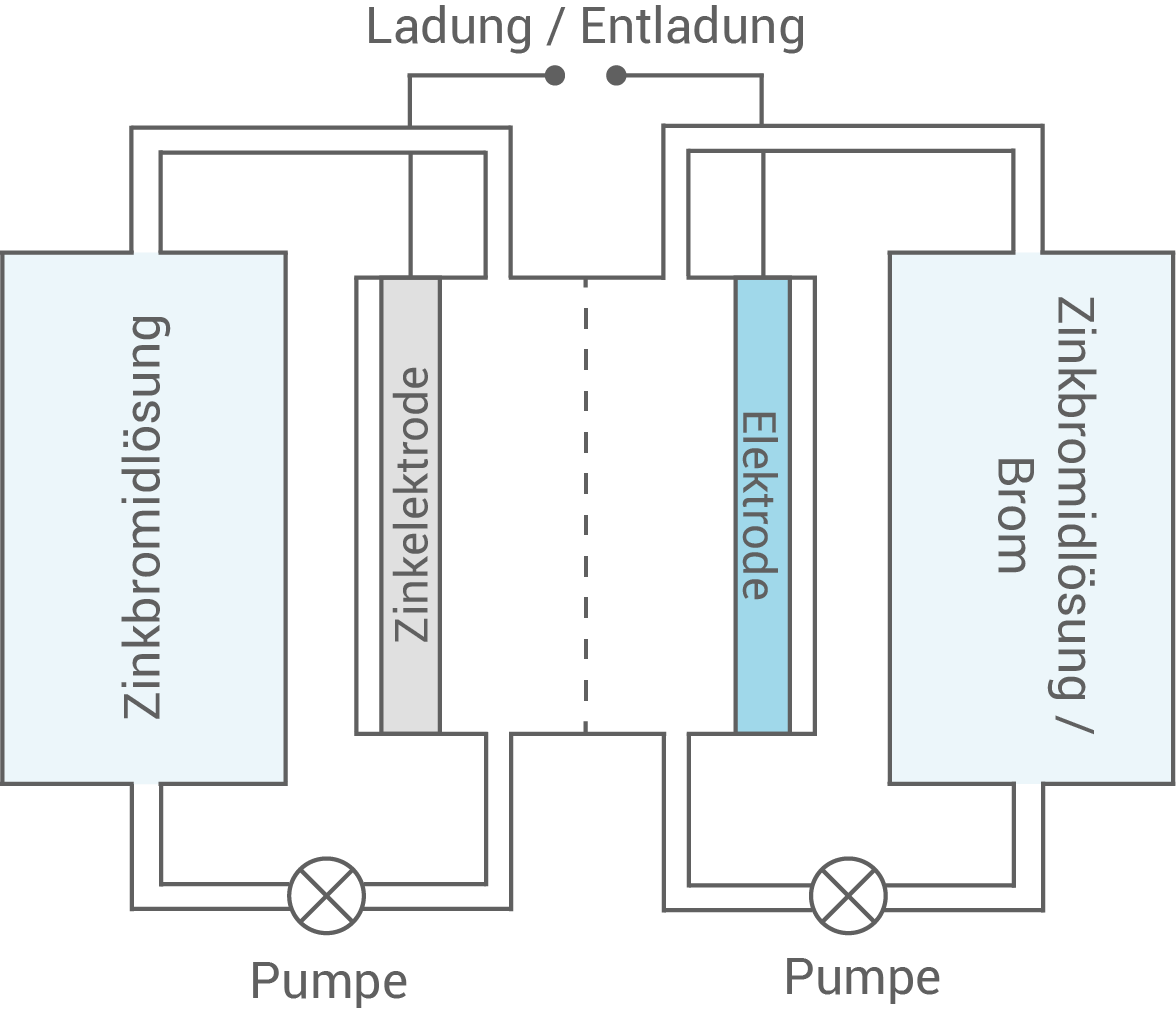

- Beschreibe mithilfe der stark vereinfachten Skizze die Veränderungen in den Elektrolytspeichern und an der Zinkelektrode während des Lade-bzw. Entladevorgangs.
- Erläutere eine Möglichkeit, um den Ladezustand eines Zink-Brom-Redox-Flow-Akkumulators zu überprüfen.
(4 VP)
(20 VP)
1.1
Reaktionsgleichung
 Redoxreaktion
Die Oxidationszahlen in der Reaktionsgleichung zeigen Elektronenübergänge:
Brom wirkt als Oxidationsmittel und wird selbst reduziert: 0
Redoxreaktion
Die Oxidationszahlen in der Reaktionsgleichung zeigen Elektronenübergänge:
Brom wirkt als Oxidationsmittel und wird selbst reduziert: 0  -I
-I
Die Schwefelatome werden disproportioniert: +II +IV und 0
+IV und 0

Die Schwefelatome werden disproportioniert: +II
1.2
Herstellung der Natriumthiosulfatlösung
Für die Herstellung einer  -igen Natriumthiosulfatlösung werden
-igen Natriumthiosulfatlösung werden  Natriumthiosulfat eingewogen. Anschließend wird mit Wasser auf
Natriumthiosulfat eingewogen. Anschließend wird mit Wasser auf  aufgefüllt.
Überprüfung der Unschädlichkeit
Basierend auf der Reaktionsgleichung gilt:
aufgefüllt.
Überprüfung der Unschädlichkeit
Basierend auf der Reaktionsgleichung gilt:
 Es folgt:
Es folgt:
![\(\begin{array}[t]{rll}
n(Br_2)&=& \dfrac{m(Br_2)}{M(Br_2)} \\[5pt]
&=& \dfrac{1\,\text{g}}{159,8\,\text{g}\cdot \text{mol}^{-1} } \\[5pt]
&\approx& 0,00626\,\text{mol} \\[15pt]
\end{array}\)](https://mathjax.schullv.de/95d51387fc5ce156d2bc5913a882b9fdee187b8b091b9f620954eb2cf7ae80f5?color=5a5a5a)
 Brom können also mit einer
Brom können also mit einer  -igen Natriumthiosulfatlösung unschädlich gemacht werden.
-igen Natriumthiosulfatlösung unschädlich gemacht werden.
1.3
Erklärung des Sachverhalts
Brom-Moleküle werden über VAN-DER-WAALS-Wechselwirkungen zusammengehalten und Wasser-Moleküle bilden Wasserstoffbrücken aus.
VAN-DER-WAALS-Kräfte können schon mit einem geringen Energieaufwand überwunden werden. Wasserstoffbrückenbindungen hingegen sind stärker und erfordern für die Spaltung einen hohen Ernergieaufwand. Deswegen besitzt Brom im Gegensatz zu Wasser eine realtiv niedrige Siedetemperatur.
VAN-DER-WAALS-Kräfte können schon mit einem geringen Energieaufwand überwunden werden. Wasserstoffbrückenbindungen hingegen sind stärker und erfordern für die Spaltung einen hohen Ernergieaufwand. Deswegen besitzt Brom im Gegensatz zu Wasser eine realtiv niedrige Siedetemperatur.
2.1
Skizze einer Zink-Brom-Zelle
 Teilreaktionen beim Lade- und Entladevorgang
Folgende Reaktionen laufen freiwillig ab und entsprechen dem Entladevorgang:
Beim Laden, also beim Anschluss an eine Spannungsquelle, wandelt sich die Zink-Brom-Zelle in eine Elektrolyse-Zelle um.
Zu erwartende Spannung
Teilreaktionen beim Lade- und Entladevorgang
Folgende Reaktionen laufen freiwillig ab und entsprechen dem Entladevorgang:
Beim Laden, also beim Anschluss an eine Spannungsquelle, wandelt sich die Zink-Brom-Zelle in eine Elektrolyse-Zelle um.
Zu erwartende Spannung
![\(\begin{array}[t]{rll}
U&=&\Delta E^0 \\[5pt]
&=&E^0(Kathode)-E^0(Anode)\\[5pt]
&=&1,10\,V-(-0,76\,V)\\[5pt]
&=&1,86\,V
\end{array}\)](https://mathjax.schullv.de/ba36a46201fb839912f4fc97fa1f801edcbd2c6a998800a9e6fdc3bd0eec5e69?color=5a5a5a)

2.2
Veränderungen in den Elektrolytspeichern und an der Zinkelektrode
Überprüfung des Ladezustandes eines Zink-Brom-Redox-Flow-Akkumulators
Der Ladezustand kann über die Konzentration bestimmt werden. Da die Zink-Ionen-Konzentration und die Brom-Konzentration miteinander gekoppelt sind, reicht es eine der beiden Konzentrationen zu bestimmen.
Die Konzentration kann durch Titration oder Leitfähigkeitsmessung bestimmt werden. Es wäre aber auch eine photometrische Bestimmung von Brom möglich.
| Entladung |
|---|
|
| Ladung |
|---|
|