Aufgabe 1 – Kohlenstoffdioxid
Die Konzentration von Kohlenstoffdioxid in der Atmosphäre hat seit Beginn der Messungen im Jahr 1958 stetig zugenommen.
1
Große Mengen des Kohlenstoffdioxids in der Atmosphäre werden von den Weltmeeren aufgenommen. Hierbei laufen drei Teilprozesse ab, die durch die Reaktionsgleichungen A, B und C ausgedrückt werden.









A:
B:
C:
1.1
Der größte Teil des vom Wasser aufgenommenen Kohlenstoffdioxids liegt in der hydratisierten Form  vor. Davon reagiert nur ein kleiner Teil zu Oxonium-Ionen weiter und wirkt sich so auf den pH-Wert des Meerwassers aus.
vor. Davon reagiert nur ein kleiner Teil zu Oxonium-Ionen weiter und wirkt sich so auf den pH-Wert des Meerwassers aus.
- Begründe mithilfe einer geeigneten Strukturformeldarstellung, dass bei der Hydratation von Kohlenstoffdioxid-Molekülen Wasserstoffbrücken ausgebildet werden können.
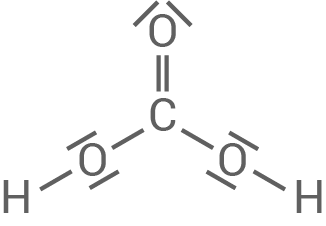
- Zeichne die Strukturformel des Kohlensäure-Moleküls in Lewis-Schreibweise (mit bindenden und nichtbindenden Elektronenpaaren).
- Erkläre ausgehend von Reaktionsgleichung C das Säure-Base-Konzept nach BRØNSTED.
- Erläutere die Auswirkung einer zunehmenden Konzentration von Kohlenstoffdioxid in der Atmosphäre auf den pH-Wert des Meerwassers nach dem Prinzip von LE CHATELIER.
(16 BE)
1.2
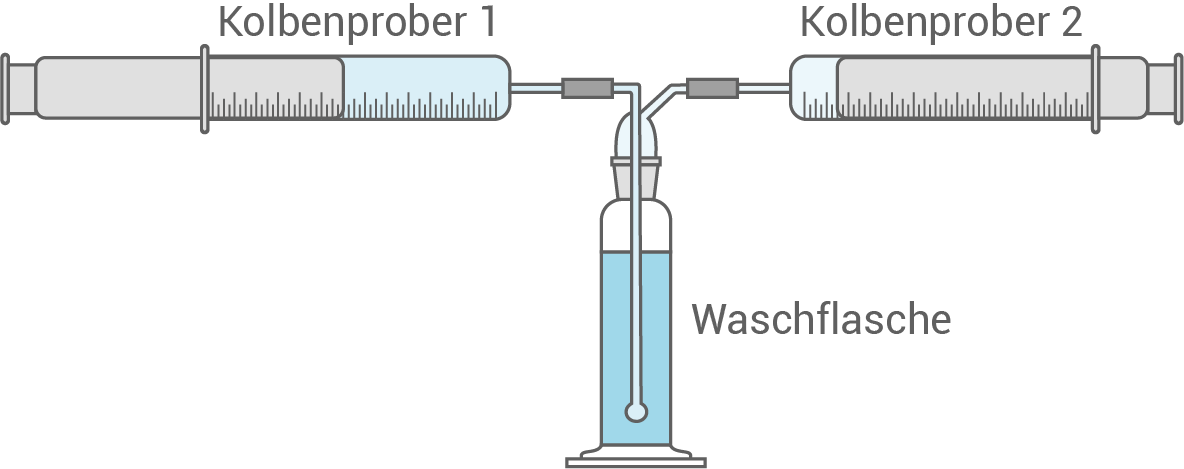
In einem Schulexperiment soll ausgehend von der abgebildeten Apparatur (Abbildung 1) bestimmt werden, welcher Anteil des Kohlenstoffdioxids zu Oxonium-Ionen weiterreagiert. Kolbenprober 1 ist mit  Kohlenstoffdioxid befüllt. In der Waschflasche befinden sich
Kohlenstoffdioxid befüllt. In der Waschflasche befinden sich  schwach saures demineralisiertes Wasser
schwach saures demineralisiertes Wasser 
 Das Kohlenstoffdioxid aus Kolbenprober 1 wird langsam durch die Waschflasche geleitet. Der
Das Kohlenstoffdioxid aus Kolbenprober 1 wird langsam durch die Waschflasche geleitet. Der  -Wert des Wassers verringert sich dabei von
-Wert des Wassers verringert sich dabei von  auf
auf  In Kolbenprober 2 wird am Ende des Versuchs ein Volumen von
In Kolbenprober 2 wird am Ende des Versuchs ein Volumen von  Kohlenstoffdioxid gemessen.
Kohlenstoffdioxid gemessen.

Abbildung 1: Schematische Darstellung des Experiments
- Berechnen die Stoffmenge an Kohlenstoffdioxid, die bei diesem Experiment vom Wasser aufgenommen wurde.
Hinweis: Verwende als molares Volumen - Zeige durch Berechnung, dass sich bei dem Experiment die Konzentration der Oxonium-Ionen um
erhöht.
- Bestimme den Anteil des vom Wasser aufgenommenen Kohlenstoffdioxids, der zu der oben angegebenen
-Wert-Änderung führt.
(8 BE)
2
Zur Verminderung der Kohlenstoffdioxid-Emission wird Wasserstoff als Energieträger verwendet. Um Wasserstoff zu speichern, werden seit einigen Jahren organische Flüssigkeiten eingesetzt, z. B. Dibenzyltoluol (DBT). Hierbei wird DBT zu Perhydro-DBT hydriert. Durch Dehydrierung von Perhydro-DBT kann der gespeicherte Wasserstoff wieder freigesetzt werden (Abbildung 2).
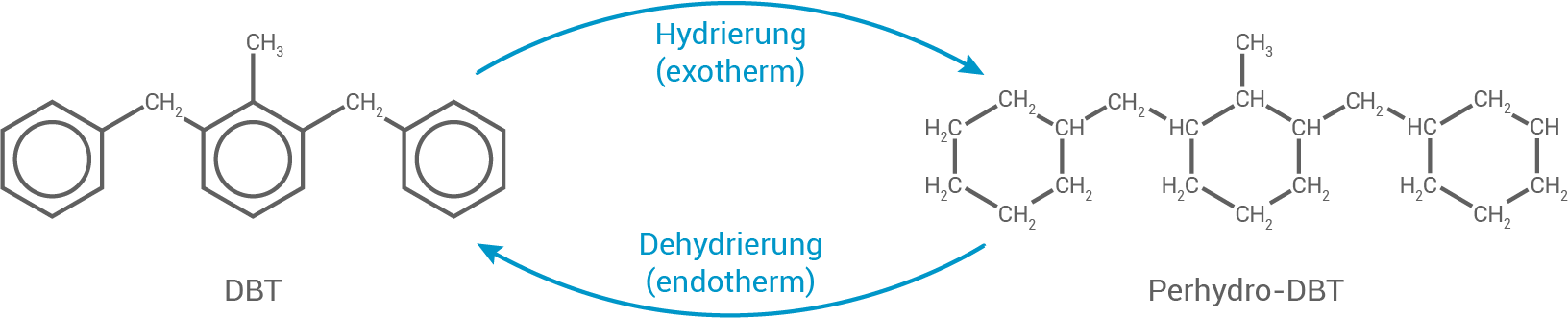

Abbildung 2: Schematische Darstellung der Prozesse für die Speicherung und Freisetzung von Wasserstoff
- Stelle die Reaktionsgleichung für die Dehydrierung von Perhydro-DBT als Gleichgewichtsreaktion auf.
- Erkläre, wie die Ausbeute von Wasserstoff durch Änderung der Temperatur und durch Änderung des Drucks erhöht werden kann.
- Berechne die Masse an Wasserstoff, die bei der Dehydrierung von
Perhydro-DBT maximal freigesetzt werden kann.
Hinweis: Verwende als Dichte von Perhydro-DBT
(16 VP)
(40 VP)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Begründung der Ausbildung von Wasserstoffbrückenbindungen
Dass bei der Hydratation von Kohlenstoffdioxid-Molekülen Wasserstoffbrückenbindungen ausgebildet werden können, liegt an der Polarität. Das Sauerstoffatom hat eine hohe Elektronegativität und zieht die Elektronen stärker an sich, wodurch am Sauerstoff eine negative Teilladung  und am Kohlenstoff eine positive Teilladung
und am Kohlenstoff eine positive Teilladung  entsteht:
entsteht:
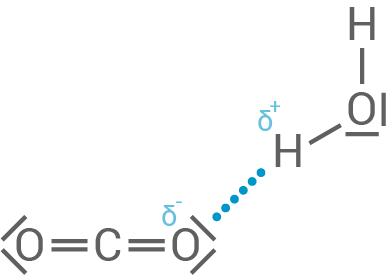 Dadurch kann das Sauerstoffatom des
Dadurch kann das Sauerstoffatom des  -Moleküls Wasserstoffbrückenbindungen mit den Wasserstoffatomen des Wassers eingehen.
Strukturformel des Kohlensäure-Moleküls
-Moleküls Wasserstoffbrückenbindungen mit den Wasserstoffatomen des Wassers eingehen.
Strukturformel des Kohlensäure-Moleküls
 Erklärung des Säure-Base-Konzepts nach BRØNSTED
Nach dem Säure-Base-Konzept von BRØNSTED ist eine Säure ein Protonendonator und eine Base ein Protonenakzeptor.
Erklärung des Säure-Base-Konzepts nach BRØNSTED
Nach dem Säure-Base-Konzept von BRØNSTED ist eine Säure ein Protonendonator und eine Base ein Protonenakzeptor.
In Reaktionsgleichung C fungiert Kohlensäure als Säure, da sie ein Proton
als Säure, da sie ein Proton  an das Wasser
an das Wasser  abgibt. Diese fungiert hier wiederum als Base. Durch diesen Protonenübergang entstehen Hydrogencarbonat-Ionen
abgibt. Diese fungiert hier wiederum als Base. Durch diesen Protonenübergang entstehen Hydrogencarbonat-Ionen  und Oxonium-Ionen
und Oxonium-Ionen  Erläuterung der Auswirkungen einer zunehmenden Konzentration
Nach dem Prinzip von LE CHATELIER wird ein System, das sich im Gleichgewicht befindet, einem äußeren Zwang (wie einer Konzentrationsänderung) so entgegenwirken, dass das Gleichgewicht wiederhergestellt wird. Eine erhöhte Konzentration von
Erläuterung der Auswirkungen einer zunehmenden Konzentration
Nach dem Prinzip von LE CHATELIER wird ein System, das sich im Gleichgewicht befindet, einem äußeren Zwang (wie einer Konzentrationsänderung) so entgegenwirken, dass das Gleichgewicht wiederhergestellt wird. Eine erhöhte Konzentration von  in der Atmosphäre führt zu einer erhöhten Aufnahme von
in der Atmosphäre führt zu einer erhöhten Aufnahme von  in das Meerwasser (Reaktion A). Das fördert wiederum die Bildung von Kohlensäure (Reaktion B) und deren Dissoziation zu
in das Meerwasser (Reaktion A). Das fördert wiederum die Bildung von Kohlensäure (Reaktion B) und deren Dissoziation zu  ⁻ und
⁻ und  (Reaktion C). Die erhöhte Konzentration von
(Reaktion C). Die erhöhte Konzentration von  -Ionen führt zu einer Absenkung des pH-Wertes des Meerwassers, was das Wasser saurer macht.
-Ionen führt zu einer Absenkung des pH-Wertes des Meerwassers, was das Wasser saurer macht.


In Reaktionsgleichung C fungiert Kohlensäure
1.2
Berechnung der aufgenommenen  -Stoffmenge
Für die Berechnung wird zunächst das aufgenommene
-Stoffmenge
Für die Berechnung wird zunächst das aufgenommene  -Volumen bestimmt:
-Volumen bestimmt:
 Weiterhin gilt:
Weiterhin gilt:
![\(\begin{array}[t]{rll}
n &=& \dfrac{V}{V_m} & \\[5pt]
&=& \dfrac{55\,\text{mL}}{24,5\,\text{L} \cdot \text{mol}^{-1}} & \\[5pt]
&=& \dfrac{55 \cdot 10^{-3}\,\text{L}}{24,5\,\text{L} \cdot \text{mol}^{-1}} & \\[5pt]
&\approx& 2,24 \cdot 10^{-3}\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/a8a698e472482359453f2d13949d62e5ee170884657cc829478513138f4ce49a?color=5a5a5a) Das Wasser nimmt bei diesem Experiment etwa
Das Wasser nimmt bei diesem Experiment etwa  die Stoffmenge an Kohlenstoffdioxid, die bei diesem Experiment vom Wasser aufgenommen wurde.
Berechnung der Konzentrationsänderung der Oxonium-Ionen
Für die Berechnung der Konzentration gilt:
die Stoffmenge an Kohlenstoffdioxid, die bei diesem Experiment vom Wasser aufgenommen wurde.
Berechnung der Konzentrationsänderung der Oxonium-Ionen
Für die Berechnung der Konzentration gilt:
 Es folgt:
Die Berechnung der Konzentrationsveränderung zeigt, dass sich bei dem Experiment die Konzentration der Oxonium-Ionen um
Es folgt:
Die Berechnung der Konzentrationsveränderung zeigt, dass sich bei dem Experiment die Konzentration der Oxonium-Ionen um  erhöht.
Bestimmung des Anteils des aufgenommenen
erhöht.
Bestimmung des Anteils des aufgenommenen  Das Volumen des Wassers in der Waschflasche beträgt
Das Volumen des Wassers in der Waschflasche beträgt  Um zu berechnen, wie viel
Um zu berechnen, wie viel  zur Änderung des
zur Änderung des  -Werts führt, wird zuerst die Gesamtzunahme an
-Werts führt, wird zuerst die Gesamtzunahme an  -lonen berechnet:
Da für die Bildung jedes Oxonium-Ions ein Kohlenstoffdioxid-Molekül weiter reagieren muss, gilt:
-lonen berechnet:
Da für die Bildung jedes Oxonium-Ions ein Kohlenstoffdioxid-Molekül weiter reagieren muss, gilt:
 Für den Anteil an aufgenommenem Kohlenstoffdioxid, das weiter reagiert, folgt:
Für den Anteil an aufgenommenem Kohlenstoffdioxid, das weiter reagiert, folgt:
![\(\begin{array}[t]{rll}
\text { Anteil }&=& \dfrac{n_2(CO_2)}{n_1(CO_2)} & \\[5pt]
&=& \dfrac{1,53 \cdot 10^{-5} \,\text{mol}}{2,24 \cdot 10^{-3}\,\text{mol}} & \\[5pt]
&\approx& 6,83 \cdot 10^{-3}
\end{array}\)](https://mathjax.schullv.de/4e86e8afe7427ad926f5c1495e635a8bbe625364fe0e039ca97251400fabb1b8?color=5a5a5a) Der Anteil entspricht etwa
Der Anteil entspricht etwa  des aufgenommenen
des aufgenommenen 
2
Reaktionsgleichung für die Dehydrierung von Perhydro-DBT


 Erhöhung der Wasserstoff-Ausbeute durch Temperatur- und Druckänderung
Nach dem Prinzip von LE CHATELIER wird ein System, das sich im Gleichgewicht befindet, einem äußeren Zwang so entgegenwirken, dass das Gleichgewicht wiederhergestellt wird.
Nach dem Prinzip wird bei einer Temperaturerhöhung die endotherme bevorzugt. Da die Dehydrierung von Perhydro-DBT endotherm ist, verschiebt sich das Gleichgewicht bei einer Temperaturerhöhung auf die Produktseite und steigert somit die Ausbeute an Wasserstoff.
Eine Druckerhöhung verschiebt das Gleichgewicht auf die Seite mit dem kleineren Volumen. Da dies hier die Produktseite ist, bewirkt eine Druckerhöhung ebenfalls die Verschiebung des Gleichgewichts auf die Produktseite, was die Ausbeute an Wasserstoff erhöht.
Berechnung der maximal freisetzbaren Masse an Wasserstoff
Mit der gegebenen Dichte und dem Volumen lässt sich zunächst die Masse von Perhydro-DBT berechnen:
Erhöhung der Wasserstoff-Ausbeute durch Temperatur- und Druckänderung
Nach dem Prinzip von LE CHATELIER wird ein System, das sich im Gleichgewicht befindet, einem äußeren Zwang so entgegenwirken, dass das Gleichgewicht wiederhergestellt wird.
Nach dem Prinzip wird bei einer Temperaturerhöhung die endotherme bevorzugt. Da die Dehydrierung von Perhydro-DBT endotherm ist, verschiebt sich das Gleichgewicht bei einer Temperaturerhöhung auf die Produktseite und steigert somit die Ausbeute an Wasserstoff.
Eine Druckerhöhung verschiebt das Gleichgewicht auf die Seite mit dem kleineren Volumen. Da dies hier die Produktseite ist, bewirkt eine Druckerhöhung ebenfalls die Verschiebung des Gleichgewichts auf die Produktseite, was die Ausbeute an Wasserstoff erhöht.
Berechnung der maximal freisetzbaren Masse an Wasserstoff
Mit der gegebenen Dichte und dem Volumen lässt sich zunächst die Masse von Perhydro-DBT berechnen:
![\(\begin{array}[t]{rll}
m &=& \rho \cdot V & \\[5pt]
&=& 0,91\,\text{kg} \cdot \text{L}^{-1} \cdot 1000\,\text{L} & \\[5pt]
&=& 910\,\text{kg}
\end{array}\)](https://mathjax.schullv.de/f638dc7be5663cd42f34c562c3766fda95099de92f053871fa6b3a151d32e77e?color=5a5a5a) Nun kann mithilfe der molaren Masse die Stoffmenge berechnet werden:
Nun kann mithilfe der molaren Masse die Stoffmenge berechnet werden:
![\(\begin{array}[t]{rll}
n &=& m \cdot M & \\[5pt]
&=& 910\,\text{kg} \cdot 290 \,\text{g} \cdot \text{mol}^{-1} & \\[5pt]
&=& 910\ 000 \,\text{g} \cdot 290 \,\text{g} \cdot \text{mol}^{-1} & \\[5pt]
&\approx& 3137,9\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/62392872e840f8d8624bd4c742f20845323f7f33fb13453ff8dcfe7ac431b098?color=5a5a5a) Weiterhin gilt:
Weiterhin gilt:
![\(\begin{array}[t]{rll}
n (H_2) &=& 9 \cdot n(\text{Perhydro−DBT}) & \\[5pt]
&=& 9 \cdot 3137,9\,\text{mol} & \\[5pt]
&\approx& 28241\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/56f448eec01a8e1727a758ce65bc5da9139f5da67e479780264d6a7ad8dbc365?color=5a5a5a) Für die Masse ergibt sich:
Für die Masse ergibt sich:
![\(\begin{array}[t]{rll}
m (H_2) &=& n \cdot M & \\[5pt]
&=& 28241\,\text{mol} \cdot 2,0\,\text{g} \cdot \text{mol}^{-1} & \\[5pt]
&=& 56482 \,\text{g} = 56,482\,\text{kg}
\end{array}\)](https://mathjax.schullv.de/c0e0025dff587ab33595d32088588500809a78a49bd43b9cf3722ea21caf6976?color=5a5a5a)