Aufgabe 1 – Ammoniak
1
Ammoniak  ist eines der wichtigsten Industriegase. Es wird unter anderem als Ausgangsstoff für die Herstellung von Düngern, Medikamenten, Sprengstoffen, Farben, Lacken und Kunststoffen verwendet.
ist eines der wichtigsten Industriegase. Es wird unter anderem als Ausgangsstoff für die Herstellung von Düngern, Medikamenten, Sprengstoffen, Farben, Lacken und Kunststoffen verwendet.
1.1
Beim HABER-BOSCH-Verfahren wird Ammoniak aus Wasserstoff und Stickstoff in einer Gleichgewichtsreaktion synthetisiert.
- Stelle die Reaktionsgleichung der Ammoniaksynthese auf.
- Begründe anhand der Reaktionsenthalpie, ob es sich bei der Ammoniaksynthese um eine exotherme oder eine endotherme Reaktion handelt.
- Leite aus Tabelle 1 die Bedingungen für eine hohe Ammoniakausbeute ab. Begründe diese anhand des Prinzips von LE CHATELIER.
(4 VP)
1.2
In einem Versuchsreaktor befinden sich vor Reaktionsbeginn  Stickstoff und
Stickstoff und  Wasserstoff. Bei einer Temperatur von
Wasserstoff. Bei einer Temperatur von  und einem Druck von
und einem Druck von  liegen im Gleichgewicht
liegen im Gleichgewicht  Ammoniak vor.
Ammoniak vor.
- Berechne die Stoffmengen an Wasserstoff und Stickstoff im Gleichgewicht.
- Zeige durch Berechnung, dass im Gleichgewicht
Ammoniak einem Stoffmengenanteil von
entsprechen.
(3 VP)
2
Die Verbrennungsenthalpie von Ammoniak soll experimentell bestimmt werden. Dazu wird Ammoniak in einem Verbrennungskalorimeter für Gase verbrannt (Abb. 1). In diesem werden  Trichlormethan
Trichlormethan  spez. Wärmekapazität
spez. Wärmekapazität  als Kalorimeterflüssigkeit genutzt.
als Kalorimeterflüssigkeit genutzt.
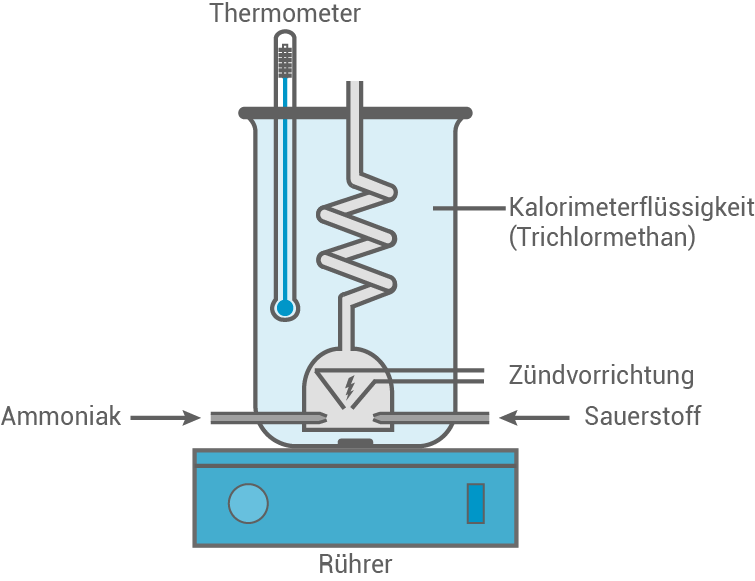

Abbildung 1: Verbrennungskalorimeter
2.1
In einem Experiment wird die Temperatur in Abhängigkeit von der Zeit gemessen. Nach Beginn der Messung wird eine Masse von  Ammoniak kontinuierlich mit Sauerstoff in das Reaktionsgefäß eingeleitet und verbrannt. Es wird folgender Temperaturverlauf aufgezeichnet:
Ammoniak kontinuierlich mit Sauerstoff in das Reaktionsgefäß eingeleitet und verbrannt. Es wird folgender Temperaturverlauf aufgezeichnet:
| Zeit in Minuten | Temperatur in |
|---|---|
| Zeit in Minuten | Temperatur in |
|---|---|
Tabelle 2: Temperaturverlauf bei der Verbrennung des Ammoniaks
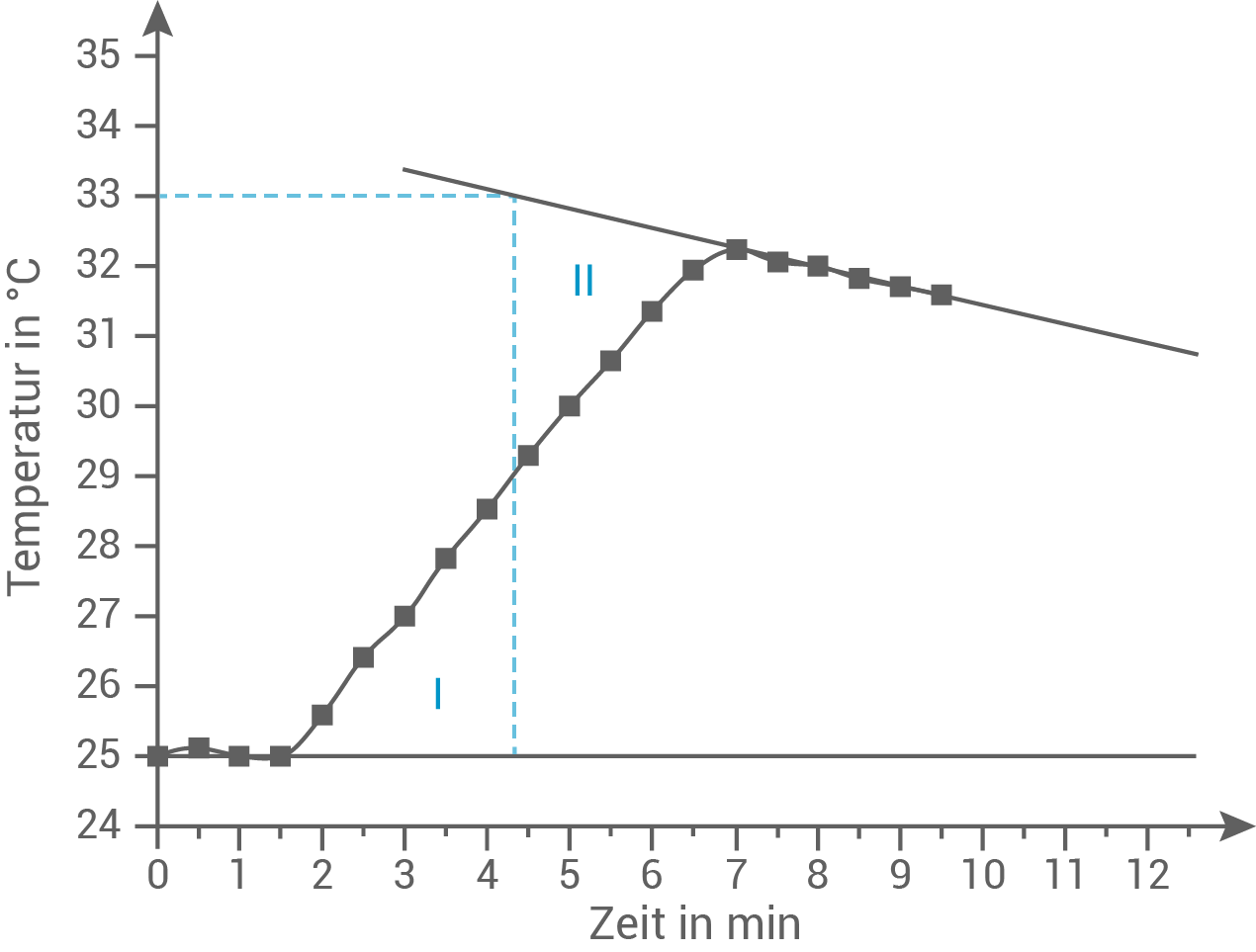
- Stelle die Daten aus Tabelle 2 in einem Diagramm dar.
- Ermittle anhand deiner Darstellung jeweils den Zeitpunkt, zu dem die Verbrennung von Ammoniak beginnt und zu dem sie endet.
- Begründe die fallende Temperatur in den letzten Minuten der Messung.
- Ermittle die vom Trichlormethan während der Verbrennung aufgenommene Wärmemenge
.
(7 VP)
2.2
In einem weiteren Experiment mit diesem Verbrennungskalorimeter wird bei der Verbrennung von  Ammoniak eine Wärmemenge
Ammoniak eine Wärmemenge  bestimmt. Das Ergebnis des Experiments soll anhand von Literaturwerten überprüft werden.
bestimmt. Das Ergebnis des Experiments soll anhand von Literaturwerten überprüft werden.
- Berechne die Reaktionsenthalpie für die Verbrennung von
Ammoniak ausgehend von der experimentell bestimmten Wärmemenge
(Fall A).
- Berechne die Reaktionsenthalpie für die Verbrennung von
Ammoniak unter Verwendung der thermodynamischen Daten aus Anlage 4 (Fall B).
Ammoniak reagiert bei der Verbrennung vereinfacht nach folgender Gleichung: - Überprüfe qualitativ, ob die folgenden Aussagen die Abweichung zwischen Fall A und Fall B erklären können:
a)Es wurden unwissentlich mehr als
Trichlormethan in die Apparatur gegeben.
b)Ein Teil des entstehenden Wassers ist nicht kondensiert.
(6 VP)
(20 VP)
1.1
Reaktionsgleichung der Ammoniaksynthese


 Reaktionsenthalpie
Die Tabelle mit den thermodynamischen Daten zeigt für die Ammoniak-Bildung unter Standardbedingungen eine Reaktionsenthalpie von
Reaktionsenthalpie
Die Tabelle mit den thermodynamischen Daten zeigt für die Ammoniak-Bildung unter Standardbedingungen eine Reaktionsenthalpie von  Das negative Vorzeichen zeigt, dass es sich um eine exotherme Reakton handelt.
Bedingungen für eine hohe Ammoniakausbeute
Da es sich um eine Gleichgewichtsreaktion handelt, gilt das Prinzip von LE CHATELIER:
Das negative Vorzeichen zeigt, dass es sich um eine exotherme Reakton handelt.
Bedingungen für eine hohe Ammoniakausbeute
Da es sich um eine Gleichgewichtsreaktion handelt, gilt das Prinzip von LE CHATELIER:
Die Tabelle zeigt:
Spalte mit  Die Synthese von Ammoniak bei einem Bar und verschiedenen Temperaturen zeigt, je höher die Temperatur wird, desto kleiner ist der prozentuale Volumenanteil des Produktes.
Zeile mit
Die Synthese von Ammoniak bei einem Bar und verschiedenen Temperaturen zeigt, je höher die Temperatur wird, desto kleiner ist der prozentuale Volumenanteil des Produktes.
Zeile mit  Die Synthese von Ammoniak bei
Die Synthese von Ammoniak bei  und verschiedenen Drücken zeigt, je höher der Druck, desto höher der Produktanteil.
Für eine hohe Ausbeute muss die Ammoniak-Synthese also bei möglichst niedrigen Temperaturen und möglichst hohen Drücken durchgeführt werden.
und verschiedenen Drücken zeigt, je höher der Druck, desto höher der Produktanteil.
Für eine hohe Ausbeute muss die Ammoniak-Synthese also bei möglichst niedrigen Temperaturen und möglichst hohen Drücken durchgeführt werden.
| Druckänderung |
|---|
| Übt man auf eine sich im Gleichgewicht befindliche Reaktion durch Druckänderung einen Zwang aus, weicht das System so aus, dass bei einer Erhöhung die volumenverkleinernde Reaktion gefördert wird und umgekehrt. |
| Die Reaktionsgleichung zeigt links vier Mol Gas und rechts zwei Mol Gas. Damit nimmt bei der Ammoniak-Synthese das Gesamtvolumen ab und eine Druckerhöhung führt zur Gleichgewichtsverschiebung auf die Seite der Produkte. |
| Temperaturänderung |
|---|
| Übt man auf eine sich im Gleichgewicht befindliche Reaktion durch Temperaturänderung einen Zwang aus, weicht das System so aus, dass bei einer Erhöhung die endotherme Reaktion gefördert wird und umgekehrt. |
| Die Ammoniak-Synthese ist exotherm. Damit führt eine Temperaturerhöhung zu einer Gleichgewichtsverschiebung auf die Seite der Produkte. |
1.2
Stoffmengen an Wasserstoff und Stickstoff im Gleichgewicht
Die Aufgabenstellung zeigt, dass nach Gleichgewichtseinstellung  Ammoniak vorliegen:
Ammoniak vorliegen:


 Demnach betragen die Gleichgewichtsstoffmengen:
Demnach betragen die Gleichgewichtsstoffmengen:
![\(\begin{array}[t]{rll}
n_{N_2}&=&(1 - 0,8925) \,\text{mol} & \\[5pt]
&=& 0,1075\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/aa93d0e75c8beb695704b57c94baa505874b6ad21504e9522e9dcfcb0dc319f2?color=5a5a5a)
![\(\begin{array}[t]{rll}
n_{H_2}&=&(3 - 3 \cdot 0,8925) \,\text{mol} & \\[5pt]
&=& 0,3225\,\text{mol}
\end{array}\)](https://mathjax.schullv.de/64be96c36c86e154d77b58ede4fd2a9b75ebd54298e52b4d0340baf7d8b35d1e?color=5a5a5a) Stoffmengenanteil von Ammoniak im Gleichgewicht
In einer Mischung lässt sich für eine Komponente A der Stoffmengenanteil
Stoffmengenanteil von Ammoniak im Gleichgewicht
In einer Mischung lässt sich für eine Komponente A der Stoffmengenanteil  als den Quotienten aus der Stoffmenge A und der Gesamtstoffmenge aller Mischungsbestandteile definieren:
als den Quotienten aus der Stoffmenge A und der Gesamtstoffmenge aller Mischungsbestandteile definieren:
 =
=  Der Stoffmengenanteil
Der Stoffmengenanteil  von Ammoniak im Gleichgewicht ist also:
Zum Schluss wird das Ergebnis mit
von Ammoniak im Gleichgewicht ist also:
Zum Schluss wird das Ergebnis mit  multipliziert und es ergibt sich ein Stoffmengenanteil von
multipliziert und es ergibt sich ein Stoffmengenanteil von 

2.1
Grafische Darstellung der kalorimetrischen Daten
 Beginn und Ende der Ammoniak-Verbrennung
Die Tabellendaten zeigen, dass die Temperatur im Kalorimeter ab zwei Minuten anfängt zu steigen. Der Beginn der Verbrennung fand demnach zwischen
Beginn und Ende der Ammoniak-Verbrennung
Die Tabellendaten zeigen, dass die Temperatur im Kalorimeter ab zwei Minuten anfängt zu steigen. Der Beginn der Verbrennung fand demnach zwischen  und
und  Minuten statt.
Nach sieben Minuten wird das Maximum erreicht. Das Ende der Verbrennung liegt zeitlich kurz davor, was etwa
Minuten statt.
Nach sieben Minuten wird das Maximum erreicht. Das Ende der Verbrennung liegt zeitlich kurz davor, was etwa  Minuten entspricht.
Begründung der fallenden Temperatur
Idealen Kalorimeter geben die gesamte Verbrennungswärme an die Kalorimeterflüssigkeit ab, wodurch kein Wärmeverlust stattfindet. In der Realität nimmt das Kalorimeter jedoch immer eine gewisse Wärmemenge auf. Folglich nimmt die Temperatur der Kalorimeterflüssigkeit nach Ende des Experiments langsam ab.
Ermittlung der von Trichlormethan aufgenommenen Wärmemenge
Um die während der Verbrennung aufgenommene Wärmemenge zu bestimmen, wird die Temperaturkurve aus dem Versuch auf Basis der Flächengleichheit ausgewertet:
Minuten entspricht.
Begründung der fallenden Temperatur
Idealen Kalorimeter geben die gesamte Verbrennungswärme an die Kalorimeterflüssigkeit ab, wodurch kein Wärmeverlust stattfindet. In der Realität nimmt das Kalorimeter jedoch immer eine gewisse Wärmemenge auf. Folglich nimmt die Temperatur der Kalorimeterflüssigkeit nach Ende des Experiments langsam ab.
Ermittlung der von Trichlormethan aufgenommenen Wärmemenge
Um die während der Verbrennung aufgenommene Wärmemenge zu bestimmen, wird die Temperaturkurve aus dem Versuch auf Basis der Flächengleichheit ausgewertet:
![\(\begin{array}[t]{rll}
Q&=& C_{CHCl_3} \cdot M_{CHCl_3} \cdot \Delta T& \\[5pt]
&=& 0,95 \,\text{J} \cdot \text{g}^{-1} \cdot \text{K}^{-1} \cdot 1000\,\text{g} \cdot 8\,\text{K} & \\[5pt]
&=& 7600 \,\text{J}
\end{array}\)](https://mathjax.schullv.de/4b64fe1bd5467706386867aeb4b7fac4af698fca61caa96679c9f8d1f5283005?color=5a5a5a)

- Anlegen von Ausgleichsgeraden durch die Daten jeweils zu Beginn und Ende der Messung.
- Ziehen einer Linie, die diese Geraden und die Messkurve schneidet. Dabei sollen die eingeschlossenen Flächen I und II gleich groß sein
- Die Schnittpunkte der Ausgleichsgeraden mit diesen Linien ergeben die Anfangs-bzw. Endtemperatur.
- Die maximale Temperaturdifferenz ergibt sich aus der Differenz der
-Werte;
hier:oder
2.2
Reaktionsenthalpie mit der experimentell bestimmten Wärmemenge  Folgende Werte sind gegeben:
Folgende Werte sind gegeben:


![\(\begin{array}[t]{rll}
n_{NH_3}&=& \dfrac{0,5 \,\text{g}}{17 \,\text{g}\cdot \text{mol}^{-1} } & \\[5pt]
&\approx& 0,0294
\end{array}\)](https://mathjax.schullv.de/b03275fdec4eaaea614d9864ebe7f2943a4662a1cfec95e30ecd3aaf2ce2477c?color=5a5a5a) Daraus folgt:
Daraus folgt:
![\(\begin{array}[t]{rll}
\Delta_cH_{NH_3}&=& -\dfrac{Q}{n_{NH_3}} & \\[5pt]
&=& -\dfrac{9,5 \,\text{kJ}}{0,0294 \,\text{mol}} & \\[5pt]
&\approx& -323,1 \,\text{kJ} \cdot \text{mol}^{-1}
\end{array}\)](https://mathjax.schullv.de/eae0fee5719ea8996b6f524ccf63ad8b659cb10e10f18d2623cc05c3c31e5ef2?color=5a5a5a) Reaktionsenthalpie mit den thermodynamischen Daten
Für die Berechnung gilt:
Aus der Reaktionsgleichung ergibt sich damit:
Zuletzt muss die Verbrennungsenthalpie auf ein Mol Ammoniak bezogen werden:
Reaktionsenthalpie mit den thermodynamischen Daten
Für die Berechnung gilt:
Aus der Reaktionsgleichung ergibt sich damit:
Zuletzt muss die Verbrennungsenthalpie auf ein Mol Ammoniak bezogen werden:
![\(\begin{array}[t]{rll}
\Delta_cH_{NH_3}&=& \dfrac{-1532 \,\text{kJ} \cdot \,\text{mol}^{-1}}{4}& \\[5pt]
&=& -383 \,\text{kJ} \cdot \,\text{mol}^{-1}
\end{array}\)](https://mathjax.schullv.de/a75660a231e4c850492591cbf282f99310f08a4bf79119f13126a4dc9498f412?color=5a5a5a) Überprüfung der Aussagen
Überprüfung der Aussagen
a)
Es wurden unwissentlich mehr als  Trichlormethan in die Apparatur gegeben.
Wenn im Kalorimeter mehr als die in der Rechnung eingesetzten
Trichlormethan in die Apparatur gegeben.
Wenn im Kalorimeter mehr als die in der Rechnung eingesetzten  Trichlormethan enthalten war, wäre der berechnete Wert für
Trichlormethan enthalten war, wäre der berechnete Wert für  zu klein und würde damit die Abweichung zwischen Fall A und Fall B erklären.
zu klein und würde damit die Abweichung zwischen Fall A und Fall B erklären.
b)
Ein Teil des entstehenden Wassers ist nicht kondensiert.
Phasenübergänge von gasförmigem zu flüssigem Wasser setzen Kondensationswärme frei. Wenn die gesamte freigesetzte Wassermenge nicht im Kalorimeter kondensieren würde, wäre die gemessene Wärmemenge zu klein. Damit würde sich für das Experiment der (betragsmäßig) zu kleine Wert der Reaktionsenthalpie erklären lassen.