C1 Lebensmittelverpackungen
Lebensmittel werden zum Verkauf, zum Transport und um sie vor dem Verderben zu schützen in verschiedene Materialien verpackt.
1
Ein biologisch abbaubarer Kunststoff, der in Lebensmittelverpackungen Verwendung findet, ist PBAT (Polybutylenadipat-terephthalat). Ein Strukturformelausschnitt ist in Abbildung 1 dargestellt:
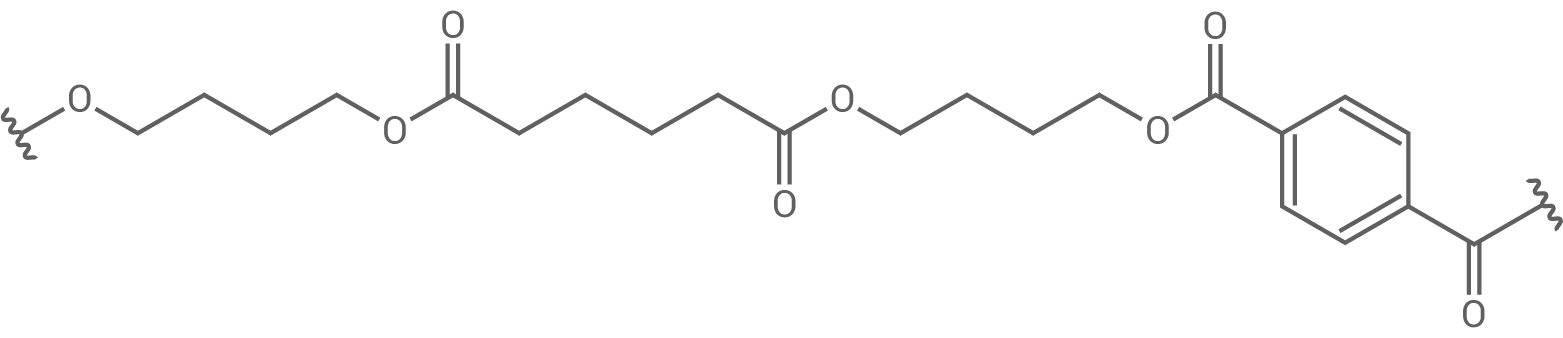

Abb. 1: Strukturformelausschnitt aus einem PBAT-Molekül
1.1
Eines der Monomere zur Synthese von PBAT ist Terephthalsäure. Diese lässt sich aus nachwachsenden Rohstoffen nach dem in Abbildung 2 dargestellten Schema herstellen:
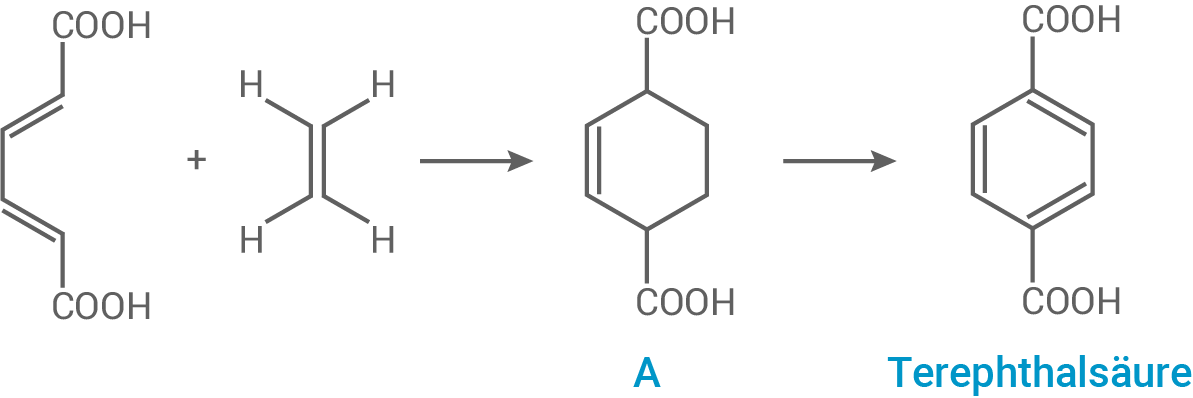

Abb. 2: Reaktionsschema zur Herstellung von Terephthalsäure
1.1.1
Vergleiche den räumlichen Bau der ringförmigen Molekülteile von Molekül A und dem Terephthalsäure-Molekül.
(5 BE)
1.1.2
Ermittle die Strukturformeln und Namen der zwei weiteren Monomere neben Terephthalsäure, aus denen sich PBAT synthetisieren lässt. Ordne den Kunststoff PBAT (Abb. 1) aufgrund der Verknüpfung der Monomer-Bausteine einer Kunststoffklasse zu.
(5 BE)
1.1.3
Ethen für die Synthese von Terephthalsäure soll aus Graphit (Kohlenstoff) und Wasserstoff synthetisiert werden. Die Reaktionsenthalpie für diese Reaktion beträgt  Tabelle 1 zeigt die Standardentropien der beteiligten Stoffe:
Tabelle 1 zeigt die Standardentropien der beteiligten Stoffe:
| Stoff | Standardentropie in |
|---|---|
| Graphit |
|
| Wasserstoff |
|
| Ethen |
Tab. 1: Standardentropien der an der Ethen-Synthese beteiligten Stoffe
Formuliere die Reaktionsgleichung für die Synthese von Ethen aus Graphit und Wasserstoff. Beurteile mithilfe der Gibbs-Helmholtz-Gleichung, ob diese Reaktion freiwillig ablaufen kann.
(5 BE)
1.2
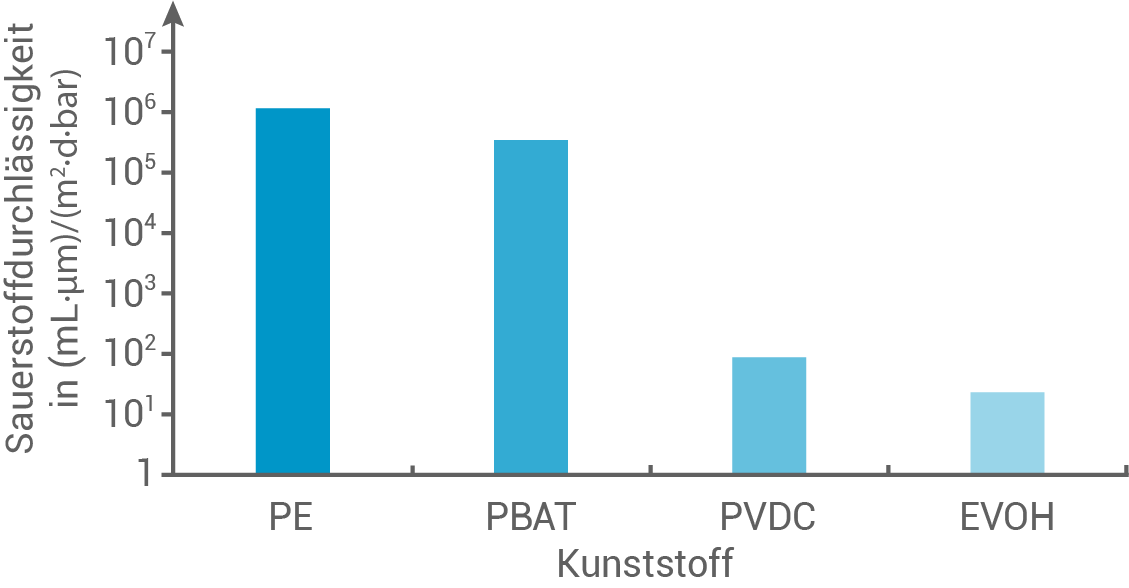
Kunststoffverpackungen für Milch sollten sowohl für Wasserdampf als auch für Sauerstoff undurchlässig sein, um das Verderben der Milch zu verlangsamen. Tabelle 2 und Abbildung 3 zeigen die Wasserdampf- und Sauerstoffdurchlässigkeit verschiedener Kunststoffe:
| Kunststoff | Wasserdampfdurchlässigkeit in |
|---|---|
| PE | |
| PBAT | |
| PVDC | |
| EVOH |
Tab. 2: Wasserdampfdurchlässigkeit verschiedener Kunststoffe
nach: https://www.degruyter.com/document/do/10.1515/npprj-2020-0042/ asset/graphic/j_npprj-2020-0042_fig_002.jpg, zuletzt aufgerufen am 28.10. 2021

Abb. 3: Sauerstoffdurchlässigkeit verschiedener Kunststoffe
verändert nach: https://www.degruyter.com/document/do/10.1515/npprj-2020-0042/asset/ graphic/j_npprj-2020-0042_fig_002.jpg, zuletzt aufgerufen am 28.10. 2021
(1 BE)
1.2.1
Zeichne einen charakteristischen Strukturformelausschnitt aus einem Polyethen-Molekül. Vergleiche die Wasserdampfdurchlässigkeit von PE (Polyethen) und PBAT (Abb. 1) und begründe diese anhand der Molekülstrukturen.
(6 BE)
1.2.2
Diskutiere anhand der in Aufgabe 1.2 genannten Kriterien und mithilfe von Tabelle 2 und Abbildung 3 die Eignung von PVDC und EVOH für Milchkartons.
(5 BE)
1.2.3
Die Sauerstoffdurchlässigkeit von Kunststoffen hängt hauptsächlich von zwei Faktoren ab: der Stärke der Wechselwirkungen und den Abständen zwischen den Polymerketten.
Zur Verminderung der Sauerstoffdurchlässigkeit eines Kunststoffs wird dieser "verstreckt", d. h. er wird in die Länge gezogen, wodurch sich die Anordnung der Polymerketten verändert.
Stelle eine Hypothese auf, mit der die Verminderung der Sauerstoffdurchlässigkeit des Kunststoffs beim Verstrecken erklärt werden kann.
Zur Verminderung der Sauerstoffdurchlässigkeit eines Kunststoffs wird dieser "verstreckt", d. h. er wird in die Länge gezogen, wodurch sich die Anordnung der Polymerketten verändert.
Stelle eine Hypothese auf, mit der die Verminderung der Sauerstoffdurchlässigkeit des Kunststoffs beim Verstrecken erklärt werden kann.
(4 BE)
2
Um das Austrocknen zu verhindern, können Lebensmittel mit Bienenwachs beschichtet werden. Dieses Wachs besteht aus verschiedenen Verbindungen. Der größte Anteil mit ca.  entfällt dabei auf Myricylpalmitat (Abb. 4):
entfällt dabei auf Myricylpalmitat (Abb. 4):
 Aufgrund des hohen Preises versuchen Betrüger, Bienenwachs durch das deutlich billigere Paraffin zu ersetzen. Dabei handelt es sich um ein Gemisch aus verschiedenen n-Alkanen mit langkettigen Molekülen mit molaren Massen zwischen
Aufgrund des hohen Preises versuchen Betrüger, Bienenwachs durch das deutlich billigere Paraffin zu ersetzen. Dabei handelt es sich um ein Gemisch aus verschiedenen n-Alkanen mit langkettigen Molekülen mit molaren Massen zwischen  und
und 

Abb. 4: Strukturformel von Myricylpalmitat
2.1
In einem Experiment soll Bienenwachs von Paraffin unterschieden werden. Dazu wird je eine Probe von Bienenwachs und von Paraffin mit geringen Mengen an Natronlauge versetzt und anschließend unter Rühren erhitzt. Bei einem Ansatz ändert sich der pH-Wert des Gemischs, beim anderen nicht.
Erkläre die unterschiedlichen Beobachtungen unter Verwendung einer Reaktionsgleichung. Nicht an der Reaktion beteiligte Molekülabschnitte können abgekürzt werden.
Erkläre die unterschiedlichen Beobachtungen unter Verwendung einer Reaktionsgleichung. Nicht an der Reaktion beteiligte Molekülabschnitte können abgekürzt werden.
(6 BE)
2.2
Eine weitere Möglichkeit zur Unterscheidung von Bienenwachs und Paraffin besteht in der Bestimmung der molaren Massen.
Berechne die Anzahl der Kohlenstoff-Atome pro Molekül in einem Paraffin mit einer molaren Masse von
Berechne die Anzahl der Kohlenstoff-Atome pro Molekül in einem Paraffin mit einer molaren Masse von
(4 BE)
(40 BE)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1.1
Vergleich der beiden Moleküle
| Molekül A | Terephthalsäure-Molekül |
|---|---|
| Sechsring | Sechsring |
| einzelne isolierte Doppelbindung |
drei konjugierte Doppelbindungen |
| Variation der Bindungslängen |
Bindungslängen gleich, da vollständige Delokalisation der |
| Kohlenstoffatome der Doppelbindung liegen mit ihren Anhängseln in einer Ebene; die übrigen Kohlenstoffatome im Ring bilden gemäß dem VSEPR-Modell einen Tetraeder |
alle sechs Kohlenstoffatome im Ring liegen mit ihren Anhängseln in einer Ebene |
1.1.2
Strukturformeln und Namen
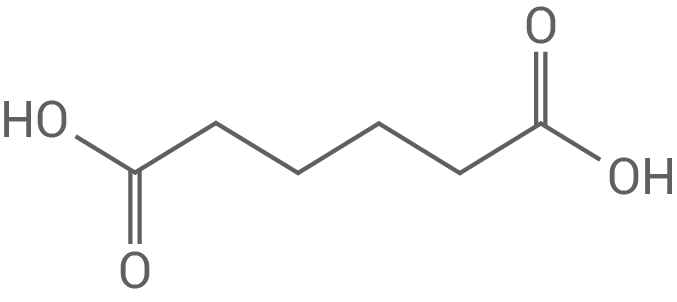
Folgende beiden Monomere sind auch an der Polymer-Synthese beteiligt:
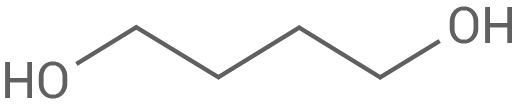
 Zuordnung einer Kunststoffklasse
Die Monomere sind durch Esterbindungen verknüpft, weswegen das Polymer PBAT zur Kunststoffklasse der Polyester zählt.
Zuordnung einer Kunststoffklasse
Die Monomere sind durch Esterbindungen verknüpft, weswegen das Polymer PBAT zur Kunststoffklasse der Polyester zählt.

Butan-1,4-diol

Hexan-1,6-disäure
1.1.3
Formulierung der Reaktionsgleichung


 Beurteilung der Freiwilligkeit
Eine Reaktion läuft freiwillig ab, wenn die freie Enthalpie kleiner null ist
Beurteilung der Freiwilligkeit
Eine Reaktion läuft freiwillig ab, wenn die freie Enthalpie kleiner null ist 
Dafür wird die Gibbs-Helmholtz-Gleichung betrachtet: Die Reaktionsenthalpie von
Die Reaktionsenthalpie von  zeigt, dass die Reaktion endotherm ist.
Weiterhin ergibt sich für die Entropieänderung:
Im Verlauf der Reaktion nimmt die Entropie, das Maß der Unordnung, ab. Gemäß der Gibbs-Helmholtz-Gleichung kann der Wert für
zeigt, dass die Reaktion endotherm ist.
Weiterhin ergibt sich für die Entropieänderung:
Im Verlauf der Reaktion nimmt die Entropie, das Maß der Unordnung, ab. Gemäß der Gibbs-Helmholtz-Gleichung kann der Wert für  bei keiner Temperatur kleiner als null sein, womit die Reaktion nicht spontan abläuft.
bei keiner Temperatur kleiner als null sein, womit die Reaktion nicht spontan abläuft.
Dafür wird die Gibbs-Helmholtz-Gleichung betrachtet:
1.2.1
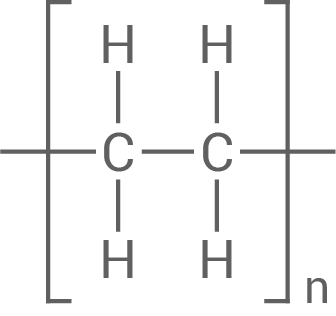
Charakteristischer Strukturformelausschnitt von Polyethen (PE)
 Vergleich der Wasserdampfdurchlässigkeit
Die Bindungen in Polyethen sind alle unpolar, weswegen das Polymer stark hydrophob ist. Da Wasser-Moleküle polare Atombindungen aufweisen, lässt eine PE-Verpackung nur sehr wenig Wasserdampf durch.
Im Gegensatz dazu enthält das PBAT-Polymer viele polare Carbonyl-Gruppen. Dadurch ist das Polymer deutlich hydrophiler als Polyethen, und Verpackungen aus diesem Polymer zeigen eine höhere Wasserdampfdurchlässigkeit.
Vergleich der Wasserdampfdurchlässigkeit
Die Bindungen in Polyethen sind alle unpolar, weswegen das Polymer stark hydrophob ist. Da Wasser-Moleküle polare Atombindungen aufweisen, lässt eine PE-Verpackung nur sehr wenig Wasserdampf durch.
Im Gegensatz dazu enthält das PBAT-Polymer viele polare Carbonyl-Gruppen. Dadurch ist das Polymer deutlich hydrophiler als Polyethen, und Verpackungen aus diesem Polymer zeigen eine höhere Wasserdampfdurchlässigkeit.

1.2.2
Diskussion der Eignung von PVDC und EVOH
Abbildung 3 zeigt, dass EVOH (Ethylenvinylalkohol) in Verpackungen eine geringere Sauerstoffdurchlässigkeit aufweist als PVDC (Polyvinylidenchlorid). Allerdings ist PVDC für Milchkartons besser geeignet, da das EVOH gemäß Tabelle 2 eine signifikant höhere Wasserdampfdurchlässigkeit als PVDC hat.
1.2.3
Hypothese zur Verminderung der Sauerstoffdurchlässigkeit
Durch das "Verstrecken" der Moleküle richten sich die Polymerketten parallel zueinander aus, wodurch der Abstand zwischen den Molekülen sinkt und sie sich besser aneinander anlagern können. Gleichzeitig verstärken sich die zwischenmolekularen Kräfte mit zunehmender Länge der gestreckten Moleküle. Daher führt das "Verstrecken" von Kunststoffen zu einer Verringerung der Sauerstoffdurchlässigkeit.
2.1
Erklärung der unterschiedlichen Beobachtungen
Bei der Versetzung von Bienenwachs mit Natronlauge wird die Estergruppe hydrolysiert:
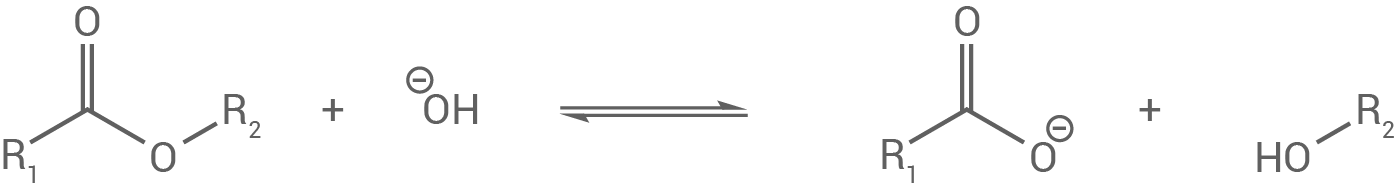 Hierbei werden die Hydroxyl-Ionen der Natronlauge aufgebraucht, wodurch der pH-Wert der Lösung abnimmt.
Hierbei werden die Hydroxyl-Ionen der Natronlauge aufgebraucht, wodurch der pH-Wert der Lösung abnimmt.
Paraffin, ein Gemisch aus n-Alkanen, reagiert nicht mit Natronlauge und bewirkt somit einen konstanten pH-Wert der Lösung.

Paraffin, ein Gemisch aus n-Alkanen, reagiert nicht mit Natronlauge und bewirkt somit einen konstanten pH-Wert der Lösung.
2.2
Berechnung der Anzahl der Kohlenstoff-Atome
Paraffine bestehen aus n-Alkanen mit der allgemeinen Summenformel 
Mit der gegebenen Molekülmasse und den einzelnen molaren Massen aus dem PSE kann die Anzahl der Kohlenstoff-Atome berechnet werden: Die Anzahl der Kohlenstoff-Atome pro Molekül in einem Paraffin beträgt
Die Summenformel lautet daher: Probe:
Probe:
Mit der gegebenen Molekülmasse und den einzelnen molaren Massen aus dem PSE kann die Anzahl der Kohlenstoff-Atome berechnet werden: Die Anzahl der Kohlenstoff-Atome pro Molekül in einem Paraffin beträgt
Die Summenformel lautet daher: