B2 Mais
Mais nimmt mit über 1,17 Mrd. Tonnen (2020) bei der Weltgetreideernte vor Weizen und Reis den ersten Platz ein und ist damit das am häufigsten angebaute Getreide.
1
Die gelbe Farbe des Maiskorns stammt vom Farbstoff Zeaxanthin. Dieser liegt im Maiskorn in der Regel einfach oder zweifach mit Fettsäuren verestert vor. Aus dem fetthaltigen Keim des Maiskorns kann das farblose und geschmacksneutrale Maiskeimöl gewonnen werden. Durch Zugabe von β-Carotin wird die vom Verbraucher erwartete gelbe Farbe des Öls erreicht. Die Haltbarkeit des Öls wird durch Zugabe von farblosem  -Tocopherol (Vitamin E) verbessert.
-Tocopherol (Vitamin E) verbessert.
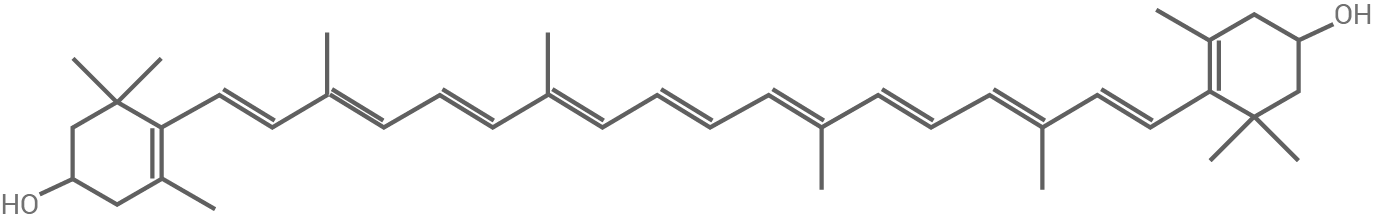
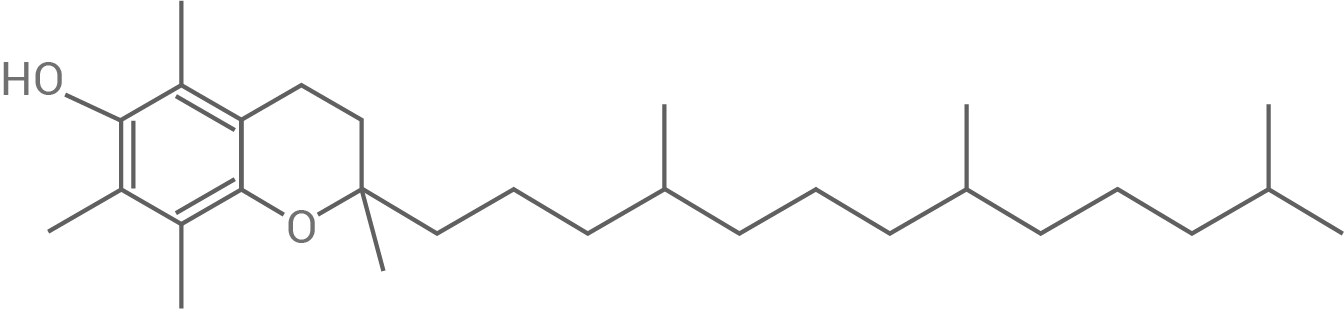
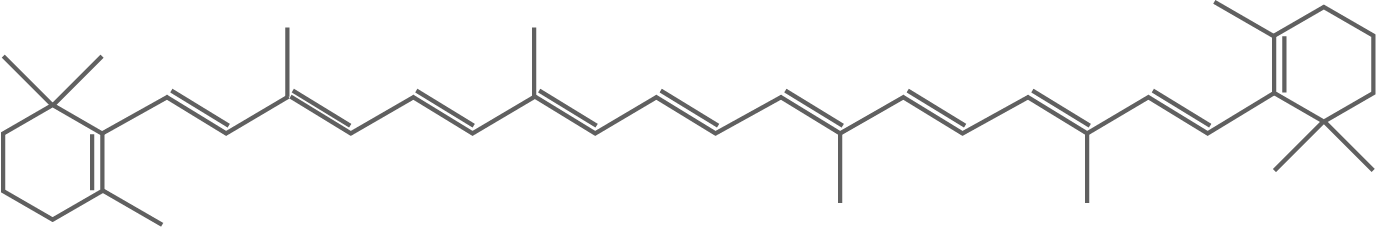
Erkläre den Zusammenhang zwischen Molekülstruktur und Farbigkeit und ordne die Strukturformeln A bis C den Stoffen  -Carotin,
-Carotin,  -Tocopherol und Zeaxanthin begründet zu.
-Tocopherol und Zeaxanthin begründet zu.
|
|
|
|
|
Tab. 1: Strukturformeln ausgewählter Inhalts- und Zusatzstoffe von Maiskeimöl
(8 BE)
2
Der Maisbeulenbrand (Ustilago maydis) ist ein Pilz, der den Kulturmais schädigen kann, aber auch in der industriellen Biotechnologie eine wichtige Rolle spielt. Mit seiner Hilfe können vielfältig einsetzbare Chemikalien wie Ustilaginsäure A und D-Mannose produziert werden.
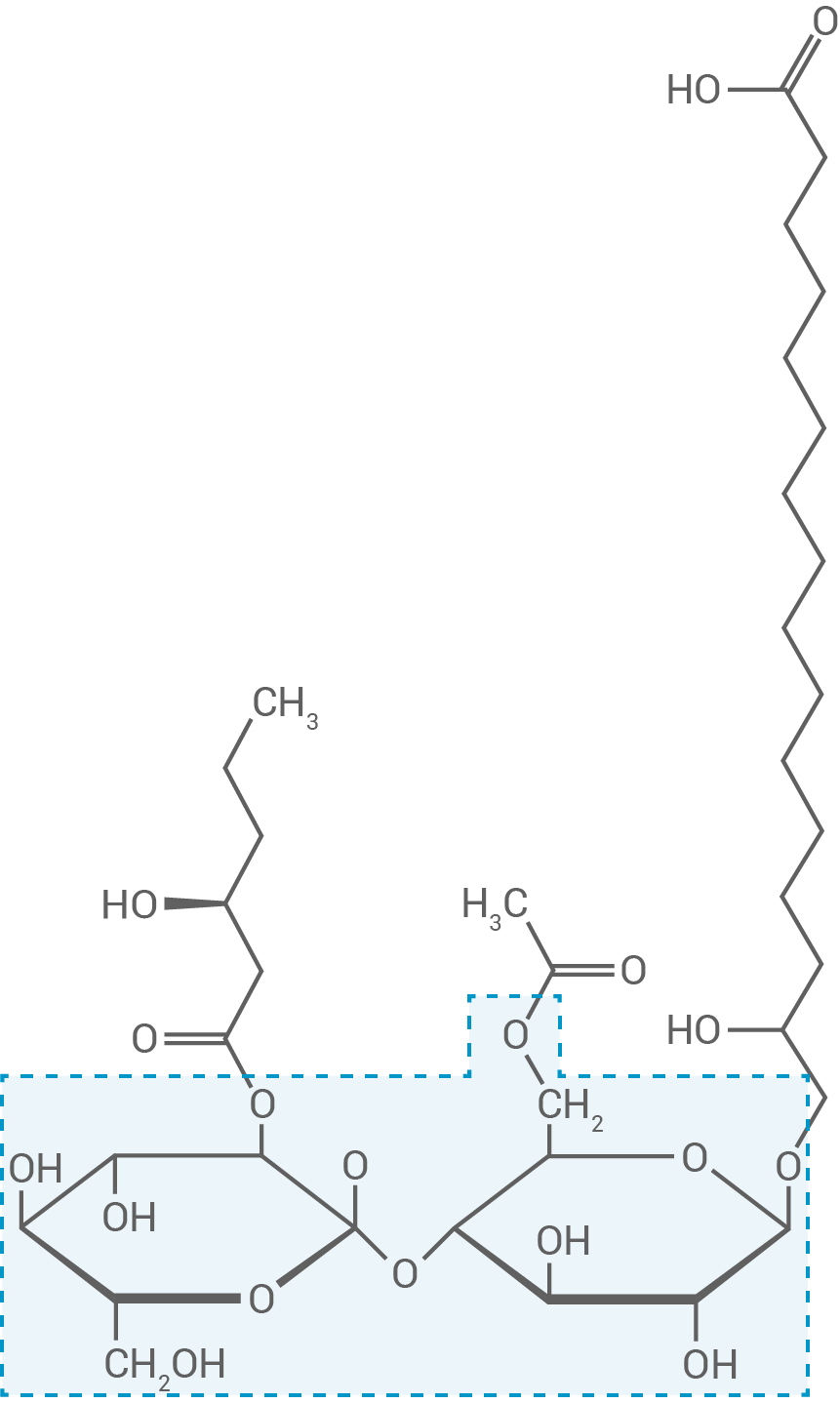

Abb. 1: Strukturformel von Ustilaginsäure A
nach: Geiser, E., Wiebach, V., Wierckx, N. & Blank, L. M. (2014). Prospecting the biodiversity of the fungal family Ustilaginaceae for the production of value-added chemicals. Fungal Biology and Biotechnology, 1(1)
2.1
Ustilaginsäure A kommt aufgrund ihrer Eigenschaften in der Lebensmittelindustrie sowie der pharmazeutischen und chemischen Industrie als Tensid zum Einsatz.
2.1.1
Begründe ausgehend von der Strukturformel der Ustilaginsäure A deren Eignung als Tensid.
(4 BE)
2.1.2
Gib den Namen des Disaccharids an, das dem markierten Ausschnitt in Abbildung 1 zugrunde liegt, und nennen Sie den Typ der glykosidischen Bindung zwischen den beiden Monosaccharid-Bausteinen.
(4 BE)
2.2
D-Mannose unterscheidet sich von D-Glucose durch die Stellung der Hydroxygruppe am  -Atom.
-Atom.
2.2.1
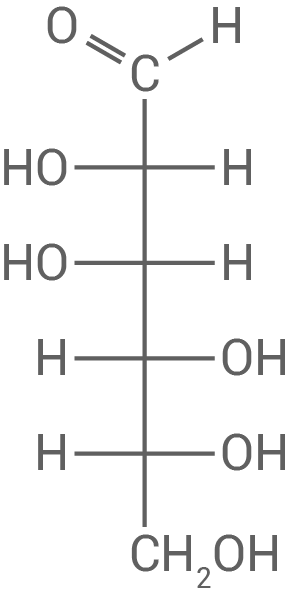
Zeichne ein D-Mannose-Molekül in der FISCHER-Projektion.
Beschreibe die Durchführung der FEHLING-Probe mit Ustilaginsäure A und D-Mannose und erklären Sie die zu erwartenden Versuchsergebnisse.
Beschreibe die Durchführung der FEHLING-Probe mit Ustilaginsäure A und D-Mannose und erklären Sie die zu erwartenden Versuchsergebnisse.
(7 BE)
2.2.2
Bei polarimetrischen Messungen über einen Zeitraum von  Stunden können für Lösungen der beiden Anomere der D-Mannopyranose bei gleichen Konzentrationen folgende Drehwinkel bestimmt werden:
Stunden können für Lösungen der beiden Anomere der D-Mannopyranose bei gleichen Konzentrationen folgende Drehwinkel bestimmt werden:
Ergänze die Tabelle um die zu erwartenden Werte für die Drehwinkel bei  Zeichne auf Basis der Tabelle ein Diagramm zur Abhängigkeit des Drehwinkels von der Zeit und begründe die Messergebnisse mithilfe von Strukturformeln.
Zeichne auf Basis der Tabelle ein Diagramm zur Abhängigkeit des Drehwinkels von der Zeit und begründe die Messergebnisse mithilfe von Strukturformeln.
| Versuchs-ansatz ausgehend von | Dreh-winkel der Lösung zum Zeitpunkt |
Dreh-winkel der Lösung zum Zeitpunkt |
Dreh-winkel der Lösung zum Zeitpunkt |
|---|---|---|---|
Tab. 2: Bestimmung der Drehwinkel von Lösungen der D-Mannopyranose-Anomere
(8 BE)
3
Maltodextrin ist ein wasserlösliches Kohlenhydratgemisch, das durch enzymatische Hydrolyse von Maisstärke hergestellt wird.
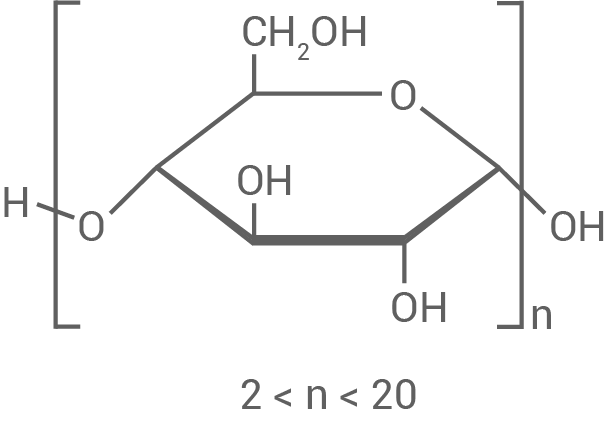 Maltodextrin kann zum Betrieb von sogenannten Zuckerbatterien eingesetzt werden. Diese erzeugen elektrischen Strom durch die Reaktion von Maltodextrin mit Sauerstoff. Der Prozess, bei dem Kohlenstoffdioxid und Wasser entstehen, läuft in saurer Lösung ab. Da die Maltodextrin- Moleküle vor der Redoxreaktion in Monosaccharid-Bausteine gespalten werden, setzt man beim Aufstellen der Redoxteilgleichung als Formel für das Edukt
Maltodextrin kann zum Betrieb von sogenannten Zuckerbatterien eingesetzt werden. Diese erzeugen elektrischen Strom durch die Reaktion von Maltodextrin mit Sauerstoff. Der Prozess, bei dem Kohlenstoffdioxid und Wasser entstehen, läuft in saurer Lösung ab. Da die Maltodextrin- Moleküle vor der Redoxreaktion in Monosaccharid-Bausteine gespalten werden, setzt man beim Aufstellen der Redoxteilgleichung als Formel für das Edukt  ein.
ein.
Formuliere die Teilgleichungen der in einer Zuckerbatterie ablaufenden Redoxreaktion.

Abb. 2: Strukturformelausschnitt von Maltodextrin
Formuliere die Teilgleichungen der in einer Zuckerbatterie ablaufenden Redoxreaktion.
(5 BE)
4
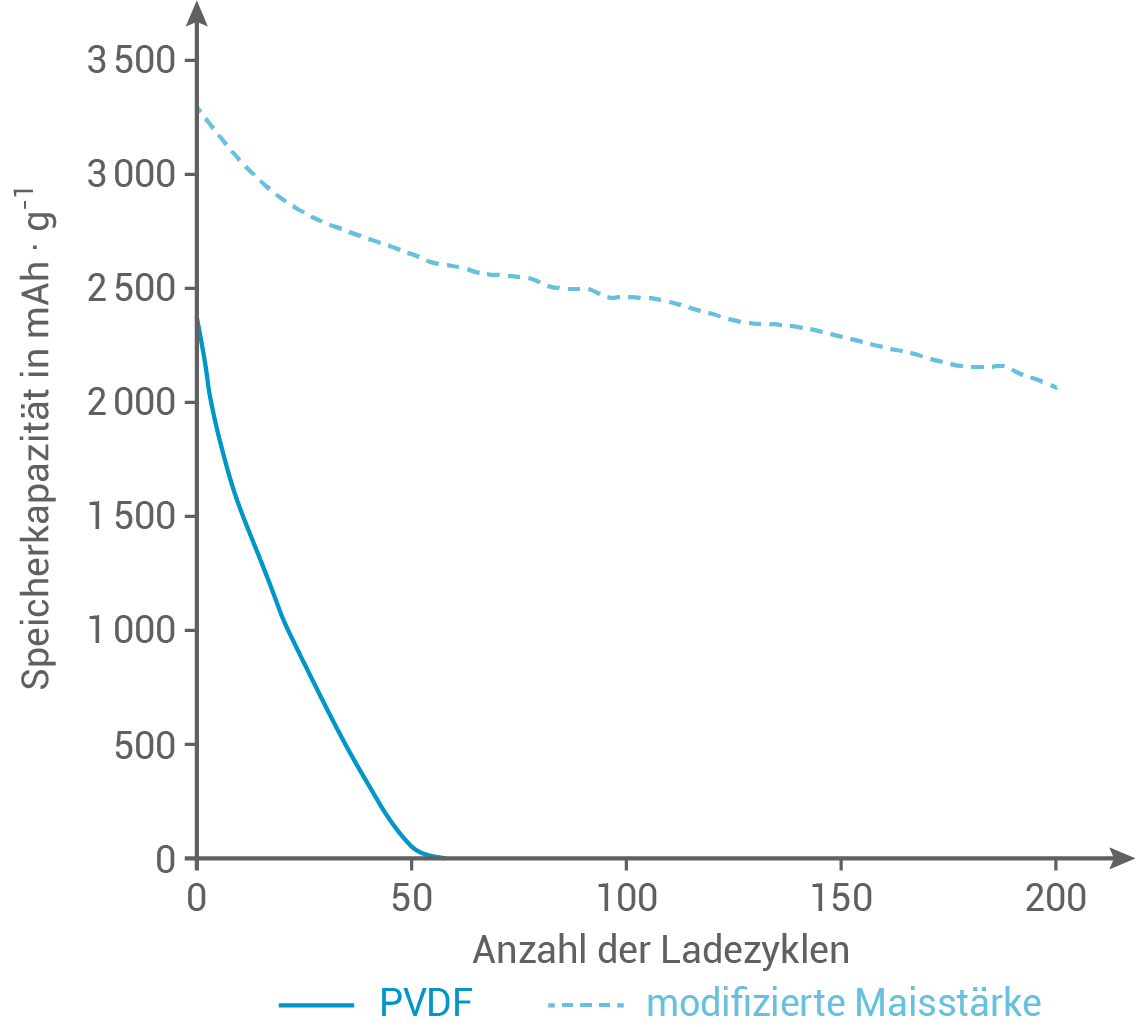
Entwickler von Lithium-Ionen-Akkus versuchen, eine gleichbleibend hohe Speicherkapazität ihrer Akkus zu gewährleisten. Dafür sind u. a. Bindemittel nötig, um den Verschleiß an der Graphitelektrode zu reduzieren. Als Bindemittel können z. B. PVDF, ein erdölbasierter Kunststoff, oder modifizierte Maisstärke verwendet werden. In einer Versuchsreihe werden Akkus mit je einem dieser beiden Bindemittel auf ihre Speicherkapazität nach mehrmaligem Auf- und Entladen untersucht.
 Bewerte auf Basis der gegebenen Informationen den Einsatz der beiden Bindemittel auch unter dem Aspekt der Nachhaltigkeit.
Bewerte auf Basis der gegebenen Informationen den Einsatz der beiden Bindemittel auch unter dem Aspekt der Nachhaltigkeit.

Abb. 3: Ergebnisse der Versuchsreihe zur Speicherkapazität von Lithium-Ionen-Akkus
nach: Rohan, R., Kuo, T. C., Chiou, C. Y., Chang, Y. L., Li, C. C. & Lee, J. T. (2018). Low- cost sustainable com starch as a high-performance aqueous binder in silicon anodes via situ cross-linking. Journal of Power Sources, 396, 459 – 466.
(4 BE)
(40 BE)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Zusammenhang zwischen Molekülstruktur und Farbigkeit
Mit zunehmender Größe des Chromophors im Molekül und somit dem Vorhandensein von mehr konjugierten Doppelbindungen mit delokalisierten  -Elektronen nimmt die Wellenlänge des absorbierten Lichts zu, da die erforderliche Anregungsenergie der Elektronen abnimmt.
Zuordnung der Strukturformeln
Substanz B besitzt keine konjugierten Doppelbindungen und absorbiert kein Licht im sichtbaren Bereich des elektromagnetischen Spektrums, deswegen ist es dem farblosen
-Elektronen nimmt die Wellenlänge des absorbierten Lichts zu, da die erforderliche Anregungsenergie der Elektronen abnimmt.
Zuordnung der Strukturformeln
Substanz B besitzt keine konjugierten Doppelbindungen und absorbiert kein Licht im sichtbaren Bereich des elektromagnetischen Spektrums, deswegen ist es dem farblosen  -Tocopherol (Vitamin E) zuzuordnen.
Zeaxanthin und
-Tocopherol (Vitamin E) zuzuordnen.
Zeaxanthin und  -Carotin erzeugen einen ähnlichen Farbeindruck, da sie Licht ähnlicher Wellenlängen absorbieren. Molekül A und C besitzen beide den gleichen Chromophor, weswegen die Unterscheidung über die beiden Hydroxygruppen in Molekül A erfolgt. Für die im Text erwähnte Veresterung von Zeaxanthin mit Fettsäuren ist eine alkoholische Komponente erforderlich. Somit handelt es sich bei Molekül A um Zeaxanthin und bei Molekül C um
-Carotin erzeugen einen ähnlichen Farbeindruck, da sie Licht ähnlicher Wellenlängen absorbieren. Molekül A und C besitzen beide den gleichen Chromophor, weswegen die Unterscheidung über die beiden Hydroxygruppen in Molekül A erfolgt. Für die im Text erwähnte Veresterung von Zeaxanthin mit Fettsäuren ist eine alkoholische Komponente erforderlich. Somit handelt es sich bei Molekül A um Zeaxanthin und bei Molekül C um  -Carotin.
-Carotin.
2.1.1
Begründung der Eignung als Tensid
Tenside sind grenzflächenaktive Substanzen, die über ein amphiphiles Molekül verfügen. Im Molekül der Ustilaginsäure A sind sowohl ein langer, unpolarer Rest mit zahlreichen C–C- bzw. C–H-Bindungen als auch polare Molekülteile mit Hydroxy- oder Carbonylgruppen vorhanden. Aus diesem Grund findet Ustilaginsäure A Anwendung als Tensid in der Lebensmittelindustrie.
2.1.2
Benennung des Disaccharids und der Bindung
Der markierte Ausschnitt stellt den Disaccharid Cellobiose dar.
Die Verknüpfung der beiden Monosaccharid-Bausteine erfolgt -1,4-glykosidisch.
-1,4-glykosidisch.
Die Verknüpfung der beiden Monosaccharid-Bausteine erfolgt
2.2.1
D-Mannose-Molekül in der FISCHER-Projektion
 Durchführung der FEHLING-Probe
Bei der FEHLING-Probe werden eine wässrige Lösung von Kupfer
Durchführung der FEHLING-Probe
Bei der FEHLING-Probe werden eine wässrige Lösung von Kupfer -sulfat (FEHLING I) und eine alkalische Lösung von Kalium-Natrium-Tartrat (FEHLING II) gemischt. Dabei entsteht ein tiefblauer Kupferkomplex. Nachfolgend wird die zu testende Substanz hinzugefügt und die Lösung vorsichtig erwärmt.
Zu erwartende Versuchsergebnisse
D-Mannose enthält eine freie Aldehydgruppe, weswegen die FEHLING-Probe positiv verläuft und sich ein rotbrauner Niederschlag bildet.
-sulfat (FEHLING I) und eine alkalische Lösung von Kalium-Natrium-Tartrat (FEHLING II) gemischt. Dabei entsteht ein tiefblauer Kupferkomplex. Nachfolgend wird die zu testende Substanz hinzugefügt und die Lösung vorsichtig erwärmt.
Zu erwartende Versuchsergebnisse
D-Mannose enthält eine freie Aldehydgruppe, weswegen die FEHLING-Probe positiv verläuft und sich ein rotbrauner Niederschlag bildet.
Ustilaginsäure A hingegen besitzt keine freien Aldehydgruppen und die anomeren -Atome sind mit glykosidischen Bindungen verknüpft. Demnach ist keine Ringöffnung möglich und die FEHLING-Probe verläuft negativ.
-Atome sind mit glykosidischen Bindungen verknüpft. Demnach ist keine Ringöffnung möglich und die FEHLING-Probe verläuft negativ.

Ustilaginsäure A hingegen besitzt keine freien Aldehydgruppen und die anomeren
2.2.2
Ergänzung der zu erwartenden Werte
Diagramm und Begründung der Messergebnisse
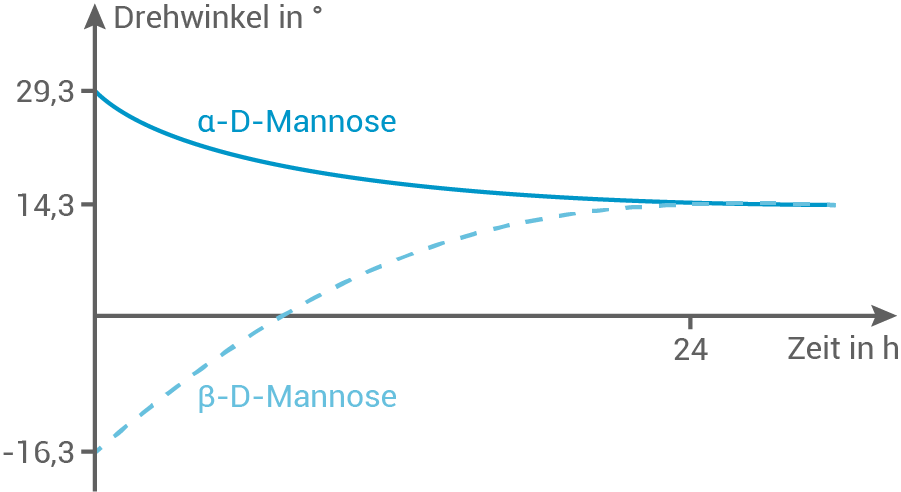 Es entsteht ein Gleichgewicht zwischen den beiden Anomeren und offenkettigen Form, wenn eines der beiden reinen Anomeren in Wasser gelöst wird:
Es entsteht ein Gleichgewicht zwischen den beiden Anomeren und offenkettigen Form, wenn eines der beiden reinen Anomeren in Wasser gelöst wird:
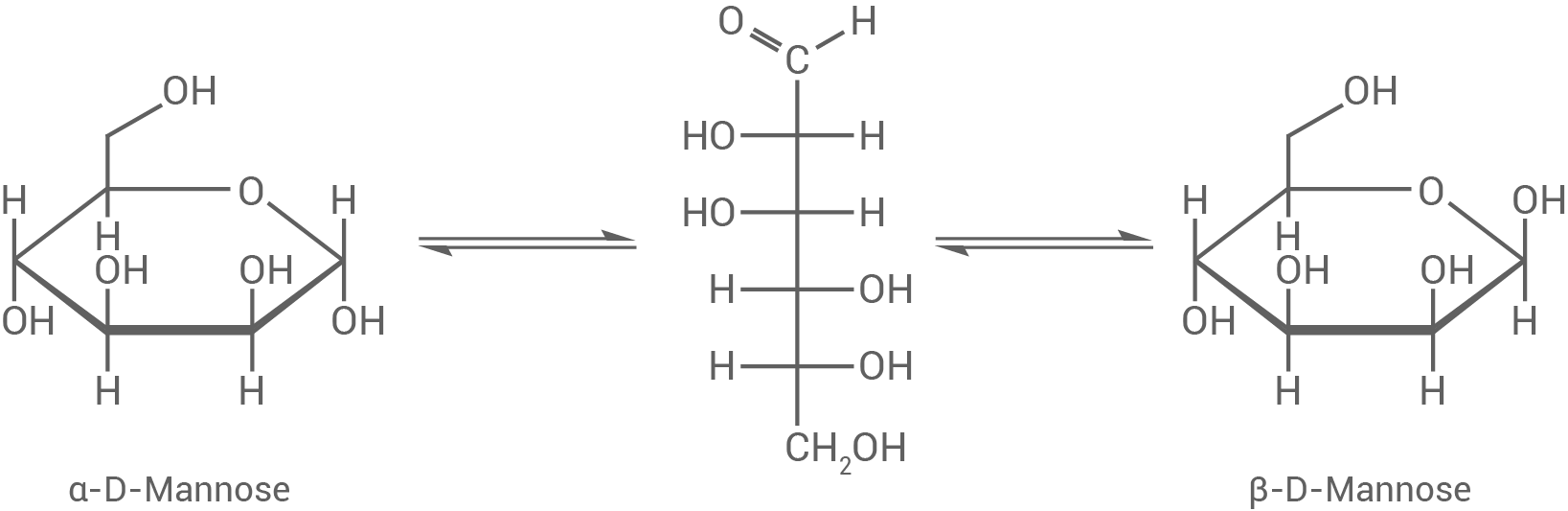 Bei allen drei Formen ist eine optische Aktivität und ein charakteristischer Drehwinkel vorhanden. Die Gleichgewichtseinstellung kann mit einem Polarimeter durch die Drehwinkeländerung (Mutarotation) beobachtet werden. Der Durschnitt der einzelnen Drehwinkel der verschiedenen Formen gemäß ihren Anteilen im Gleichgewicht stellt den finalen Drehwinkel der Lösung dar.
Bei allen drei Formen ist eine optische Aktivität und ein charakteristischer Drehwinkel vorhanden. Die Gleichgewichtseinstellung kann mit einem Polarimeter durch die Drehwinkeländerung (Mutarotation) beobachtet werden. Der Durschnitt der einzelnen Drehwinkel der verschiedenen Formen gemäß ihren Anteilen im Gleichgewicht stellt den finalen Drehwinkel der Lösung dar.
| Versuchs-ansatz ausgehend von | Dreh-winkel der Lösung zum Zeitpunkt |
Dreh-winkel der Lösung zum Zeitpunkt |
Dreh-winkel der Lösung zum Zeitpunkt |
|---|---|---|---|


3
Teilgleichungen der Redoxreaktion in einer Zuckerbatterie
4
Bewertung des Einsatzes der Bindemittel
In Lithium-Ionen-Akkus werden durch Bindemittel die Speicherkapazitäten erhalten. Aus der Nachhaltigkeitsperspektive wird Maisstärke als erneuerbarer Rohstoff bevorzugt, da PVDF fossile Rohstoffe verbraucht.
Des Weiteren nimmt die Ladekapazität von Akkus mit PVDF-Bindemitteln bereits nach wenigen Ladezyklen stark ab, im Gegensatz zu Akkus mit Maisstärke als Bindemittel. Das bedeutet, dass die Speicherkapazität der Maisstärke-Akkus länger erhalten bleibt.
Insgesamt ist Maisstärke als Bindemittel besser geeignet als PVDF.
Des Weiteren nimmt die Ladekapazität von Akkus mit PVDF-Bindemitteln bereits nach wenigen Ladezyklen stark ab, im Gegensatz zu Akkus mit Maisstärke als Bindemittel. Das bedeutet, dass die Speicherkapazität der Maisstärke-Akkus länger erhalten bleibt.
Insgesamt ist Maisstärke als Bindemittel besser geeignet als PVDF.