A2 Manuka-Honig
Aus dem Nektar des neuseeländischen Manuka-Baumes (Leptospermum scoparium) stellen Bienen den sogenannten Manuka-Honig her, dem eine gesundheitsfördernde Wirkung zugeschrieben wird.
1
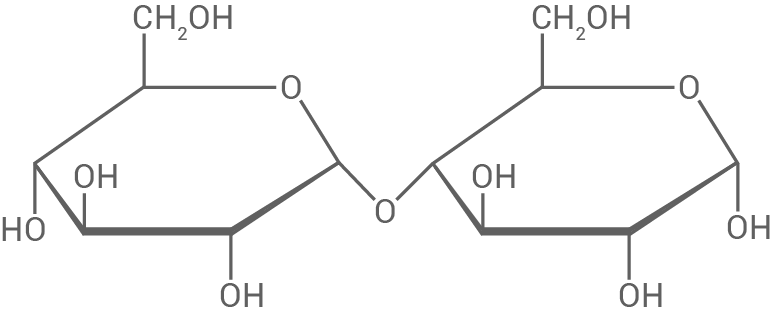
Ein im Manuka-Honig nachgewiesenes Disaccharid ist die Nigerose (Abb. 1), die den Isomaltosen zugeordnet wird.
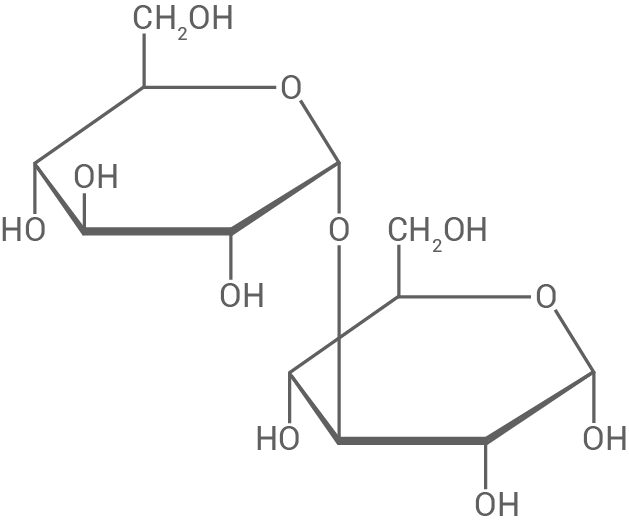

Abb. 1: Haworth-Projektion eines Nigerose-Moleküls
1.1
Zeichne ein Maltose-Molekül in der Haworth-Projektion und vergleiche das Maltose- und das Nigerose-Molekül hinsichtlich der jeweiligen Monosaccharid-Bausteine sowie deren Verknüpfung.
(6 BE)
1.2
In einem Versuch wird die Fehling-Probe mit Nigerose durchgeführt. Beschreibe die Durchführung dieses Nachweises und begründe das zu erwartende Ergebnis.
(5 BE)
2
Manuka-Honig enthält neben verschiedenen Zuckern auch Aminosäuren (Tab.):
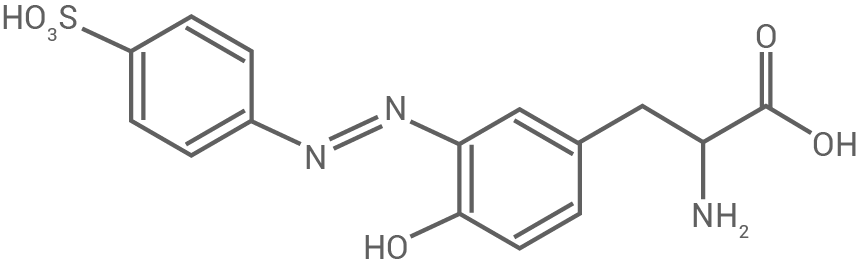
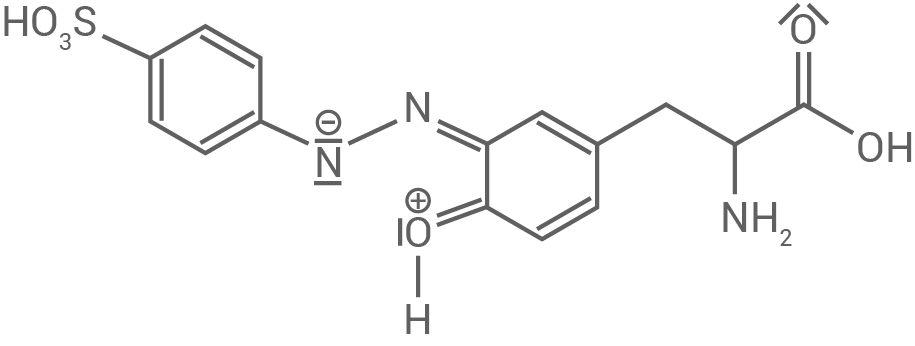
Die Aminosäure Tyrosin lässt sich mithilfe der Pauly-Reaktion nachweisen. Dabei kommt es durch Reaktion mit Sulfanilsäure zur Bildung eines roten Farbstoffs. Die Strukturformel des Farbstoff-Moleküls ist in Abbildung 2 dargestellt:
| Name der Aminosäure | Strukturformel |
|---|---|
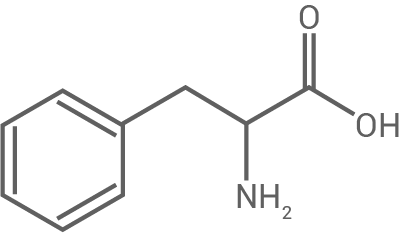
| Phenylalanin |
|
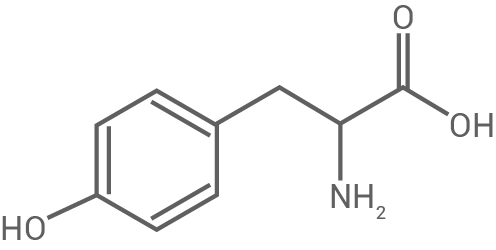
| Tyrosin |
|
Tab.: Strukturformeln ausgewählter Aminosäuren

Abb. 2: Strukturformel des farbigen Produkts der Pauly-Reaktion mit Tyrosin
2.1
Erkläre den Zusammenhang zwischen Molekülstruktur und Farbigkeit des farbigen Produkts der Pauly-Reaktion anhand einer weiteren mesomeren Grenzstrukturformel.
(5 BE)
2.2
Die Bildung des roten Farbstoffs erfolgt ausgehend von Tyrosin und Sulfanilsäure in zwei Schritten. Formuliere die Strukturformelgleichungen für die beiden Syntheseschritte und benenne diese.
(7 BE)
2.3
Die Moleküle von Tyrosin und Phenylalanin sind ähnlich gebaut. Dennoch verläuft die Pauly-Reaktion mit Phenylalanin negativ. Begründe die unterschiedlichen Reaktivitäten der beiden Stoffe.
(3 BE)
3
Manuka-Honig hat einen pH-Wert von ca.  Dieser ist auf die im Honig enthaltenen organischen Säuren wie Zimtsäure ((E)-3-Phenylpropensäure) zưrückzuführen. Der
Dieser ist auf die im Honig enthaltenen organischen Säuren wie Zimtsäure ((E)-3-Phenylpropensäure) zưrückzuführen. Der  -Wert dieser Säure beträgt
-Wert dieser Säure beträgt 
3.1
Formuliere die Strukturformelgleichung für die Protolysereaktion von Zimtsäure mit Wasser.
(3 BE)
3.2
Berechne die Anfangskonzentration einer Zimtsäurelösung mit einem pH-Wert von  und vergleiche diesen Wert mit der Konzentration einer Salzsäurelösung des gleichen pH-Werts. Begründe den Unterschied.
und vergleiche diesen Wert mit der Konzentration einer Salzsäurelösung des gleichen pH-Werts. Begründe den Unterschied.
(6 BE)
4
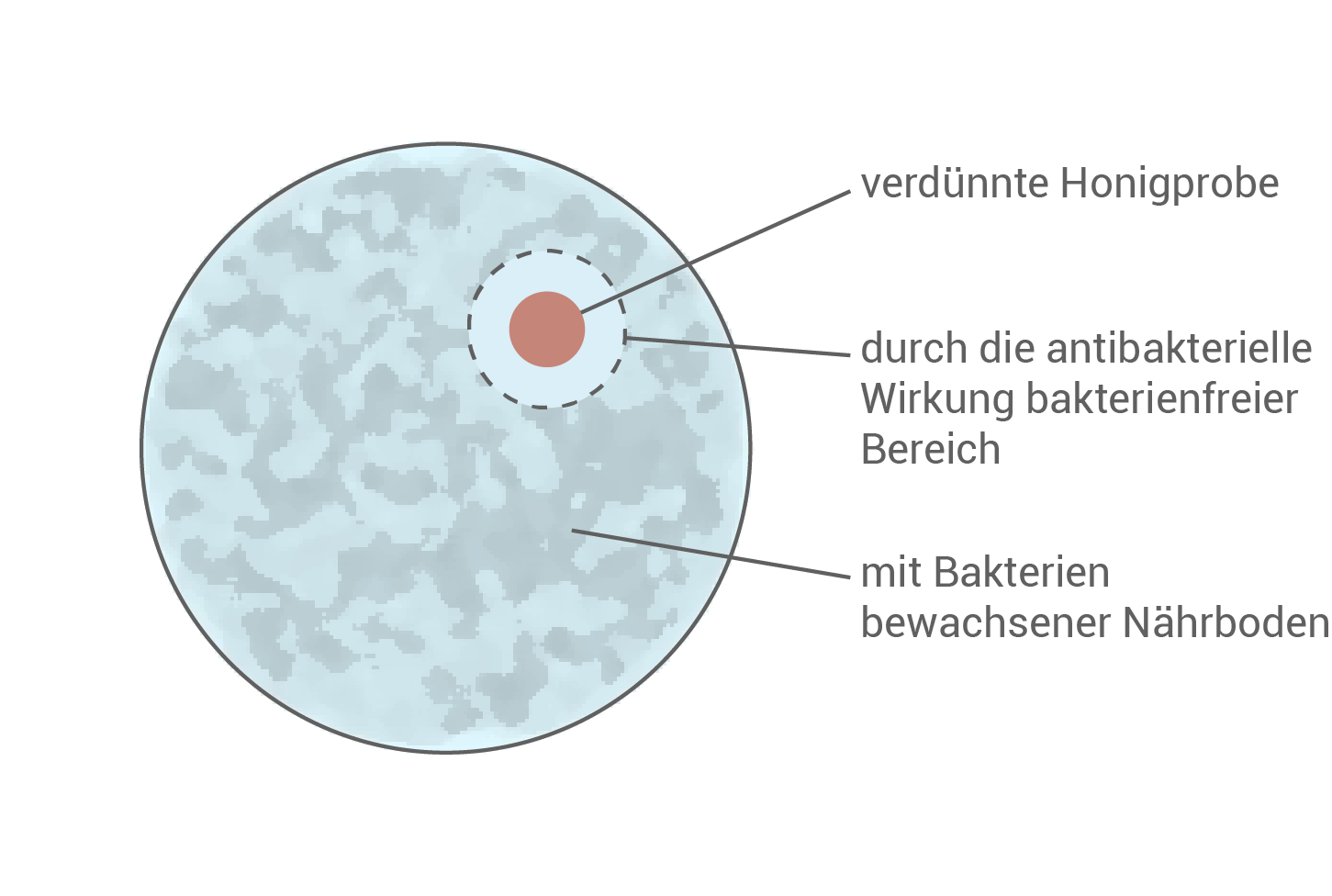
Die Ureinwohner Neuseelands nutzen den Manuka-Honig unter anderem aufgrund seiner antibakteriellen Wirkung traditionell als Heilmittel. Diese Eigenschaft wird in der Werbung für Manuka-Honig betont. In einem Experiment wird die antibakterielle Wirkung eines ManukaHonigs mit der eines Scheinulmen-Honigs aus Südamerika verglichen. Dazu werden auf einzelnen, mit Bakterien bewachsenen Nährböden jeweils unterschiedlich verdünnte Honigproben aufgebracht. Dabei gilt: Je größer der bakterienfreie Ring um die Probe ist (Abb. 3), desto stärker ist die antibakterielle Wirkung.
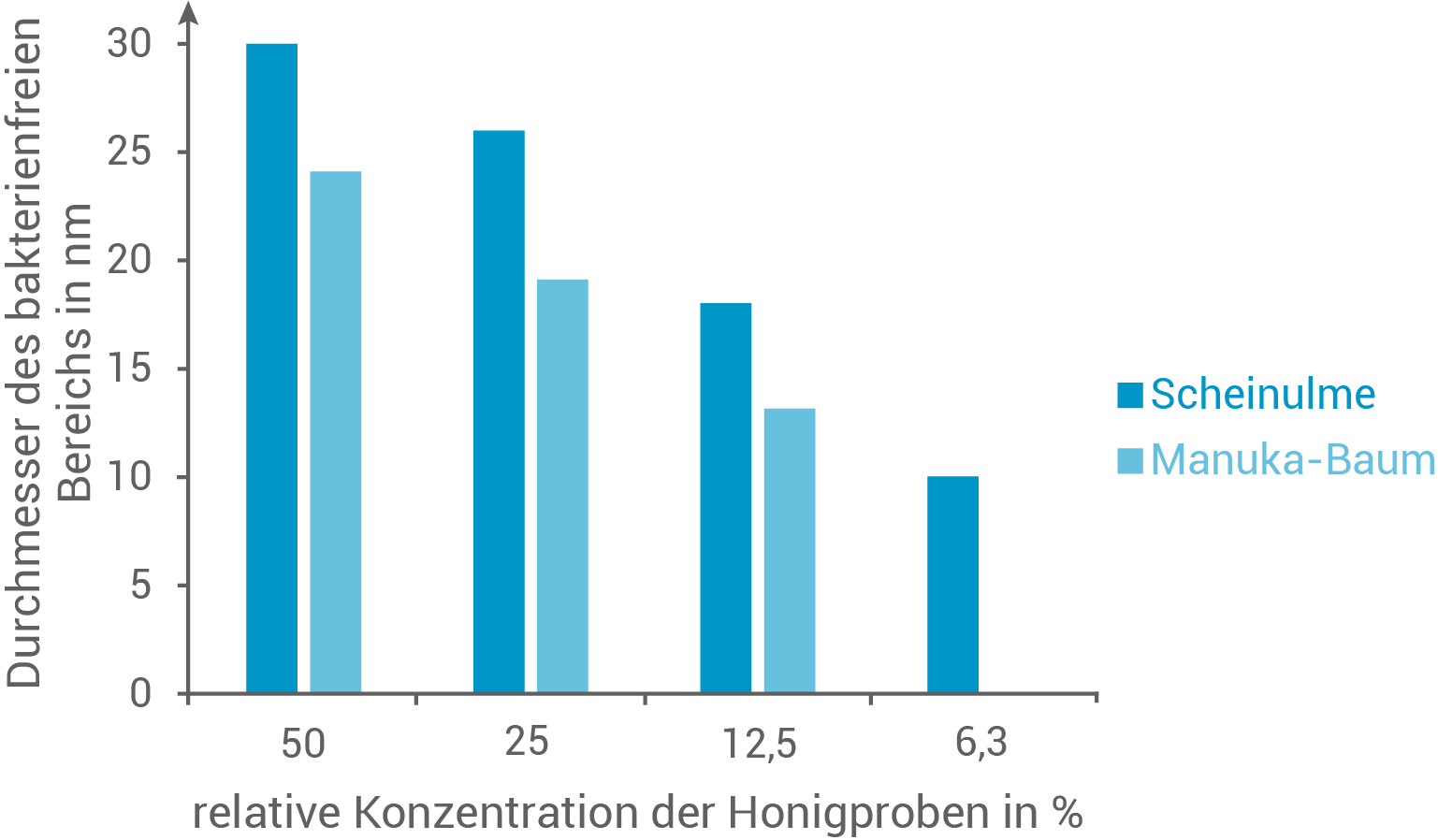 Bewerte mithilfe der in Abbildung 4 gezeigten Versuchsergebnisse den Export des Manuka-Honigs nach Südamerika sowohl unter Wirksamkeits- als auch unter Nachhaltigkeitsaspekten.
Bewerte mithilfe der in Abbildung 4 gezeigten Versuchsergebnisse den Export des Manuka-Honigs nach Südamerika sowohl unter Wirksamkeits- als auch unter Nachhaltigkeitsaspekten.

Abb. 3: Bestimmung der antibakteriellen Wirkung einer Honigprobe

Abb. 4: Durchmesser der bakterienfreien Bereiche in Abhängigkeit von Honigsorte und Verdünnung
verändert nach: O. Sherlock et al.: Comparison of the antimicrobial activity of Ulmo honey from Chile and Manuka honey against methicillin-resistant Staphylococcus aureus, Escherichia coli and Pseudomonas aeruginosa. In: BMC Complementary and Alternative Medicine, 10:47 (2010).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Strukturformel von Maltose in Haworth-Projektion
 Vergleich vom Maltose- und Nigerose Molekül
Die Verknüpfung der beiden D-Glucopyranose-Einheiten erfolgt
Vergleich vom Maltose- und Nigerose Molekül
Die Verknüpfung der beiden D-Glucopyranose-Einheiten erfolgt  -1,4-glykosidisch.
-1,4-glykosidisch.
In Nigerose sind die D-Glucopyranose-Monomere -1,3-glykosidisch verknüpft.
-1,3-glykosidisch verknüpft.

In Nigerose sind die D-Glucopyranose-Monomere
1.2
Durchführung der Fehling-Probe
Mit der Fehling-Probe werden reduzierbare Zucker nachgewiesen.
Für die Nachweisreaktion wird eine 1:1 Lösung aus einer alkalischen Kupfer(II)-sulfat-Lösung (FEHLING I) und einer Kalium-Natrium-Tartrat-Lösung (FEHLING II) hergestellt. Diese Lösung ist tiefblau. Anschließend wird die zu testende Substanz zugemischt und der gesamte Ansatz erhitzt. Der Nachweis verläuft positiv, wenn ein ziegelroter Niederschlag aus Kupfer(I)-oxid gebildet wird.
Wenn es sich um keinen reduzierbaren Zucker handelt, bleibt die Lösung unverändert, also dunkelblau. Begründung des zu erwartenden Ergebnis Nigerose besitzt anomere -Atome, die nicht in glykosidischen Bindungen sind, wodurch eine Ringöffnung möglich ist. Folglich kann die Aldehyd-Gruppe oxidiert werden und die Fehling-Probe zeigt einen positiven Nachweis.
-Atome, die nicht in glykosidischen Bindungen sind, wodurch eine Ringöffnung möglich ist. Folglich kann die Aldehyd-Gruppe oxidiert werden und die Fehling-Probe zeigt einen positiven Nachweis.
Für die Nachweisreaktion wird eine 1:1 Lösung aus einer alkalischen Kupfer(II)-sulfat-Lösung (FEHLING I) und einer Kalium-Natrium-Tartrat-Lösung (FEHLING II) hergestellt. Diese Lösung ist tiefblau. Anschließend wird die zu testende Substanz zugemischt und der gesamte Ansatz erhitzt. Der Nachweis verläuft positiv, wenn ein ziegelroter Niederschlag aus Kupfer(I)-oxid gebildet wird.
Wenn es sich um keinen reduzierbaren Zucker handelt, bleibt die Lösung unverändert, also dunkelblau. Begründung des zu erwartenden Ergebnis Nigerose besitzt anomere
2.1
Zusammenhang zwischen Molekülstruktur und Farbigkeit
Das farbige Reaktionsprodukt der Pauly-Reaktion mit Tyrosin zeigt ein umfangreiches System konjugierter Doppelbindungen. Dieses wird als Chromophor bezeichnet wird. Die Elektronen dieses Molekülteils sind delokalisiert, was bedeutet, dass sie durch Lichtquanten aus dem sichtbaren Bereich des elektromagnetischen Spektrums angeregt werden können. Diese Absorption von Licht einer spezifischen Wellenlänge und die Reflexion des restlichen sichtbaren Lichts führen dazu, dass der Stoff für das menschliche Auge eine bestimmte Farbe aufweist.
Folgende Abbildung zeigt eine weitere mesomere Grenzstrukturformel:

2.2
Strukturformelgleichungen der Syntheseschritte
Schritt 1: Diazotierung (Bildung eines Diazonium-Ions)
 Schritt 2: Azokupplung
Schritt 2: Azokupplung
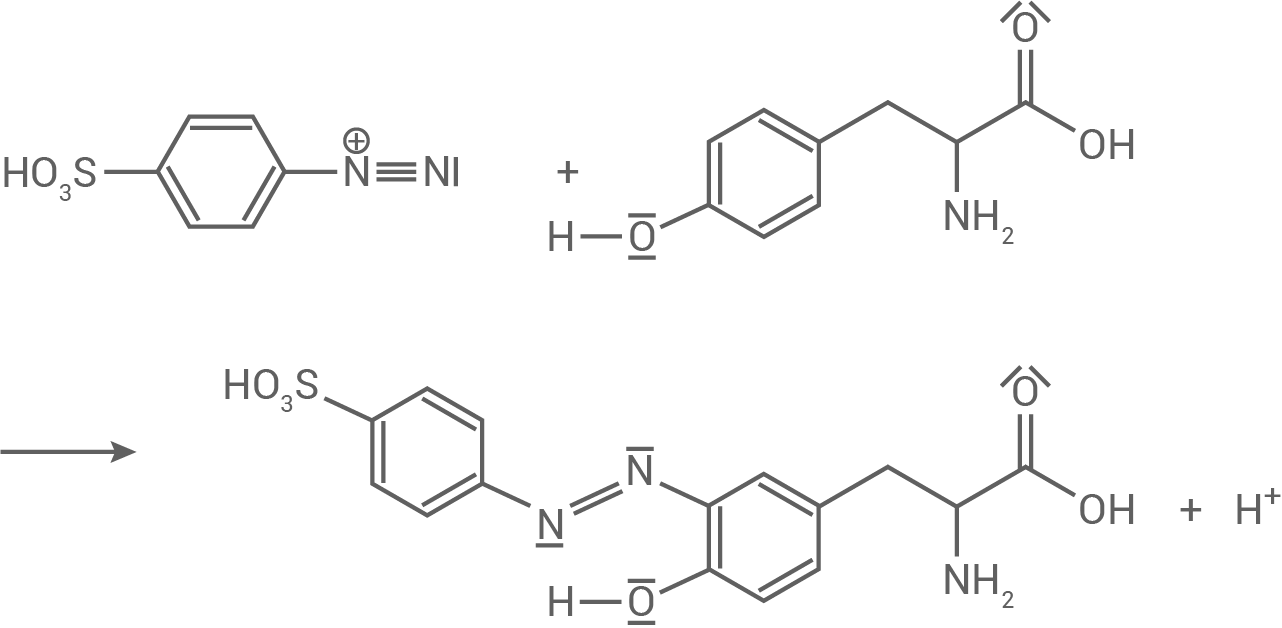


2.3
Begründung der unterschiedlichen Reaktivität
Da Phenylalanin keine elektronenschiebende  -Gruppe am aromatischen Ringsystem aufweist, ist die negative Ladungsdichte am Ring geringer. Dadurch wird die elektrophile Addition des Diazonium-Ions an den Ring von Phenylalanin erschwert.
-Gruppe am aromatischen Ringsystem aufweist, ist die negative Ladungsdichte am Ring geringer. Dadurch wird die elektrophile Addition des Diazonium-Ions an den Ring von Phenylalanin erschwert.
3.1
Strukturformelgleichung für die Protolysereaktion von Zimtsäure mit Wasser


3.2
Berechnung der Anfangskonzentration einer Zimtsäurelösung
Da Zimtsäure  eine schwache Säure ist, dissoziiert sie nicht vollständig:
eine schwache Säure ist, dissoziiert sie nicht vollständig:


 Das Massenwirkungsgesetz lautet:
Das Massenwirkungsgesetz lautet:
 Mit
Mit  folgt:
folgt:
 Weiterhin gilt:
Weiterhin gilt:
![\(\begin{array}[t]{rll}
c(\text{A}^-) &=& c(H_3O^+) & \\[5pt]
c(\text{HA}) &\sim& c_0(\text{HA})
\end{array}\)](https://mathjax.schullv.de/5811c1065c2ca98ac04ae846305df87ec38be35d1ebfd4ae6d52aba240ed83e5?color=5a5a5a) Daraus folgt:
Daraus folgt:
![\(\begin{array}[t]{rll}
K_S &=& \dfrac{c^2(H_3O^+)}{c_0(\text{HA})} & \\[5pt]
c_0(\text{HA}) &=& \dfrac{c^2(H_3O^+) }{K_S} & \\[5pt]
&=& \dfrac{(10^{-pH})^2}{10^{-pK_S}} & \\[5pt]
&=& \dfrac{10^{-4,01 \cdot 2}}{10^{-4,4}} & \\[5pt]
&=& 2,4 \cdot 10^{-4}\,\text{mol} \cdot \text{L}^{-1}
\end{array}\)](https://mathjax.schullv.de/8e650165b3b0993c9853ef8570bc9cd4e67020c9564d7ece28775fc8ec5b86a9?color=5a5a5a) Vergleich mit einer Salzsäurelösung des gleichen pH-Werts
Da Salzsäure als starke Säure vollständig dissoziiert, entspricht die Konzentration der Oxonium-Ionen der Anfangskonzentration der Salzsäurelösung.
Daraus folgt:
Vergleich mit einer Salzsäurelösung des gleichen pH-Werts
Da Salzsäure als starke Säure vollständig dissoziiert, entspricht die Konzentration der Oxonium-Ionen der Anfangskonzentration der Salzsäurelösung.
Daraus folgt:
![\(\begin{array}[t]{rll}
c(H_3O^+) &=& 10^{-pH} & \\[5pt]
&=& 10^{-4,01} \,\text{mol} \cdot \text{L}^{-1} & \\[5pt]
&=& 9,77 \cdot 10^{-5} \,\text{mol} \cdot \text{L}^{-1} & \\[5pt]
&=& c(HCl)
\end{array}\)](https://mathjax.schullv.de/5e55033d0c5abc7a83ac7bae86f2c3b7af80c339ad5bce9d389782f00e33c1de?color=5a5a5a) Für den gleichen pH-Wert sind in einer Salzsäurelösung weniger Säure-Moleküle pro Volumeneinheit nötig als in einer Zimtsäurelösung.
Für den gleichen pH-Wert sind in einer Salzsäurelösung weniger Säure-Moleküle pro Volumeneinheit nötig als in einer Zimtsäurelösung.
4
Bewertung des Exports
Mögliche Lösung:
Die Honigproben aus Scheinulmen weisen bei allen Verdünnungsgraden eine höhere Wirksamkeit auf als diejenigen aus dem Manuka-Baum, da der bakterienfreie Bereich größer ist. Es ist wichtig zu berücksichtigen, dass der Transport von Honig von Neuseeland nach Südamerika mit ökologischen Problemen verbunden ist, wie z. B. der Emission von Treibhausgasen.
Allgemein ist es nicht empfehlenswert, den Scheinulmen-Honig nach Südamerika zu transportieren, da der Manuka-Honig sowohl in Bezug auf Nachhaltigkeit als auch Wirksamkeit schlechter abschneidet als der lokale Scheinulmen-Honig.
Allgemein ist es nicht empfehlenswert, den Scheinulmen-Honig nach Südamerika zu transportieren, da der Manuka-Honig sowohl in Bezug auf Nachhaltigkeit als auch Wirksamkeit schlechter abschneidet als der lokale Scheinulmen-Honig.