B1 Babyprodukte
Hersteller von Babyprodukten werden oft vor die Herausforderung gestellt, „ohne Chemie“ eine maximale Funktionalität zu bieten. Genau betrachtet ist dies aber nicht möglich.
1
In Babyshampoos werden immer häufiger Betain-Tenside wie z. B. Lauramidopropylbetain (Abb. 1) eingesetzt, deren Fettsäurereste aus Kokosöl gewonnen werden. Aus Kokosöl kann man alternativ auch Seifen herstellen.
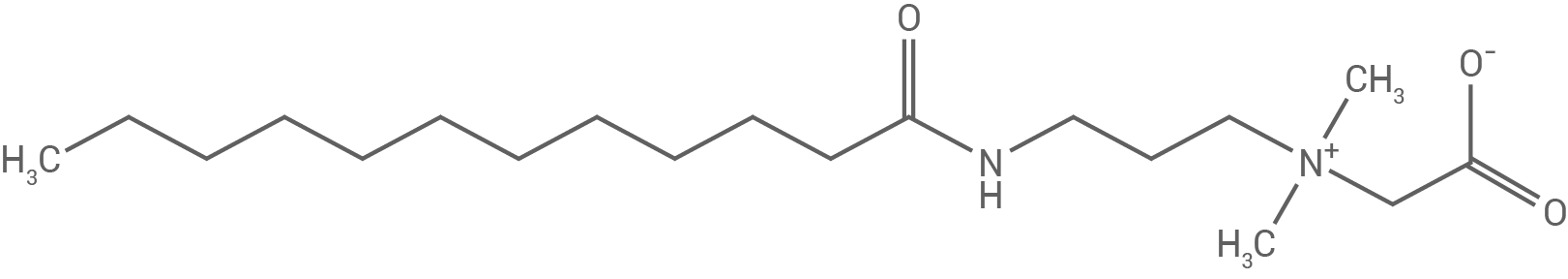

Abb. 1: Strukturformel von Lauramidopropylbetain
1.1
Formuliere die Strukturformelgleichung für die Verseifung eines Fettmoleküls mit drei unterschiedlichen Fettsäure-Resten.
(4 BE)
1.2
Babyshampoos mit Betain-Tensiden  -Werte ca.
-Werte ca.  werden u. a. damit beworben, dass sie im Vergleich zu Seifen eine sanftere unc hautverträglichere Reinigungswirkung erzielen.
werden u. a. damit beworben, dass sie im Vergleich zu Seifen eine sanftere unc hautverträglichere Reinigungswirkung erzielen.
Erläutere anhand einer modellhaften Skizze die Reinigungswirkung von Betain-Tensiden. Begründe die positive Werbeaussage durch den Vergleich der Eigenschaften eines Betain-Tensids mit denen einer Seife.
Erläutere anhand einer modellhaften Skizze die Reinigungswirkung von Betain-Tensiden. Begründe die positive Werbeaussage durch den Vergleich der Eigenschaften eines Betain-Tensids mit denen einer Seife.
(8 BE)
2
Babywindeln enthalten sogenannte Superabsorber, die ein Vielfaches ihres Eigengewichts an Wasser aufnehmen können. Ein solcher Superabsorber wird in zwei Stufen hergestellt: Im ersten Schritt wird aus den Monomeren Propensäure und Natriumpropenoat ein Polymer aus linearen Molekülen erzeugt. Diese werden im zweiten Schritt quervernetzt.
2.1
Formuliere den Reaktionsmechanismus für die Polymerisation von Propensäure ausgehend von einem Startermolekül  Gib den Namen und die Strukturformel eines für die Quervernetzung geeigneten Stoffes an.
Gib den Namen und die Strukturformel eines für die Quervernetzung geeigneten Stoffes an.
(8 BE)
2.2
Abbildung 2 zeigt modellhaft die Wasseraufnahme eines Superabsorbers:
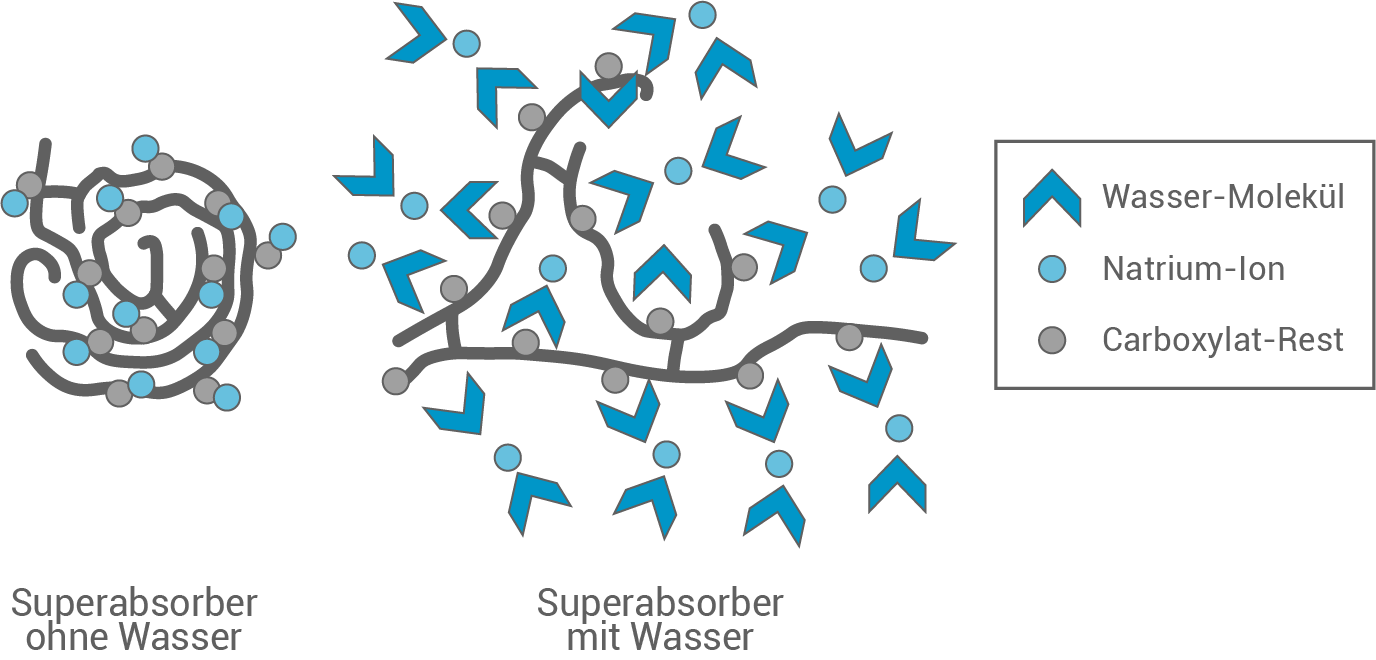 Erläutere anhand von Abbildung 2 das große Wasseraufnahmevermögen des Superabsorbers.
Erläutere anhand von Abbildung 2 das große Wasseraufnahmevermögen des Superabsorbers.

Abb. 2: Modellhafte Darstellung der Wirkungsweise eines Superabsorbers
(5 BE)
3
Viele Eltern wünschen sich für Kleinkinder weichmacherfreie Kunststoffartikel, da Weichmacher wegen ihrer möglichen gesundheitsschädlichen Wirkung in die Kritik geraten sind. Sie sind aber oft unabdingbar, um ein hartes Polymer elastisch und verformbar zu halten. Ein Beispiel für einen solchen Weichmacher ist  -Butylbenzolsulfonamid (Abb. 3):
-Butylbenzolsulfonamid (Abb. 3):
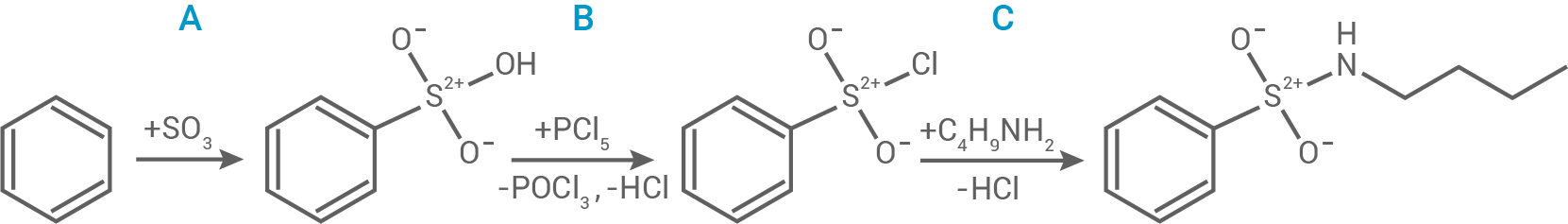

Abb. 3: Reaktionsschema für die Synthese von  -Butylbenzolsulfonamid
-Butylbenzolsulfonamid
3.1
Formuliere den Reaktionsmechanismus für Schritt A der Synthese von  -Butylbenzolsulfonamid (Abb. 3). Als Elektrophil dient ein Schwefeltrioxid-Molekül.
-Butylbenzolsulfonamid (Abb. 3). Als Elektrophil dient ein Schwefeltrioxid-Molekül.
(6 BE)
3.2
In Schritt B wird Phosphorpentachlorid eingesetzt. Dieses steht mit Phosphortrichlorid und Chlor in folgendem Gleichgewicht:


 Thermodynamische Daten für die Hinreaktion:
Thermodynamische Daten für die Hinreaktion:



3.2.1
Berechne die Temperatur in Kelvin, für die  gilt.
gilt.
Erkläre die Auswirkungen einer Temperaturerhöhung über diesen Wert hinaus auf den freiwilligen Verlauf der Reaktion.
Erkläre die Auswirkungen einer Temperaturerhöhung über diesen Wert hinaus auf den freiwilligen Verlauf der Reaktion.
(4 BE)
3.2.2
In einem geschlossenen Gefäß hat sich ein chemisches Gleichgewicht zwischen den gasförmigen Stoffen Phosphortrichlorid, Phosphorpentachlorid und Chlor eingestellt (Abb. 4):
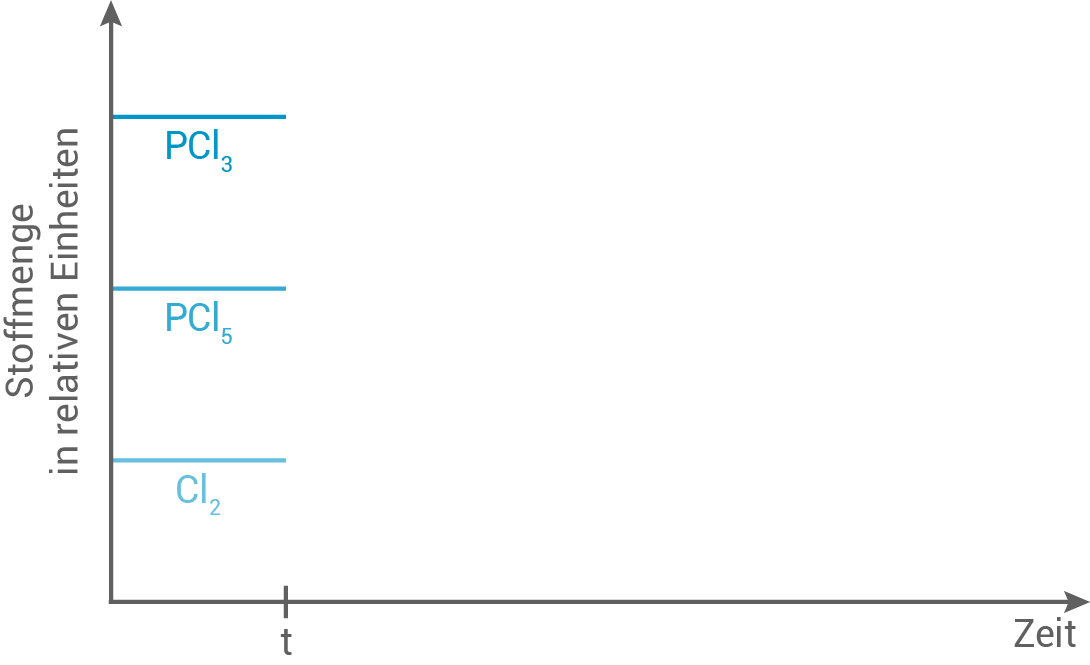 Zum Zeitpunkt
Zum Zeitpunkt  wird der Gesamtdruck im Gefäß erhöht. Skizziere in Abbildung 4 die mögliche Entwicklung der drei Stoffmengen ab dem Zeitpunkt
wird der Gesamtdruck im Gefäß erhöht. Skizziere in Abbildung 4 die mögliche Entwicklung der drei Stoffmengen ab dem Zeitpunkt  und erläutere diese.
und erläutere diese.

Abb. 4: Stoffmengen von Phosphortrichlorid, Phosphorpentachlorid und Chlor in einem geschlossenen Gefäß
(5 BE)
(40 BE)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1.1
Formulierung der Strukturformelgleichung für die Verseifung
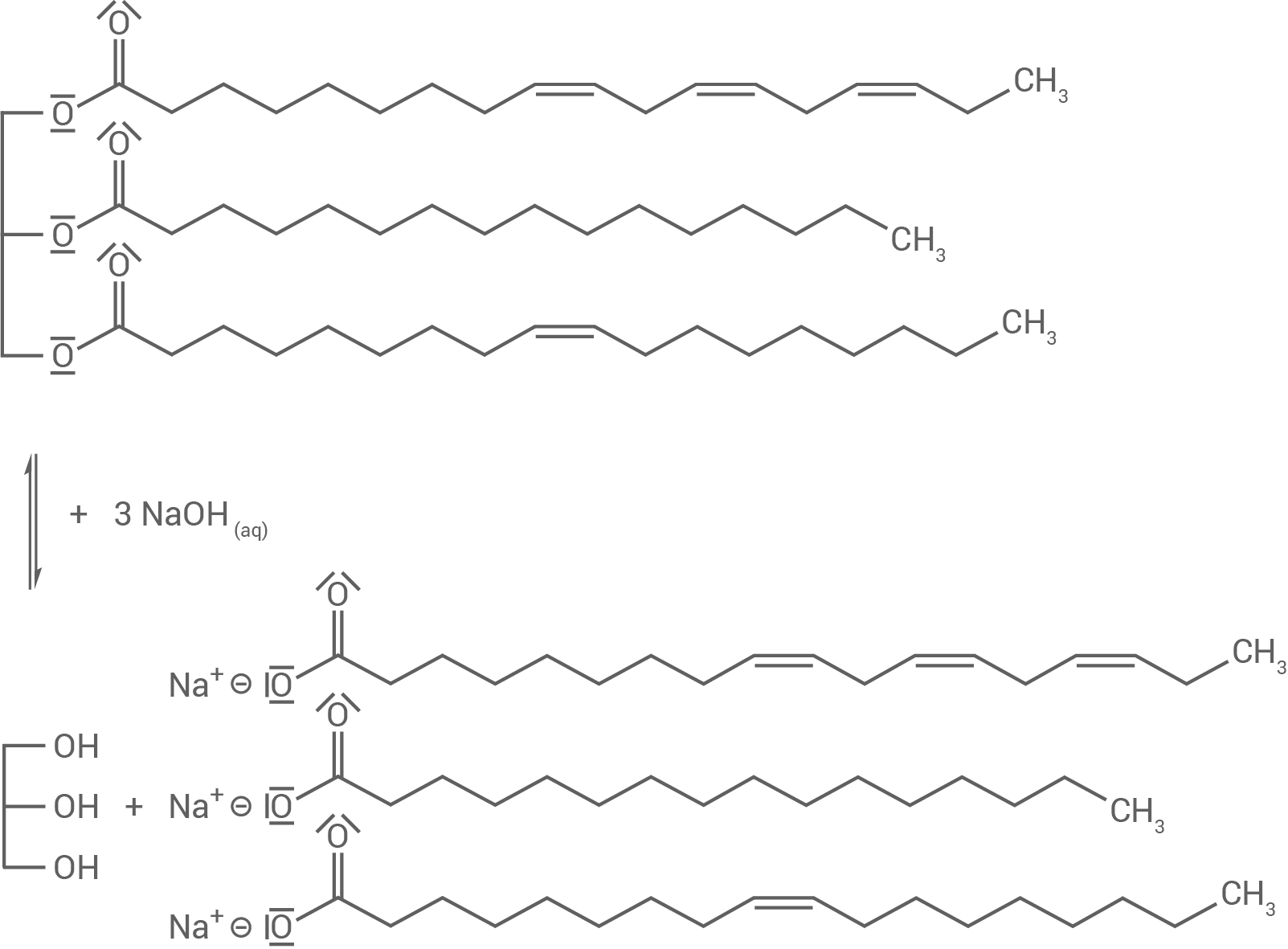

Verseifung (alkalische Hydrolyse) eines Fett-Moleküls mit z.B. Natronlauge
1.2
Erläuterung der Reinigungswirkung von Betain-Tensiden
So wie alle grenzflächenaktiven Stoffe sind Betain-Tenside amphiphil. Sie besitzen einen zwitterionischen Bereich, der polar und somit hydrophil ist, sowie einen langen Kohlenwasserstoffrest, der unpolar und damit lipophil ist:
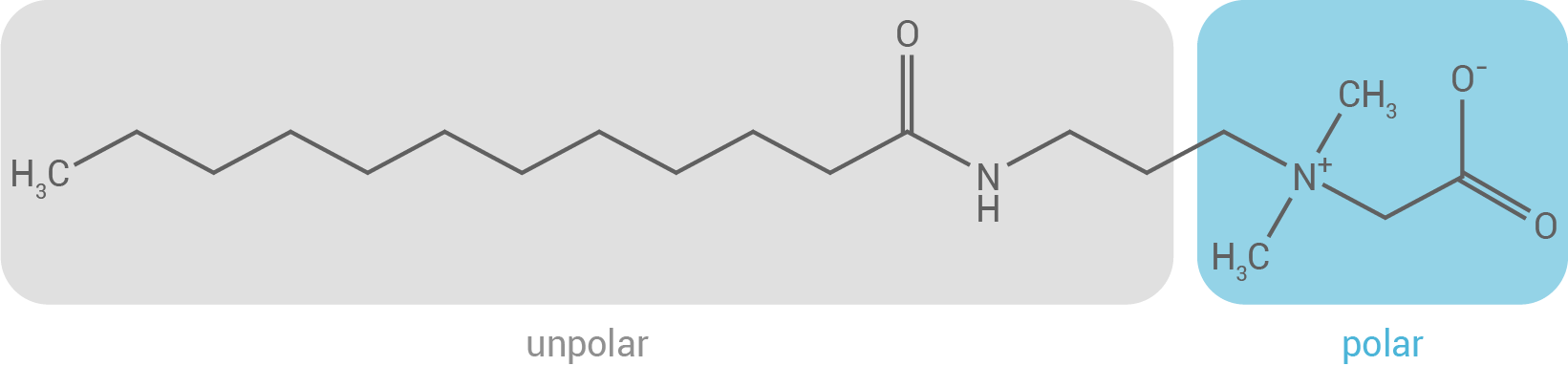 Beim Waschvorgang lagern sich die Tensid-Moleküle mit ihrem lipophilen Rest in die fettartige Verschmutzung ein und lösen diese durch Wechselwirkungen zwischen Wasser und ihren hydrophilen Köpfen vom Haar ab. Dabei entstehen Micellen, die von Tensid-Molekülen umgeben sind und mit Wasser ausgespült werden können:
Beim Waschvorgang lagern sich die Tensid-Moleküle mit ihrem lipophilen Rest in die fettartige Verschmutzung ein und lösen diese durch Wechselwirkungen zwischen Wasser und ihren hydrophilen Köpfen vom Haar ab. Dabei entstehen Micellen, die von Tensid-Molekülen umgeben sind und mit Wasser ausgespült werden können:
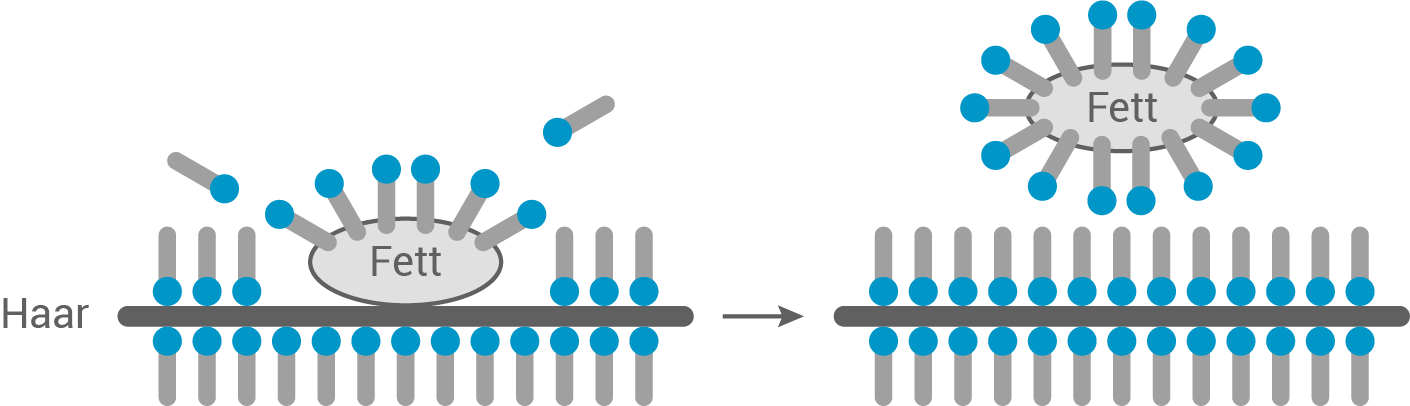 Vergleich der Eigenschaften
Da die menschliche Haut einen schwach sauren pH-Wert und eine schützende Lipidschicht hat, kann deren Störung zu Austrocknung und Hautreizungen führen.
Die hautreizende Wirkung klassischer Seifen lässt sich demnach dadurch erklären, dass sie eine stark entfettende Wirkung haben und Seifenlösungen einen basischen pH-Wert, also einen Überschuss an Hydroxid-Ionen, aufweisen. Diese Eigenschaften sind nachteilig für die Haut.
Betain-Tenside hingegen haben einen hohen
Vergleich der Eigenschaften
Da die menschliche Haut einen schwach sauren pH-Wert und eine schützende Lipidschicht hat, kann deren Störung zu Austrocknung und Hautreizungen führen.
Die hautreizende Wirkung klassischer Seifen lässt sich demnach dadurch erklären, dass sie eine stark entfettende Wirkung haben und Seifenlösungen einen basischen pH-Wert, also einen Überschuss an Hydroxid-Ionen, aufweisen. Diese Eigenschaften sind nachteilig für die Haut.
Betain-Tenside hingegen haben einen hohen  -Wert und bilden demnach als schwächere Basen weniger Hydroxid-Ionen in Wasser. Der hautreizende Effekt wird also verringert.
-Wert und bilden demnach als schwächere Basen weniger Hydroxid-Ionen in Wasser. Der hautreizende Effekt wird also verringert.


2.1
Reaktionsmechanismus für die Polymerisation von Propensäure
Der Mechanismus folgt einer radikalischen Polymerisation.
Startreaktion:
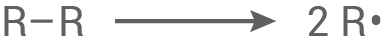 Kettenstart:
Kettenstart:
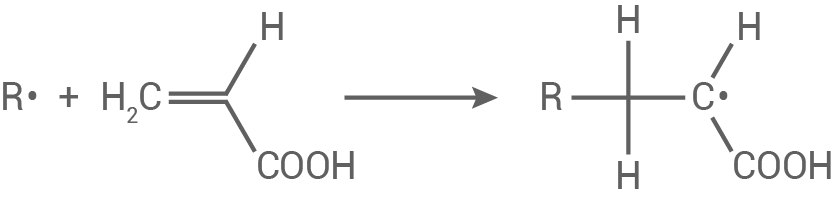 Kettenwachstum:
Kettenwachstum:
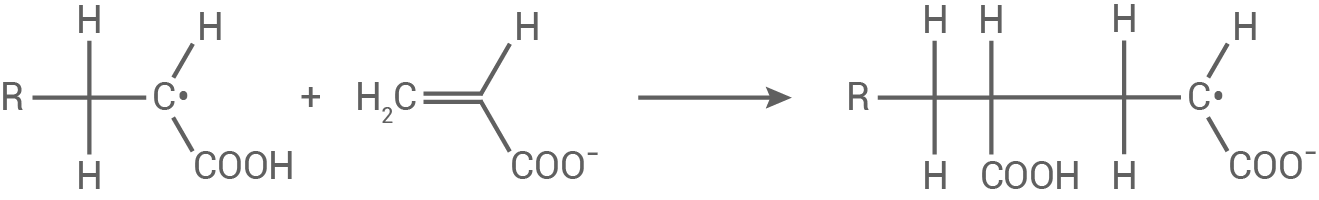 Mögliche Abbruchreaktion:
Mögliche Abbruchreaktion:
(Kombination zweier Radikale)
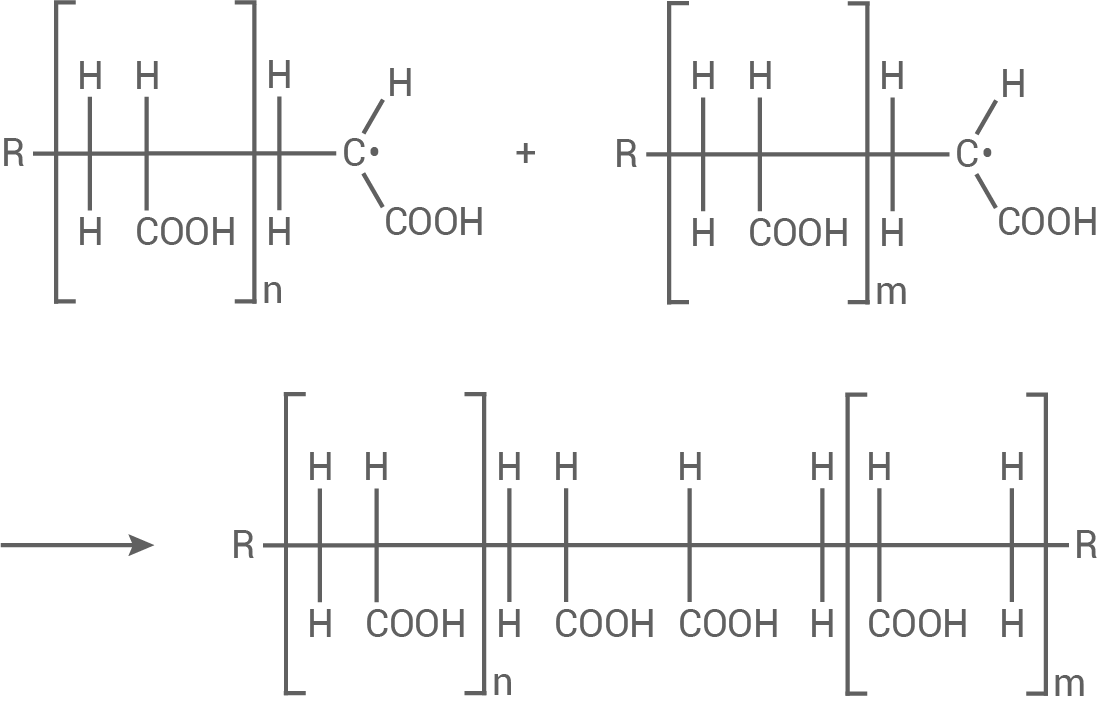 Namen und Strukturformel eines geeigneten Stoffes
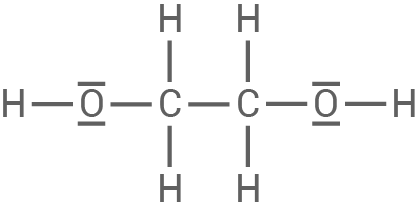
Für die Quervernetzung wäre beispielsweise Ethan-1,2-diol geeignet:
Namen und Strukturformel eines geeigneten Stoffes
Für die Quervernetzung wäre beispielsweise Ethan-1,2-diol geeignet:
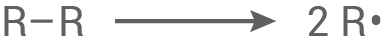

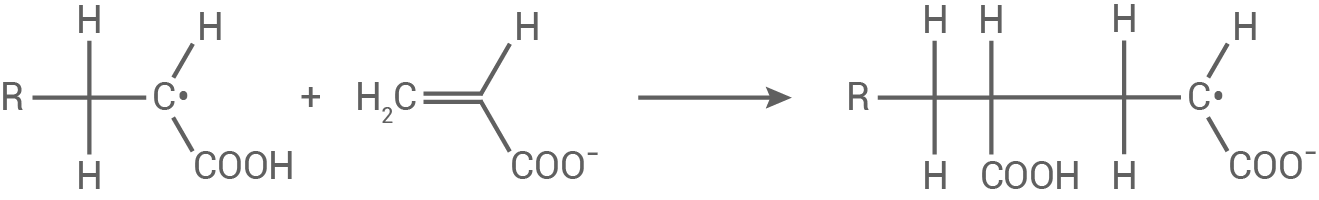
(Kombination zweier Radikale)


2.2
Erläuterung vom Wasseraufnahmevermögen des Superabsorbers
In Abbildung 2 ist ein Polymer mit Carboxylat-Resten und Natrium-Ionen zu sehen, welche negativ bzw. positiv geladen sind. Aufgrund ihres Dipol-Charakters und ihrer Polarität gehen Wasser-Moleküle Wechselwirkungen mit den geladenen Resten im Polymer ein, werden eingelagert und verändern die räumliche Struktur des Polymers. Dies bewirkt eine signifikante Volumenzunahme.
3.1
Reaktionsmechanismus für Schritt A der  -Butylbenzolsulfonamid-Synthese
Benzol und Schwefeltrioxid reagieren nach dem Mechanismus einer elektrophilen Substitution am aromatischen Ring:
Schritt 1: Elektrophiler Angriff des
-Butylbenzolsulfonamid-Synthese
Benzol und Schwefeltrioxid reagieren nach dem Mechanismus einer elektrophilen Substitution am aromatischen Ring:
Schritt 1: Elektrophiler Angriff des  -Moleküls
-Moleküls
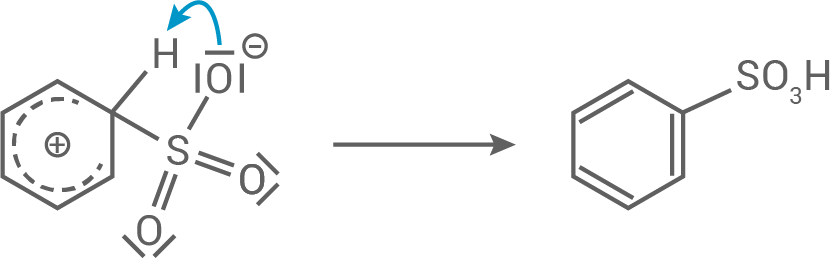
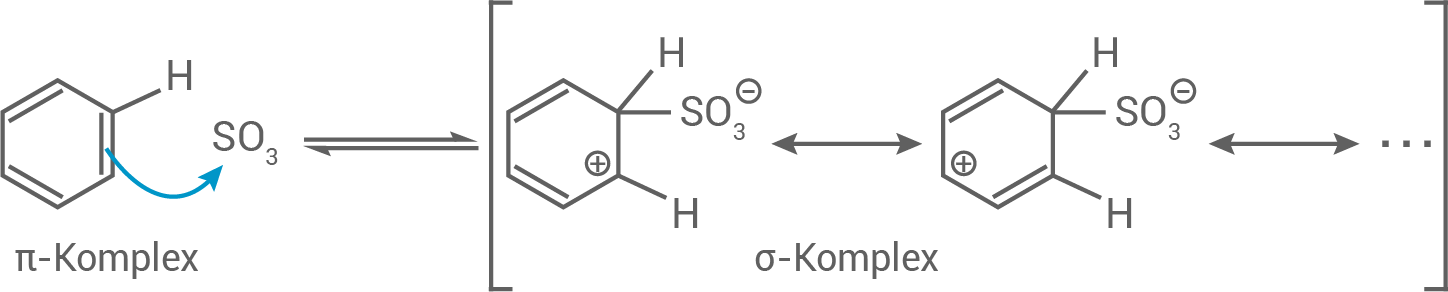 Schritt 2: Rearomatisierung durch intramolekulare Umlagerung von
Schritt 2: Rearomatisierung durch intramolekulare Umlagerung von  -Atomen
-Atomen


3.2.1
Berechnung der Temperatur
Für die Berechnung wird die Gibbs-Helmholtz-Gleichung herangezogen:
 Mit
Mit  gilt:
gilt:
![\(\begin{array}[t]{rll}
T &=& \dfrac{\Delta H}{\Delta S} & \\[5pt]
&=& \dfrac{87,88 \,\text{kJ} \cdot \text{mol}^{-1}}{0,17004\,\text{kJ} \cdot \text{K}^{-1} \cdot \text{mol}^{-1}} & \\[5pt]
&=& 517\,\text{K}
\end{array}\)](https://mathjax.schullv.de/85a1defaffab4a082df16d9b7aff92d60c8c2de62538d93e2dd5e9075df05f85?color=5a5a5a) Auswirkungen einer Temperaturerhöhung
Für eine sich im Gleichgewicht befindliche Reaktion gilt
Auswirkungen einer Temperaturerhöhung
Für eine sich im Gleichgewicht befindliche Reaktion gilt 
Für gilt
gilt  womit der Prozess exergonisch wird und freiwillig abläuft.
womit der Prozess exergonisch wird und freiwillig abläuft.
Für
3.2.2
Skizzierung und Erläuterung der möglichen Entwicklung
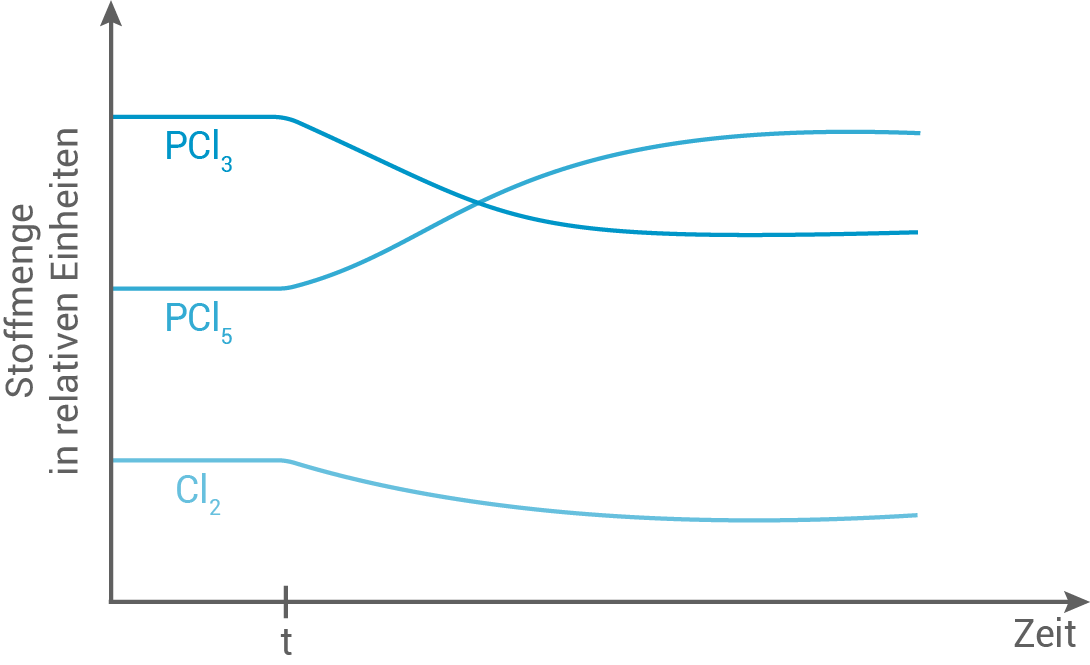 Das Prinzip von Le Chatelier bzw. des kleinsten Zwangs besagt: wenn ein äußerer Einfluss auf ein System ausgeübt wird, das sich im chemischen Gleichgewicht befindet, verschiebt sich die Position des Gleichgewichts so, dass die Auswirkung des Einflusses minimiert wird.
Das Prinzip von Le Chatelier bzw. des kleinsten Zwangs besagt: wenn ein äußerer Einfluss auf ein System ausgeübt wird, das sich im chemischen Gleichgewicht befindet, verschiebt sich die Position des Gleichgewichts so, dass die Auswirkung des Einflusses minimiert wird.
Bei einer Druckerhöhung wird demnach die volumenverkleinernde Reaktion bevorzugt. Hier verschiebt sich das Gleichgewicht auf die Seite von Phosphorpentachlorid da die Stoffmenge im Gleichgewicht zunimmt. Phosphorpentachlorid wird aus Phosphortrichlorid und Chlor gebildet, weswegen deren Stoffmengen bei einer Druckerhöhung im Gleichgewicht abnehmen.
da die Stoffmenge im Gleichgewicht zunimmt. Phosphorpentachlorid wird aus Phosphortrichlorid und Chlor gebildet, weswegen deren Stoffmengen bei einer Druckerhöhung im Gleichgewicht abnehmen.

Bei einer Druckerhöhung wird demnach die volumenverkleinernde Reaktion bevorzugt. Hier verschiebt sich das Gleichgewicht auf die Seite von Phosphorpentachlorid