HT 3 – Genetik
Thema: Erbliche Netzhauterkrankung
1.
Ermittle den Erbgang der Leberschen kongenitalen Amaurose (LCA), indem du andere Erbgänge begründend ausschließt, und leite für die Personen 2, 7, 12, 13 und 15 den jeweiligen Genotyp ab (Material A).
(9 Punkte)
2.
Fasse den Retinal-Zyklus zusammen (Material B). Erläutere mithilfe der Materialien A und B die Symptome der Leberschen kongenitalen Amaurose.
(18 Punkte)
3.
Beschreibe die Funktion des Spleißens während der RNA-Prozessierung bei Eukaryoten. Gib die Aminosäuresequenzen zu den in Tabelle 1 gezeigten DNASequenzen an (Materialien C und E). Ermittle für die in Tabelle 1 angegebenen Sequenzen die Mutationstypen und erläutere die möglichen Folgen der jeweiligen Mutation für das RPE65-Protein (Materialien C und E).
(17 Punkte)
4.
Beschreibe anhand von Abbildung 4 den Ablauf einer RT-PCR (Material D) und werte Abbildung 5 aus (Materialien C und D). Erläutere, warum in Familie B nur das Mädchen, aber nicht die Eltern an LCA erkrankt waren (Materialien A bis D).
(22 Punkte)
Material A: Vererbung der Leberschen kongenitalen Amaurose
Die Lebersche kongenitale Amaurose (LCA) ist eine vererbbare, schwere Form einer Netzhauterkrankung, bei der es zu einer fortschreitenden Zerstörung von Zellen der Netzhaut kommt. Dies ist mit einer starken Verminderung der Sehschärfe und einer Einschränkung des Gesichtsfeldes verbunden. Die Erkrankung schreitet chronisch fort und führt letztlich zur vollständigen Erblindung. Betroffene werden häufig bereits mit schweren Sehbehinderungen oder sogar blind geboren. In anderen Fällen treten die Symptome der Krankheit in den ersten Lebensjahren auf.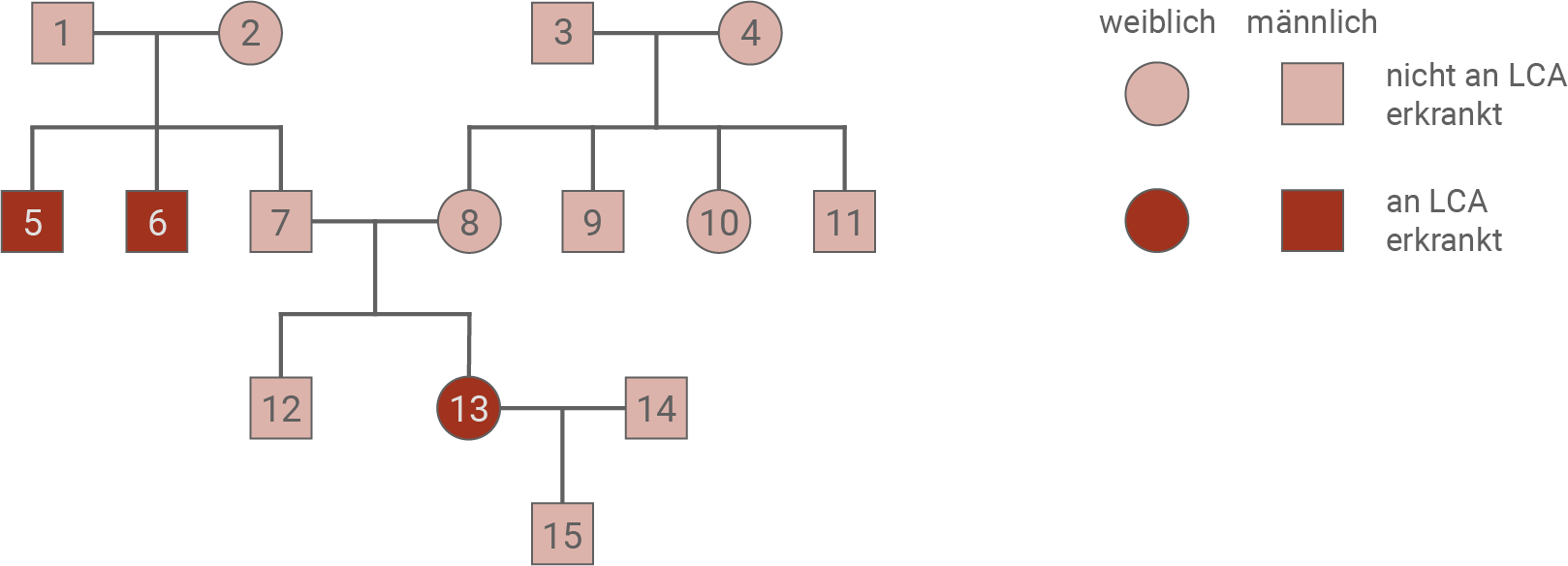
Abb. 1: Stammbaum einer von LCA betroffenen Familie (Familie A)
Material B: Aufgaben der Pigmentschicht
Die Pigmentschicht ist eine dunkel gefärbte Zellschicht im Auge. Sie liegt innen auf der Aderhaut und steht mit den Außensegmenten der Lichtsinneszellen in direkter Verbindung. Die Pigmentschicht absorbiert Streulicht im Auge und transportiert die beim Aufnehmen des Lichtes anfallende Wärme ab. Sie versorgt die Lichtsinneszellen mit Wasser, Ionen und Nährstoffen, baut abgestorbene Lichtsinneszellen ab und ist am Retinal-Zyklus beteiligt (Abbildung 2). Das bei der Fototransduktion gebildete trans-Retinal ist ein Zellgift und kann Schäden an den Proteinen der Außensegmente der Lichtsinneszellen verursachen. Störungen im Stoffwechsel der Pigmentschicht führen zur fortschreitenden Zerstörung ihrer Zellen. Mutationen im RPE65-Gen können sich auf den Stoffwechsel der Zellen in der Pigmentschicht auswirken und letztlich LCA verursachen.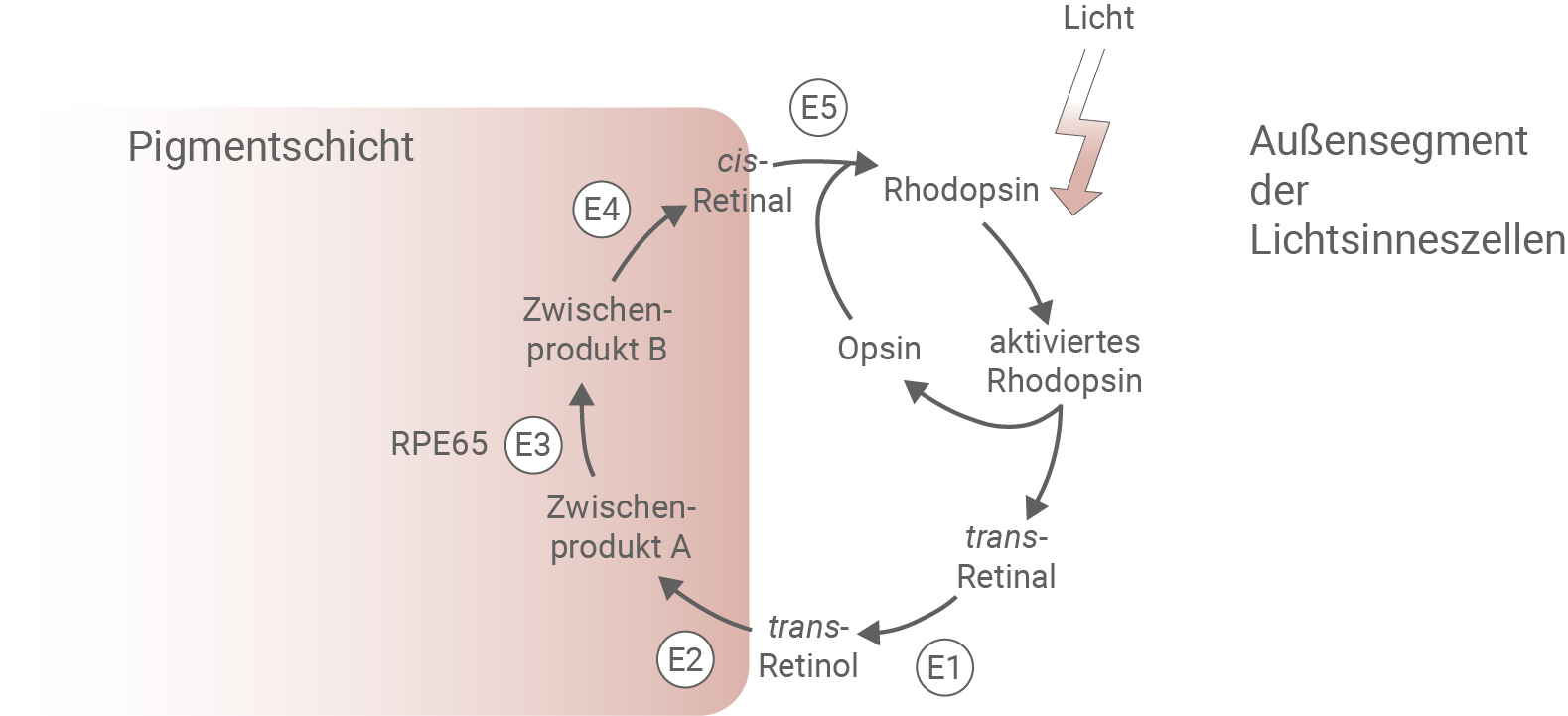
Abb. 2: Der Retinal-Zyklus.
E1 bis E5 kennzeichnen die beteiligten Enzyme.
E1 bis E5 kennzeichnen die beteiligten Enzyme.
Material C: Molekulare Ursachen der LCA
Bisher sind mehr als 17 verschiedene Gene bekannt, deren Mutationen LCA auslösen können. Mutationen im RPE65-Gen sind besonders häufig die Ursache der Krankheit. Es wurden in diesem Gen mehr als 65 verschiedene Mutationen nachgewiesen, die zu LCA führen können. Das RPE65-Gen besteht aus 14 Exons und 13 Introns und codiert für das 533 Aminosäuren umfassende RPE65-Protein (Abbildung 3).
Abb. 3: Schematische Darstellung eines Ausschnitts des RPE65-Gens.
Die Pfeile kennzeichnen die Positionen der in Tabelle 1 dargestellten Mutationen.
Die Pfeile kennzeichnen die Positionen der in Tabelle 1 dargestellten Mutationen.
Tab. 1: In Familie B beobachtete Mutationen im RPE65-Gen im Vergleich zu den jeweils nicht mutierten Sequenzabschnitten (Normal-Allel). Das erste dargestellte Nukleotid entspricht jeweils der ersten Base eines Tripletts im Sequenzabschnitt. Alle Mutationen lagen heterozygot vor.

Material D: Analyse von Mutation 2 mittels RT-PCR
Die Reverse-Transkriptase-Polymerase-Kettenreaktion (RT-PCR) ist eine molekularbiologische Methode zur Untersuchung von RNA (Abbildung 4). Die Reverse Transkriptase ist ein Enzym, das zu einer RNA den komplementären DNA-Strang, die cDNA, herstellt.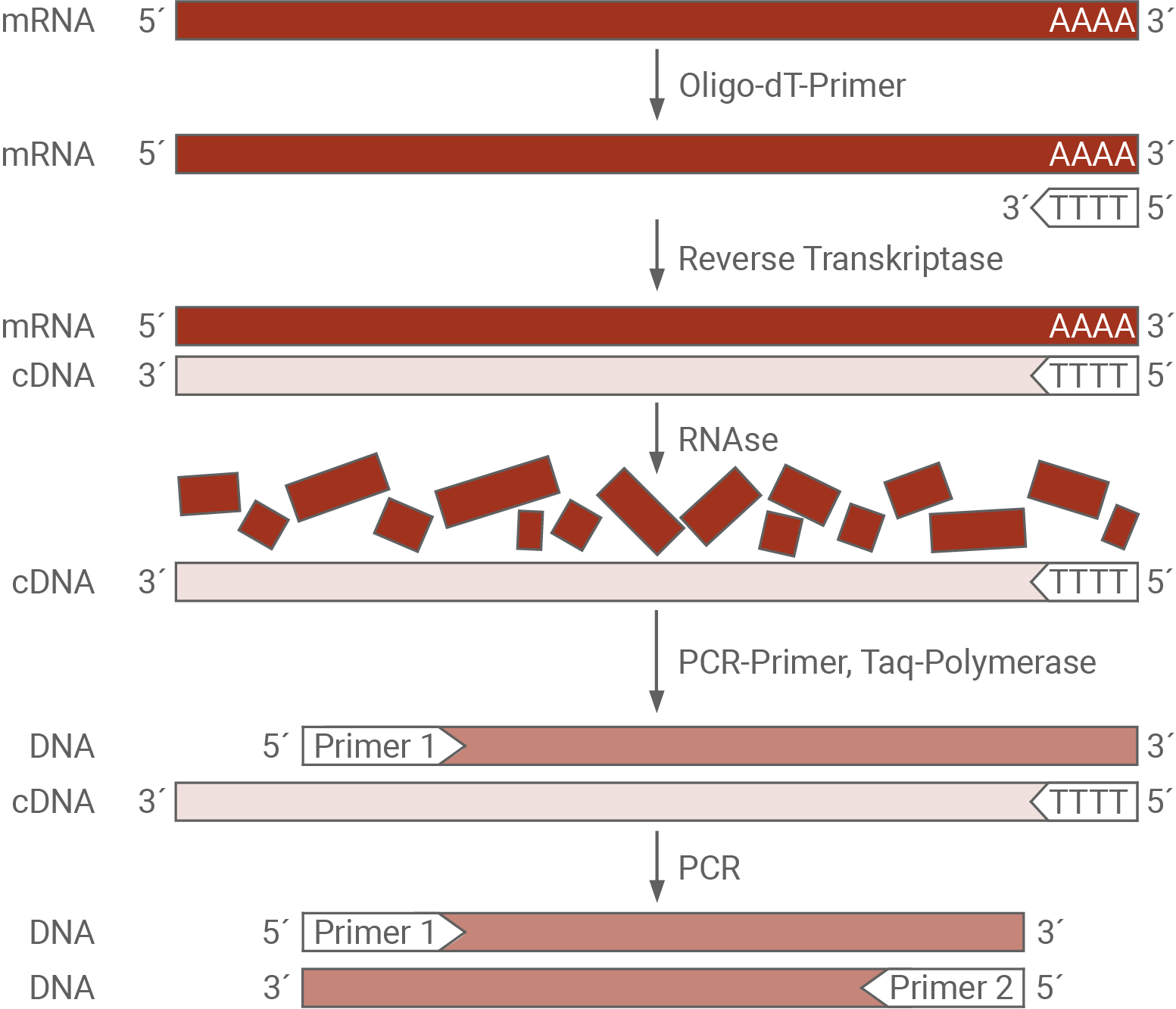
Abb. 4: Ablauf einer RT-PCR.
Waagerechte Pfeile kennzeichnen Primer.
Oligo-dT-Primer: DNA-Primer, der nur aus Thymin-Nukleotiden besteht;
RNAse: RNA-abbauendes Enzym
Die Auswirkung der in Tabelle 1 gezeigten Mutation 2 auf die Expression des RPE65-Gens wurde mithilfe einer RT-PCR untersucht (Abbildung 5A). Dazu wurde sowohl die RNA aus Zellen mit dem Normal-Allel als auch die RNA aus Zellen mit dem Allel mit Mutation 2 isoliert und mithilfe der RT-PCR analysiert. Die erhaltenen RT-PCR-Produkte wurden mittels Gelelektrophorese aufgetrennt und sichtbar gemacht (Abbildung 5B).
Waagerechte Pfeile kennzeichnen Primer.
Oligo-dT-Primer: DNA-Primer, der nur aus Thymin-Nukleotiden besteht;
RNAse: RNA-abbauendes Enzym
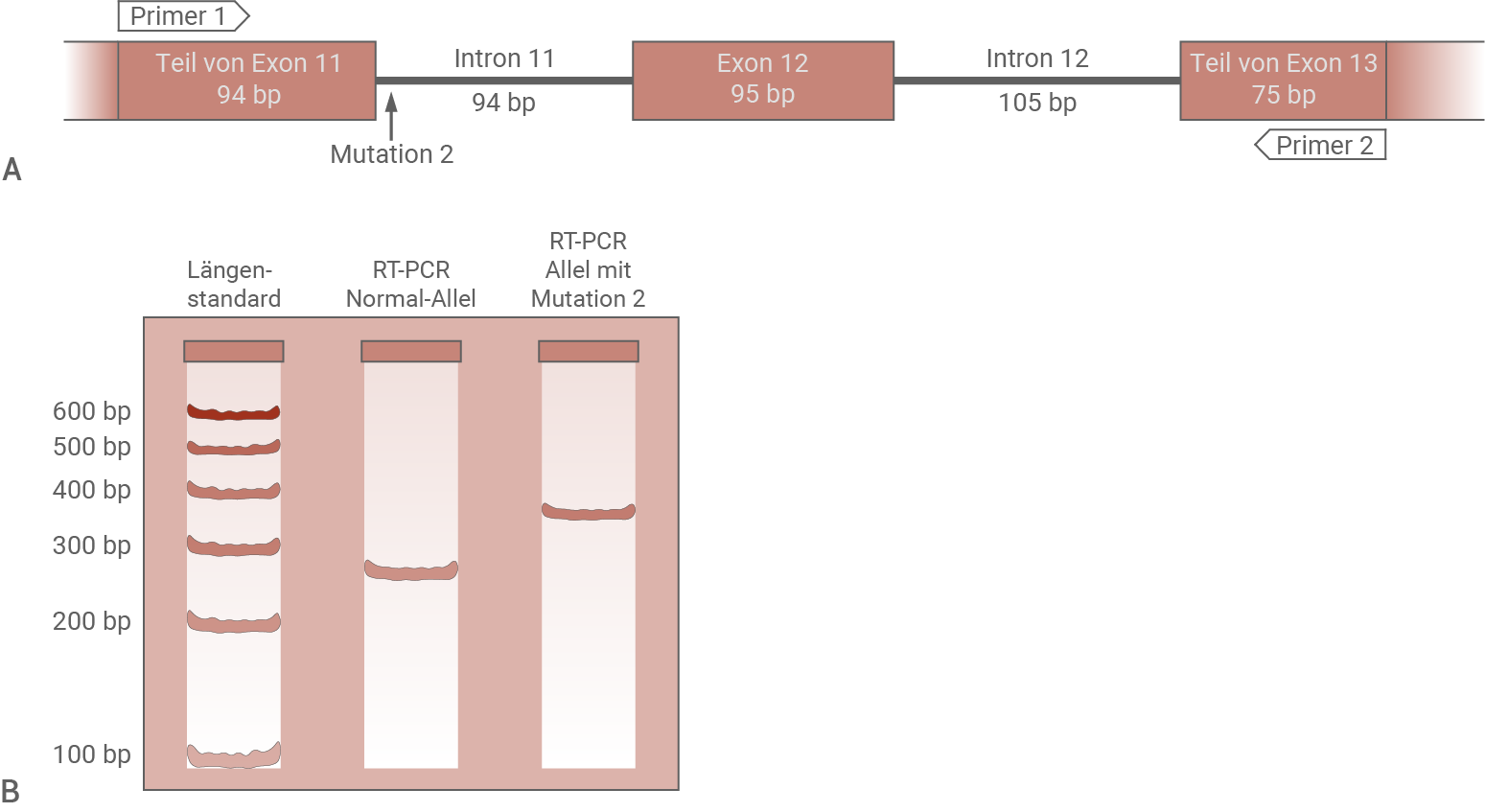
Abb. 5: RT-PCR-Analyse der Expression des RPE65-Gens.
A Schema des untersuchten Genausschnitts. Die Pfeile geben die Positionen der für die RT-PCR verwendeten Primer an.
Die Größen der Intron- und Exonbereiche sind angegeben (bp: Basenpaare);
B Ergebnis der RT-PCR nach Gelelektrophorese
A Schema des untersuchten Genausschnitts. Die Pfeile geben die Positionen der für die RT-PCR verwendeten Primer an.
Die Größen der Intron- und Exonbereiche sind angegeben (bp: Basenpaare);
B Ergebnis der RT-PCR nach Gelelektrophorese
Material E: Codesonne und Tabelle zum genetischen Code
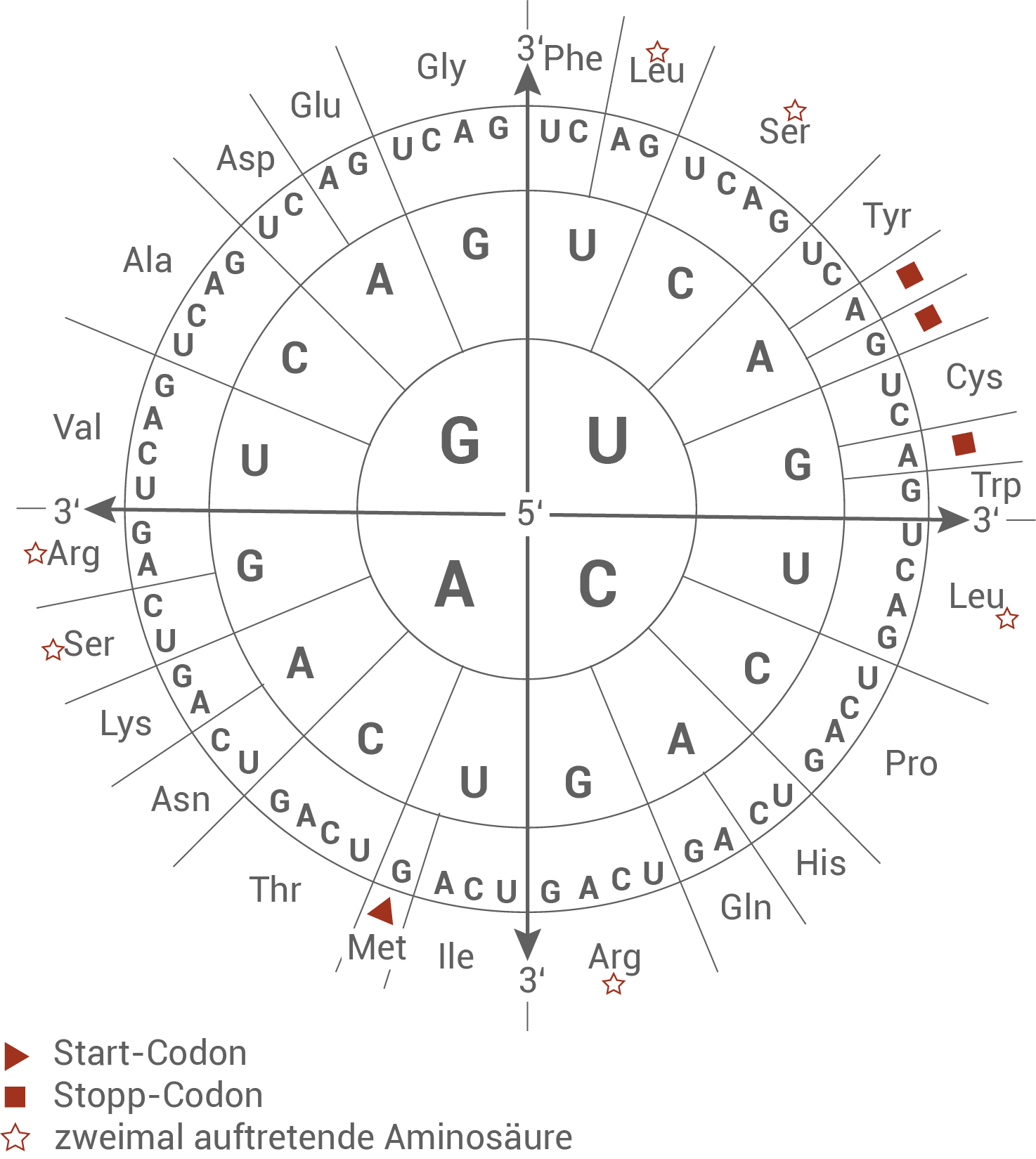
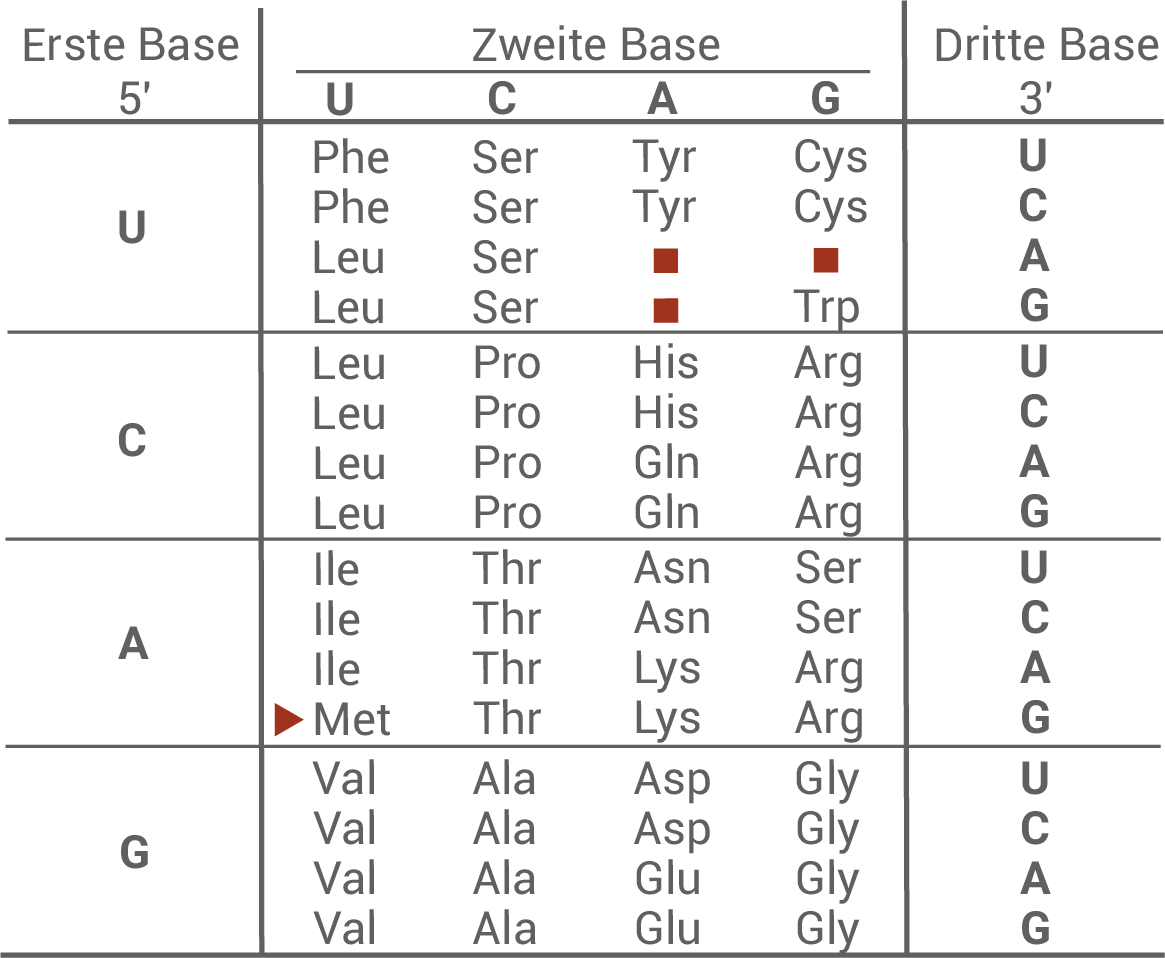
| Ala | Alanin |
|---|---|
| Arg | Arginin |
| Asn | Asparagin |
| Asp | Asparaginsäure |
| Cys | Cystein |
| Gln | Glutamin |
| Glu | Glutaminsäure |
| Gly | Glycin |
| His | Histidin |
| Ile | Isoleucin |
| Leu | Leucin |
| Lys | Lysin |
| Met | Methionin |
| Phe | Phenylalanin |
| Pro | Prolin |
| Ser | Serin |
| Thr | Threonin |
| Trp | Tryptophan |
| Tyr | Tyrosin |
| Val | Valin |
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
Hinweis: Die aufgeführten Lösungen sind stichpunktartig notiert. In der Prüfung ist ein die Stichpunkte inhaltlich umfassender Fließtext erforderlich, um die volle Punktzahl zu erreichen.
1.
Erbgang der Leberschen kongenitalen Amaurose (LCA):
- Da nicht erkrankte Eltern (Nummer 7 und 8) ein krankes Kind (Nummer 13) haben, kann ein dominanter Erbgang ausgeschlossen werden.
- Ein Y-chromosomaler Erbgang kann ausgeschlossen werden, da auch Frauen (Nummer 13) von der Krankheit betroffen sind.
- Ein X-chromosomaler Erbgang kann ausgeschlossen werden, da der Vater (Nummer 7) von der erkrankten Tochter (Nummer 13) gesund ist.
- LCA wird somit autosomal-rezessiv vererbt.
- Die Krankheit wird autosomal rezessiv vererbt, das heißt, Personen mit dem Genotyp aa sind erkrankt. Personen mit Genotyp Aa sind Konduktoren, selbst aber nicht erkrankt, und Personen mit AA sind gesund.
- Die Personen 2 und 7 müssen Konduktoren sein, da sie erkrankte Kinder haben.
- Person 12 ist gesund, wobei der Genotyp AA oder Aa möglich ist.
- Person 13 ist an LCA erkrankt, daher muss sie den Genotyp aa haben.
- Person 15 ist selbst gesund. Da sie aber einen erkrankten Elternteil hat, muss sie Genotyp Aa haben.
2.
Zusammenfassung des Retinal-Zyklus:
- Im Außensegment der Lichtsinneszellen verändert cis-Retinal durch die Absorption von Licht seine räumliche Struktur zu trans-Retinal. Dadurch kann Rhodopsin aktiviert werden.
- Das aktivierte Rhodopsin zerfällt zu Opsin und trans-Retinal. Durch den Retinal-Zyklus wird cis-Retinal und somit Rhodopsin recycelt.
- In diesem Prozess wird trans-Retinal über mehrere Zwischenprodukte unter Beteiligung des Enzyms RPE65 zu cis-Retinal recycelt.
- Das cis-Retinal wird wieder in das Außensegment der Lichtsinneszellen transportiert und bildet dort mit Opsin Rhodopsin, welches dann wieder für die Fototransduktion zur Verfügung steht.
- LCA kann durch eine Mutation des RPE65-Gens ausgelöst werden. Dessen Genprodukt – das Enzym RPE65 ist unter normalen Umständen am Recycling von cis-Retinal aus trans-Retinal beteiligt.
- Ist das Enzym funktionsunfähig, so findet dieser Recyclingprozess nicht statt.
- Trans-Retinal wirkt als Zellgift und kann Schäden an den Proteinen der Außensegmente der Lichtsinneszellen verursachen. Die Zellen sterben nach und nach ab, was zur Entstehung eines größeren, funktionslosen Netzhautbereiches führt.
- Die Sehschärfe nimmt so mit der Zeit stark ab, bis es zu einer vollständigen Erblindung kommt.
- Außerdem kann der Retinal-Zyklus bei einem funktionslosen RPE65 Enzym nicht richtig ablaufen. Cis-Retinal kann nicht in ausreichender Menge gebildet werden. Es folgt ein Mangel an Rhodopsin, und die Fototransduktion ist eingeschränkt. Die Sehschärfe nimmt ab.
- Wenn die Pigmenthaut zerstört oder beschädigt ist, kann Wärme nicht richtig abtransportiert werden. Dadurch können die Lichtsinneszellen geschädigt werden, und das Sehvermögen ist eingeschränkt.
3.
Funktion des Spleißens während der RNA-Prozessierung bei Eukaryoten:
 Hinweis: Die Angabe der mRNA-Sequenz ist für keinen Fall erforderlich
Ermittlung der Mutationstypen:
Hinweis: Die Angabe der mRNA-Sequenz ist für keinen Fall erforderlich
Ermittlung der Mutationstypen:
- Das Spleißen dient der Entfernung der nicht-codierenden Introns, und führt zu einer reifen mRNA mit durchgehendem Leseraster.

- In allen drei Fällen liegt eine Substitution einer Base vor.
- Die erste Mutation liegt im Exon 10 vor. Der Austausch von der Base G zu A ist eine stumme Mutation, da für die gleiche Aminosäure codiert wird.
- Bei Mutation 2 liegt ein Substitution der Base Thymin gegen Adenin vor. Da die Mutation auf Intron 11 liegt, wird sie nicht transliert, da das Intron nicht Teil der reifen mRNA ist.
- Mutation 3 liegt im Exon 14. Der Austausch von C zu A führt zu einer Missense-Mutation. Statt Phe wird Leu exprimiert.
- Da die erste Mutation stumm ist, sollte sie ohne Folgen für das RPE65-Protein bleiben, da die Aminosäure nicht verändert wird.
- Die Intronmutation 2 sollte ebenfalls ohne Folgen bleiben, da hier keine Aminosäure transliert wird.
- Mutation 3 im Exon 14 führt vermutlich zu einer veränderten Raumstruktur des Proteins, da eine andere Aminosäure eingebaut wird. Das RPE65-Protein könnte somit in seiner Funktion eingeschränkt sein.
4.
Ablauf einer RT-PCR:
- An den Poly-A-Schwanz der mRNA wird ein komplementärer Oligo-dT-Primer hybridisiert. Das Enzym Reverse Transkriptase synthetisiert ausgehend von diesem Primer den zur mRNA komplementären DNA-Strang (cDNA).
- Es entsteht ein Doppelstrang aus RNA und DNA. Mittels des Enzyms RNAse kann die RNA aus dem Doppelstrang eliminiert werden.
- Die cDNA liegt nun einzelsträngig vor. An diesen Einzelstrang bindet ein PCR-Primer, welcher durch die Taq-Polymerase einen zu der cDNA komplementären DNA-Strang synthetisiert.
- Der dadurch entstandene DNA Doppelstrang dient in einer nachfolgenden PCR als Matrizenstrang. Ausgehend von diesem Strang wird das gewünschte DNA-Fragment vervielfältigt.
- Durch die RT-PCR konnte ein Fragment von ca. 260 bp Länge des Normal-Allels hergestellt werden. Dies entspricht gerundet der Summe der in Teil A dargestellten, amplifizierten Bereiche der DNA (Exon 11, 12 und 13), die 264 Basenpaare umfassen.
- Im Fall des mutierten Allels wurde ein etwa 360 bp langes Fragment durch die PCR nachgewiesen. Durch Mutation konnte Intron 11 nicht prozessiert werden, und verblieb in der reifen mRNA. Der vervielfältigte Bereich war dadurch 358 Basenpaare lang.
- Der Vater war gesund, da er keine Mutation im RPE65-Gen besaß.
- LCA weist einen autosomal-rezessiven Erbgang auf. Die Mutter besitzt eine Mutation im Intron 11, die sie an ihre Tochter weitergegeben hat. Sie selbst war gesund, da sie nur ein mutiertes Allel besitzt.
- Bei der Tochter lagen Mutationen an drei verschiedenen Stellen vor. Damit sie erkranken konnte, mussten Mutation 2 und 3 auf zwei unterschiedlichen Allelen vorliegen. Mutation 1 ist stumm und kann entweder auf einem oder auf dem anderen Allel liegen.
- Mutation 1 und 3 kamen nur bei der Tochter vor. Vermutlich handelte es sich bei diesen Mutationen also um Spontanmutationen.