Vorschlag A – TRPV1-Rezeptor
Hinweis: Von den Vorschlägen A, B und C soll in der Prüfung nur einer bearbeitet werden.
Der TRPV1-Rezeptor und die Wahrnehmung von Hitzeschmerz
Die Haut ist unser größtes Sinnesorgan. Sie ist dicht besetzt mit Sinneszellen, die verschiedenste Reize registrieren, von Kälte bis Hitze, vom leichten Windhauch bis zum schmerzhaften Stich einer Nadel. Welche Sinneszellen jedoch welche Reize erspüren und wie sie aussehen, hat neben anderen der Medizin-Nobelpreisträger aus dem Jahr 2021, David Julius, herausgefunden. David Julius befasste sich schwerpunktmäßig mit dem Rezeptor für Hitzeschmerz-Wahrnehmung (TRPV1-Rezeptor). Er erkannte, dass das durch Chili ausgelöste Schmerzempfinden dem von Hitze stark ähnelt und konnte so der Funktion des Rezeptors auf die Spur kommen. Für die Untersuchungen am TRPV1-Rezeptor wurden DNA-Bibliotheken hergestellt.Neurophysiologische und sinnesphysiologische Aspekte
1
Skizziere ein myelinisiertes (markhaltiges) Neuron und beschrifte fünf typische Bestandteile dieses Neurons. Ordne die beiden in Material 1 beschriebenen Typen von Schmerzsinneszellen jeweils einem myelinisierten oder nicht myelinisierten (marklosen) Neuron zu und erkläre die unterschiedlichen Leitungsgeschwindigkeiten dieser Neurone. (Material 1)
(14 BE)
2
Beschreibe den Bau und die Funktion des TRPV1-Rezeptors. (Material 2)
(5 BE)
3
Fasse die in der Abbildung in Material 3 dargestellten Versuchsergebnisse einschließlich der Zusatzversuche zusammen und deute diese. Erkläre den Zweck der Untersuchungen an Zellen ohne Rezeptor sowie den Zweck der beiden Zusatzversuche. (Material 2 und 3)
(17 BE)
4
Werte die Versuchsergebnisse aus, die in den Abbildungen 4.1 und 4.2 dargestellt sind. Formuliere zwei Hypothesen zum molekularen Wirkmechanismus von Capsazepin (CAZ). (Material 2 und 4)
(13 BE)
5
Prüfe die Eignung von Capsazepin (CAZ) als Schmerzmittel für chronische Schmerzpatienten sowie von Resiniferatoxin (RTX) als Medikament zur Behandlung von Kniearthrose. (Material 2 und 4)
(10 BE)
Genetische Aspekte
6
Beschreibe den molekularen und räumlichen Aufbau der DNA.
(8 BE)
7
Beschreibe die wesentlichen Schritte zur gentechnischen Veränderung eines Bakteriums mithilfe eines Plasmids.
(8 BE)
8
Beschreibe und erläutere die in Material 6 dargestellte Synthese von doppelsträngiger cDNA. (Material 5 und 6)
(9 BE)
9
Erkläre die Vorteile der Nutzung einer cDNA-Bibliothek für die Transformation der HEK-Zellen mit dem TRPV1-Gen gegenüber einer genomischen DNA-Bibliothek. (Material 5 und 7)
(11 BE)
10
Begründe die Tatsache, dass DNA aus eukaryotischen Zellen ungeeignet ist, um Bakterien mit dem Ziel zu transformieren, eukaryotische Proteine herstellen zu lassen. (Material 5)
(5 BE)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1
Schmerzsinneszellen
Damit der Mensch Schmerz wahrnehmen kann, verfügt er über ein weit verzweigtes System von Sinneszellen, die unterschiedliche schädigende Reize, wie Hitze oder starken Druck, in elektrische Erregungen umwandeln. Diese Erregungen werden dann an das zentrale Nervensystem weitergeleitet. Es gibt zwei Typen von Schmerzsinneszellen, die für zwei unterschiedliche Arten der Schmerzwahrnehmung zuständig sind:Schmerzsinneszellen mit A-delta-Fasern haben schnell leitende Axone, die die Erregung mit einer Geschwindigkeit von ungefähr 20 Metern pro Sekunde weiterleiten. Sie geben die Erregung für ein helles, stechendes Schmerzempfinden weiter. Zu diesen gehören auch die Schmerzsinneszellen, die den TRPV1-Rezeptor (siehe Material 2) enthalten.
Schmerzsinneszellen mit C-Fasern haben langsam leitende Axone mit einer Leitungsgeschwindigkeit von ungefähr 2 Metern pro Sekunde. Sie sind für ein eher stumpfes, tieferes Schmerzempfinden zuständig.
Material 2
Struktur und Funktion des TRPV1-Rezeptors
Der TRPV1-Rezeptor ist ein Ionenkanal, der durch Hitze, aber auch durch Capsaicin, einen Inhaltsstoff der Chilischoten, aktiviert wird. Capsaicin kann als lipophiles Molekül frei durch die Zellmembran diffundieren und so an seine Bindungsstellen gelangen. Inzwischen hat man auch andere Stoffe gefunden, die den TRPV1-Rezeptor beeinflussen. Er nimmt eine zentrale Funktion bei der Vermittlung verschiedener Schmerzreize, insbesondere des Hitzeschmerzes, ein. Außerdem spielt dieser Rezeptor eine wichtige Rolle bei der Regulation der Körpertemperatur.Der TRPV1-Rezeptor im aktivierten Zustand
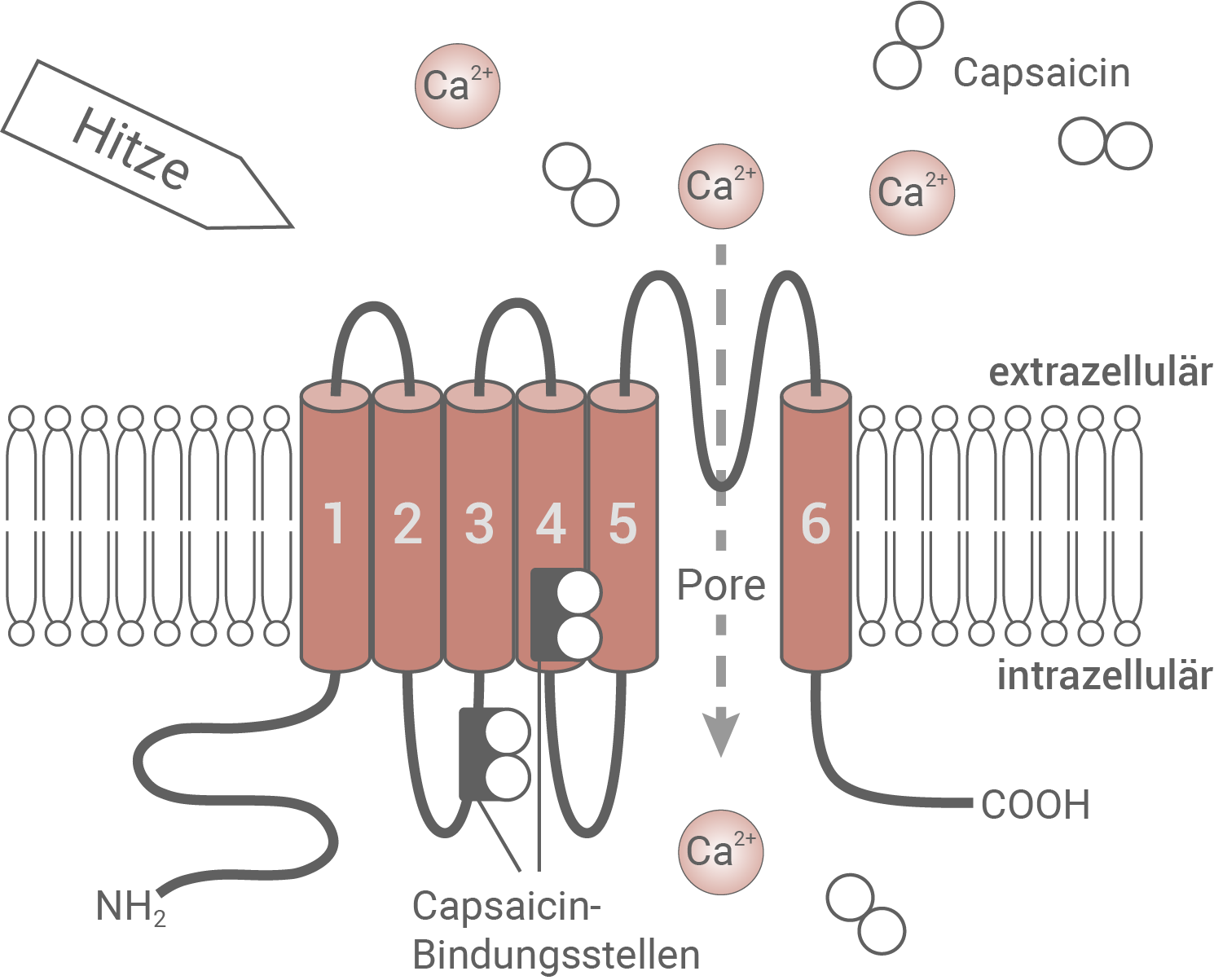
Material 3
Wirkung von Hitzereizen auf den TRPV1-Rezeptor
Experimentelle Untersuchungen zur Wirkung von Hitzereizen erfolgten an Zellkulturen, die den TRPV1-Rezeptor natürlicherweise nicht exprimieren, und an solchen, die durch Einschleusen des TRPV1-Gens dazu gebracht wurden, diesen Rezeptor zu bilden.Für die Untersuchungen wurde allen Zellen ein Farbstoff zugesetzt, den diese intrazellulär binden. In Anwesenheit von Calcium-Ionen kann der Farbstoff durch Laserlicht zum Leuchten angeregt werden (Fluoreszenz). Die Stärke der Fluoreszenz dient als Maß für die Aktivität des TRPV1-Rezeptors. Zunächst wurden beide Zelltypen mehrfach Hitzereizen ausgesetzt. Die Temperatur in den Versuchsansätzen und die Intensität der Fluoreszenz wurden jeweils aufgezeichnet. Weiterhin wurden folgende Zusatzversuche durchgeführt:
1.
Gegen Ende des Experiments, zum Zeitpunkt  , wurde allen Zellen Capsaicin zugesetzt.
, wurde allen Zellen Capsaicin zugesetzt.
2.
Kurze Zeit nach dem Zusetzen von Capsaicin, zum Zeitpunkt  , wurde allen Zellen ein Calcium-Ionophor zugesetzt. Calcium-lonophore ermöglichen Calcium-lonen den Durchtritt durch die Zellmembran, indem sie Calcium-Ionen im Extrazellularraum binden und in der Zelle freisetzen.
, wurde allen Zellen ein Calcium-Ionophor zugesetzt. Calcium-lonophore ermöglichen Calcium-lonen den Durchtritt durch die Zellmembran, indem sie Calcium-Ionen im Extrazellularraum binden und in der Zelle freisetzen.
Versuche zur Wirkung von Hitzereizen auf Zellen mit und ohne TRPV1-Rezeptor
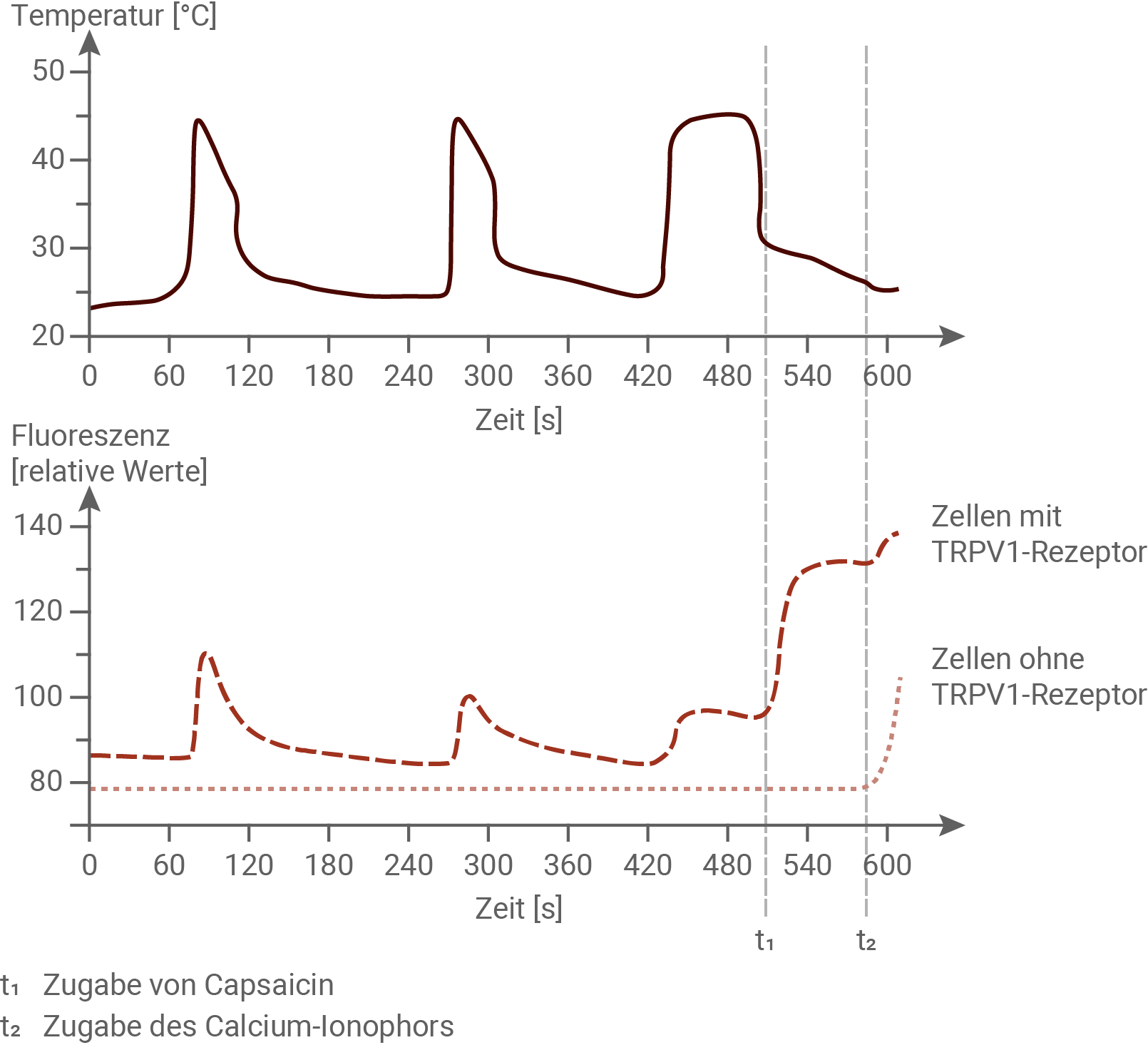
Material 4
Die Wirkung verschiedener Substanzen auf den TRPV1-Rezeptor
Der TRPV1-Rezeptor spielt auch eine wichtige Rolle bei der Überempfindlichkeit für Schmerzempfindungen, die man bei chronischen Schmerzpatienten findet.In der Schmerzforschung werden unterschiedliche Substanzen geprüft, die den TRPV1-Rezeptor beeinflussen können und damit eine Rolle bei der Therapie von chronischen Schmerzen spielen könnten.
Resiniferatoxin (RTX) ist eine Substanz aus Wolfsmilchgewächsen und wird als möglicher Wirkstoff zur Behandlung von Arthrose des Kniegelenks diskutiert. Arthrose ist eine stark schmerzhafte, chronische Entzündungskrankheit. Auch der synthetische Wirkstoff Capsazepin (CAZ) könnte eine Rolle bei der Schmerztherapie spielen. Die Ergebnisse von Untersuchungen zu diesen beiden Wirkstoffen sind in den Abbildungen 4.1 und 4.2 dargestellt. Die Stärke des Calcium-Ioneneinstroms durch den TRPV1-Rezeptor wurde wie in Material 3 anhand der Fluoreszenz gemessen.
Abb. 4.1: Wirkung von RTX und Capsaicin auf TRPV1-Rezeptoren
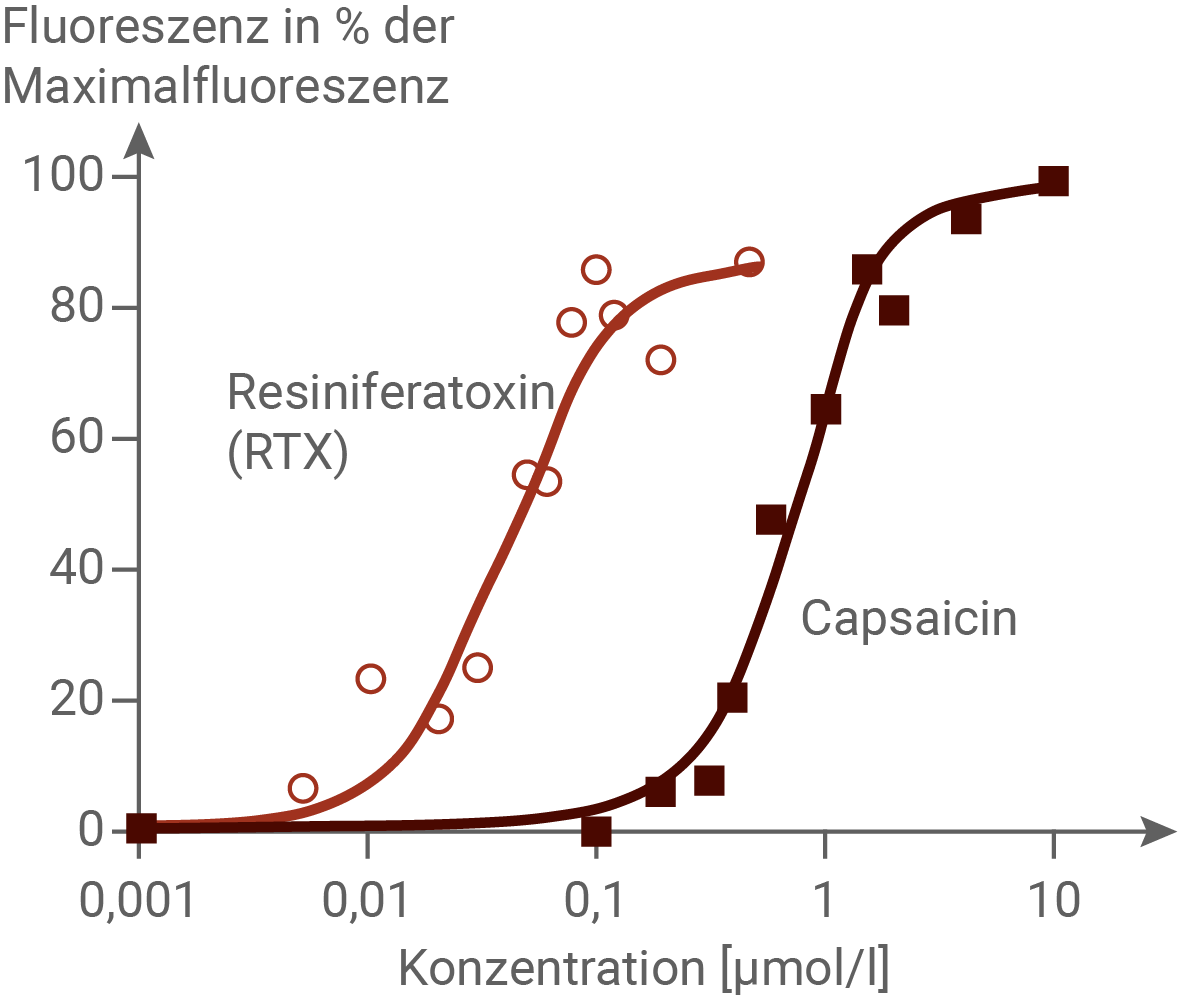

Abb. 4.2: Wirkung von CAZ auf durch Capsaicin aktivierte TRPV1-Rezeptoren
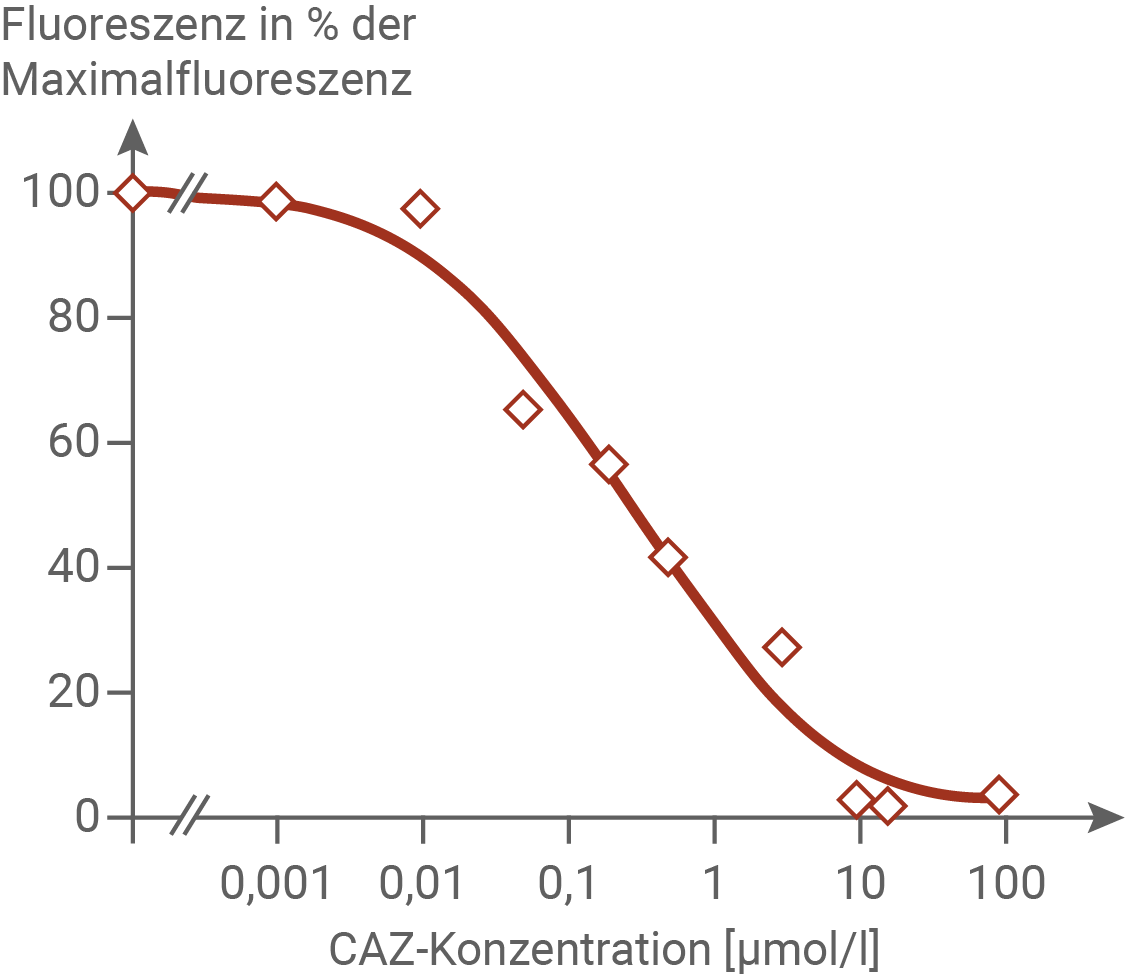
Im Zusammenhang mit der Therapie von Schmerzen wurde zusätzlich die Beobachtung gemacht, dass in der Langzeitanwendung ein gegenteiliger Effekt eintreten kann: Die Empfindlichkeit von Schmerzsinneszellen mit TRPV1-Rezeptoren ist nach einer lang einwirkenden höheren Konzentration an Capsaicin oder von RTX für längere Zeit herabgesetzt.

Material 5
Die Expression des TRPV1-Rezeptors in Zellkulturen
Die in Material 3 und 4 dargestellten Versuchsergebnisse beruhen auf Versuchen mit Zellkulturen. Um sicherzustellen, dass die Ergebnisse ausschließlich auf den TRPV1-Rezeptor und nicht auf andere Rezeptoren mit Ionenkanalfunktion zurückzuführen sind, wurden vom Team um den Nobelpreisträger David Julius Zellen ausgewählt, die natürlicherweise keine Rezeptoren zur Aufnahme von Reizen exprimieren. Sogenannte HEK-Zellen stammen von menschlichen embryonalen Nierenzellen ab und erfüllen diese Bedingung. Um die Funktion des TRPV1-Rezeptors mithilfe dieser Zellen erforschen zu können, wurde das TRPV1-Gen in HEK-Zellen eingebracht und exprimiert. So war sichergestellt, dass keine anderen Rezeptoren zur Reizaufnahme die Versuchsergebnisse beeinflussten. Zum Einschleusen des TRPV1-Gens in die HEK-Zellen arbeiteten die Forscher mit Bakterien, die sie transformierten.Ein Problem beim Einschleusen des TRPV1-Gens bestand darin, dass sowohl seine Sequenz als auch seine Lage im Genom der Schmerzsinneszellen unbekannt waren. Daher musste eine ganze Sammlung von Genen, die das TRPV1-Gen mit Sicherheit enthielt, eine sogenannte DNA-Bibliothek (s. u.), in die HEK-Zellen eingebracht werden. Im Anschluss mussten die HEK-Zellen, die in der Lage waren, den TRPV1-Rezeptor zu synthetisieren, aufgespürt und selektiert werden. Bakterien lassen sich mit unterschiedlichen Zielsetzungen transformieren, beispielsweise zur Herstellung eukaryotischer Proteine oder zum Anlegen von DNA-Bibliotheken. Zwei DNA-Bibliotheken werden im Folgenden dargestellt.
Genomische DNA-Bibliothek
Eine genomische DNA-Bibliothek enthält das gesamte Genom eines Organismus in Form von DNA-Teilstücken, eingebaut in Plasmide in Bakterien. Sie stellt eine Ansammlung der gesamten genomischen DNA eines Organismus in Form von klonierten DNA-Fragmenten dar.Um eine genomische DNA-Bibliothek eines Spenderorganismus anzulegen, wird die gesamte DNA aus Zellen des Spenderorganismus isoliert und mithilfe eines Restriktionsenzyms in tausende Fragmente zerlegt. Diese Fragmente werden jeweils einzeln in Plasmide eingebaut. Anschließend werden Bakterien mit den Plasmiden transformiert. Alle Bakterien, die ein Plasmid mit Spender-DNA aufgenommen haben, werden selektiert und auf Nährböden zu Kolonien vermehrt. Jede Kolonie, also jeder Bakterienklon, enthält nun einen DNA-Abschnitt aus dem Spenderorganismus. Die vollständige Sammlung dieser Bakterienklone mit den eingebauten DNA-Abschnitten aus dem Spenderorganismus bezeichnet man als genomische DNA-Bibliothek. Jeder Bakterienklon steht hierbei sozusagen für ein Buch in dieser Bibliothek.
cDNA-Bibliothek
Neben der genomischen DNA können auch reife mRNA als Ausgangsmoleküle für eine DNA-Bibliothek dienen. Dazu werden alle reifen mRNA-Moleküle aus einem bestimmten Zelltyp isoliert und mithilfe des Enzyms Reverse Transkriptase in cDNA (complementary DNA) umgeschrieben. Die cDNA kann dann entsprechend der genomischen DNA in ein Plasmid eingefügt werden. Auch die Transformation, Selektion und Vermehrung der Bakterien erfolgt wie beim Anlegen einer genomischen DNA-Bibliothek. In einer solchen DNA-Bibliothek, einer sogenannten cDNA-Bibliothek, steht ein Bakterienklon ebenfalls für ein Buch in dieser Bibliothek.Material 6
Synthese von doppelsträngiger cDNA mit einzelsträngigen Enden
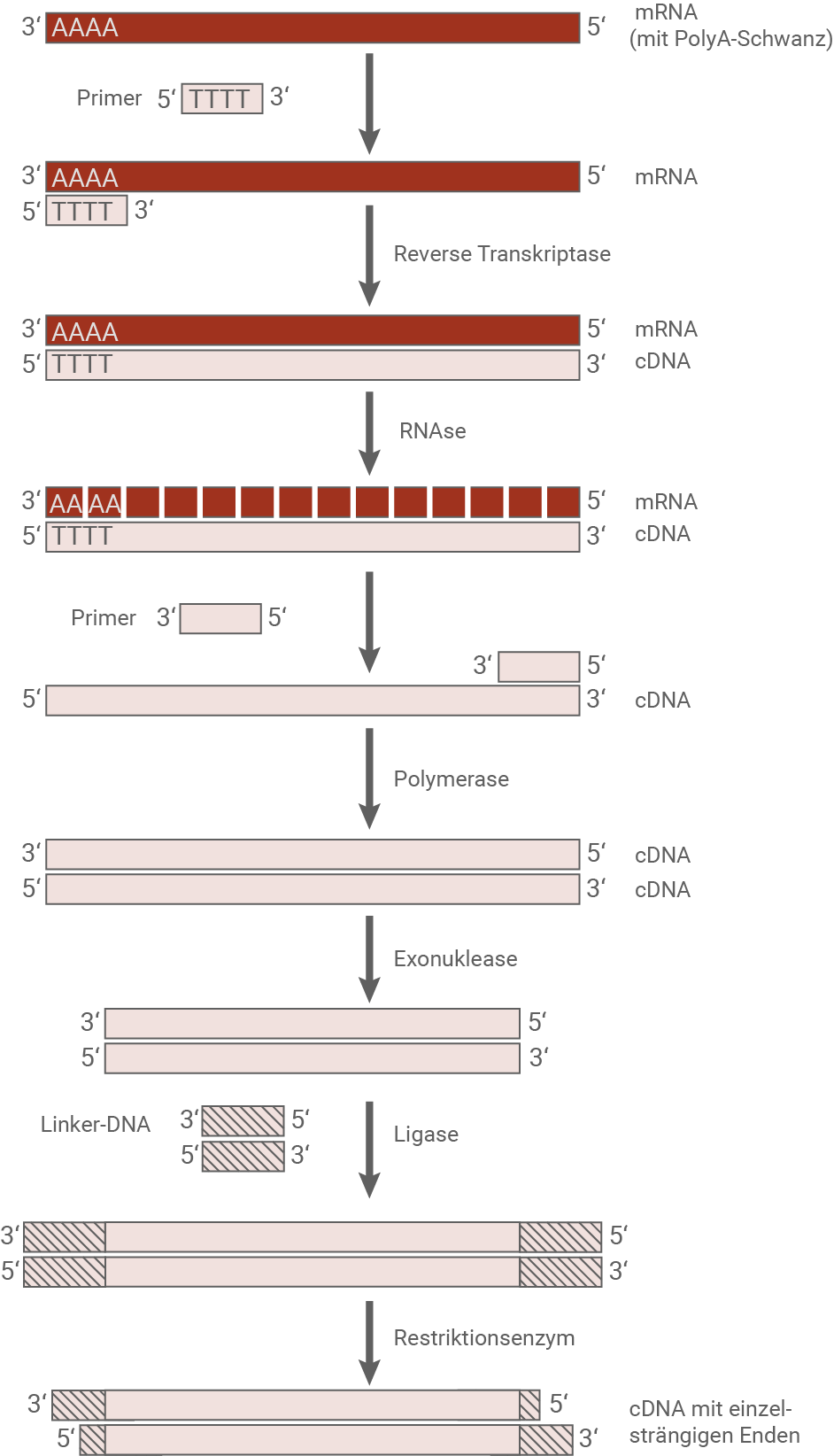
Hinweise
Exonukleasen: Enzyme, die Nukleinsäurenvon den Enden her abbauen
Linker-DNA: DNA-Abschnitte mit Schnittstellen für Restriktionsenzyme
Exonukleasen: Enzyme, die Nukleinsäurenvon den Enden her abbauen
Linker-DNA: DNA-Abschnitte mit Schnittstellen für Restriktionsenzyme
Material 7
Herstellung von HEK-Zellen mit TRPV1-Rezeptor
David Julius und seine Mitarbeiter hatten das Ziel, das Gen für den TRPV1-Rezeptor in HEK-Zellen einzubringen und zu exprimieren. Zu diesem Zweck legten sie eine cDNA-Bibliothek aus Zellen an, die den TRPV1-Rezeptor natürlicherweise exprimieren.Die Plasmide mit eingebauter cDNA wurden anschließend aus der cDNA-Bibliothek isoliert und in Kulturen menschlicher HEK-Zellen eingeschleust.
Die HEK-Zellen, die den TRPV1-Rezeptor nun herstellen konnten, wurden mithilfe von Capsaicin identifiziert und anschließend vermehrt.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
1
Skizze eines markhaltigen Neurons:
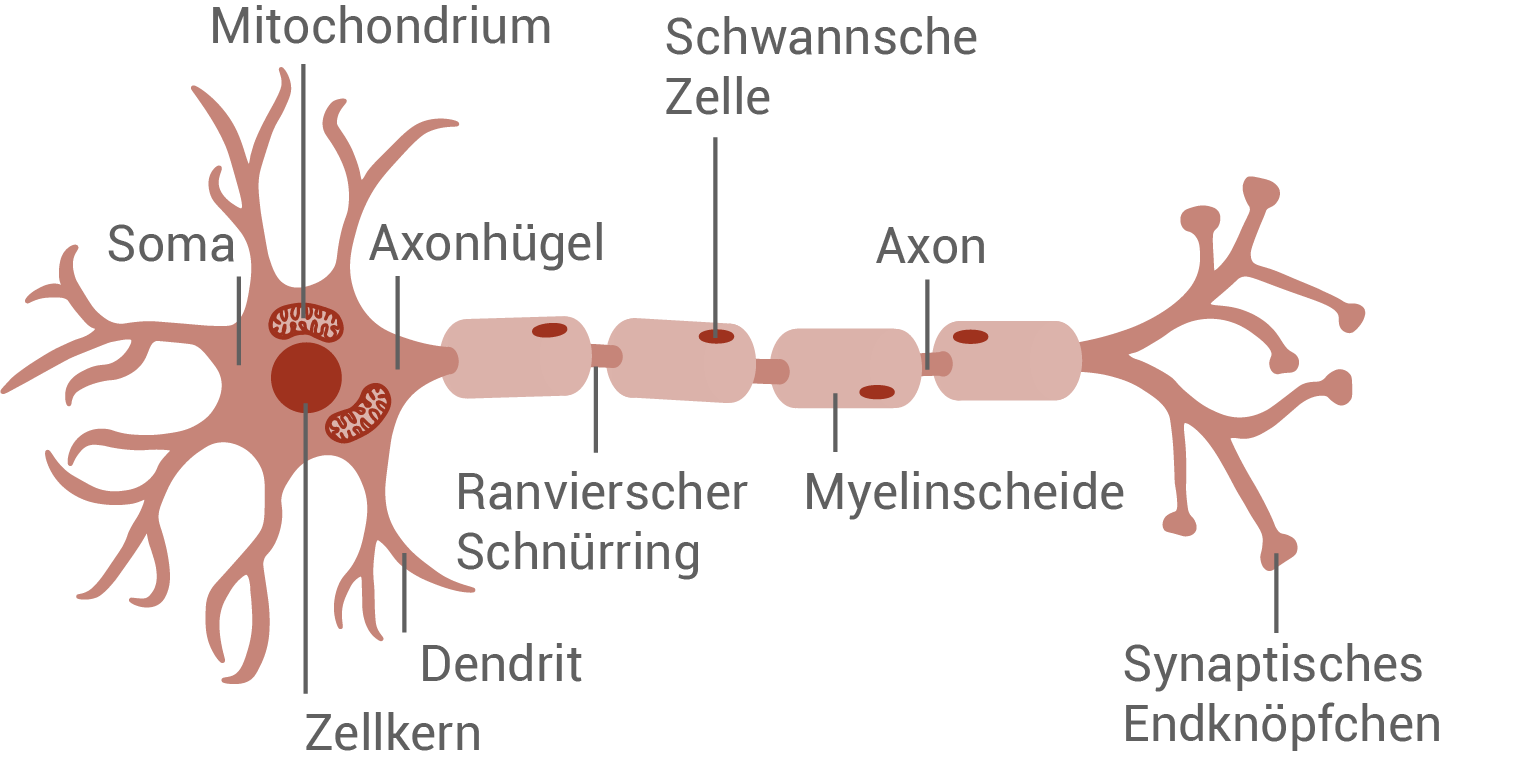 Hinweis: Um die volle Punktzahl zu erreichen genügen fünf typische Bestandteile eines Neurons.
Typen von Schmerzsinneszellen:
Schmerzsinneszellen mit A-delta-Fasern verfügen über eine schnelle Erregungsleitung. Daher sind sie myelinisiert. Die Schmerzsinneszellen mit C-Fasern haben vergleichsweise langsam leitende Axone und gehören daher dem Typ der nicht-myelinisierten Neurone an.
Unterschiedliche Leitungsgeschwindigkeit dieser Neurone:
Hinweis: Um die volle Punktzahl zu erreichen genügen fünf typische Bestandteile eines Neurons.
Typen von Schmerzsinneszellen:
Schmerzsinneszellen mit A-delta-Fasern verfügen über eine schnelle Erregungsleitung. Daher sind sie myelinisiert. Die Schmerzsinneszellen mit C-Fasern haben vergleichsweise langsam leitende Axone und gehören daher dem Typ der nicht-myelinisierten Neurone an.
Unterschiedliche Leitungsgeschwindigkeit dieser Neurone:

- Markhaltiges Neuron: Markhaltige Neurone sind von einer sogenannten Myelinscheide oder Markscheide umgeben, die sie nach außen elektrisch isoliert. Die Myelinschicht bildet aber keine durchgehende Umhüllung, sondern ist immer wieder von sogenannten Ranvier’scher Schnürringen unterbrochen. Das ermöglicht die saltatorische Erregungsleitung. Das Neuron leitet ein Aktionspotential entlang der Ranvier’schen Schnürringe „sprunghaft“ weiter. Es wird dabei immer nur an einem nicht-isolierten Bereich ein Aktionspotential gebildet. Durch die Isolation kann die Leitungsgeschwindigkeit deutlich erhöht werden.
- Markloses Neuron: Bei marklosen Neuronen ist die elektrische Isolierung nicht vorhanden. Die Erregungsweiterleitung erfolgt kontinuierlich über das gesamte Axon. An jeder Stelle der Axonmembran muss eine Depolarisation stattfinden. Daher ist diese Art der Erregungsweiterleitung vergleichsweise langsam.
2
Bau und Funktion des TRPV1-Rezeptors:
Der TRPV1-Rezeptor ist ein integral in die Membran eingelagerter Ionenkanal. Der Rezeptor besteht aus sechs analog aufgebauten Untereinheiten, die über eine Polypeptidkette miteinander gekoppelt sind. Der Ionenkanal kann durch Hitze, aber auch durch Capsaicin aktiviert werden. Eine Aktivierung bedeutet dabei, dass sich zwischen der fünften und sechsten Untereinheit des Kanals eine Pore bildet. Durch diese Pore können Calciumionen und Capsaicin entlang ihres Konzentrationsgefälles ins Zellinnere diffundieren. An der Membraninnenseite befinden sich an der dritten und vierten Untereinheit des Kanals Capsaicin-Bindungsstellen. Durch einen Reiz wird der Ionenkanal folglich ausgelöst, und es kommt zu einer Spannungsänderung der Membraninnenseite aufgrund des Einstroms positiv geladener Calciumionen.
3
Zusammenfassung und Interpretation der Versuchsergebnisse:
Im Experiment wurde die Wirkung von Hitzereizen und dem Wirkstoff Capsaicin auf Zellen ohne natürlich vorkommenden TRPV1-Rezeptor und Zellen, die den TRPV1-Rezeptor exprimieren können, getestet. Die Zellen wurden fluoreszent markiert, sodass bei der Anwesenheit von Calciumionen im Zellinneren ein Fluoreszenzsignal detektiert werden kann. Das Signal ist umso stärker, je aktiver der TRPV1-Rezeptor ist, und je mehr Calciumionen einströmen können. Der TRPV1-Rezeptor kann Hitzereize wahrnehmen. Bei Zellen mit intaktem Rezeptor kann bei Reizung mit Temperaturen von etwa 45 °C unmittelbar ein Fluoreszenzsignal detektiert werden. Bei der ersten Reizung wird eine relative Fluoreszenz von 110 gemessen. Die relative Fluoreszenz nimmt bei den beiden weiteren Reizen leicht ab. Bei Zellen ohne Rezeptor kann kein Fluoreszenzsignal detektiert werden, wenn diese einem Hitzereiz ausgesetzt werden. Zum Zeitpunkt  wird den Zellen der Wirkstoff Capsaicin zugesetzt. Bei den Zellen mit Rezeptor ist dieser sehr aktiv, und es kann eine relative Fluoreszenz von 130 detektiert werden. Zellen ohne Rezeptor reagieren auch auf diesen Reiz nicht. Zum Zeitpunkt
wird den Zellen der Wirkstoff Capsaicin zugesetzt. Bei den Zellen mit Rezeptor ist dieser sehr aktiv, und es kann eine relative Fluoreszenz von 130 detektiert werden. Zellen ohne Rezeptor reagieren auch auf diesen Reiz nicht. Zum Zeitpunkt  wird den Zellen Calcium-Ionophor zugesetzt. Calcium-Ionophor bringen Calciumionen künstlich in die Zelle. Sowohl bei den Zellen mit TRPV1-Rezeptor als auch bei den Zellen ohne TRPV1-Rezeptor kann Fluoreszenz beobachtet werden.
Dass bei Zellen mit Rezeptor ein Signal auf den Hitzereiz nachgewiesen kann, lässt sich damit erklären, dass die in diesen Zellen vorhandenen Rezeptoren auf einen Hitzereiz mit dem Öffnen der porenbildenden Untereinheiten der TRPV1-Rezeptoren reagieren. Folglich können Calciumionen ins Zellinnere gelangen, wo sie den Fluoreszenzfarbstoff aktivieren. Bei einer Reizung mit Capsaicin läuft der gleiche Prozess ab, da die Rezeptoren auch für diesen Wirkstoff empfindlich sind. Werden Zellen mit Rezeptor zusätzlich mit Cacium-Ionophor behandelt, so werden Calciumionen in die Zelle eingeschleust, ohne, dass sie die Pore im TRPV1-Rezeptor passieren müssen. Daher kann eine Fluoreszenz beobachtet werden, die nicht auf die Aktivität des TRPV1-Rezeptors zurückzuführen ist. Bei Zellen, die den Rezeptor nicht exprimieren können, kann bei einer Reizung mit Hitze oder Capsaicin kein Fluoreszenzsignal detektiert werden. Ohne TRPV1-Rezeptor können keine Calciumionen durch die Pore in die Zelle einströmen. Daher kann auch keine Fluoreszenz wahrgenommen werden. Die gleiche Erklärung für das ausbleibende Fluoreszenzsignal gilt auch für die Reizung mit Capsaicin. Wird nun ein Calcium-Ionophor zugesetzt, können Calciumionen in die Zelle gelangen, ohne dass sie die Pore im TRPV1-Rezeptor passieren müssen. Dort binden die Calciumionen den Fluoreszenzfarbstoff, und es kann ein Signal aufgezeichnet werden.
Zweck der Untersuchungen und der Zusatzversuche:
Die Untersuchung von Zellen, die den TRPV1-Rezeptor exprimieren können, und Zellen, die den Rezeptor nicht exprimieren können, soll beweisen, dass ausschließlich TRPV1-Rezeptoren für den durch einen Hitzereiz ausgelösten Calcium-Ioneneinstrom verantwortlich sind. Sind diese Rezeptoren nicht vorhanden, kann auch kein Hitzereiz wahrgenommen werden. Die Zugabe von Capsaicin diente der Beantwortung zweier Fragen. Zum einen sollte durch die Zugabe von Capsaicin herausgefunden werden, ob Thermorezeptoren wie TRPV1-Rezeptoren auch durch chemische Substanzen aktiviert werden können. Zum anderen wurde dadurch untersucht, ob die Zellen nach mehrfacher Hitzereizung immer noch aktiv waren. Die Zugabe von Calcium-Ionophor diente dem Zweck herauszufinden, ob der Fluoreszenzfarbstoff funktionell war.
wird den Zellen Calcium-Ionophor zugesetzt. Calcium-Ionophor bringen Calciumionen künstlich in die Zelle. Sowohl bei den Zellen mit TRPV1-Rezeptor als auch bei den Zellen ohne TRPV1-Rezeptor kann Fluoreszenz beobachtet werden.
Dass bei Zellen mit Rezeptor ein Signal auf den Hitzereiz nachgewiesen kann, lässt sich damit erklären, dass die in diesen Zellen vorhandenen Rezeptoren auf einen Hitzereiz mit dem Öffnen der porenbildenden Untereinheiten der TRPV1-Rezeptoren reagieren. Folglich können Calciumionen ins Zellinnere gelangen, wo sie den Fluoreszenzfarbstoff aktivieren. Bei einer Reizung mit Capsaicin läuft der gleiche Prozess ab, da die Rezeptoren auch für diesen Wirkstoff empfindlich sind. Werden Zellen mit Rezeptor zusätzlich mit Cacium-Ionophor behandelt, so werden Calciumionen in die Zelle eingeschleust, ohne, dass sie die Pore im TRPV1-Rezeptor passieren müssen. Daher kann eine Fluoreszenz beobachtet werden, die nicht auf die Aktivität des TRPV1-Rezeptors zurückzuführen ist. Bei Zellen, die den Rezeptor nicht exprimieren können, kann bei einer Reizung mit Hitze oder Capsaicin kein Fluoreszenzsignal detektiert werden. Ohne TRPV1-Rezeptor können keine Calciumionen durch die Pore in die Zelle einströmen. Daher kann auch keine Fluoreszenz wahrgenommen werden. Die gleiche Erklärung für das ausbleibende Fluoreszenzsignal gilt auch für die Reizung mit Capsaicin. Wird nun ein Calcium-Ionophor zugesetzt, können Calciumionen in die Zelle gelangen, ohne dass sie die Pore im TRPV1-Rezeptor passieren müssen. Dort binden die Calciumionen den Fluoreszenzfarbstoff, und es kann ein Signal aufgezeichnet werden.
Zweck der Untersuchungen und der Zusatzversuche:
Die Untersuchung von Zellen, die den TRPV1-Rezeptor exprimieren können, und Zellen, die den Rezeptor nicht exprimieren können, soll beweisen, dass ausschließlich TRPV1-Rezeptoren für den durch einen Hitzereiz ausgelösten Calcium-Ioneneinstrom verantwortlich sind. Sind diese Rezeptoren nicht vorhanden, kann auch kein Hitzereiz wahrgenommen werden. Die Zugabe von Capsaicin diente der Beantwortung zweier Fragen. Zum einen sollte durch die Zugabe von Capsaicin herausgefunden werden, ob Thermorezeptoren wie TRPV1-Rezeptoren auch durch chemische Substanzen aktiviert werden können. Zum anderen wurde dadurch untersucht, ob die Zellen nach mehrfacher Hitzereizung immer noch aktiv waren. Die Zugabe von Calcium-Ionophor diente dem Zweck herauszufinden, ob der Fluoreszenzfarbstoff funktionell war.
4
Auswertung der Versuchsergebnisse in Abbildung 4.1 und 4.2:
In den Experimenten wurde der Calcium-Ionenstrom durch die TRPV1-Rezeptoren unter Einfluss verschiedener Wirkstoffe gemessen. Bei einer Behandlung mit RTX wurde bei einer Konzentration von etwa 0,7 µmol/l eine Fluoreszenz von etwa 87 % der Maximalfluoreszenz beobachtet. Bei dem Wirkstoff Capsaicin wurde die Maximalfluoreszenz (100 %) erst bei einer Konzentration von etwa 10 µmol/l erreicht. Daraus kann geschlossen werden, dass RTX prinzipiell eine ähnliche Wirkung auf die Zelle hat wie Capsaicin. Bei RTX ist allerdings eine vergleichsweise geringere Konzentration ausreichend, um einen Schmerzreiz hervorzurufen. Der Wirkstoff CAZ hat eine umgekehrte Wirkung auf den Calcium-Ioneneinstrom in die Zelle als Capsaicin und RTX. CAZ bewirkt eine Abnahme der Fluoreszenz, die umso stärker ist, je höher CAZ konzentriert ist. Bei einer Konzentration von 100 µmol/l kann keine Fluoreszenz beobachtet werden. CAZ scheint also den Calcium-Ioneneinstrom ins Zellinnere zu unterbinden.
Hypothesen zum molekularen Wirkmechanismus von Capsazepin:
- Möglich wäre, dass Capsazepin TRPV1-Rezeptoren bindet, und eine Öffnung der Pore verhindert. So kommt ein Einstrom der Calciumionen gar nicht erst zustande.
- Alternativ könnte Capsazepin die Capsaicin Bindestelle im Zellinneren blockieren, sodass Capsaicin keinen Calcium-Ioneneinstrom mehr auslöst.
5
Eignung von CAZ als Schmerzmittel:
CAZ eignet sich als Schmerzmittel für Patienten mit chronischen Schmerzen. Es sorgt dafür, dass an den Schmerzsinneszellen die physikalische oder chemische Reizung nicht mehr in eine elektrische Erregung umgewandelt wird. Dadurch wird die Erregung nicht ans Zentrale Nervensystem weitergegeben, und der Patient nimmt den chronischen Schmerz nicht mehr (oder nur vermindert) wahr. Ein mögliches Risiko bei der Einnahme von CAZ ist allerdings, die stark verminderte Wahrnehmung von Hitzeschmerz. Patienten könnten sich so schneller unbemerkt verbrennen. Da die TRPV1-Rezeptoren auch an der Regulation der Körpertemperatur beteiligt sind, könnte eine Blockade der Rezeptoren die Steuerung des Wärmehaushaltes beeinträchtigen.
RTX als Medikament zur Behandlung von Kniearthrose:
RTX wirkt bei kurzer Anwendungsdauer schmerzfördernd, da es den Calcium-Ioneneinstrom ins Zellinnere verstärkt, und dadurch eine Erregungsweiterleitung verbunden mit dem Empfinden von Schmerzen stattfindet. Bei einer langfristigen Anwendung kann allerdings ein gegenteiliger Effekt eintreten, sodass die Empfindlichkeit von TRPV1-Rezeptoren herabgesetzt ist. Die starken Schmerzen bei Kniearthrose können dadurch gelindert werden, aber die Ursache der Erkrankung wird nicht bekämpft. Der Wirkstoff kann daher eine mögliche Behandlungsmöglichkeit darstellten, sollte aber nur ergänzend zu einer anderen Therapieform erfolgen.
6
Molekularer und räumlicher Aufbau der DNA:
Die DNA besteht aus Nukleotiden, die sich aus dem Zuckermolekül Desoxyribose, einem Phosphatrest und einer der vier organischen Basen Adenin, Cytosin, Guanin und Thymin zusammensetzen. Das Zuckermolekül Desoxyribose besteht aus insgesamt 5 Kohlenstoffatomen. Nummeriert man diese durch, so ist am C1-Atom stets eine der vier Basen gebunden. Zwischen dem 3. Kohlenstoffatom des ersten, und dem 5. Kohlenstoffatom des darauffolgenden Desoxyribosemoleküls befindet sich der Phosphatrest. In einem Einzelstrang sind die Nukleotide so angeordnet, dass abwechselnd ein Zucker- und Phosphatmolekül nach außen zeigen, und das Rückgrat bilden. Dadurch kann den Einzelsträngen eine Strichrichtung zugeordnet werden, wobei die Einzelstränge antiparallel zueinander verlaufen. Die DNA liegt in Form einer Doppelhelix vor, welche in ihrem Inneren durch Wasserstoffbrücken der Basen verbunden ist. Dabei bindet je eine der Purinbasen (Adenin und Guanin) mit einer Pyrimidinbasen (Thymin und Cytosin). Adenin und Thymin binden über zwei Wasserstoffbrücken, wohingegen Guanin und Cytosin über drei Wasserstoffbrücken binden.
7
Gentechnische Veränderung eines Bakteriums mittels Plasmid:
Für den plasmidvermittelten Gentransfer muss das gewünschte Plasmid zunächst isoliert, und mit einem Restriktionsenzym geschnitten werden, sodass „sticky ends“ entstehen. Diese wenigen, überstehenden Basen, dienen später einer vereinfachten Ligation mit dem einzuschleusenden Gen. Dieses wird mit dem gleichen Restriktionsenzym geschnitten, und kann dann über die jeweils komplementären Überhänge mit dem Plasmid durch das Enzym Ligase verbunden werden. Das entstandene rekombinante Plasmid kann nun in eine Bakterienzelle eingeschleust (Transformation), und dort amplifiziert werden. Um die Zellen für die Aufnahme eines Plasmids kompetent zu machen, können diese zum Beispiel einem Hitzeschock ausgesetzt werden.
8
Synthese von doppelsträngiger cDNA:
Die cDNA ist DNA, die aus einer RNA mittels reverser Transkriptase hergestellt wird. Dazu wird zunächst an den Poly-A-Schwanz am 3'-Ende der mRNA ein Poly-T-Primer angelagert, der zu diesem komplementär ist. Ausgehend von diesem Primer werden mit Hilfe des Enzyms Reverse Transkriptase DNA-Nukleotide komplementär an den Matrizenstrang angelagert. Es entsteht ein Doppelstrang aus mRNA-Vorlage und neu synthetisierter cDNA, wobei die mRNA durch das Enzym RNAse abgebaut wird. An das 3'-Ende des verbleibenden cDNA-Strang kann sich ein neuer Primer anlagern. Durch eine DNA-Polymerase wird dieser in 5'-Richtung mit DNA-Nukleotiden komplementär ergänzt, sodass ein cDNA-Doppelstrang entsteht. Durch das Enzym Exonuklease werden die Enden des cDNA-Doppelstranges teilweise abgebaut. Durch das Enzym Ligase wird nun Linker-DNA an die Enden angesetzt. In der Linker-DNA sind Schnittstellen enthalten, die die Erzeugung von sticky ends durch Restriktionsenzyme ermöglichen.
9
Vorteile der Nutzung einer cDNA-Bibliothek:
Eine genomische DNA-Bibliothek enthält das gesamte Genom des Spenderorganismus. Im Gegensatz dazu sind in einer cDNA-Bibliothek nur diejenigen Gene enthalten, die vom jeweiligen Zelltyp (in diesem Fall Schmerzsinneszellen) tatsächlich exprimiert werden. Die cDNA-Bibliothek ist also weniger umfangreich, da sie im Gegensatz zur genomischen DNA-Bibliothek nur codierende Sequenzen (Exons) enthält. Das hat den Vorteil, dass die Sequenz für das Zielgen in weniger Bakterien gespeichert werden kann. Das Einbringen des Zielgens in HEK-Zellen gestaltet sich dadurch wesentlich einfacher. Es müssen insgesamt weniger Fragmente, die potenziell für die TRPV1-Rezeptoren codieren könnten, in die Zellen eingebracht werden. Dadurch wird auch die Identifikation und Selektion der transformierten Zellen erleichtert. Beim Anlegen einer genomischen DNA-Bibliothek werden zur Fragmentierung Restriktionsenzyme genutzt, die durch Zufall auch das Zielgen zerschneiden könnten.
10
Warum Bakterien zur Exprimierung eukaryotischer Proteine ungeeignet sind:
Bei Bakterien findet die Translation unmittelbar nach der Transkription statt. Es findet kein Spleiß-Vorgang im Zellkern statt. Würde man ein eukaryotisches Gen in eine Bakterienzelle einschleusen, so würde zunächst wie in Eukaryoten eine prä-mRNA entstehen. Diese würde dann aber direkt in ein Protein umgeschrieben werden, da Bakterien die für das Prozessieren notwendigen Faktoren fehlen. Das so entstehende Protein wäre vermutlich aufgrund der zusätzlichen Länge und einer abweichenden 3D-Struktur stark in seiner Funktion eingeschränkt. Daher eignen sich Bakterienzellen nicht für die Exprimierung eukaryotischer Proteine.