Vorschlag B – Götterspeise und Färbemittel
Für Menschen, die sich vegetarisch oder vegan ernähren, gibt es heute im Handel Götterspeiseprodukte auf Basis von Agarose, einem Polysaccharid, das aus Rotalgen gewonnen wird.
Zum Einfärben von Lebensmitteln werden verschiedene Farbstoffe verwendet. Für die Herstellung sogenannter Azofarbstoffe wird der Stoff Aminobenzol benötigt.
Auch zum Einfärben von Götterspeise bzw. Götterspeiseprodukten werden verschiedene Farbstoffe verwendet, wobei zum Beispiel Saflorkonzentrat zum Einsatz kommen kann. Die Bezeichnung Saflor wird jedoch in verschiedenen Zusammenhängen für Stoffe verwendet, die sich zum Färben eignen. So gibt es diesen Begriff neben der Verwendung für die Färber-Distel-Pflanze, die zum Beispiel für das Färben von Lebensmitteln eingesetzt wird, auch für den sogenannten Cobalt-Saflor. Cobalt-Saflor besteht aus Cobaltoxiden und bildet sich bei der Verarbeitung von cobalthaltigen Gesteinen (Cobalterzen). Früher wurde Cobalt-Saflor beispielsweise zum Färben von Porzellan und Glas verwendet.
Material 1
Gelatine
In Gelatine kommt die Aminosäure Glycin (Aminoethansäure) mit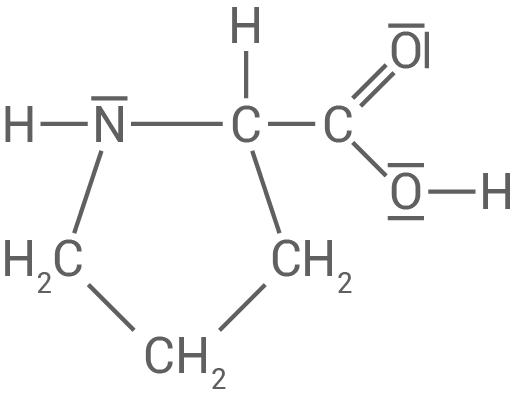
Material 2
Alanin
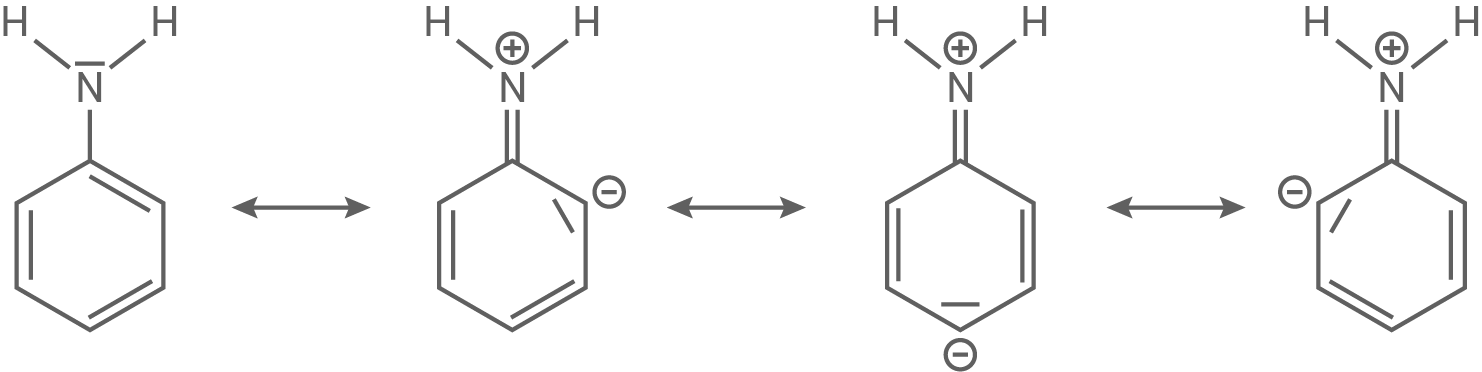
Aminobenzol
Material 3
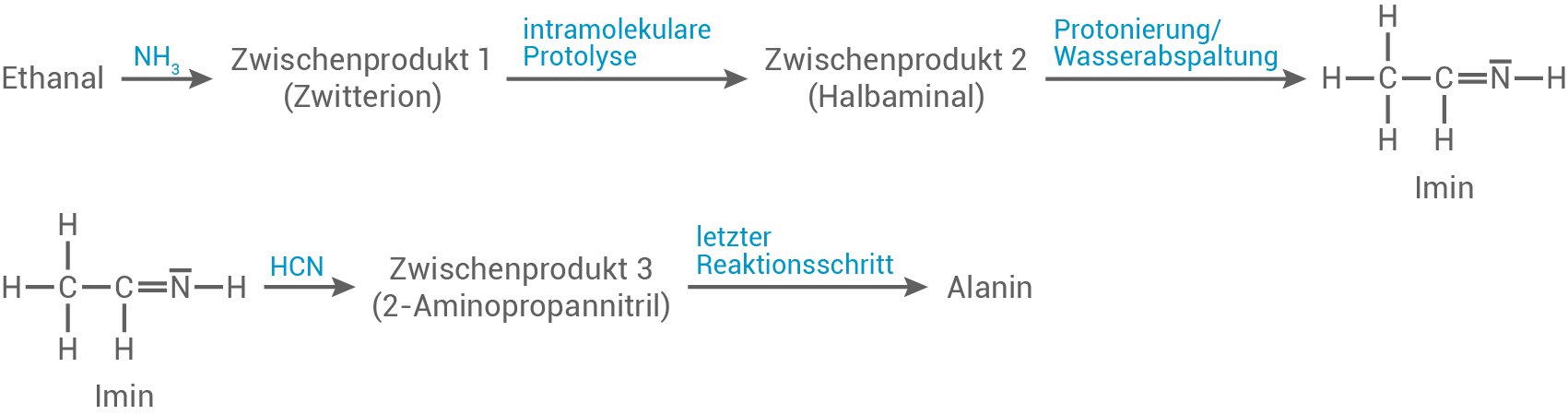
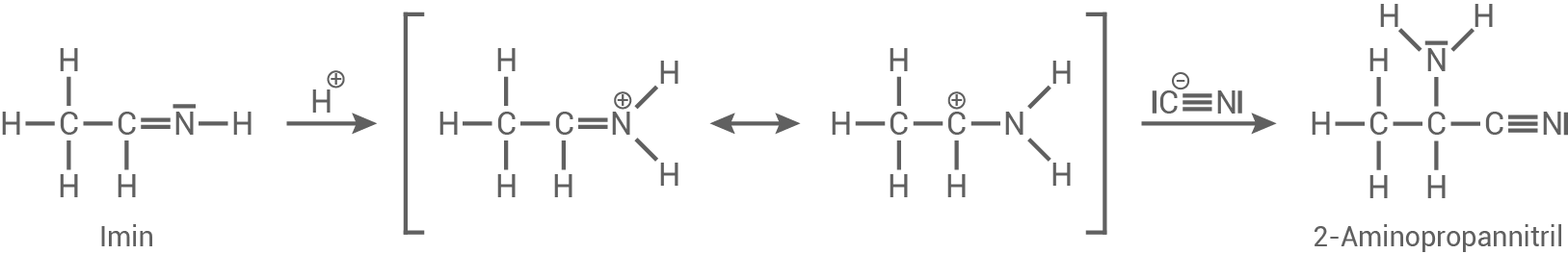
Strecker-Synthese von Alanin
Material 4
Raumstrukturen von Kollagen und Gelatine
Gelatine besteht aus tierischen Proteinen und wird aus Kollagenen (Bindegewebsproteinen) verschiedener Tierarten gewonnen. In der Struktur von Kollagenen sind jeweils drei Protein-Moleküle (jeweils in Helix-Struktur) zusammengelagert. Bei jeder dadurch vorliegenden sogenannten „Tripel-Helix" ragen die hydrophoben (wasserabweisenden) Reste aus der Helix-Struktur heraus, während die hydrophilen (,wasserliebenden") Reste in das Innere der Helix-Struktur weisen.Bei der Herstellung von Gelatine werden die Kollagene zunächst erhitzt und anschließend wieder abgekühlt. Dadurch wird die Raumstruktur verändert (siehe Abbildung).
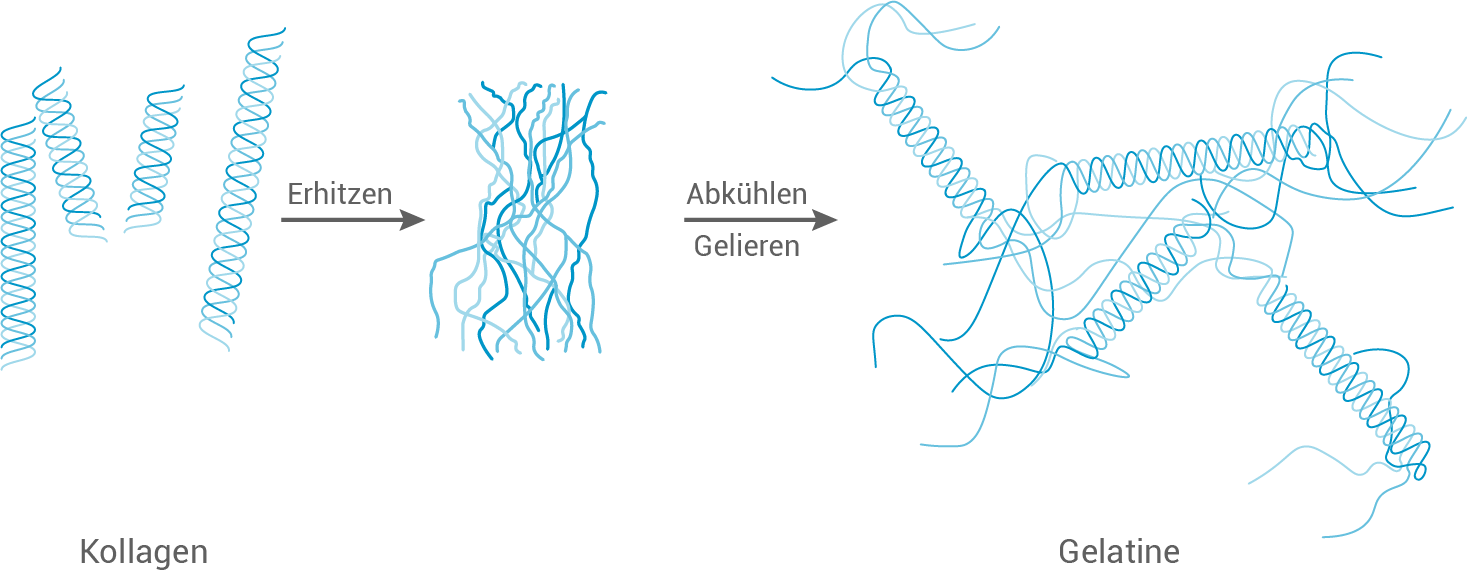
In dieser schematischen Abbildung entspricht die Darstellung der Länge einzelner Tripel-Helix-Strukturen und Helix-Strukturen jeweils im Vergleich (siehe vor, während und nach dem Erhitzen) nicht den tatsächlichen Verhältnissen. Im Gegensatz zu Kollagenen quillt Gelatine in Wasser auf. Beim Aufquellen der Gelatine kommt es durch die Einwirkung des Wassers zu einer Zunahme des Volumens.
Material 5
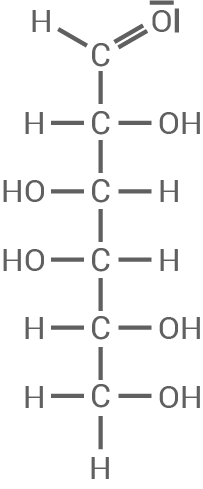
Agarose
Agarose ist ein Polysaccharid, das aus D-Galactose-Bausteinen und 3,6-Anhydro-L-galactose-Bausteinen besteht, die glycosidisch miteinander verknüpft sind (siehe Abbildung).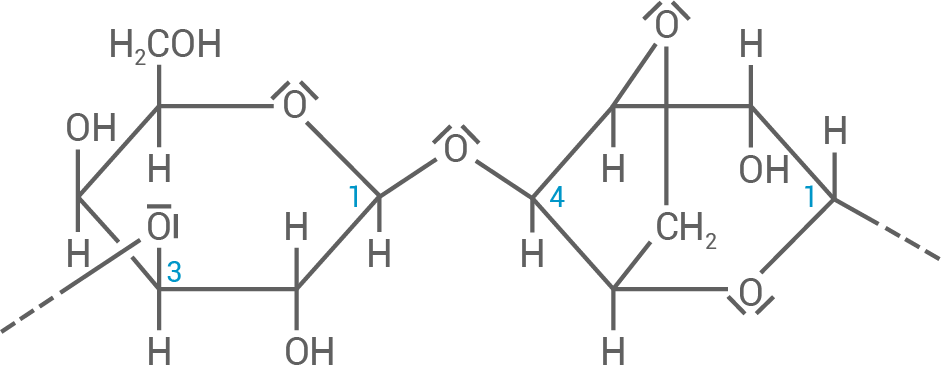
Material 6
Herstellung von Cobalt-Saflor
Cobalt-Saflor entsteht beim Erhitzen von CobaltarsenidenIn der Verbindung
Zum besseren Verständnis des Aufbaus dieser Verbindung lässt sich das Anzahlverhältnis der Ionen auch folgendermaßen darstellen bzw. verdeutlichen:
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
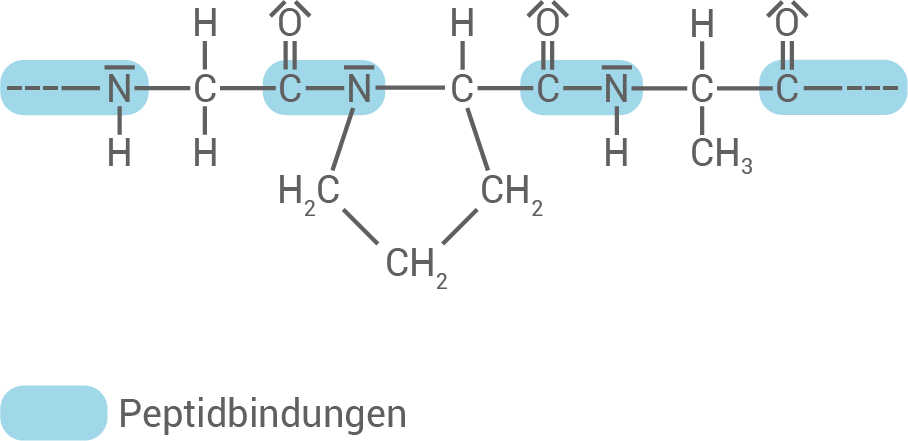

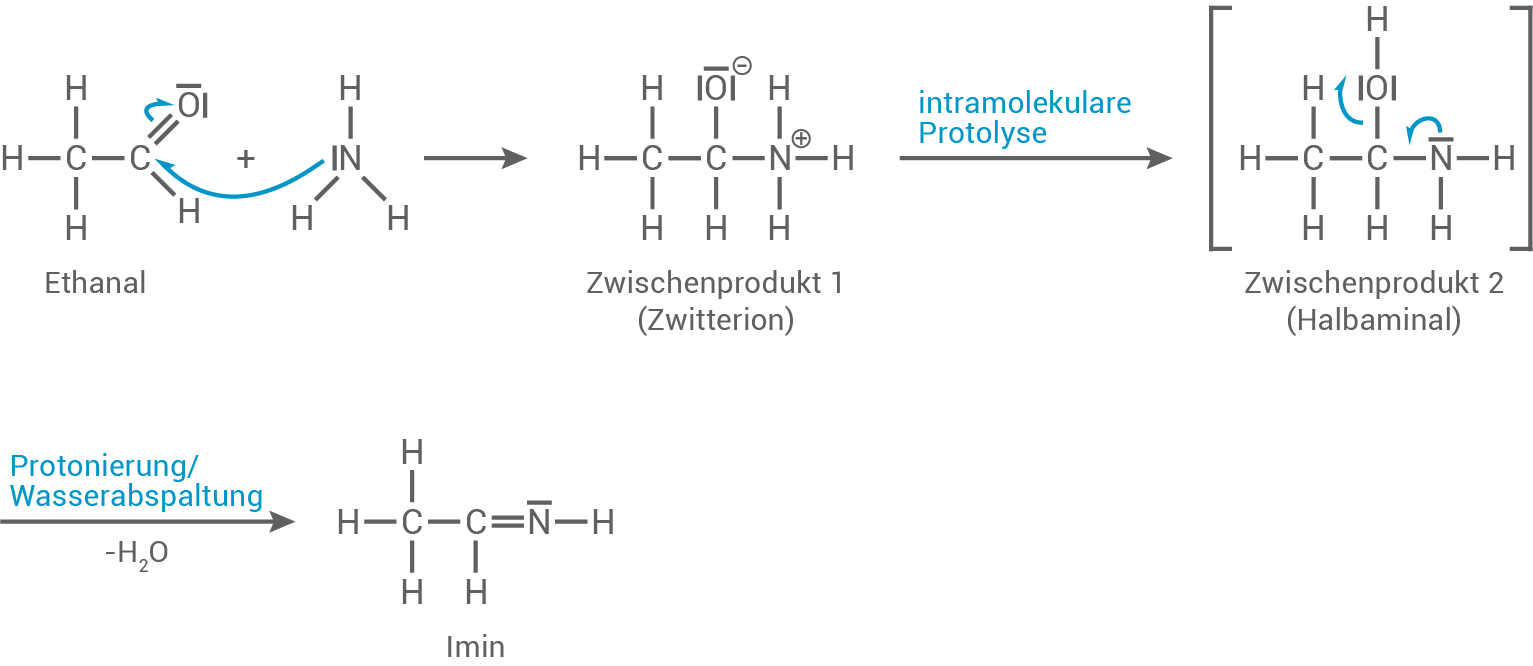
Die Raumstruktur von Kollagen besteht aus drei Polypeptidketten, die zu einer Tripelhelix verdrillt sind. Diese Struktur wird durch Wasserstoffbrückenbindungen und hydrophobe Wechselwirkungen stabilisiert. Die hydrophoben Reste der Aminosäuren ragen nach außen, während die hydrophilen Reste nach innen weisen, was die Struktur zusätzlich stabilisiert.
Bei der Herstellung von Gelatine wird das Kollagen zunächst erhitzt. Durch das Erhitzen brechen die Wasserstoffbrückenbindungen und die hydrophoben Wechselwirkungen, wodurch die Tripelhelix aufgelöst wird. Beim anschließenden Abkühlen bildet sich eine ungeordnete random-coil-Struktur, die für Gelatine typisch ist.
Verhalten von Kollagen und Gelatine in WasserKollagen quillt in Wasser nur sehr wenig auf, da die Tripelhelix durch die starken Bindungen sehr stabil ist. Die dichte Packung der hydrophoben Reste trägt dazu bei, dass wenig Wasser eindringen kann. Gelatine hingegen quillt in Wasser stark auf, da die random-coil-Struktur weniger stabil ist und flexibler auf äußere Einflüsse reagiert. Durch diese Flexibilität kann Gelatine Wasser leichter aufnehmen, was zu einer Volumenzunahme führt.
Die Reaktionsgleichung lautet:
- Bei der Bildung von
aus
bleibt die Oxidationszahl für zwei der Kobalt-Atome bei
während ein Kobalt-Atom von
auf
reduziert wird. Daher wird ein Elektron pro Cobalt reduziert
pro
was insgesamt
Elektronen für Kobalt ergibt.
- Jedes Arsen-Atom wird um
Elektronen oxidiert
von
zu
Da es in
insgesamt
Arsen-Atome gibt
Moleküle, jedes enthält
Arsen-Atome
ergibt dies
Elektronen für Arsen.