Vorschlag C – Chemie der Banane
Es gibt keine andere Obstart, die weltweit so beliebt ist wie die Banane. Durchschnittlich verzehrt jeder Deutsche  Bananen pro Jahr. Reife Obstbananen enthalten etwa
Bananen pro Jahr. Reife Obstbananen enthalten etwa  Wasser,
Wasser,  Kohlenhydrate und zahlreiche weitere Inhaltsstoffe.
Das charakteristische Bananenaroma wird durch eine Vielzahl von Stoffen geprägt. So gehören Ester aus Pentanol-Isomeren und Ethansäure bzw. Butansäure sowie verschiedene Hepten-Verbindungen zu den wichtigsten Aromastoffen in Bananen. Weiterhin ist auch das sogenannte „Glückshormon“ Serotonin in Bananen enthalten.
Kohlenhydrate und zahlreiche weitere Inhaltsstoffe.
Das charakteristische Bananenaroma wird durch eine Vielzahl von Stoffen geprägt. So gehören Ester aus Pentanol-Isomeren und Ethansäure bzw. Butansäure sowie verschiedene Hepten-Verbindungen zu den wichtigsten Aromastoffen in Bananen. Weiterhin ist auch das sogenannte „Glückshormon“ Serotonin in Bananen enthalten.
Aus der Reaktion von Pent-2-en mit Wasser entsteht Pentan-2-ol. Reaktion B: 2-Chlorpentan reagiert mit Hydroxid-Ionen zu Pentan-2-ol und einem Anion. Reaktion C: Setzt man Pentan-2-on mit elementarem Wasserstoff um, erhält man ebenfalls Pentan-2-ol.
3.1
Formuliere den Mechanismus der säurekatalysierten Veresterung von Ethansäure mit Ethanol.
Entwickle für jeden Teilschritt dieses Reaktionsmechanismus unter Nutzung der Fachsprache eine passende Überschrift.
(11 BE)
3.2
Die beiden Ester 2-Pentylethanoat und (2-Methylbutyl)butanoat (Material 1) gehören zu den wichtigsten Aromastoffen in Bananen. Beide Moleküle enthalten jeweils ein asymmetrisches Kohlenstoff-Atom.
Formuliere mithilfe von Material 1 die Strukturformeln der beiden Ester mit allen bindenden und nichtbindenden Elektronenpaaren.
Gib an, was man unter den Begriffen „asymmetrisches Kohlenstoff-Atom“ und „Enantiomere" versteht und beschrifte in den beiden Strukturformeln der Ester jeweils das asymmetrische Kohlenstoff-Atom.
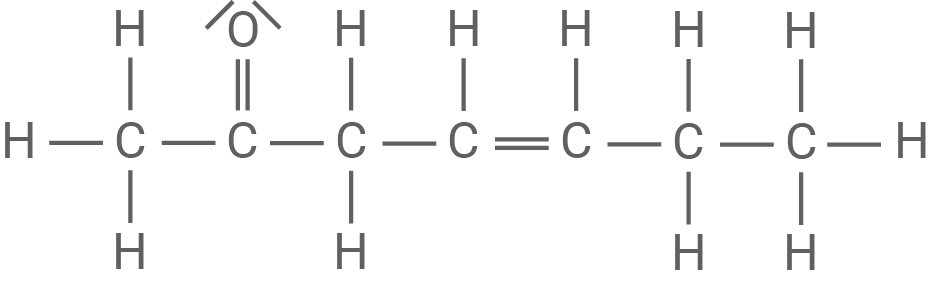
Benenne den ebenfalls in Bananen enthaltenen Aromastoff in Material 2 sowie dessen charakteristische funktionelle Gruppen.
(10 BE)
3.3
Material 3 beschreibt drei Reaktionen zur Synthese von Pentan-2-ol, einem Ausgangsstoff für die Herstellung des Aromastoffs 2-Pentylethanoat.
Formuliere für die drei Reaktionen zur Synthese von Pentan-2-ol jeweils eine Reaktionsgleichung, verwende für die organischen Verbindungen Strukturformeln.
Benenne für Reaktion A den Reaktionsmechanismus sowie für die Reaktionen B und C jeweils den Reaktionstyp.
(8 BE)
3.4
Kohlenhydrate sind – nach Wasser – der Hauptbestandteil von Bananen.
Zeichne für ein Stärke-Molekül (Amylose) einen Strukturformelausschnitt aus drei Monomer-Einheiten und beschreibe den Aufbau eines Amylose-Moleküls.
Deute das in Material 4 beschriebene Experiment und begründe den wesentlich süßeren Geschmack einer reifen Banane im Vergleich mit einer unreifen Banane.
(10 BE)
3.5
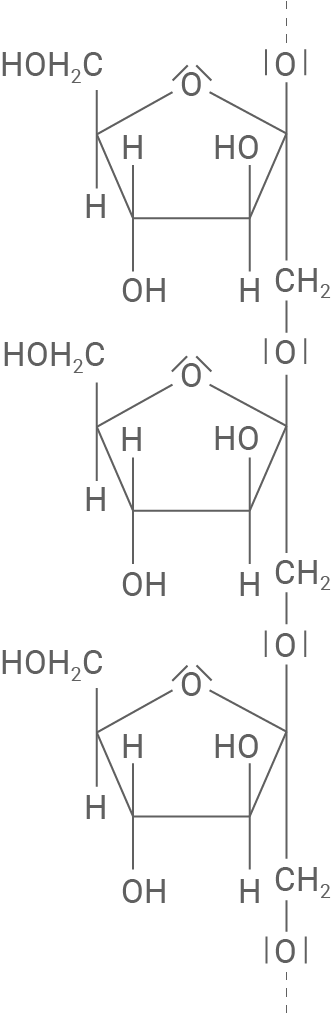
Material 5 zeigt einen Strukturformelausschnitt aus einem weiteren in Bananen enthaltenen Kohlenhydrat.
Formuliere die HAWORTH- und die FISCHER-Projektion des Monomers.
Benenne das Monosaccharid (HAWORTH-Projektion) und die Verknüpfungsart der Monomere in dem Kohlenhydrat.
(6 BE)
3.6
Der Gehalt an Serotonin  in Bananen wurde mit
in Bananen wurde mit  Serotonin pro
Serotonin pro  Fruchtfleisch ermittelt.
Berechne die Stoffmenge an Serotonin in einer Portion von
Fruchtfleisch ermittelt.
Berechne die Stoffmenge an Serotonin in einer Portion von  Bananenfruchtfleisch.
Bananenfruchtfleisch.
(5 BE)
(50 BE)
Material 1
Aromastoffe in Bananen: Ester
| Edukte | Name des entstehenden Esters |
|---|---|
| Ethansäure und Pentan-2-ol | 2-Pentylethanoat |
| Butansäure und 2-Methylbutan-1-ol | (2-Methylbutyl)butanoat |
Material 2
Ein weiterer Aromastoff in Bananen

Material 3
Synthese von Pentan-2-ol
Pentan-2-ol kann durch folgende drei Reaktionen hergestellt werden: Reaktion A:Aus der Reaktion von Pent-2-en mit Wasser entsteht Pentan-2-ol. Reaktion B: 2-Chlorpentan reagiert mit Hydroxid-Ionen zu Pentan-2-ol und einem Anion. Reaktion C: Setzt man Pentan-2-on mit elementarem Wasserstoff um, erhält man ebenfalls Pentan-2-ol.
Material 4
Unreife und reife Bananen im Vergleich
Beim Reifeprozess ändern die Bananen die Farbe ihrer Schale von grün nach gelb. Mit zunehmendem Reifegrad wird ihr Fruchtfleisch weicher und die Bananen schmecken wesentlich süßer. Auch experimentell lassen sich unreife und reife Bananen unterscheiden. Dazu wird etwas bräunliche Iod-Kalium-Iodid-Lösung (LUGOL' sche Lösung) auf das Fruchtfleisch von unreifen und reifen Bananen getropft. Bei unreifen Bananen färbt sich das Fruchtfleisch tief dunkelblau, bei sehr reifen Bananen beobachtet man nur an wenigen Stellen einige punktförmige blaue Bereiche. Das übrige Fruchtfleisch zeigt eine bräunliche Verfärbung.Material 5
Strukturformelausschnitt eines Kohlenhydrats in Bananen

Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?
3.1
Reaktionsmechanismus
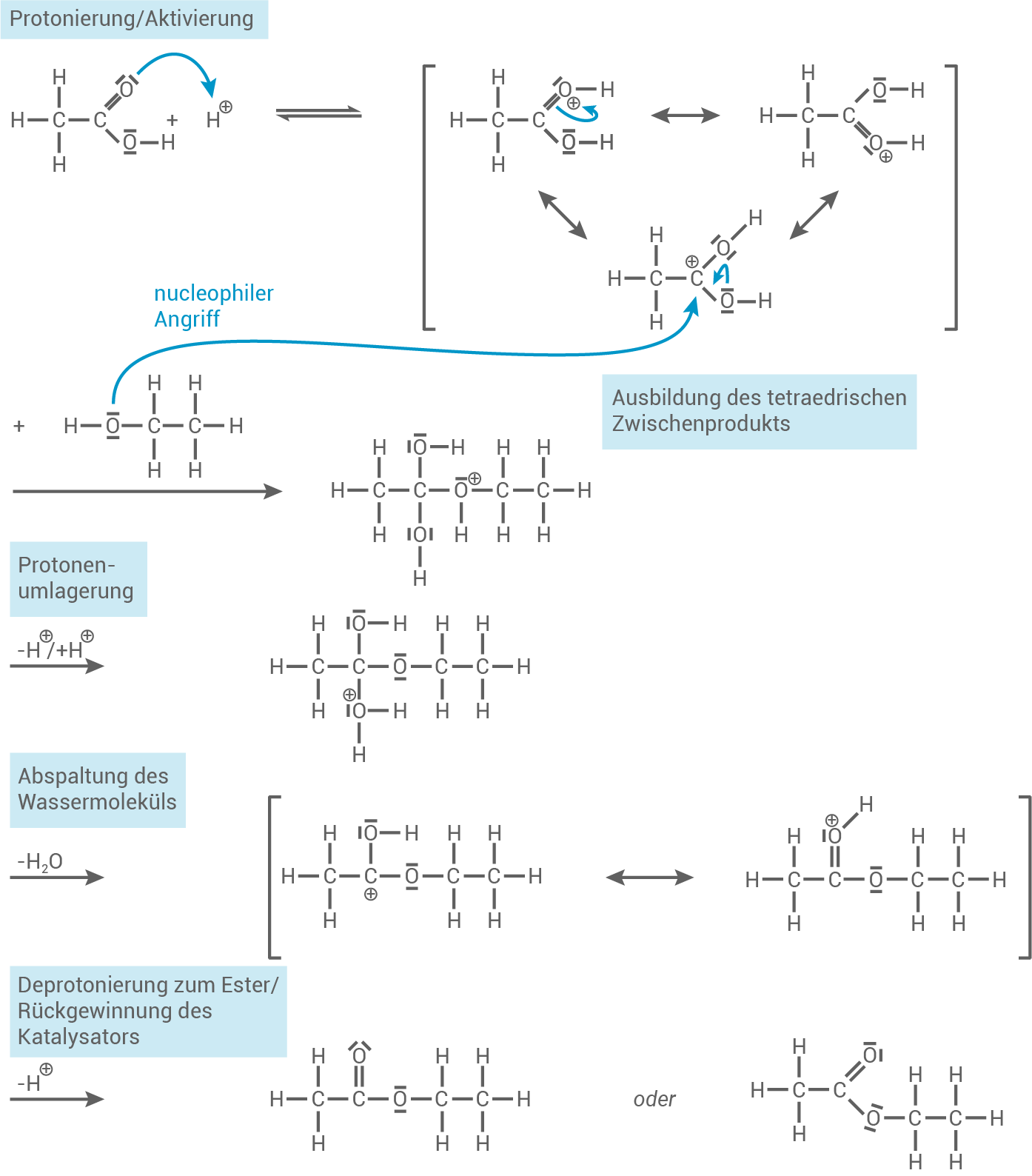

Säurekatalysierten Veresterung von Ethansäure mit Ethanol, inklusive Überschriften
3.2
Strukturformeln der beiden Ester-Moleküle
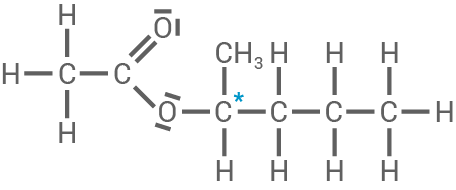
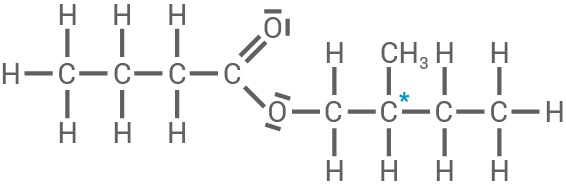 Asymmetrisches Kohlenstoff-Atom und Enantiomere
Asymmetrisches Kohlenstoff-Atom und Enantiomere

2-Pentylethanoat

2-(Methylbutyl)butanoat
- Das asymmetrische
-Atom ist mit * gekennzeichnet.
- Ein Kohlenstoff-Atom ist asymmetrisch, wenn es vier verschiedene Substituenten besitzt. Dadurch ist es ihnen möglich, linear polarisiertes Licht zu drehen.
- Als Enantiomere werden Moleküle bezeichnet, die sich wie Bild- und Spiegelbild zueinander verhalten.
- Ein Molekül, mit einem asymmetrischen
-Atom, besitzt genau ein Isomer, welches sich wie dessen Spiegelbildmolekül verhält.
- Benannt nach IUPAC-Nomenklatur heißt der weitere Aromastoff, der auch in Bananen enthalten ist, Hept-4-en-2-on.
- Seine funktionellen Gruppen sind zum einen die
-Doppelbindung und eine Ketogruppe.
3.3
Reaktionsgleichungen zur Synthese von Pentan-2-ol
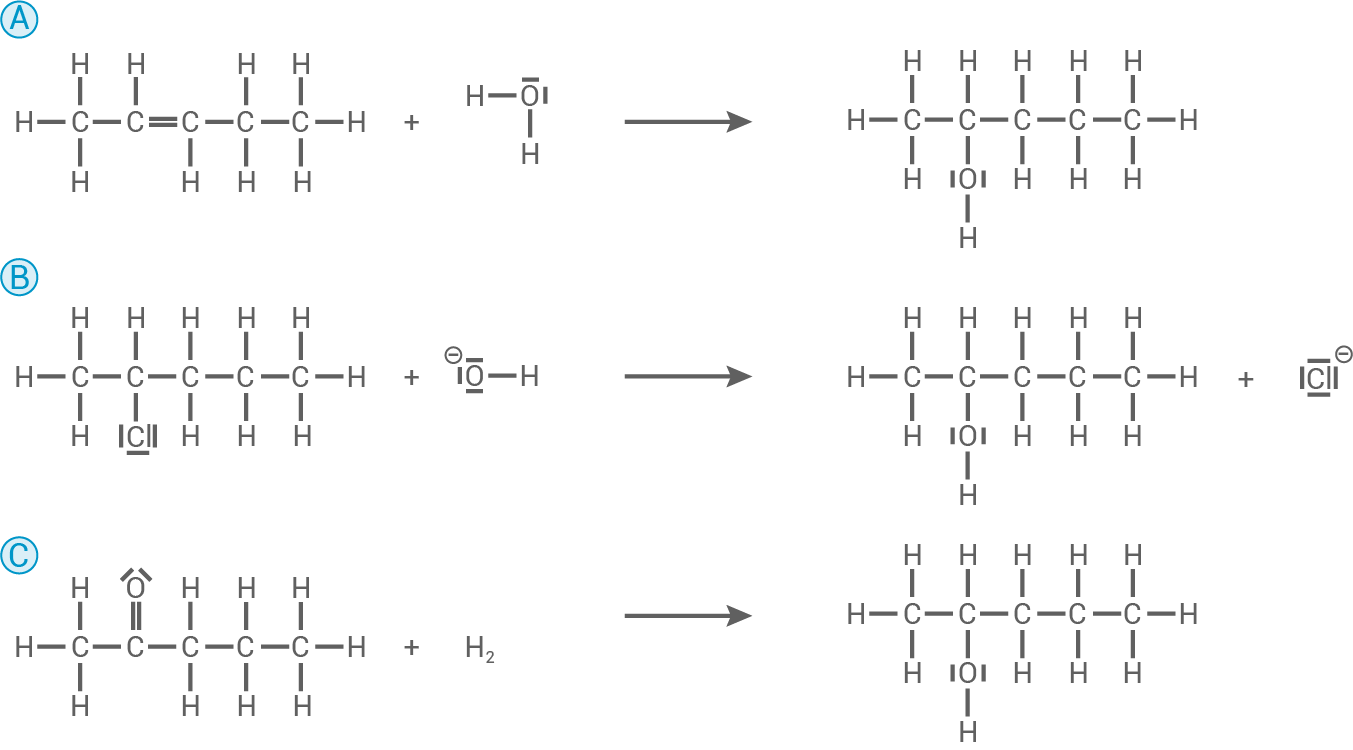 Benennung des Reaktionsmechanismus / Reaktionstyp
Benennung des Reaktionsmechanismus / Reaktionstyp

- Reaktion A: elektrophile Addition
- Reaktion B: nucleophile Substitutionsreaktion
- Reaktion C: Redoxreaktion
Hydrierung
3.4
Amylose-Molekül
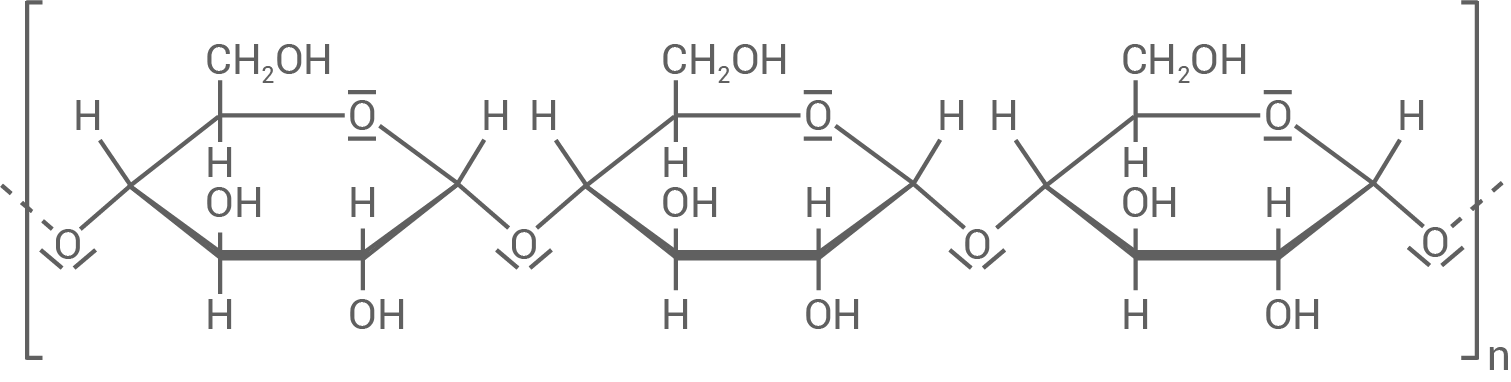

Strukturformelausschnitt (drei Monomer-Einheiten)
- Die Strukturformel zeigt ein unverzweigtes Polysaccharid.
- Das Amylose-Molekül besteht aus
-D-Glucose-Einheiten.
- Die einzelnen Monomerbausteine sind
-1,4-glycosidisch verknüpft.
- Eine Iod-Stärke-Probe soll Stärke in Form von Amylose nachweisen. Der Nachweis ist positiv, wenn sich die bräunliche Iod-Kaliumiodid-Lösung tiefblau färbt.
- Im Experiment zeigt also nur die helikalen, dreidimensionalen Amylose solch eine tiefblaue Färbung. Wenn diese durch Abbau nicht mehr vorhanden ist, ist auch keine Blaufärbung mehr sichtbar.
- Der Stärkeanteil ist in unreifen Bananen sehr hoch, was im Experiment durch die tiefblaue Farbe erkennbar ist.
- Je reifer eine Banane wird, desto mehr Stärke wird zu Glucose abgebaut. Daraus folgt eine schwächere bzw. gar keine Blaufärbung.
- Reife Bananen schmecken süßer als unreife. Diese Tatsache lässt sich ebenfalls damit begründen, dass Stärke beim Reifungsprozess zu Glucose abgebaut wird.
- Während in unreifen Bananen die Glucoseeinheiten noch über glycosidische Bindungen miteinander verknüpft sind, liegt in reifen Bananen ein hoher Anteil an süß schmeckenden Glucose-Monosaccharideinheiten vor.
3.5
Weiteres Kohlenhydrat
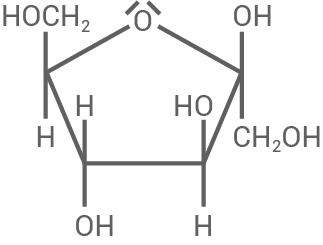
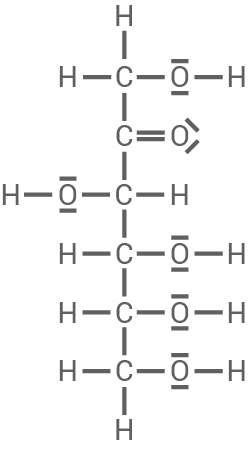

HAWORTH-Projektion

FISCHER-Projektion
- Bei diesem Monosaccharid handelt es sich um
-D-Fructose.
- Die einzelnen Fructose-Einheiten sind
-1,2-glycosidisch miteinander verknüpft.
3.6
Berechnung der Stoffmenge an Serotonin
Gegeben sind eine Masse von  und mit der Summenformel auch die molare Masse
und mit der Summenformel auch die molare Masse  Es gilt:
Es gilt:  und damit ergibt sich für
und damit ergibt sich für  Banane:
Banane:
![\(\begin{array}[t]{rll}
n&=& \dfrac{0,0061\,\text{g} }{176 \,\text{g} \cdot \text{mol}^{-1}} & \\[5pt]
&\approx& 3,466 \cdot 10^{-5} \,\text{mol}
\end{array}\)](https://mathjax.schullv.de/04ab9b41ee66daf9f7f026a024d599b940686cb00691523263d8c6037082df2f?color=5a5a5a) Für
Für  Bananen ergibt sich also:
Bananen ergibt sich also:
![\(\begin{array}[t]{rll}
n&=& 5 \cdot 3,466 \cdot 10^{-5} \,\text{mol} & \\[5pt]
&\approx& 1,733 \cdot 10^{-4} \,\text{mol}
\end{array}\)](https://mathjax.schullv.de/d219dc5acbb6adc2fbaefbfa64aaeb95815e66d0d87fbded0afb8644aeda870c?color=5a5a5a) In
In  Bananen sind also ca.
Bananen sind also ca.  Serotonin enthalten.
Serotonin enthalten.